Профилактика и лечение острых респираторных инфекций у детей с бронхиальной астмой
СтатьиОпубликовано в журнале:
«Доктор.Ру » № 9 (87), 2013
Е. Г. Кондюрина, Т. Н. Елкина, В. В. Зеленская, М. В. Штейнберг, Н. Г. Тиминская
Новосибирский государственный медицинский университет
E. G. Kondyurina, T. N. Elkina, V. V. Zelenskaya, M. V. Steinberg, N. G. Timinskaya
Novosibirsk State Medical University
У детей с бронхиальной астмой (БА) вирусная инфекция является основной причиной обострения заболевания (80-85%) [1, 2, 14] и главным фактором риска госпитализации каждой осенью [16, 20, 30]. До 70% пациентов с БА в зимний период страдают ее обострениями после перенесенной вирусной инфекции [22]. Риновирусы человека (HRV) наиболее часто вызывают острые инфекции респираторного тракта как в популяции, так и у детей с БА, способствуя появлению приступов БА [26]. Обострения БА (оБА) также могут вызвать респираторно-синцитиальные вирусы (RSV), вирусы гриппа и парагриппа, коронавирусы, метапневмовирусы человека, аденовирусы и бокавирусы. Показана роль RSV в дисрегуляции ответа ткани легких на воспаление [27], у мышей RSV-инфекция может вызывать ремоделирование дыхательных путей [28]. Госпитализация по поводу RSV-бронхиолита является фактором риска развития БА у детей [32].
Большинство исследований сфокусировано на роли риновирусов в патогенезе и течении БА. В когортном исследовании Childhood Origin of Asthma (COAST) свистящее дыхание из-за RSV (OR = 2,6), HRV (OR = 9,8) и сочетания HRV и RSV (OR = 10,0) было связано с повышенным риском развития БА в возрасте 6 лет [31].
Внедрение риновирусов в нормальные эпителиальные клетки инициирует различные варианты иммунного ответа с секрецией интерферонов (ИФН-α, ИФН-ß, ИФН-γ) и апоптозом. В экспериментальных исследованиях с участием здоровых добровольцев и пациентов с БА показано снижение продукции ИФН-ß и ИФН-α, при риновирусных инфекциях [24]. In vitro эпителиальные клетки у взрослых с БА по сравнению со здоровыми при риновирусной инфекции продуцируют меньше ИФН-ß [15] и ИФН-α, [29], что замедляет элиминацию вирусов и приводит к вирусиндуцированной клеточной цитотоксичности. Описано снижение продукции ИФН-α мононуклеарными клетками периферической крови и плазматическими дендритическими клетками у взрослых и детей с БА в ответ на вирусы гриппа А [17], RSV и HRV [23]. Эпителиальные клетки у астматиков при экзогенном лечении ИФН-ß уменьшают высвобождение риновирусов [19].
Таким образом, адекватный антивирусный ответ ограничивает инфекцию в пределах верхних отделов респираторного тракта (течение болезни, типичное для здоровых людей). Если ответ дефицитный, то инфекции, обычно поражающие верхние дыхательные пути, например риновирусная, предоминантно могут распространяться в нижние отделы, вызывая соответствующие респираторные симптомы и оБА у предрасположенных индивидуумов [13]. Критическим периодом старта БА являются первые 2-3 года жизни. В этом возрасте рост и ремоделирование легких и дыхательных путей происходят максимально быстро, поэтому воспаление в результате атопии или тяжелых инфекций нижних отделов респираторного тракта гипотетически может нарушить программы дифференциации подлежащих тканей, что приводит к разрушительным долговременным эффектам в респираторном тракте. Меры, которые могут снизить частоту и/или тяжесть инфекций нижних дыхательных путей среди детей с высоким риском атопии, вероятно, будут эффективными в предупреждении БА, что сможет сократить распространенность хронических заболеваний в обществе [21, 25].
Иммунная функция и антивирусная защита имеют многочисленные специфические и неспецифические компоненты. Здоровый образ жизни, соблюдение принципов индивидуальной гигиены, регулярная физическая нагрузка, сбалансированная диета, адекватный сон, отсутствие стресса, табачного дыма в окружающей среде и отказ от излишнего использования антибиотиков могут снизить частоту вирусных инфекций у детей с БА и улучшить иммунный ответ. Обсуждается также роль активных пробиотических добавок, продуктов бактериального происхождения, таких как OM-85, но в настоящее время нет антивирусной терапии, пригодной для повсеместного распространения [13]. Профилактическое применение интраназальных рекомбинантных ИФН-α и ИФН-ß эффективно против риновирусной инфекции у человека [12, 18]. Однако требуется уточнение их дозировок, что в сочетании с локальными побочными эффектами, нейтропенией и высокой стоимостью ограничивает возможность использования этих лекарственных средств для ежедневной профилактики.
На протяжении последних 10 лет накоплен значительный опыт эффективного применения индуктора интерферонов Анаферона детского (АнД) для профилактики и лечения ОРВИ у детей с аллергическими заболеваниями [4-6, 8]. Ключевые механизмы действия АнД заключаются в повышении продукции эндогенных интерферонов и усилении взаимодействия ИФН-γ с его рецептором [3, 11]. В серии доклинических исследований показано, что при профилактическом и/или лечебном применении препарат обладает противовирусным действием по отношению к РНК- и ДНК-содержащим вирусам и иммунотропной активностью [3].
Влияние АнД на продукцию эндогенных интерферонов зависит от присутствия вируса в организме. Избирательность лечебного действия АнД проявляется в повышении продукции интерферонов в острый период вирусной инфекции, что приводит к росту сывороточной концентрации ИФН-γ и ИФН-α до уровней, достаточных для борьбы с инфекцией. В отсутствие вируса препарат практически не стимулирует продукцию интерферонов, поэтому к моменту выздоровления их содержание в сыворотке крови снижается до нормы, что предотвращает развитие гипореактивности. Вместе с тем у реконвалесцентов действие АнД проявляется более высокими (например, по сравнению с плацебо) уровнями индуцированной продукции иФН-γ и ИФН-α. именно эти эффекты, проявляющиеся и при профилактическом приеме, обеспечивают большие функциональные возможности системы интерферонов в случае развития новой/повторной инфекции [10]. Наличием описанных свойств обосновывается возможность безопасного и эффективного применения АнД повторными лечебными и профилактическими курсами во время подъема заболеваемости ОРВи, в том числе у детей, посещающих детские сады [7, 9].
Нарушение интерферонопродукции и обусловленная этим склонность к поражению нижних отделов респираторного тракта при риновирусной инфекции (самая частая этиология ОРВи), высокая распространенность вирусиндуцированного фенотипа БА у дошкольников делают перспективным профилактическое и лечебное применение АнД у детей.
Целью исследования, проведенного сотрудниками кафедр педиатрии и поликлинической педиатрии Новосибирского государственного медицинского университета на базе дошкольных учреждений г. Новосибирска и Новосибирской области, явилась оценка эффективности АнД в профилактике и лечении повторных эпизодов ОРВи у детей с БА.
Материал и методы
Проведено двойное слепое плацебо-контролируемое рандомизированное клиническое исследование, для участия в котором с 2006 по 2008 г. в городе Новосибирске и в Новосибирской области были отобраны 200 детей в возрасте от 1 года до 5 лет. Большинство детей посещали детские дошкольные учреждения. Критериями включения были давность верификации диагноза БА не менее шести месяцев, легкое или среднетяжелое течение БА, наличие письменно подтвержденного согласия родителей на участие их ребенка в исследовании. К критериям невключения относились тяжелое течение БА, тяжелые приступы удушья, применение системных глюкокортикостероидов в течение последних шести месяцев и использование других схем профилактики ОРВи, кроме применения АнД. Набор детей осуществлялся в период с сентября по ноябрь, наблюдение длилось 3 месяца.
С помощью процедуры простой рандомизации рекрутированные пациенты были распределены в две группы, равные по численности (табл. 1) и репрезентативные по тяжести основного заболевания (табл. 2). Базисная терапия БА в группах проводилась в зависимости от степени тяжести патологии, соответствовала стандартам лечения и была сопоставимой.
Дети, распределенные в основную группу, принимали АнД по профилактической схеме: по 1 таблетке 1 раз в день на протяжении 3 месяцев. Пациенты, включенные в контрольную группу, по аналогичной схеме получали плацебо, также в течение 3 месяцев. АнД и плацебо не различались внешне или органолептически и были упакованы в идентичные флаконы.
При появлении признаков ОРВИ дети применяли препарат (АнД или плацебо) по лечебной схеме: в начале заболевания по 1 таблетке через каждые 30 минут в течение первых 2 часов, затем по 1 таблетке 3 раза до ночного сна с примерно равными промежутками времени между приемами, в течение последующих дней по 1 таблетке 3 раза в день. Курс лечения составлял 5 дней. Все дети, включенные в исследование, по показаниям получали симптоматические и патогенетические препараты. Базисная терапия БА продолжалась в соответствии со степенью тяжести патологии, при возникновении бронхиальной обструкции использовались общепринятые схемы лечения, при необходимости осуществлялась госпитализация ребенка в профильный стационар. По окончании лечения ОРВИ дети вновь переводились на профилактическую схему вплоть до окончания исследования.
При оценке профилактической эффективности сравнивали доли детей, заболевших ОРВИ за период наблюдения, в группах. При оценке лечебных эффектов фиксировали продолжительность температурной реакции, интоксикационных и катаральных симптомов со стороны верхних и нижних дыхательных путей. Дополнительно анализировали частоту развития оБА на фоне ОРВИ, сравнивали доли детей, перенесших больше одной ОРВИ за период наблюдения, в группах. Для оценки эффективности АнД в лечении повторных ОРВИ проводили сравнение средней продолжительности первого эпизода ОРВИ с аналогичным показателем второго эпизода в группе у детей, перенесших более одной ОРВИ за период наблюдения.
Статистическую обработку данных проводили с помощью статистического пакета Statistica 6.0. В целях оценки различий непрерывных переменных, полученных в двух разных группах, использовали t-критерий Стьюдента для независимых выборок. Частотный анализ долей пациентов из разных групп выполняли с применением точного критерия Фишера и критерия х2, для анализа влияния факторов «прием АнД» и «количество эпизодов ОРВИ» на продолжительность оБА применяли дисперсионный анализ.
Результаты
Анализ анамнестических данных показал, что все дети за предшествующие исследованию 12 месяцев перенесли ОРВИ
в среднем 4,1 ± 0,1 раза (от 2 до 8) при средней продолжительности одного эпизода ОРВИ 15,7 ± 0,4 суток. Катаральные явления, в частности кашель, отмечались в среднем около 3 недель (22,3 ± 0,2 суток). В 79,0% случаев к третьему дню ОРВИ появлялись типичные изменения дыхания, что позволяет сделать вывод о триггерной роли ОРВИ в развитии оБА у детей.
При изучении заболеваемости ОРВИ за период наблюдения было выявлено, что в основной группе ОРВИ перенесли 40,0% детей, из них у 20 пациентов было по 2 эпизода заболевания, общее число ОРВИ составило 60 случаев. В контрольной группе за 3 месяца было зарегистрировано 132 случая ОРВИ, при этом болели 76 детей, из которых 36 пациентов перенесли по 2 эпизода респираторной инфекции, а 10 детей - по 3 эпизода (табл. 3).
Средняя продолжительность отдельных симптомов и заболевания в целом в основной группе была значимо меньше, чем в контрольной (табл. 4). Наибольшие различия отмечались в длительности лихорадочной реакции, кашля и хрипов, выявлявшихся при аускультации. Частота назначения антибактериальной терапии составила 11,7% в основной группе против 32,6% в контрольной (p = 0,002).
За время наблюдения 20,0% детей из основной и 64,0% детей из контрольной группы перенесли оБА (p<0,001). Все случаи оБА были вызваны ОРВИ, в том числе при повторных эпизодах респираторных инфекций (табл. 5, 6).
В основной группе вирусиндуцированные оБА развивались значительно реже, чем в группе плацебо. Эти отличия были особенно заметны у детей, перенесших более одного эпизода ОРВИ. Частота оБА на фоне первой ОРВИ в основной группе была меньше аналогичного показателя в контрольной группе на 34,0%. При этом второй эпизод ОРВИ в основной группе вызвал оБА в 35,0% случаев, тогда как в группе контроля - в 93,0% случаев (разница увеличилась до 58,0%, p<0,001).
Средняя продолжительность оБА за весь период наблюдения составила в основной группе 6,8 ± 1,1 дня против 12,2 ± 0,6 дня в группе плацебо-контроля (p<0,001). Анализ средней продолжительности оБА, развившихся на фоне первого и второго эпизодов ОРВИ, показал, что в обоих случаях сохранялась та же направленность различий: при первом эпизоде 7,9 ± 1,5 дня в основной группе против 12,1 ± 0,9 дня в контрольной (p<0,05) и при втором эпизоде 4,6 ± 1,5 дня против 12,0 ± 0,8 дня (p<0,001) в основной и контрольной группах соответственно (рис. 1).
Дисперсионный анализ «2 х 3» факторов «прием АнД» (F1) и «количество эпизодов ОРВи» (F2) продемонстрировал их статистически значимые влияния на продолжительность оБА: F1/286 = 84,3 (p<0,001) и F2/286 = 3,8 (p = 0,02). Совокупное воздействие данных факторов в основной и контрольной группах также зн лось: F1+2/286 = 9,5, p = 0,0001.
Таблица 1. Характеристика групп наблюдения
| Группы больных | Число участников | Возраст, лет | Доля мальчиков, % | Количество посещающих ДДУ*, % |
| Основная | 100 | 4,1 ± 0,3 | 63,0 | 75,0 |
| Контрольная | 100 | 4,4 ± 0,2 | 60,0 | 70,0 |
Таблица 2. Распределение больных в группах по степени тяжести бронхиальной астмы (БА), %
| Группы больных | Легкая БА | Среднетяжелая БА | |
| интермиттирующая | персистирующая | ||
| Основная | 67,0 | 24,0 | 9,0 |
| Контрольная | 64,0 | 29,0 | 7,0 |
Таблица 3. Частота развития и количество эпизодов ОРВИ в группах за период наблюдения
| Частота эпизодов ОРВИ | Основная группа (n = 100) | Контрольная группа (n = 100) | |||
| доля детей, % | число ОРВИ | доля детей, % | число ОРВИ | ||
| Не болели | 60,0** | - | 24,0 | - | |
| Болели | 1 раз | 20,0 | 20 | 30,0 | 30 |
| 2 раза | 20,0* | 40 | 36,0 | 72 | |
| 3 раза | 0 | 0 | 10,0 | 30 | |
| Всего | 100,0 | 60 | 100,0 | 132 | |
Таблица 4. Продолжительность клинических симптомов ОРВИ у детей с бронхиальной астмой, дни (M ± m)
| Группы больных | Симптомы ОРВИ | Заболевание | ||||
| повышение температуры тела | интоксикация | выделения из носа | кашель | хрипы в легких в целом | ||
| Основная (n = 60) | 1,6 ± 0,2** | 2,8 ± 0,2** | 4,7 ± 0,2 | 4,6 ± 0,9** | 4,8 ± 0,8* | 5,5 ± 0,9* |
| Контрольная (n = 132) | 3,0 ± 0,2 | 4,4 ± 0,4 | 5,2 ± 0,3 | 9,2 ± 0,8 | 7,9 ± 0,7 | 9,4 ± 1,1 |
** Различия основной группы с контрольной статистически значимы: p<0,01.
Таблица 5. Доли детей с вирусиндуцированным обострением бронхиальной астмы (оБА) в зависимости от частоты ОРВИ
| Частота ОРВИ | Основная группа | Контрольная группа | ||
| число детей, болевших ОРВИ | из них с оБА, абс. (%) | число детей, болевших ОРВИ | из них с оБА, абс. (%) | |
| Болели 1 раз | 20 | 13 (65,0) | 30 | 21 (70,0) |
| Болели 2 раза | 20 | 7 (35,0)* | 36 | 33 (92,0) |
| Болели 3 раза | 0 | 0 | 10 | 10 (100,0) |
Таблица 6. Частота развития обострений бронхиальной астмы (оБА) на фоне ОРВИ при разных эпизодах заболевания
| Эпизоды ОРВИ | Основная группа | Контрольная группа | ||
| число ОРВИ | из них с оБА, абс. (%) | число ОРВИ | из них с оБА, абс. (%) | |
| 1-й эпизод | 40 | 20 (50,0)* | 76 | 64 (84,0) |
| 2-й эпизод | 20 | 7 (35,0)* | 46 | 43 (93,0) |
| 3-й эпизод | 0 | 0 | 10 | 10 (100,0) |
| Всего | 60 | 27 (45,0)* | 132 | 117 (88,6) |
При анализе показателей повторной заболеваемости ОРВИ нами было выявлено, что в основной группе 20% детей перенесли более одного эпизода ОРВИ, тогда как в контрольной группе 46% детей болели 2 и 3 раза (p<0,001). Сравнение средней продолжительности первых и повторных (вторых) эпизодов ОРВИ показало, что в основной группе она была статистически значимо меньше, чем в контрольной (p<0,001) (рис. 2). В обеих группах не наблюдалось значимых изменений средней продолжительности течения ОРВИ от первого эпизода ко второму.
Заключение
Представленные данные свидетельствуют, что применение Анаферона детского (АнД) для профилактики ОРВИ у детей с бронхиальной астмой (БА) по сравнению с плацебо статистически значимо предотвращает развитие респираторных инфекций, в том числе снижает частоту повторных эпизодов ОРВИ. Лечебное применение АнД позволяет добиться сокращения продолжительности ведущих симптомов заболевания и эпизода ОРВИ в целом. Наряду с этим лечебно-профилактическое использование АнД способствует снижению частоты и продолжительности вирусиндуцированных осложнений БА (оБА) у детей. АнД значимо влияет на частоту повторных ОРВИ, что также способствует уменьшению риска развития оБА и может улучшать контроль за течением БА у детей.
Применение АнД и в профилактическом, и в лечебном режиме характеризуется хорошей переносимостью: за время наблюдения не было зарегистрировано каких-либо нежелательных явлений, требовавших отмены препарата.
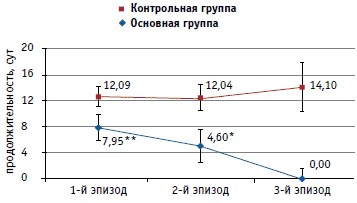
* Различия основной группы с контрольной статистически значимы: p<0,05.
** Различия основной группы с контрольной статистически значимы: p<0,001
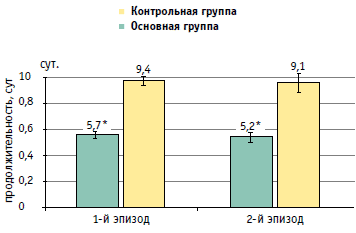
* Различия основной группы с контрольной статистически значимы: p<0,001
Резюме
Цель исследования: оценка эффективности Анаферона детского (АнД) в профилактике и лечении повторных ОРВИ у детей с бронхиальной астмой (БА).
Дизайн: рандомизированное двойное слепое плацебо-контролируемое клиническое исследование.
Материал и методы. Дети (возраст - 1-5 лет; течение БА - легкое или среднетяжелое) были рандомизированы в основную группу (n = 100; 3 месяца получали АнД по стандартной профилактической схеме с временным переводом на стандартную лечебную схему в случае развития ОРВИ) и контрольную группу (n = 100; получали плацебо по аналогичным схемам). В обеих группах для лечения ОРВИ дополнительно применяли патогенетическую и симптоматическую терапию.
Результаты. В основной группе болели ОРВИ 40 детей, из них 20 дважды (всего 60 ОРВИ), а в контроле - 76 детей, из них 36 дважды и 10 детей по 3 раза (132 ОРВИ). Средняя продолжительность 1 и 2-го эпизодов ОРВИ составила в основной группе 5,7 ± 0,4 и 5,2 ± 0,5 дня, в контроле - 9,4 ± 0,6 и 9,1 ± 0,8 дня соответственно. Обострение БА (оБА) перенесли 20% детей из основной и 64% детей из контрольной группы (p Заключение. Лечебно-профилактическое применение АнД у детей с БА по сравнению с плацебо понизило заболеваемость ОРВИ, в том числе повторную, сократило продолжительность ОРВИ и способствовало снижению частоты и продолжительности вирусиндуцированных оБА у детей, что улучшило контроль БА.
Ключевые слова: вирусиндуцированное обострение, бронхиальная астма, Анаферон детский (АнД), индуктор интерферонов, повторные ОРВИ.
Summary
Study Objective: To assess the efficacy of Anaferon for Kids, a Russian preparation of anti-interferon gamma antibodies, in preventing and treating repeated acute respiratory viral infections (ARVI) in children with asthma. Study Design: This was a double-blind, placebo-controlled, randomized clinical study. Materials and Methods: Children, aged 1 to 5, with mild or moderate-to-severe asthma were randomized into the main group (n = 100) or the control group (n = 100). In the main group, children received a standard preventive regimen of Anaferon for Kids for 3 months and were temporally switched to a standard therapeutic regimen in case of ARVI. In the control group, subjects received the same regimens of placebo. In both groups, pathogenesis-based and symptomatic treatment was additionally used in case of ARVI. Results: In the main group, 40 children had ARVI and 20 of them had these infections twice (60 ARVI events in total). In the control group, 76 children had ARVI, while 36 had had two events and 10 had had three events (132 ARVI events in total). The mean duration of the first and second ARVI episodes was 5.7 ± 0.4 and 5.2 ± 0.5 days in the main group and 9.4 ± 0.6 and 9.1 ± 0.8 days in the control group. Asthma exacerbations were reported in 20% and 64% of children in the main and control groups, respectively (p<0,001). Conclusion: The study showed that, compared to a placebo, preventive and therapeutic treatment with Anaferon for Kids in children with asthma reduced the rates of ARVI, including the rates of repeated episodes, and the duration of ARVI episodes. Such treatment also contributed to a reduction in the frequency and duration of virus-induced asthma exacerbations in these patients and, therefore, improved asthma control.
Keywords: virus-induced exacerbation, asthma, Anaferon for Kids, interferon inductor, repeated ARVI.
Литература
- Геппе Н. А. Актуальность проблемы бронхиальной астмы у детей // Педиатрия. 2012. Т. 91. № 3. С. 76-82.
- Динамика эпидемиологии бронхиальной астмы у первоклассников города Новосибирска / Е. Г. Кондюрина, Т. Н. Елкина, B. В. Зеленская, Н. Г. Тиминская [и др.] // Доктор.Ру. Оториноларингология. Пульмонология. 2013. № 8 (86).C. 56-62.
- Жавберт Е. С. Иммунотропные свойства Анаферона и Анаферона детского / Е. С. Жавберт, Ю. Л. Дугина, О. И. Эпштейн // Антибиотики и химиотерапия. 2013. Т. 58. № 5-6. С. 17-23.
- Кондратьева Е. И. Неспецифическая профилактика острых респираторных заболеваний у детей с бронхиальной астмой / Е. И. Кондратьева, Т. А. Шемякина, Е. В. Голикова, И. Р. Пан // Педиатрия. 2007. Т. 86. № 2. С. 76-79.
- Кондюрина Е. Г. Анаферон детский. Клинические и иммунотропные эффекты в педиатрии / Е. Г. Кондюрина, А. Б. Малахов, B. А. Ревякина // Фармакотерапевт. альманах. Вып. 1 / Под ред. Ф. И. Ершова. СПб.: МедиКа, 2008. С. 80-87.
- Кондюрина Е. Г. Профилактика респираторных инфекций при бронхиальной астме у детей в возрасте от года до пяти лет / Е. Г. Кондюрина, Т. Н. Елкина, М. В. Штейнберг // Педиатрия. 2006. № 5. С. 72-76.
- Оценка эффективности повторных профилактических и лечебных курсов Анаферона детского для разработки рациональных схем применения при ОРВИ у детей / А. Л. Заплатников, Г. А. Мингалимова, В. И. Далечин, Т. Н. Носкова [и др.] // Эффектив. фармакотерапия. Педиатрия. 2010. № 4. С. 47-52.
- Современные аспекты профилактики респираторных инфекций у детей с атопией / А. Б. Малахов, Е. Г. Кондюрина, Т. Н. Елкина, В. А. Ревякина//Лечащ. врач. 2007. № 7. С. 91-93.
- Терапевтический эффект и профилактика острых респираторных инфекций при использовании повторных курсов индукторов эндогенного интерферона у детей/ А. Л. Заплатников, E. И. Бурцева, Л. М. Шамрай, Т. Н. Носкова [и др.] // Педиатрия. 2009. Т. 88. № 6. С. 111-115.
- Шамшева О. В. Опыт применения Анаферона в педиатрической практике // Эффективная фармакотерапия. Аллергология. Иммунология. 2013. № 2. С. 30-36.
- Эпштейн О. И. Релиз-активность - от феномена до создания новых лекарственных средств // Бюл. эксперим. биологии и медицины. 2012. Т. 154. № 7. С. 62-67.
- A mechanistic role for type IIIIFN-X1 in asthma exacerbations mediated by human rhinoviruses / E. K. Miller, J. Z. Hernandez, V. Wimmenauer, B. E. Shepherd [et al.] // Am. J. Respir. Crit. Care Med. 2012.Vol. 185. N 5. P. 508-516.
- Ahanchian H. Respiratory viral infections in children with asthma: do they matter and can we prevent them? / H. Ahanchian, C. M. Jones, Y. S. Chen, P. D. Sly// BMC Pediatr. 2012. N 12. P. 147.
- Asthma: a chronic infectious disease?/ G. Caramon, N. Papadopoulos, M. Contoli, B. Marku [et al.] // Clin. Chest Med. 2012. Vol. 33. N 3. P. 473-484.
- Asthmatic bronchial epithelial cells have a deficient innate immune response to infection with rhinovirus / P. A. Wark, S. L. Johnston, F. Bucchieri, R. Powell [et al.] // J. Exp. Med. 2005. Vol. 201. N 6. P. 937-947.
- Busse W. W. Role of viral respiratory infections in asthma and asthma exacerbations / W. W. Busse, R. F. Jr. Lemanske, J. E. Gern // Lancet. 2010. Vol. 376. N 9743. P. 826-834.
- Counterregulation between the FcepsilonRI pathway and antiviral responses in human plasmacytoid dendritic cells / M. A. Gill, G. Bajwa, T. A. George, C. C. Dong [et al.] // J. Immunol. 2010. Vol. 184. N 11. P. 5999-6006.
- Edwards M. R. Interferon-lambda as a new approach for treatment of allergic asthma?/ M. R. Edwards, S. L. Johnston // EMBO Mol. Med. 2011. Vol. 3. N 6. P. 306-308.
- Exogenous IFN-в has antiviral and anti-inflammatory properties in primary bronchial epithelial cells from asthmatic subjects exposed to rhinovirus/ J. A. Cakebread, Y. Xu, C. Grainge, V. Kehagia [et al.] // J. Allergy Clin. Immunol. 2011. Vol. 127. N 5. P. 1148-1154.
- Forno E. Predicting asthma exacerbations in children / E. Forno, J. C. CeledOn// Curr. Opin. Pulm. Med. 2012. Vol. 18. N 1. P 63-69.
- Holgate S. T. The sentinel role of the airway epithelium in asthma pathogenesis // Immunol. Rev. 2011. Vol. 242. N 1. P. 205-219.
- Holt P. G. Interaction between adaptive and innate immune pathways in the pathogenesis of atopic asthma: operation of a lung/bone marrow axis/ P. G. Holt, P. D. Sly// Chest. 2011. Vol. 139. N 5. P. 1165-1171.
- Holtzman M. J. Host epithelial-viral interactions as cause and cure for asthma/ M. J. Holtzman, D. A. Patel, Y. Zhang, A. C. Patel// Curr. Opin. Immunol. 2011. Vol. 23. N 4. P. 487-494.
- IFN-gamma-induced protein 10 is a novel biomarker of rhino-virus-induced asthma exacerbations / P. A. Wark, F. Bucchieri, S. L. Johnston, P. G. Gibson [et al.] // J. Allergy Clin. Immunol. 2007. Vol. 120. N 3. P. 586-593.
- Jackson D. J. The role of rhinovirus infections in the development of early childhood asthma // Curr. Opin. Allergy Clin. Immunol. 2010. Vol. 10. N 2. P. 133-138.
- Jackson D. J. The role of viruses in acute exacerbations of asthma / D. J. Jackson, S. L. Johnston // J. Allergy Clin. Immunol. 2010. Vol. 125. N 6. P. 1178-1187.
- Mohapatra S. S. Epidemiologic, experimental, and clinical links between respiratory syncytial virus infection and asthma / S. S. Mohapatra, S. Boyapalle // Clin. Microbiol. Rev. 2008. Vol. 21. N 3. P. 495-504.
- Respiratory syncytial virus infection provokes airway remodelling in allergen-exposed mice in absence of prior allergen sensitization / S. Tourdot, S. Mathie, T. Hussell, L. Edwards [et al.] // Clin. Exp. Allergy. 2008. Vol. 38. N 6. P. 1016-1024.
- Role of deficient type III interferon-lambda production in asthma exacerbations / M. Contoli, S. D. Message, V. Laza-Stanca, M. R. Edwards [et al.] // Nat. Med. 2006. Vol. 12. N 9. P. 10231026.
- The International Study of Asthma and Allergies in Childhood (ISAAC) Phase Three: a global synthesis / J. Mallol, J. Crane, E. von Mutius, J. Odhiambo [et al.] //Allergol. Immunopathol. (Madr.). 2013. Vol. 41. N 2. P. 73-85.
- Wheezing rhinovirus illnesses in early life predict asthma development in high-risk children / D. J. Jackson, R. E. Gangnon, M. D. Evans, K. A. Roberg [et al.] // Am. J. Respir. Crit. Care Med. 2008. Vol. 178. N 7. P. 667-672.
- Wu P. Evidence for a causal relationship between respiratory syncytial virus infection and asthma / P. Wu, T. V. Hartert // Expert. Rev. Anti-infect. Ther. 2011. Vol. 9. N 9. P. 731-745.
