Коррекция психосоматических расстройств в комплексной терапии артериальной гипертонии у женщин в перименопаузальном периоде
СтатьиОпубликовано в журнале, Южно-Российский медицинский журнал 2002; 3
В.Д. Пасечников, Т.В. Глухова, И.Ю. Уманская, И.Г. Септа
Кафедра терапии факультета последипломного образования Ставропольской государственной медицинской академии
Артериальная гипертония (АГ) является одним из самых распространенных заболеваний, возникновение которого сопряжено со значительным увеличением риска развития сердечно-сосудистых осложнений и смертности.
Известно, что распространенность АГ увеличивается с возрастом, причем до 40 лет это заболевание чаще наблюдается у мужчин, а после 50 отмечается увеличение частоты гипертонии у женщин. В дальнейшем уровень ее распространенности превосходит этот показатель в мужской популяции [10,28]. Такие особенности формирования АГ у женщин связывают с изменениями их гормонального фона.
В эпидемиологических исследованиях по изучению АГ обнаружено, что при развитии климактерического синдрома АГ наблюдается в два раза чаще, чем у женщин с сохраненным циклом того же возраста [8], а пациентки в постменопаузе составляют около половины всех больных с АГ [9]. Эти данные указывают на возможную роль дефицита половых гормонов в развитии АГ у женщин в указанный возрастной период.
Действительно, во многих экспериментальных и клинических исследованиях было показано, что эстрогены обладают рядом кардиопротективных свойств, которые сводятся не только к известному воздействию на липидный спектр крови, систему гемостаза, но и компоненты сосудистой стенки. Выявлено эндотелий-зависимое и эндотелий-независимое вазодилатирующее действие эстрогенов в отношении коронарных артерий [3,23].
Возможными механизмами эндотелий-зависимой дилатации являются увеличение синтеза оксида азота, а также уменьшение его окисления за счет антиоксидантных свойств эстрогенов. Эндотелий-независимая дилатация, предположительно, связана с блокированием эстрогенами кальциевых каналов [21].
Кроме того, эстрогены, снижают уровень катехоламинов в крови наряду с урежением частоты сердечных сокращений, что может быть частично связано с эстроген-опосредованным подавлением бета-адренергической активности. Таким образом, снижение сердечного выброса в сочетании с периферической вазодилатацией может объяснить более низкий уровень артериального давления (АД) у женщин репродуктивного возраста.
На фоне же гормональной перестройки организма повышается гипоталамический порог чувствительности к регулирующему влиянию половых гормонов, что проявляется увеличением возбудимости гипоталамо-гипофизарных структур и активности симпатической нервной системы [5].
В настоящее время большое внимание уделяется возможной роли инсулина в повышении АД в постменопаузе [9,20]. Повышение массы тела, наблюдаемое после наступления менопаузы, может приводить к развитию инсулинорезистентности. Это сопровождается повышением реабсорбции натрия в дистальных канальцах нефрона, повышением тонуса артерий и т.д.
Все вышеперечисленные механизмы или способствуют развитию АГ, или приводят к ухудшению ее течения, делая более лабильной и увеличивая частоту гипертонических кризов, которые носят в этот период чаще водно-солевой характер.
Известно, что АГ является типичным психосоматическим заболеванием и входит в классическую семерку психосоматозов [4,29], а у пациенток с АГ часто регистрируются тяжелые формы таких функциональных расстройств, как климактерический синдром [11,17]. Проявления климактерического синдрома встречаются у 35-70% женщин современной популяции и характеризуются вегето-сосудистыми и психоэмоциональными нарушениями [7,16].
Вегето-сосудистые расстройства проявляются приливами жара и повышенной потливостью, особенно в ночное время; головной болью; гипотонией или гипертонией; ознобом; учащенным сердцебиением; кардиалгией. Психоэмоциональные нарушения включают в себя тревогу, сопровождающуюся понижением настроения или приводящую к снижению работоспособности, раздражительность, сонливость, слабость, беспокойство, депрессию, забывчивость, невнимательность, снижение либидо. Указанные признаки, в том числе уровень тревоги, имеющийся у таких пациентов, в ряде случаев мешают успешному проведению гипотензивной терапии.
Вопрос о том, имеются ли преимущества у той или иной группы антигипертензивных средств в лечении АГ у женщин по сравнению с мужчинами, остается до конца не решенным. В исследованиях по изучению гипотензивных препаратов, включавших мужчин и женщин, не было выявлено различий в эффективности переносимости препаратов основных классов [2,24]. Однако лечение АГ на фоне климактерического синдрома, безусловно, должно быть комплексным и воздействовать на все патогенетические звенья процесса, в том числе учитывать психосоматическую картину заболевания и направленность вегето-сосудистых реакций [18].
Нами проведено исследование эффективности селективного анксиолитика Грандаксина в комплексной терапии АГ у женщин с нарушениями менструального цикла. Выбор данного препарата сделан из-за наличия у него ряда благоприятных фармакологических воздействий. Являясь производным бензодиазепина, Грандаксин дает не только анксиолитический и вегетокорригирующий эффекты, но также имеет мягкое психостимулирующее действие и не оказывает седативного, миорелаксирующего влияния; не снижает физическую и психическую активность, что делает его пригодным для терапии амбулаторных больных, продолжающих заниматься профессиональной деятельностью [6]. Сочетание этих фармакологических свойств позволяет с полным правом отнести этот препарат к средствам, улучшающим качество жизни (КЖ) больного.
Чрезвычайно важно то, что имеется аддитивность взаимодействия Грандаксина и ингибиторов ангиотензин-превращающего фермента (ИАПФ), применяемых при лечении АГ [13].
Целью исследования явилось изучение коррекции Грандаксином выраженности вегетативных и тревожно-депрессивных расстройств у женщин с АГ и сопутствующими гормональными нарушениями, а также его возможного влияния на уровень артериального давления при применении ИАПФ.
Материал и методы
Исследовались больные, проходившие лечение на базе 2-й клинической больницы г. Ставрополя. При клиническом исследовании были отобраны 24 человека, которые имели выраженные соматовегетативные и тревожно-депрессивные расстройства. Это были женщины в возрасте от 40 до 61 года (средний возраст - 49,8 лет). Длительность основного заболевания (АГ) составляла от 1 до 15 лет (в среднем - 8,5 лет). У 15 пациенток появление АГ по времени было связано с развитием климактерического синдрома. В соответствии с классификацией ВОЗ/МОГ 1999 года пограничная АГ диагностирована у 3 больных (12,5%), АГ I степени - у 10 человек (41,7%), АГ II степени - у 11 человек (45,8%).
Пациентам проводили клиническое обследование (сбор анамнеза), объективный осмотр, общеклинические анализы; биохимические, электрофизиологические (ЭКГ, эхо-кардиоскопия) исследования; а также суточное мониторирование АД (СМАД) дважды -в начале и в конце исследования.
Психологическое тестирование включало оценку вегетативных проявлений по социальной анкете; шкалы самооценки тревоги (Шихана) и общего клинического впечатления, а также оценки проявлений и степени социальной дезадаптации. Заполнение применяемых при этом анкет пациенты проводили самостоятельно, что являлось основным требованием обследования. При этом учитывалось следующее: больной, выбрав для ответов на вопросы удобное для него время, может характеризовать свое состояние более откровенно, не торопясь и внимательно.
Для изучения КЖ у больных применяли русскую версию общего опросника MOS-SF-36 (MOS-SF-Item Short Form Health Survey), который содержит следующие шкалы: физического функционирования (PF), ролевого физического функционирования (RF), боли (ВР), общего здоровья (GH), жизнеспособности (VT), социального функционирования (SF), ролевого эмоционального функционирования (RE) и психологического здоровья (МН).
Психологический статус и показатели КЖ оценивались до назначения Грандаксина и повторно после проведенной терапии - с обязательного согласия женщин.
Суточное мониторирование артериального давления (СМАД) проводили с использованием портативной системы ABPM (Венгрия) с применением компьютерной программы обработки данных. Интервалы между измерениями составляли 15 мин днем и 30 мин ночью для исключения какого-либо влияния частоты регистрации на показатели вариабельности АД. Данные СМАД анализировали по индивидуальной схеме бодрствование-сон при наличии не менее 85% успешных регистраций АД. Определяли средние показатели cистолического (САД) и диастолического (ДАД) АД за сутки, день, ночь; вариабельность АД (ВСАД и ВДАД) как стандартное отклонение от среднего значения и "нагрузку давлением", которая оценивалась по индексу времени - ИВ (доля измерений, при которых уровень АД превышает 140/90 мм рт.ст. в дневное время и 120/80 мм рт.ст. в ночное время) и индексу площади - ИП (площадь фигуры, образованной кривыми повышенного и нормального АД). Выраженность двухфазного циркадного ритма анализировали по суточному индексу (СИ) - степени снижения АД (в процентах) в период ночного сна по сравнению с периодом бодрствования.
Базисная терапия АГ включала применение эналаприла (препарат группы ИАПФ) - у 24 человек. Продолжительность предшествовавшей назначению Грандаксина терапии ИАПФ составляла от 4 недель до 2 лет, в среднем - 7,5±0,1 месяцев.
Грандаксин назначали в дозе 50 мг дважды в день на фоне основной терапии ИАПФ в течение 21 дня.
Полученные результаты
Как видно из данных психологического тестирования, представленных на рис. 1, в исследуемой группе больных до применения Грандаксина преимущественно встречались сомато-вегетативные расстройства: плохая переносимость погодных условий, повышенная потливость, головные боли, головокружение, ощущение затруднения дыхания, боли в сердце, нарушение функций желудочно-кишечного тракта и т.п. (в среднем, 80,77 балла по шкале вегетативных изменений, при норме менее 15 баллов), а также различные проявления тревоги: беспокойство, страх, раздражительность, чувство неспособности справляться с текущей ситуацией, нарушение сна и т.п. (показатель тревоги по шкале Шихана в среднем составил 63,55 балла при норме до 25 баллов).
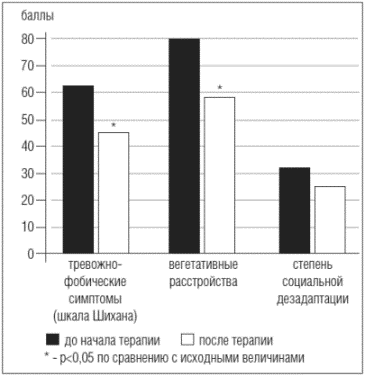
Рис. 1. Динамика показателей психологического тестирования на фоне терапии Грандаксином (n=22)
Нарушения социальной деятельности, выражающиеся в изменении отношения пациенток к домашним обязанностям, развлечениям, профессиональной деятельности, в среднем по группе наблюдения оценивались в 31,77 балла, что характеризует их как умеренно выраженные (интервал возможных колебаний по шкале составляет 0-60 баллов).
Через три недели терапии Грандаксином отмечена тенденция к уменьшению большинства тестируемых параметров психологического статуса (рис.1). Так, в процессе исследования проявления тревоги и вегетативные нарушения значительно и достоверно снизились по сравнению с исходными величинами (р<0,05).
В то же время, показатели степени социальной дезадаптации на фоне лечения изменились в меньшей степени (р>0,05) и по-прежнему, в шкале оставались на уровне умеренно выраженных (24,3 балла).
Анализ тяжести выявленных психологических изменений, проводимый по шкале общего клинического впечатления, выявил четкую положительную динамику при применении Грандаксина (рис.2).
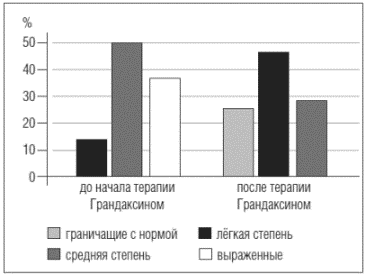
Рис. 2. Динамика тяжести психологических расстройств по шкале общего клинического впечатления (n=22)
Если в начале исследования психологические расстройства оценивались как выраженные у 37,5%, средней тяжести - у 50%, легкой - у 12,5% женщин (т.е. превалировали нарушения выраженные и средней тяжести), то на фоне терапии интенсивность их значительно изменилась. Выраженные психологические нарушения к концу трех недель лечения не зарегистрированы, а доминировали легкая (45,8%) и средняя степень тяжести (29,2%). У 25% больных выраженность симптомов к концу наблюдения граничила с нормой.
В настоящее время интенсивно изучается проблема КЖ и факторов, ухудшающих ее показатели, у больных с различными заболеваниями. Исследования КЖ, позволяющие получить ценную информацию об общем состоянии больных и оценить эффективность применяемых методов терапии, прочно входят в медицинскую практику [12,19,27]. В таблицах 1 и 2 отражена динамика показателей КЖ на фоне лечения Грандаксином.
Как видно из представленных данных (табл. 1), терапия указанным препаратом, в первую очередь, существенно и достоверно повысила КЖ пациенток по показателям психологического здоровья МН и MCS (р4,5<0,001), а также показателю жизнеспособности - VT (р1<0,001).
Таблица 1. Динамика показателей качества жизни (Психологическое здоровье) на фоне терапии Грандаксином (n=22)
| Группы | Шкалы опросника SF-36 | ||||||||
| Физическое здоровье | Суммарные измерения | Жизнеспособность (VT) | Социальное функционирование (SF) | Ролевое эмоциональное функционирование (RE) | Психологическое здоровье (МН) | Психологическое здоровье (MCS) | |||
| До начала терапии | 39,46+1,34 | 35,52+1,56 | 29,4+2,025 | 32,08+1,48 | 31,92+1,64 | ||||
| После терапии | 48,52+1,63 | 39,98+1,64 | 34,41+2,098 | 40,8+1,101 | 40,42+1,31 | ||||
| p | p1<0,001 | p2>0,05 | p3>0,05 | p4<0,001 | p5<0,001 | ||||
В то же время, достоверных различий по шкалам социального функционирования (SF) и ролевого эмоционального функционирования (RE) в процессе трехнедельного наблюдения выявлено не было (р2,3>0,05).
Среди показателей физического здоровья (табл. 2) статистически значимо изменился лишь показатель ролевого физического функционирования - RF (р2<0,05). Остальные параметры: физического функционирования (PF), боли (ВР), общего здоровья (GH) и суммарные измерения физического здоровья (PCS) - имели лишь тенденцию к уменьшению (р1,3,4,5>0,05).
Таблица 2. Динамика показателей качества жизни (Физическое здоровье) на фоне терапии Грандаксином (n=22)
| Группы | Шкалы опросника SF-36 | ||||||||
| Физическое здоровье | Суммарные измерения | Физическое функционирование (PF) | Ролевое физическое функционирование (RF) | Боль (ВР) | Общее здоровье (GH) | Физическое здоровье (PCS) | |||
| До начала терапии | 40,77+1,72 | 31,83+1,53 | 36,35+1,36 | 34,17+1,07 | 39,12+1,12 | ||||
| После терапии | 44,78+1,66 | 38,85+1,52 | 38,8+1,48 | 35,8+0,87 | 41,57+1,14 | ||||
| p | p1<0,05 | p2>0,05 | p3>0,05 | p4<0,05 | p5<0,05 | ||||
Динамика показателей СМАД на фоне трехнедельной терапии Грандаксином и ИАПФ отражена в таблице 3.
Таблица 3. Динамика показателей СМАД на фоне терапии Грандаксином и ИАПФ (n=22)
| Показатель | Исходные значения | Значения в динамике | p |
| САД среднее за сутки, мм рт.ст. | 132,26+2,66 | 127,7+3,58 | >0,05 |
| ДАД среднее за сутки, мм рт.ст. | 77,78+1,78 | 75,84+1,95 | >0,05 |
| САД день, мм рт.ст. | 137,62+2,71 | 132,1+3,52 | >0,05 |
| ДАД день, мм рт.ст. | 82,16+1,76 | 79,34+1,79 | >0,05 |
| ВСАД день, мм рт.ст. | 15,5+1,0 | 14,44+0,82 | >0,05 |
| ВДАД день, мм рт.ст. | 11,87+0,57 | 10,68+0,62 | >0,05 |
| ИВ САД день, % | 40,55+6,05 | 30,43+6,83 | >0,05 |
| ИВ ДАД день, % | 25,11+5,0 | 18,52+5,26 | >0,05 |
| ИП САД день, мм рт.ст. | 159,79+35,61 | 127,39+45,2 | >0,05 |
| ИП ДАД день, мм рт.ст. | 69,13+17,65 | 39,63+14,62 | >0,05 |
| САД ночь, мм рт.ст. | 124,11+3,16 | 118,0+3,7 | >0,05 |
| ДАД ночь, мм рт.ст. | 70,24+2,10 | 68,15+2,06 | >0,05 |
| ВСАД ночь, мм рт.ст. | 11,79+0,78 | 11,98+0,83 | >0,05 |
| ВДАД ночь, мм рт.ст. | 8,49+0,49 | 9,71+0,73 | >0,05 |
| ИВ САД ночь, % | 52,31+8,07 | 41,21+8,37 | >0,05 |
| ИВ ДАД ночь, % | 20,68+5,6 | 17,21+4,99 | >0,05 |
| ИП САД ночь, мм рт.ст. | 224,83+50,82 | 180,612+51,05 | >0,05 |
| ИП ДАД ночь, мм рт.ст. | 40,31+13,88 | 39,25+13,39 | >0,05 |
| СИ САД,% | 9,19+1,54 | 10,73+1,37 | >0,05 |
| СИ ДАД, % | 13,82+2,05 | 14,06+1,64 | >0,05 |
| ЧСС среднее за сутки | 80,09+1,56 | 79,55+2,35 | >0,05 |
По данным СМАД (табл. 3), добавление Грандаксина к основному препарату базисной терапии АГ эналаприлу не привело к существенным изменениям основных показателей АД в течение суток.
Вместе с тем, как видно из представленных данных, примененное сочетание препаратов несколько улучшило суточный профиль колебаний АД. Так, до назначения Грандаксина показатель СИ по САД в среднем составлял 9,19%. При этом у 12 пациентов (54,5%) зарегистрировано недостаточное снижение САД в ночное время, у 1 (4,55%) - чрезмерное, а у 1 больного (4,55%) - показатели САД в это время суток превышали его дневные значения. Нормальные показатели СИ по САД отмечались лишь у 8 (36,4%) женщин. Таким образом, у большинства исследуемых имел место неадекватный суточный профиль по САД, что, по данным литературы [26], является характерным для АГ в менопаузальном периоде. На фоне трехнедельной комбинированной терапии, включающей ИАПФ и Грандаксин, увеличилось количество пациентов с оптимальным снижением САД в ночное время (11 человек - 50%) за счет уменьшения числа больных с недостаточным ночным снижением АД (9 человек - 40,9%). Это нашло отражение в величине СИ по САД, который к концу наблюдения в среднем по группе стал в пределах нормальных величин - 10,73%.
Анализ полученных результатов показывает, что, несмотря на то, что средние значения САД и ДАД в процессе наблюдения практически имели лишь тенденцию к изменению (недостоверно снизились на 4,1% и 3,5% в дневное и на 5% и 3% в ночное время, соответственно), добавление Гран-даксина способствовало некоторому уменьшению параметров "нагрузки давлением" (рис. 3,4), хотя полученные изменения были статистически недостоверны. Так, показатели ИВ по САД уменьшились на 25% днем и на 21,3% ночью, а по ДАД -- на 26% и 16,8%, соответственно (рис. 3).
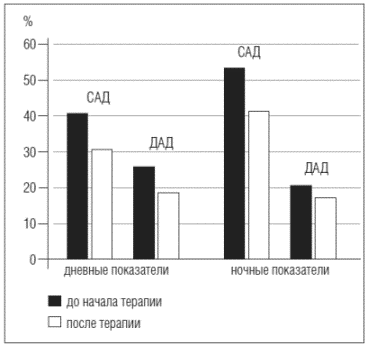
Рис. 3. Динамика индекса времени на фоне терапии Грандаксином и ИАПФ
Что касается величин ИП (рис. 4), то его изменения были преимущественно в дневное время: САД - на 20%, ДАД - на 42,7%, а в период сна - только по данным САД (на 19,7%).
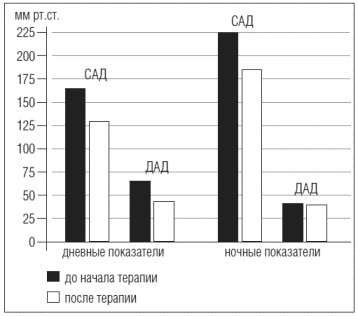
Рис. 4. Динамика индекса площади на фоне терапии Грандаксином и ИАПФ
У двух больных в процессе лечения Грандаксином появились побочные эффекты: усилились чувство тревоги, возбуждение; отмечались нарушения сна в первые двое-трое суток приема препарата. Все вышеперечисленные симптомы исчезли после его отмены.
Резюме
Таким образом, проведенное исследование показало, что у женщин в перименопаузальном периоде ведущими проявлениями психологических нарушений являются вегетативные расстройства и тревожно-фобические симптомы (в сочетании - у 95,45% больных). Причем их детальное выявление в ряде случаев было возможно только при проведении специального психологического тестирования.
Результаты трехнедельной терапии Грандаксином свидетельствуют о его более существенном положительном влиянии на вазомоторные проявления и психоэмоциональное состояние пациенток. В меньшей степени обратному изменению подверглись показатели социальной дезадаптации. Это связано, по-видимому, с преобладающим вегетокорригирующим действием Грандаксина, что было отмечено и другими авторами [1,14,15].
При оценке показателей КЖ по опроснику SF-36 видно, что Грандаксин оказался особо эффективным при купировании изменений психологического здоровья с повышением жизненного тонуса (показатель VT) и улучшением настроения (показатели МН и MCS) у большинства исследуемых. Менее убедительные результаты получены в изменении социальной активности пациенток (показатель SF - уровень взаимоотношения с окружающими) с сохранением проблем эмоционального характера у части исследуемых (показатель RE). Субъективная оценка пациентками своего общего состояния здоровья за время терапии практически не изменилась, хотя большинство женщин отметили меньшее отрицательное влияние физического состояния на свою повседневную деятельность (показатель RF).
Как видно, полученные результаты оценки КЖ согласуются с данными психологического тестирования. Отсутствие существенной динамики показателей, характеризующих социальную активность больных и их физическое состояние, может быть обусловлено небольшим сроком наблюдения.
Снижение уровня тревожности и выраженности вегетативных нарушений при использовании Грандаксина привело к некоторому улучшению суточного профиля по САД. Это является подтверждением мнения авторов [22] о значительном влиянии на уровень АД у женщин в перименопаузальном периоде активации симпатоадреналового отдела вегетативной нервной системы.
Следует обратить внимание на то, что показатели "нагрузки давлением" (ИВ и ИП) больше отражали тенденцию к положительной динамике изменения уровня АД под влиянием Грандаксина, чем средние значения САД и ДАД, что свидетельствует о важной роли СМАД как метода контроля АД на фоне проводимой терапии.
Так как Грандаксин не только уменьшил вегетативные проявления и состояние тревоги, но и оказал некоторое положительное влияние на показатели АД в течение суток, можно говорить о целесообразности его применения в комплексной терапии АГ у женщин в перименопаузальном периоде.
Литература
1. Александровский Ю.А., Аведисова А.С., Павлова М.С. 0 вегетотропном эффекте Грандаксина при лечении невротических расстройств в общесоматической практике. Терапевтический архив. 1998;10:76.
2. Арабидзе Г.Г, Арабидзе Гр. Г. Гипотензивная терапия. Кардиология. 1997;3:88-95.
3. Баранова Е.И. Гипертоническая болезнь у женщин в постменопаузе: особенности клинических проявлений патогенеза и лечения. Автореф. дисс. д.м.н, 1998. Москва. 310 с.
4. Бройтигам В, Кристиан П., Рад М. Психосоматическая медицина. М.: "Гэотар Медицина", 1999.380 с.
5. Быстрова М.М., Бритов А.Н. Артериальная гипертония у женщин в постменопаузе. Кардиология. 1999;5:72-80.
6. Вейн A.M., Артеменко А.Р., Окнин В.Ю., Поморцев И.В. Эффективность Грандаксина в коррекции психовегетативных расстройств. Клиническая медицина. 1999;6:41-45.
7. Вихляева Е.М. Менопаузальный синдром. М. Novo Nordisk. 1999.
8. Елисеева Н.А. Результаты первичной и вторичной профилактики артериальной гипертонии у женщин на одном из промышленных предприятий Москвы. Кардиология. 1982;3:69-72.
9. Заводчикова Е.Н., Стаценко М.Е., Попова А.С. Заболевания сердечно-сосудистой системы в условиях эстрогенного дефицита (методические рекомендации для врачей). Волгоград. 2000.
10. Кабалава Ж.Д., Котовская Ю.В. Артериальная гипертония. М. 2001.
11. Крылов А.А., Решетникова Е.М. Климакс в профилактике терапевта. Терапевтический архив. 1991;4:128-131.
12. Новик А.А. Концепция исследования качества жизни в здравоохранении. Проблемы стандартизации в здравоохранении. 2000;4:95-96.
13. Нанов А.В. Особенности применения психотропных средств у больных гипертонической болезнью. Грандаксин - многогранность применения в клинической практике. Материалы научно-практической конференции. Санкт-Петербург, 1999.
14. Осипенко М.Ф., Хромова ТА, Макарова ТА, Вдовенко Е.Г. Роль Грандаксина в лечении функциональных заболеваний желудочно-кишечного тракта. Терапевтический архив. 2000;10:23-26.
15. Погодин О.К. Терапия Грандаксином невротических расстройств при посткострационном и климактерических синдромах. Грандаксин - многогранность применения в клинической практике. Материалы научно-практической конференции. Санкт-Петербург, 1999:30-32.
16. Сметник В.П. Климактерический синдром / В кн. "Неоперативная гинекология". М.:Медицина, 1996.
17. Ометник В.П., Шестакова И.Г. Менопауза и сердечно-сосудистая система. Терапевтический архив. 1999;10:61-65.
18. Шаповаленко С.А. Комплексная терапия психосоматических расстройств в перименопаузальном периоде. Вестник Российской ассоциации акушеров-гинекологов. 2000.
19. Bulpitt C.J., Fletcher A.E. Quality of live and heart: evalution of therapeutic alternatives. Br. J. Clin. Pract. Symp. Suppl, 1994;73(suppl. 1):18-22.
20. Campo C., Garcia Puig J., Segura J., Maria Alcazar J., Garcia-Robles R., Ruilope L.M. Relationship between severity of essential arterial hypertension and the prevalence hyperuricemia. Med Clin (Barc) 2001 Jun 23;117(3):85-9.
21. Collins P., Rosano G.M.C., Jiano C. et al. Cardiovascular protection by oestrogen - a calcium antagonist effect? Lancet 1993;341:1264-1265.
22. Gannage-Yared M.H., Atallah C., Jambart S. Arterial hypertension, menopause and hormone substitution. J Med Liban 2000 Nov-Dec;48(6):387-91.
23. Hsia J., Simon J.A., Lin F., Applegate W.B., Vogt M.T., Hunninghake D., Carr M. Peripheral arterial disease in randomized trial of estrogen with progestin in women with coronary heart disease: the Heart and Estrogen/Progestin Replacement Study. Circulation 2000 Oct 31 ;102(18):2228-32.
24. Klungel O.H., Boed A., Paes A.H.D. et al. Sex differences in the pharmacological treatment of hypertension: a review of population - based studies. J. Hypertens 1997;15:591-600.
25. Mercuro G., Zoncu S., Cherchi A., Rosano G.M. Can menopause be considered an independent risk factor for cardiovasculardisease? Ital Heart J 2001 Oct;2(10):719-27.
26. Noto R., Rapisarda A., Mirabella C., Landolina C., Meli S., Leanza A., Quartarone D., Rizzo S., Sciacchitano G. Blood pressure variations assessed by continuous 24-hour monitoring in menopausal and climacteric women. Eur Rev Med Pharmacol Sci 2000 Jan-Apr;4(1-2):25-30.
27. Rasavi D. and Cander B. Testing Dutch and French translation of the SF-36 health surly among Belgian angina patients. Journal of Clinical Epidemiology. 1998;51(11):975-983.
28. Shalnova S.A., Deev A.D.,Oganov R., Zhukovsky G.S. Arterial hypertension impact on mortality in Russia. Eur Heart J 1998; in press.
29. Uexk ll, Th.: Psychosomatische Medizin, 4. Aufl. Urban & Schwarzenberg. Munchen 1990.
30. Wassmann S., Baumer A.T., Strehlow K., van Eickels M., Grohe C., Ahlbory K., Rosen R., Bohm M., Nickenig G. Endothelial dysfunction and oxidative stress during estrogen deficiency in spontaneously hypertensive rats. Circulation 2001 Jan 23;103(3):435-41.
