Залаин - монография для специалистов.: Механизм действия
Статьи2. Механизм действия
2.1. Фунгистатический эффект
Фунгицидная активность является следствием прямого взаимодействия сертаконазола с плазматической мембраной грибов, приводящего к образованию в ней воронок и пор и вызывающего массивный выход цитоплазмы и АТФ. Это приводит к увеличению количества нежизнеспособных клеток. Структурное сходство бензотиофена и триптофана облегчает проникновение сертаконазола в плазматическую мембрану грибов. Подавление биосинтеза эргостерола (фунгистатический механизм действия, обусловленный наличием азоловой группировки) проявляется при использовании сертаконазола даже в очень низких концентрациях.
Противогрибковый эффект сертаконазола и многих других противогрибковых средств базируется на наличии в сложной структуре клеточной мембраны грибов ригидной дисковидной молекулы эргостерола. Это соединение регулирует внутреннюю "подвижность" или "текучесть" мембраны. Любой дефицит эргостерола вызывает нарушения устойчивости и плотности мембраны.
Эргостерол образуется в результате биосинтеза из более простых веществ через цепь реакций, которая включает синтез промежуточного вещества ланостерола. Ключевую роль в превращении ланостерола в эргостерол играет фермент 14-α-деметилаза (рис. 2).
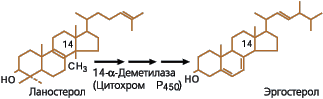 |
Рисунок 2. Превращение ланостерола в эргостерол через ряд промежуточных этапов с удалением метильной группы у С14 14-α-деметилазой |
14-α-деметилаза входит в группу ферментов, известных под общим названием цитохром Р450. Все ферменты группы цитохрома Р450 содержат гематиновый железосодержащий пигмент. Считается, что сертаконазол, подобно другим противогрибковым средствам из группы азолов, связывается с атомом железа гематиновой группы и инактивирует 14-α-деметилазу. Это приводит к нарушению синтеза эргостерола и накоплению ланостерола и других стеролов. Их включение вместо эргостерола в мембрану значительно нарушает структуру и функцию клеточной мембраны грибов (рис. 3).
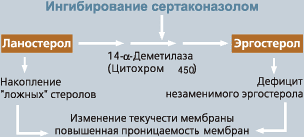 |
Рисунок 3. Изменение свойств мембраны, вызываемое включением "ложных" стеролов вместо эргостерола |
Было показано, что угнетающее действие сертаконазола на синтез эргостерола у Candida albicans является дозозависимым [2]. Сертаконазола нитрат добавляли в культуру Candida albicans в концентрациях от 2,0 × 10-7 до 7,07 × 10-8 моль/л через четыре часа после инокуляции. Через 24 часа культуры подвергали изучению. Эргостерол экстрагировали с использованием липофильного растворителя, а его концентрацию определяли методом жидкостной хроматографии высокого давления.
Результаты представлены в таблице 2 и на рисунке 4.
Таблица 2. Зависимое от концентрации угнетение сертаконазолом синтеза эргостерола у Candida albicans [2]
| Концентрация сертаконазола (моль/л) | Концентрация эргостерола в сухом мицелии (нг/мг) | Угнетение синтеза эргостерола (в % по сравнению с контролем) |
| 2.00 × 10-7 | 57.93±16,38 | 86.59 |
| 1.40 × 10-7 | 130,66±48,03 | 69.76 |
| 1.00 × 10-7 | 28,91±68,97 | 34.75 |
| 7.07 × 10-8 | 357,98±115,92 | 17.15 |
| 0 | 432,06±81,73 | 0 |
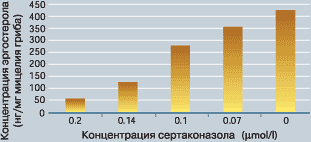 |
Рисунок 4. Концентрация эргостерола в сухом мицелии после культивирования в присутствии прогрессивно снижающихся концентраций сертаконазола [2] Зависимое от концентрации подавление сертаконазолом синтеза эргостерола |
2.2. Специфичность действия сертаконазола на синтез эргостерола
14-α-деметилаза является монооксигеназой или гидроксилазой, т.е. фермент переносит один атом кислорода из молекулы О2 на органическую молекулу, которая становится пригодной для других реакций. Этот тип реакции весьма част в метаболических реакциях, и поэтому обычно имеется большое количество монооксигеназ. Наиболее важной группой является группа цитохрома Р450, которая состоит из нескольких сотен очень схожих отдельных ферментов, хотя каждый из них имеет специфичность в отношении определенного субстрата. Помимо 14-α-деметилазы эта группа включает также некоторые ферменты, которые играют ключевую роль в синтезе половых гормонов и гормонов коры надпочечников человека. Одним из этих ферментов является 17,20-десмолаза, которая участвует в биосинтезе тестостерона, превращая 17-α-гидроксипрогестерон в андростерон за счет отщепления боковой цепи (рис. 5).
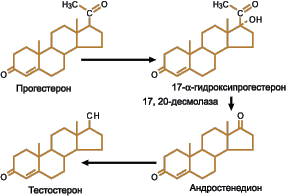 |
Рисунок 5. Превращение у человека 17-α-гидроксипрогестерона в андростендион под действием 17,20-десмолазы |
При использовании сертаконазола важно знать, может ли препарат, помимо ингибирования 14-α-деметилазы грибов, изменять активность какого-либо другого фермента млекопитающих, например, 17,20-десмолазы.
Ингибирование 17,20-десмолазы является нежелательным побочным эффектом, поскольку любой дефицит этого фермента вызывает нарушения половой функции у мужчин [3, 4]. Хотя эти соображения более важны в случае лечения противогрибковыми средствами, применяемыми системно, противогрибковые препараты для местного использования также должны иметь максимальную избирательность действия в отношении 14-α-деметилазы грибов.
Для изучения сертаконазола в этом аспекте была исследована активность 17,20-десмолазы, выделенной из тестикул крыс, по действию на 17-α-гидроксипрогестерон в присутствии сер-таконазола, эконазола, кетоконазола и бифоназола в различных концентрациях. Снижение активности фермента на 50% было выявлено в присутствии исследованных веществ в концентрациях, представленных в таблице 3 и на рис. 6.
Таблица 3. Влияние сертаконазола на 17,20-десмолазу является минимальным
| Сертаконазол | 160 нмоль/л |
| Эконазол: | 120 нмоль/л |
| Кетоконазол: | 30 нмоль/л |
| Бифоназол: | 6 нмоль/л |
Таким образом, из всех изученных противогрибковых средств сертаконазол является препаратом с наименьшим ингибирующим действием на 17,20-десмолазу [5].
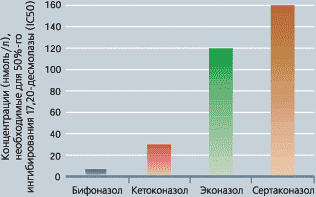 |
Рисунок 6. Ингибирование 17,20-десмолазы различными противогрибковыми средствами |
2.3. Фунгицидный эффект
Фунгицидная активность сертаконазола связана с его прямым влиянием на плазматическую мембрану грибов. Это показано экспериментально с помощью измерения внеклеточной концентрации АТФ (или К+), возрастание которой (параллельно с уменьшением внутриклеточной концентрации АТФ) совпадает с быстрым снижением числа жизнеспособных грибов.
В течение метаболических процессов в грибах, особенно в течение усвоения пищи, органические вещества распадаются на более мелкие фрагменты с помощью гидролитических реакций, катализируемых ферментами, которые грибы синтезируют и секретируют в окружающую среду (экзоферменты). Белки окружающей ткани хозяина расщепляются протеазами с образованием пептидов и свободных аминокислот, которые затем поглощаются микроорганизмом. Среди этих аминокислот имеется триптофан, аминокислота с ароматической структурой.
Транспорт или баланс аминокислот играет важную роль в изменениях морфологии клетки гриба (специфичен для перехода дрожжи-мицелий). Эти изменения также важны для успешного существования гриба в организме хозяина [6, 7].
Конкурентный антагонизм с триптофаном, о котором сообщалось при исследованиях на различных ферментах, показывает, что бензо-(β)тиофеновая группировка в молекуле сертаконазола сходна по структуре и имитирует ин-дольное кольцо триптофана [8].
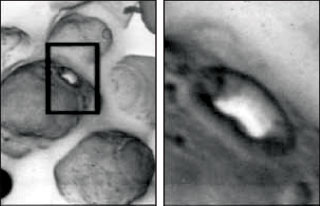 |
Изображения 2 и 3. Влияние сертаконазола на Candida albicans, наблюдаемое при сканирующей электронной микроскопии |
Из-за этого структурного сходства и липофильности указанной группировки сертаконазол легче, чем триптофан, проникает в плазматическую мембрану грибов. После вхождения в мембрану соединение вследствие высокой способности селективно взаимодействовать с компонентами клеточной мембраны вызывает образование в ней воронок, каналов и пор, видимых при электронной микроскопии. Это приводит к массивному выходу электролитов (в основном АТФ) и других жизненно важных веществ из грибковых клеток.
Разрушение плазматической мембраны вызывает деструкцию скелетона клетки и гибель ее содержимого в результате лизиса органелл [9].
Действие бензотиофена может объяснять фунгицидную активность сертаконазола в низких концентрациях, отличающую препарат от других производных имидазола, а также его эффективность в отношении штаммов грибов с перекрестной резистентностью к имидазолам. Основной эффект последних обусловлен воздействием на биосинтез эргостерола и поэтому приводит лишь к подавлению роста грибов.
Фунгистатический механизм действия, связанный с наличием азоловой группировки, выявляется у сертаконазола в концентрациях, значительно меньших минимальных ингибирующих концентраций, хотя "in vivo" превалирует фунгицидное действие препарата, обусловленное его действием на клеточную мембрану грибов [2].
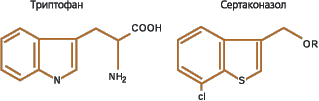 |
Рисунок 7. Структурное сходство между бензотиофеном и триптофаном |
Это дополнительное и специфическое действие сертаконазола выявляется в разных ситуациях. В частности, препарат оказывает прямое токсическое влияние на клеточную мембрану грибковых клеток всего через 10 минут после начала воздействия и вызывает выход из них внутриклеточных компонентов. Так, после 10-минутного воздействия сертаконазола в возрастающих концентрациях на Candida albicans отмечалось отчетливое увеличение концентрации аденозина трифосфата (АТФ) во внеклеточной жидкости (рис. 8).
Изменение проницаемости клеточной мембраны грибов с последующим выделением клеточных компонентов вызывает гибель грибковых клеток, что обусловливает фунгицидное действие сертаконазола. Это было доказано при 10-минутном воздействии сертаконазола и кетоконазола в возрастающих концентрациях на культуры Candida albicans (рис. 9). После ре-инокуляции в соответствующем разведении после 48-часового периода инкубации определяли количество жизнеспособных колоний грибов. До воздействия препаратов их количество в чашечках Петри варьировало от 100 до 300 (рис. 9).
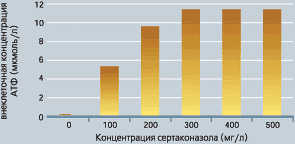 |
Рисунок 8. Демонстрация прямого токсического действия сертаконазола в высоких концентрациях на мембрану Candida albicans, обусловливающего высвобождение АТФ [10]. |
Сертаконазол: прямое токсическое действие на клеточную мембрану гриба. Высвобождение АТФ вследствие изменения проницаемости мембраны.
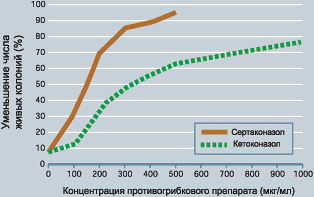 |
Рисунок 9. Влияние сертаконазола и кетоконазола на жизнеспособность колоний Candida albicans [10]. |
Далее: 3. Токсикология
Комментарии
ПРАКТИКА ПЕДИАТРА
