Натуропатические средства в профилактике острых респираторных заболеваний у детей раннего возраста
СтатьиОпубликовано в журнале:
«РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ» 2009, том 17, № 1 С. 1-8
Т.В. Казюкова1, Г.А. Самсыгина1, Т.А. Дудина1, Т.А. Бимбасова1, Н.Н. Шевченко2, В.Д. Русакова2, И.В Панкратов3
1ГОУ ВПО «РГМУ Росздрава»,
2ГУЗ«Морозовская детская городская клиническая больница»,
3ГУЗ«Детская городская поликлиника №73», г. Москва
Заболеваемость острыми респираторными инфекциями (ОРИ) и гриппом среди детей, особенно раннего возраста, в периоды сезонных эпидподъемов заболеваемости остается высокой [1,2]. Согласно данным Роспотребнадзора, в январе-феврале 2008 г., заболеваемость ОРИ составила 3 465 200 случаев, гриппом - 67300 [1]. При этом удельный вес гриппа в 2008 г. не превысил 0,3% (цит. по Интерфаксу, от 15.04.2008). В Москве за январь 2008 г. число детей, заболевших ОРИ, составило 28 966, причем на детей до 2 лет пришелся 21% всех случаев заболевания, на детей 3-6 лет -48%, на школьников 7-14 лет-31% [1], т.е. чаще заболевали дети младшей возрастной группы.
Острые респираторные заболевания (ОРЗ) составляют почти 90% всей инфекционной патологии у детей [2,3]. В этиологии ОРЗ как у детей, так и у взрослых доминируют вирусы (парагриппа 1 и 3 типов, рино-синцитиальный вирус, риновирусы и др.), на долю которых приходится свыше 75% всех случаев острых респираторно-вирусных инфекций (ОРВИ). Доля различных бактерий в этиологии ОРЗ составляет 20-23%, остальные 1-2% представлены внутриклеточными возбудителями, простейшими, грибами и их ассоциациями [4].
Следует отметить, что у детей, особенно грудного и раннего возраста, существует высокий риск развития осложнений при ОРВИ любой этиологии [4-6]. Вирусы, обладая иммуносупрессивным действием, вызывают более чем у 60% переболевших детей т.н. «синдром послевирусной астении», что проявляется снижением активности, усталостью, эмоциональными и психическими расстройствами. Высокая заболеваемость детей ОРИ и наносимый ими ущерб как здоровью конкретного ребенка, так и обществу в целом, делает разработку и внедрение в практику действенных способов профилактики ОРИ приоритетными задачами современной педиатрии [4,7].
Вместе с тем, пожалуй, только в отношении вирусов гриппа существует эффективная иммунопрофилактика, способная защитить около 80% здоровых детей и взрослых [1,8]. Причем известно, что требуется не менее 4 мес, чтобы выработать вакцину в нужном количестве и полном соответствии актуальному для данного эпидсезона штамму вируса гриппа [1,8,9]. В этот период для защиты детей и взрослых необходимы средства неспецифической профилактики гриппа и ОРВИ. Однако для профилактики ОРВИ у новорожденных и грудных детей их практически нет, а перечень для использования у детей раннего возраста весьма ограничен (причем ингибиторы нейраминидазы разрешены с 1 года, блокаторы М2-каналов, производные адамантана - с 3 лет, арбидол - с 7 лет); что и определяет использование с этой целью неспецифических лекарственных средств [4,10-13]. Кроме того, ОРИ остаются и сегодня практически неуправляемыми инфекциями и радикальных средств как для их профилактики, так и лечения, на сегодня не существует. Ситуацию осложняет к тому же наблюдающаяся в последнее время резистентность ряда респираторных вирусов к химиопрепаратам вследствие не всегда адекватной (нерациональной) фармакотерапии [11-13]. В связи с этим в последние годы всё большее внимание специалистов привлекает возможность применения для этой цели натуропатических препаратов, поскольку они не имеют противопоказаний и могут назначаться даже новорожденным детям. Отсутствие побочных эффектов и возможность их длительного приема на фоне терапии сопутствующей патологии делают их весьма привлекательными с точки зрения практического использования.
Тем интереснее оказалась работа Ferly JP, et al. [14], в которой сообщалось об эффективном профилактическом воздействии натуропатического препарата, полученного из автолизата печени и сердца барбарийской утки (Anas Barbariae), разведенного и динамизированного по Корсакову в 200 раз. Он представляет собой гомеопатические гранулы (К200), выпускаемые под названием Оциллококцинум (производитель «Лаборатории Буарон», Франция), зарегистрирован в установленном порядке (рег. удостоверение П №014236/ 01-2002) и разрешен к применению на территории РФ у людей всех возрастных групп В России высокая противовирусная активность оциллококцинума была подтверждена Сельковой Е.П. и соавт. [15] в плацебо-контролируемом исследовании, проведенном в эпидсезон 2007 г у 227 юношей и девушек (16-22 лет), не привитых против гриппа
Уместно отметить, что публикаций в научных медицинских журналах, посвященных исследованию эффективности гомеопатических препаратов, крайне недостаточно [14-16]. При этом практически нет работ, в которых обсуждались бы результаты контролируемых исследований по изучению превентивной эффективности оциллококцинума в отношении возбудителей ОРВИ у детей младшей возрастной группы.
Цель работы: на основании клинико-эпидемиологических данных оценить эффективность и обосновать возможность применения оциллококцинума для неспецифической профилактики ОРВИ и гриппа у детей грудного и раннего возраста, изучить возможные нежелательные побочные эффекты и осложнения при его использовании.
Дизайн работы: открытое плацебо-контролируемое рандомизированное клинико-эпидемиологическое наблюдение по изучению эффективности препарата оциллококцинум в качестве средства неспецифической профилактики ОРВИ и гриппа в эпидсезон 2007/2008 у детей грудного и раннего возраста.
Пациенты и методы
Оценка профилактической эффективности оциллококцинума в отношении респираторно-вирусных инфекций проведена в условиях контролируемых клинико-эпидемиологических наблюдений у детей грудного и раннего возраста, в полном соответствии с «Хельсинкской декларацией» (WMA, 1964) и «Декларацией о политике в области обеспечения прав пациента в Европе» (WHO/EURO, 1994). С целью минимизации возможных систематических ошибок, связанных с отбором испытуемых лиц, была применена тактика популяционного исследования случай-контроль, где основная и контрольные группы были отобраны по одним и тем же критериям. В клиническом наблюдениии участвовало 109 детей.
Критерии включения в клиническое наблюдение (КН):
- - дети в возрасте от 3,5 мес до 4,5 лет, без клинических признаков ОРИ и не привитые против гриппа, не имеющие сопутствующей тяжелой патологии (иммунодефицитные состояния, врожденные пороки развития, локализованные гнойные очаги инфекции, тромбоцито-, нейтропении, анемии 2-3 ст.) или обострения хронических болезней,
-понимание родителями целей, задач и хода наблюдения, а также их добровольное информированное согласие на участие в КН.
Поскольку в состав препарата качестве наполнителей входят лактоза и сахароза, особое внимание уделялось детям с лактазной недостаточностью, а также пациентам с атопическими заболеваниями, аллергическими реакциями в анамнезе
Необходимо отметить, что в наших КН дети грудного возраста составляли не менее 1/3: 28 детей из 109 наблюдаемых, - а дети второго года жизни составили 50%.
Критерий исключения: применение в течение КН других противовирусных профилактических средств.
Дети, включенные в КН, находились на обследовании в ГУЗ «Морозовская детская клиническая больница» (Набор детей в группы проводился по мере поступления детей на стационарное обследование) Департамента здравоохранения г. Москвы (n=86) или наблюдались амбулаторно в ГУЗ «Детская городская поликлиника №73» (Набор детей в группы проводился одномоментно, в середине января 2008 г.) ЮЗАО г. Москвы (n=23). Методом случайной рандомизации были сформированы 2 равноценные группы (табл. 1).
Таблица 1. Характеристика детей, включенных в клиническое наблюдение (опытная и контрольная группы) |
||
| Характеристика пациентов | Основная (опытная) группа (получали оциллококцинум) |
Группа сравнения (плацебо-контроль) |
| Мальчики | 27 (48,2%) |
26 (49%) |
| Девочки | 29(51,8%) |
27(51%) |
| Возраст | 19,2±7,3 мес |
18,7±6,8 мес |
| Дети с лактазной недостаточностью | 11 (19,6%) |
7(13,2%) |
| Аллергия/атопия в анамнезе | 17(30,4%) |
17(32,1%) |
| Всего | 56 |
53 |
Дети основной (опытной) группы получали оциллококцинум перорально по 1 дозе (1 туба), разведенной в 5,0 мл воды, 1 раз в неделю в течение 3-х недель; дети группы сравнения - плацебо по той же схеме. Детям, находившимся на стационарном обследовании, препараты давались медицинским персоналом, детям, наблюдавшимся в амбулаторных условиях, - родителями (препарат выдавался на руки с рекомендациями по режиму дозирования), что обеспечивало проведение беспрерывной профилактики с целью достижения 100% комплаентности пациентов.
Наблюдение проводилось в период эпидподъема респираторно-вирусных инфекций 2007/2008 (с 20.12.07 по 31.03.08). При этом для определения начала эпидемии использовались официальные источники информации (Федеральное Агентство по социальному развитию и здравоохранению, Роспотребнадзор), что позволяло еженедельно отслеживать эволюцию заболеваемости респираторными и гриппозными инфекциями на региональном и национальном уровне. Необходимо отметить, что в 72,5% случаев набор пациентов для проведения КН пришелся на пик эпидемии (с 15.01.08 по 10.03.08).
Дизайн КН включал клинико-эпидемиологический мониторинг:
«0» визит - первичный осмотр (1-я доза препарата),
«1» визит-через 7 дней с момента назначения препарата (2-я доза),
«2» визит - через 14 дней после начала терапии (3-я доза),
«3» визит и
«4» визит -соответственно через 21 и 28 дней с момента первичного осмотра и приема 1-й дозы препарата.
Состояние детей оценивали при клиническом осмотре, на основании симптоматики со стороны отдельных органов и систем, выраженной математически по 4-балльной шкале: 0 - отсутствие симптома (норма), 1 - минимальное проявление, 2 - умеренно выраженная и 4 - максимальная интенсивность того или иного симптома.
В случае появления первых симптомов ОРИ дети основной группы переводились на лечебный режим приема препарата (1 доза 3 раза в день с интервалом 6 час, затем - по 1 дозе утром и вечером в течение 1-3 дней), при этом не исключалась возможность использования других лекарственных средств. Дети контрольной группы в случае заболевания ОРВИ применяли жаропонижающие, антигистаминные препараты, при необходимости - антибактериальные средства. Все данные фиксировались в индивидуальных картах наблюдения.
Полностью завершили наблюдение 104 ребенка (95,4%): 54 (96,4%) - в основной группе и 49 (92,5%) -из группы сравнения. Из КН выбыло 5 детей: у одного из этих детей, страдавшего атопическим дерматитом (стадия ремиссии), отмечалось обострение кожных проявлений заболевания. Еще 4 ребенка выбыли после 3-го визита из-за смены места жительства, однако данные этих детей, полученные на начальном этапе КН, были подвергнуты статистическому анализу.
Статистическая обработка результатов проведена с применением ПО Microsoft Office Excel и Statistica. Параметрические показатели представлены в виде средних значений (М) и стандартных отклонений (±m). Достоверность различий оценивали по t-критерию Стьюдента и с помощью непараметрического критерия Фишера; различия считались достоверными при р≤0,05. Для создания интервального образа модели и прогноза событийной вероятности применялась полиномиальная регрессия (на графике изображены линиями трендов); достоверность точности и надежности приближения (аппроксимации) считали высокой при значениях R2≥0,85 [17].
Результаты и их обсуждение
Соответственно цели наблюдения, нами проанализирована заболеваемость ОРВИ и гриппом в группе детей, получавших оциллококцинум, и группе плацебо (табл. 2).
Таблица 2. Заболеваемость ОРИ в группах детей грудного и раннего возраста (основная и контрольная группы) | |||
| Группы детей | Число наблюдаемых n | Общее число заболевших ОРИ | |
n | % | ||
| Основная (опытная) группа | 56 | 6 | 10,7*** |
| Группа сравнения (плацебо-контроль) | 53 | 11 | 20,8 |
| Примечание: *** - р<0,001 | |||
Как видно из таблицы 2, на фоне 3х-недельного приема оциллококцинума число заболевших ОРВИ составило 10,7% (6) детей, в то время как в группе плацебо за период проведения КН заболело 20,8% (11) детей (р<0,001). Т.о., в период эпидподъема респираторно-вирусных заболеваний терапия оциллококцинумом позволяет защитить от респираторной инфекции 89,3% детей раннего возраста.
Нами выявлены различия в сроках возникновения ОРИ у детей основной и контрольной групп (рис. 1).
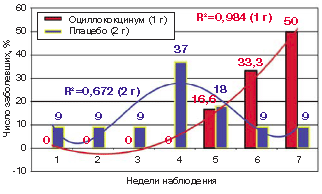
Рис. 1. Сроки возникновения острых респираторно-вирусных заболеваний у детей на протяжении периода наблюдения:
1 группа - основная (принимали оциллококцинум),
2 группа - плацебо-контроль (R2 - достоверность аппроксимации).
Как видно из рисунка, в основной группе на фоне приема оциллококцинума не заболел никто из детей, первый случай заболевания ОРИ зафиксирован на 5-й неделе наблюдения (через 2 нед после окончания приема препарата), два случая - на 6-й нед, три - на 7-й нед наблюдения, соответственно через 3 нед и через 4 нед после завершения терапии. Важно отметить, что событийная вероятность подобного развития «сценария», в действительности, чрезвычайно высока (R2=0,984, p<0,001), что, во-первых, подтверждает данные других исследователей о необходимости приема препарата на всем протяжении эпидсезона, а, во-вторых, свидетельствует, весьма вероятно, о сохраняющейся его противовирусной активности, как минимум, в течение 10-14 дней после окончания терапии (однако такое заключение можно сделать только после проведения сравнительных контролируемых вирусологических исследований).
Из представленных данных также следует, что у детей группы плацебо кривая заболеваемости (линия тренда) подчинена общим физическим закономерностям, хотя сама вероятность подобного развития событий недостоверна (R2=0,672, p>0,5).
Таким образом, сравнительная оценка профилактической эффективности препарата оциллококцинум (опытная группа) по отношению к группе плацебо-контроля, показывает, что в основной группе дети были достоверно больше защищены от возникновения ОРВИ В период эпидподъема респираторных инфекций и гриппа сезона 2007/2008 из числа детей, получавших профилактическую терапию гомеопатическим препаратом оциллококцинум, заболели ОРВИ 10,7% детей раннего возраста, в то время как в группе плацебо-контроля заболеваемость составила 20,8%.
Следует особо отметить, что всем заболевшим детям в обеих исследуемых группах был выставлен диагноз ОРВИ, заболеваний гриппом зафиксировано не было.
Нам представлялось важным проанализировать тяжесть и длительность течения респираторно-вирусных инфекций у заболевших детей опытной и контрольной групп. Обнаружено, что у пациентов основной группы, получавших оциллококцинум, заболевания чаще протекали в легкой (абортивной) форме, в то время как у детей, получавших плацебо, картина была прямо противоположной (табл. 3).
Таблица 3. Оценка тяжести острых респираторно-вирусных инфекций у детей опытной и контрольной групп |
|||||
| Группы детей | Общее число заболевших n (%) |
Тяжелые формы ОРВИ |
Легкие формы ОРВИ |
||
Число больных |
|||||
n |
% |
n |
% |
||
| Основная (опытная) группа | 6(10,7) |
1 |
16,7*** |
5 |
83,3*** |
| Группа сравнения (плацебо-контроль) | 11 (20,8) |
10 |
90,9 |
1 |
9,1 |
| Примечание: *** - p<0,001 в сравнении показателей между исследуемыми группами | |||||
Уместно подчеркнуть, что у 6 заболевших детей основной группы длительность течения ОРВИ составила в среднем 3,3±0,7 дня, причем у них наблюдались только катаральные проявления в носоглотке на фоне субфебрильной температуры, которые у 5 из них купировались в течение 48 час, у 1 - в течение 5 дней приема оциллококцинума по лечебной схеме. Тогда как в группе плацебо-контроля длительность ОРИ составила 10,8±1,7 дня, что было обусловлено развитием осложнений (отит, бронхит) и требовало назначения комплексной терапии с включением антибактериальных, антигистаминных, жаропонижающих, симптоматических препаратов. Это нанесло ощутимый вред здоровью детей и увеличило материальные затраты на лечение в семьях пациентов контрольной группы, а также было сопряжено с моральными страданиями этих маленьких детей и их родителей.
Таким образом, длительность течения ОРВИ при использовании оциллококцинума достоверно меньше, чем в группе плацебо (3,3±0,7 и 10,7±1,7 дня соответственно, p<0,01).
Оценка безопасности препарата Оциллококцинум
Как уже сказано выше, в основной группе у одного ребенка с атопическим дерматитом (в стадии ремиссии) через 40-50 мин после приема 2-й дозы оциллококцинума наблюдалось обострение кожного процесса (появление гиперемии с элементами строфулюса на щеках, руках, ягодицах, сильного зуда), что, по всей вероятности, можно связать с применением препарата. В остальных случаях не было зафиксировано нежелательных явлений и аллергических реакций. Препарат пациентами переносился хорошо.
Поскольку в состав препарата входят лактоза и сахароза, а среди 109 пациентов, участвовавших в данном КН, было 18 детей (16,5%) с лактазной недостаточностью (степень расщепления лактозы в пределах 50-75%), мы опасались появления у них диарейного синдрома. Однако ни в одном случае не было зарегистрировано побочных эффектов или осложнений со стороны желудочно-кишечного тракта.
Заключение
Гомеопатический препарат оциллококцинум («Лаборатории Буарон», Франция) прошел постмаркетинговое плацебо-контролируемое рандомизированное клинико-эпидемиологическое исследование на репрезентативной и статистически достоверной группе пациентов по изучению его эффективности как средства неспецифической профилактики ОРВИ и гриппа у детей с целью расширения показаний к его применению. Комплаентность пациентов, включенных в КН, составила 95,4%. В ходе проведенного КН по изучению эффективности препарата оциллококцинум как средства неспецифической профилактики ОРИ у не привитых против гриппа детей грудного и раннего возраста было выявлено, что в период эпидподъема респираторно-вирусных инфекций в опытной группе (получали препарат) происходит снижение заболеваемости ОРИ по сравнению с группой плацебо-контроля в 1,9 раза.
Прием препарата оциллококцинум позволил эффективно и безопасно проводить профилактические мероприятия у детей младшей возрастной группы (от 3,5 мес до 4,5 лет). В ходе КН препарат показал высокое профилактическое действие (89,3%) в отношении респираторных вирусов и гриппа в период эпидподъема инфекционной заболеваемости. Было выявлено, что препарат не только высокоэффективен, но и безопасен, и может применяться, в том числе, у детей с лактазной недостаточностью Вероятность развития нежелательных явлений и аллергических реакций невелика (в 1,7% случаев), но требует острожного назначения у детей с атопическими заболеваниями.
Профилактический курс оциллококцинумом (1 доза 1 раз в неделю) у детей раннего возраста следует проводить на протяжении всего эпидсезона. При появлении первых симптомов ОРВИ необходим прием препарата в лечебных дозировках (1 доза 3 раза в день с интервалом 6 час, затем - по 1 дозе утром и вечером в течение 1-3 дней).
В заключение целесообразно подчеркнуть, что, хотя механизмы противовирусного действия оциллококцинума до конца не расшифрованы, использование его с целью профилактики и лечения респираторно-вирусных инфекций у детей грудного и раннего возраста следует признать обоснованным, эффективным и безопасным, что позволяет рекомендовать оциллококцинум в качестве средства превентивной защиты данной когорты детского населения от ОРИ.
Литература
- Заболеваемость гриппом и ОРВИ в РФ. Еженедельный информационный бюллетень Роспотребнадзора. http://www.rospotrebnadzorru/sanepid
- Заболеваемость населения Российской Федерации. Здоровье населения и среда обитания, 2008. http://www.bibliomedru/publications
- Глобальный план ВОЗ по подготовке к борьбе с гриппом. WHO/CDS/CSR/GIP/2005.5
- Острые респираторные заболевания у детей: лечение и профилактика. М.: Союз педиатров России, 2002.
- Коровина Н.А., Заплатников А.Л. Острые респираторные вирусные инфекции в амбулаторной практике врача-педиатра М.: Медпрактика, 2004/
- Nicholson K, WoodJM, Zambon M. Influenza. Lancet, 2003; 362: 1733-1745.
- Prevention and control of influenza. Recommendations of the ACIP. Morbid Mortal Wkly Rep, 2004; 53: RR-6.
- Таточенко В.К. Безопасность вакцинации: современные данные. Вакцинация, 2007; 11:6-7.
- Колбин А.С. Комментарий на статью Белоусова Д.Ю. «Экономический анализ вакцинопрофилактики гриппа у детей и подростков». Пед. фармакология, 2007; 4(3): 22-24.
- Дарманян А.С. Эффективность и безопасность ингибитора нейраминидазы осельтамира у детей. Пед фармакология, 2007; 4(3): 44-46.
- Намазова Л.С., ВолковК.С., Торшхоева Р.М., Алекссева А.А. Новые возможности иммуномодулирующей терапии часто болеющих детей. Пед. фармакология, 2008; 5(2): 9-13.
- Заплатников А.Л. Иммунопрофилактика и иммунотерапия острых респираторных инфекций у детей. Леч. врач, 2006; 9:50-56.
- Киселев О. И. и др. Антивирусные препараты для лечения гриппа и ОРВИ. СПб.: ИД «Питер», 2000.
- Ferly JP, Zmiroux D, D'Ademare, et al. Контролируемая клиническая оценка гомеопатического препарата для лечения гриппозных состояний. Brit J Clin Pharmacol, 1989; 27:329-335.
- Reilly DT, Taylor MA, McSharry C, Aitchison T. Is homeopathy a placebo response? Controlled trial of homeopathic potency, with pollen in hay fever as model. Lancet, 1986; 2(8512): 881-886.
- Селькова Е.П., Семененко Т.А., Ленева И А. и др. Натуропатические средства в лечении и профилактике гриппа и ОРВИ. Леч. врач, 2007; 2:76-77.
- Подружко А.А., Подружко А.С. Интервальное представление полиномиальных регрессий. Серия: Труды Института системного анализа РАН. М., 2003.


