Эффективность и перспективы применения нифуратела в терапии лямблиоза у детей
Статьи Опубликовано в журнале:
« Вопросы современной педиатрии » 2005, Tом 4, №5. С.Ю.Конаныхина1, О.А.Сердюк2
1 НИИ вакцин и сывороток им. И.И.Мечникова РАМН, Москва;
2 Институт диагностики и профилактики социально значимых заболеваний Министерства образования и науки, Москва
Оценено воздействие на микробиоценоз кишечника препарата нифурател у 38 детей с лямблиозной инвазией на основании результатов паразитологического (обнаружение цист лямблий), иммунологического (выявление антигена и секреторного IgA) и микробиологического методов исследования проб фекалий. Результаты исследования показали высокую клиническую и паразитологическую эффективность препарата: антиген лямблий не определяется уже после 4-го дня, а цисты лямблий в пробах фекалий не обнаруживаются с 3 дня терапии. Выявлено, что нифурател оказывает санирующий эффект в отношении представителей условно-патогенной микрофлоры и не подавляет облигатную флору кишечника.
Ключевые слова: дети, лямблиоз, лечение, нифурател, антиген лямблий в фекалиях, секреторный IgA в фекалиях, дисбиоз кишечника
Заболевания желудочно-кишечного тракта занимают значительное место в патологии человека, особенно детей. Они возникают не только в результате нарушения режима питания, попадания в организм бактерий кишечной группы, но в ряде случаев вызываются кишечными простейшими. Одним из самых распространенных и часто встречающихся кишечных протозоозов является лямблиоз – заболевание, вызываемое присутствием в полости тонкого кишечника чело- века паразитических жгутиконосцев рода Lamblia – Lamblia intestinalis (Giardia lamblia).
Лямблиоз остается актуальной проблемой здравоохранения многих стран мира. По данным экспертов ВОЗ, ежегодно лямблиозом заражается около 200 млн человек, из них клинически заболевание проявляется у 500 тыс. человек (0,25%).
Пораженность взрослого населения, выявленная при массовых обследованиях, составляет в среднем 2%, а у детей достигает 7–15% (США – 10–20%, Италия – 5,2%, Франция – 5,8%, Польша – 8%, Бразилия – 18%) [1]. На территории Российской Федерации, по данным официальной отчетности, регистрируется около 150 тыс. случаев в год, при этом 80% из них приходится на детей до 14 лет [2].
Заражение происходит только перорально, при проглатывании зрелых инвазионных цист (заражающая доза – 10–100 цист); механизм передачи – фекально-оральный, пути распространения возбудителя – контактный, пищевой, водный. Источником инвазии служат человек или животные, однако ведущая роль принадлежит человеку [3].
Как и у многих простейших, жизненный цикл лямблий включает существование организма в вегетативной стадии (трофозоит) и покоящейся, цистной. Наиболее важна активная, размножающаяся вегетативная стадия, особенности морфологии и физиологии которой способствуют специализации этих паразитов к обитанию на поверхности щеточной каймы эпителия тонкого кишечника человека – важнейшем участке его пищеварительной системы. Наибольшее количество трофозоитов обнаруживается на уровне верхних петель (≈2,5 м длины) тонкого кишечника. Поселяясь на щеточной кайме и отсасывая продукты гидролиза, лямблии воздействуют на процесс мембранного пищеварения и могут явиться причиной изменения функционального состояния эпителия ворсинок. Это выражается в увеличении количества митозов в криптах кишечного эпителия и снижении скорости всасывания липидов [4]. В 50% случаев происходит нарушение всасывания Д-ксилозы, цианокобаламина и синтеза ферментов – инвертазы, лактазы. Однако эти изменения оказываются неблагоприятными для самих паразитов и приводят к снижению их численности.
До 1970-х гг. патогенность лямблий ставилась под сомнение, что было связано с отсутствием отчетливых клинических симптомов заболевания и характерных паталогоанатомических изменений пораженных органов при лямблиозе, а также с широким распространением случаев носительства паразитов. С 1981 г. Lamblia intestinalis отнесена к патогенным кишечным простейшим (ВОЗ, 1981) [5].
Особенностью лямблиозной инвазии является разнообразие клинических проявлений, степень выраженности которых зависит от вирулентности штаммов, интенсивности инвазии, возраста и состояния иммунной системы хозяина.
Клинический диагноз лямблиоза представляет сложную проблему, что можно объяснить полиморфизмом и неспецифичностью симптоматики. При этом часто не учитываются факторы, которые, независимо от присутствия лямблий, могут быть основной причиной выявленных патологических расстройств в организме (функциональные и воспалительные изменения верхних отделов желудочно-кишечного тракта, хронические субклинически протекающие респираторные заболевания, гельминтозы). Все это приводит к переоценке патогенного значения лямблий [6].
В настоящее время выделяют три клинические формы лямблиозной инвазии – острую, хроническую с вероятностью повторных заражений и бессимптомную.
Острая форма лямблиоза сопровождается анорексией, тошнотой, диареей, рвотой, болями в верхней и средней частях эпигастральной области, вздутием кишечника, головной болью, повышенной утомляемостью, снижением массы тела. Инкубационный период продолжается от 1 до 4, чаще – 2 нед. Наибольшая выраженность клинических симптомов совпадает с периодами максимальной интенсивности цистовыделения. Течение этой формы кратковременное, обычно происходит быстрое спонтанное выздоровление, или заболевание хорошо поддается лечению [7].
Длительная персистенция лямблий (хроническая форма) чаще встречается у лиц с нарушением резистентности слизистой кишечника специфической или неспецифической природы [2]. Проведенные в последнее время исследования показали, что выраженность и тяжесть клинических проявлений при хронической форме лямблиоза обусловлены воспалительными и функциональными изменениями верхних отделов желудочно-кишечного тракта, а роль лямблий в формировании патологических синдромов не является ведущей [8].
В большинстве случаев лямблиоз – самокупирующая инвазия. Считается, что основная роль в «иммунологической иммобилизации» паразитов принадлежит IgA, который преобладает среди иммуноглобулинов во всех секретах и в собственной пластинке кишечника. Секреторный IgA является блокатором адгезии патогенов (в том числе бактерий, вирусов, простейших) к поверхности слизистой эпителия, а его уровень отражает состояние местного иммунитета. Попадание паразитов в желудочно-кишечный тракт вызывает ответную реакцию системы местного иммунитета в виде нарастания концентрации IgA, который приводит к элиминации паразитов [9]. В случаях неполноценности системы защиты (транзиторный и врожденный дефицит IgA) формируются условия для персистенции лямблий.
Диагноз лямблиоза обязательно должен быть подтвержден результатами лабораторного паразитологического анализа, который входит в перечень обязательных исследований, проводимых клинико-диагностическими лабораториями, и включает методы обогащения: формалин-эфирного осаждения и флотации.
Материалом для исследования являются пробы фекалий и дуоденальное содержимое. В плотных, оформленных фекалиях обнаруживаются только цисты (время исследования не ограничено), а в полуоформленных и жидких – вегетативные формы, изредка – цисты, при этом исследование необходимо провести в течение 1 ч при условии хранения проб при +3–15°С. Вегетативные стадии простейших также обнаруживаются в дуоденальном содержимом. Необходимо отметить, что исследование дуоденального содержимого не дает особых преимуществ перед таковым фекалий, особенно в случаях па- разитирования лямблий только в средних и дистальных отделах тонкой кишки.
Положительный ответ выдается лабораториями при обнаружении вегетативных форм и/или цист простейших с указанием интенсивности инвазии (число паразитов в поле зрения); отрицательный – только после 3-х кратного исследования материала с промежутками в 2–3 дня.
В нашей стране в настоящее время наиболее доступным и информативным считается исследование проб фекалий методом обогащения («золотой стандарт»). Чувствительность это- го метода составляет 76–90% (при однократном исследовании – 60–80%; при 2-х кратном – 80–90%; при 3-х кратном – более 90%) [10].
В большинстве случаев цисты лямблий обнаруживаются уже при первом исследовании. У 10–15% пациентов инвазия лямблий не диагностируется или выявляется после многократных исследований проб фекалий, что можно объяснить большими перерывами в выделении цист (от нескольких дней до 2 нед) и небольшим их количеством [11].
Более чувствительными и перспективными, особенно при проведении эпидемиологических исследований, являются иммунологические методы диагностики, основанные на выявлении специфического лямблиозного антигена в пробах фекалий (ИФА, РНИФ, иммунохроматографический анализ). Чувствительность этих методов варьирует от 95 до 100%, а специфичность составляет 100% [12, 13].
В последнее время отмечается тенденция к назначению ис-следования сыворотки крови в реакции ИФА на специфические антитела к лямблиозному антигену без проведения паразитологического обследования и обнаружения возбудителя (в фекалиях, дуоденальном содержимом), что зачастую приводит к гипердиагностике лямблиоза и необоснованному назначению специфического лечения. Диагностические лаборатории и коммерческие учреждения используют набор Лямблия-АТ-стрип (ЗАО «Вектор Бест»), для выявления суммарных иммуноглобулинов классов А, М, G. Наличие специфических антител не всегда является прямым доказательством инвазии, поскольку IgG-АТ могут определяться в течение нескольких месяцев (до 1,5 лет) после элиминации паразитов [14].
Терапия лямблиоза у детей должна быть комплексной и максимально индивидуализированной. Лечебная тактика определяется особенностями и выраженностью ведущих клинических синдромов, а также резервными возможностями организма хозяина в системе защиты от возбудителя.
Специфическое лечение обычно назначают пациентам при обнаружении возбудителя и выраженных клинических проявлениях, а также при бессимптомной форме лямблиоза в неэндемичных районах [15].
В настоящее время для лечения лямблиоза у детей используют следующие группы препаратов:
- производные нитроимидазола (метронидазол 15 мг/кг 7–10 дней, орнидазол 40 мг/кг однократно, тинидазол 50 мг/кг однократно в течение 2 дней);
- производные нитрофурана (фуразолидон 6 мг/кг 7–10 дней, нифурател 30 мг/кг 7–10 дней);
- производные бензимидазола (мебендазол, албендазол 15 мг/кг 5–7 дней). Последние перспективны для лечения лямблиоза в сочетании с гельминтозами.
При выборе препарата для лечения лямблиоза у детей необходимо учитывать не только его противолямблиозную активность, но и (что более важно) безопасность и хорошую переносимость. Полностью отвечает этим требованиям производное нитрофурана – нифурател (Макмирор, «ПолиИндустрияКимика», Италия). Препарат обладает выраженным антибактериальным, противопротозойным и противогрибковым действием при низкой токсичности. Механизм действия нифуратела заключается в блокировании ряда энзимных цепочек и ингибировании синтеза белка в рибосомах на самых ранних этапах трансляции, что препятствует появлению устойчивых штаммов микроорганизмов и развитию перекрестной резистентности к антибиотикам. Препарат применяется для терапии острых кишечных инфекций бактериальной этиологии, кишечного лямблиоза и амебиаза, инфекций мочеполового тракта, эрадикации Helicobacter pylori [17].
Целью настоящего исследования было изучение действия нифуратела на микробиоценоз кишечника при лечении лямблиозной инвазии у детей.
Пациенты и методы
В исследование было включено 38 детей: 18 (47,4%) мальчиков и 20 (52,6%) девочек в возрасте от 2 до 15 лет (средний возраст 9,1 ± 0,62) с установленной лямблиозной инвазией.
В основную группу вошли дети, у которых в пробах фекалий обнаруживались цисты, трофозоиты и/или антиген L. intestinalis, на момент исследования отсутствовали сопутствующие паразитарные инвазии и имелось согласие родителей.
Контрольную группу, в которой определяли уровень секреторного IgA в фекалиях, составили 20 здоровых детей в воз- расте 3–9 лет.
Всем детям произведено обследование, включающее:
1. паразитологические методы (исследование фекалий на наличие простейших, яиц и личинок методами формалин- эфирного обогащения, Бермана и липкой ленты);
2. иммунологические методы (определение антигена L. intestinalis и уровня секреторного IgA в пробах фекалий);
3. микробиологическое исследование фекалий.
Определение антигена L. intestinalis в пробах фекалий проводили методом ИФА с использованием моноклональных антител к антигенам цист лямблий [13].
В работе использовали полученные нами моноклональные антитела к поверхностным антигенам стенки цист лямблий (мол. масса 28 и 30 кД); конъюгат мкАТ с пероксидазой из корня хрена; в качестве субстрата ТМБ в цитратном буфере с 33% перекисью водорода; положительный и отрицательный образцы фекалий, подтвержденные с помощью микроскопического исследования и в ИФА-наборе ProSpecT Giardia (Alexon Trend, США). Образцы фекалий готовили путем суспендирования в дистиллированной воде в соотношении 1 : 3. Постановку реакции осуществляли в объеме 100 мкл с 1-часовой инкубацией на каждом этапе при комнатной температуре и в защищенном от прямого света месте.
Учет результатов проводили на спектрофотометре типа МР-5000 фирмы «Dynatheh» (ФРГ) при длине волны 450 нм.
Среднее значение оптической плотности (ОП) отрицательных образцов (30 проб) составило 0,069 ± 0,025 (диапазон колебаний 0,069–0,097). Среднее значение ОП положительных образцов (10 проб) соответствовало 1,172 ± 0,322 (диапазон колебаний 0,147–3,276). Значение ОП в исследуемых пробах более 0,1 расценивалось как положительный результат, свидетельствующий о наличии антигена L. intestinalis в фекалиях.
Определение уровня sIgA в пробах фекалий производили с использованием набора реагентов ИФА для количественного определения уровня sIgA (ООО «Прогрессивные Био-Медицинские Технологии», Россия).
Состояние микрофлоры кишечника изучали с помощью стандартной методики Р.В.Эпштейн-Литвак, Ф.Вильшанской с определением КОЕ в 1 г фекалий в пересчете на десятичный логарифм.
Лечение детей проводили нифурателем (Макмирор, «По-лиИндустрияКимика», Италия), таблетками по 200 мг, в течение 5–7 дней в дозе 20 мг/кг/сут, по 2 приема в сут. Всем детям с хронической формой лямблиоза была назначена общепринятая при лечении основного заболевания базисная терапия: диета №5, ферменты, желчегонные и седативные средства, комплекс витаминов, физиотерапевтические процедуры.
Эффективность проводимой терапии оценивали со 2 дня приема препарата по результатам паразитологического (обнаружение цист лямблий) и иммунологического (выявление антигена) методов исследования проб фекалий. В конце лечения (на 7 день с момента приема препарата) проводили оперативный контроль за состоянием кишечной микрофлоры и определение уровня секреторного IgA в образцах фекалий.
Контрольное обследование проводили через 2 нед после окончания лечения с оценкой клинической эффективности, элиминации паразитов (наличие цист и/или антигена в пробах фекалий), а также микробиологического статуса детей.
Методы статистического анализа. Статистическая обработка полученных данных включала определение достоверности различий средних значений количественных данных по критерию Стьюдента.
Результаты исследования и их обсуждение
В ходе обследования диагноз лямблиозной инвазии был установлен у всех 38 (100%) детей на основании выявления антигена лямблий в пробах фекалий и обнаружения их цист у 33 (86,8%) из них.
У 18 (47,4%) детей диагностирована бессимптомная форма лямблиоза (1 группа). Клинические проявления заболевания у них отсутствовали, лямблиозная инвазия обнаружена случайно, при оформлении детей в оздоровительные лагеря.
У 20 (52,6%) детей диагностирована хроническая форма лямблиоза (2 группа), при этом у 16 из них лямблии были выявлены впервые, а у 4 детей – обнаруживались ранее.
Обследование детей на лямблиоз проводилось в связи с предъявляемыми жалобами и клиническими симптомами: абдоминальные боли в околопупочной области, тошнота и рвота по утрам, метеоризм, склонность к запорам. У 15 пациентов отмечались неврологические расстройства: частые головные боли, общая слабость, повышенная утомляемость, нарушение сна. У всех детей 2 группы было сопутствующее поражение органов желудочно-кишечного тракта (ДЖВП, гастро-дуоденит, реактивный панкреатит), половина (11 человек) имели хронические субклинически протекающие заболевания носоглотки (тонзиллиты, синуситы, аденоидиты). В этой группе отмечалась высокая заболеваемость острыми респираторными инфекциями (6–10 раз в год). Таким образом, хроническая форма лямблиоза была диагностирована в группе часто болеющих детей, имеющих сопутствующие хронические заболевания.
Микробиологическое исследование фекалий выявило диcбиотические изменения у всех пациентов с лямблиозной инвазией, при этом наиболее выраженные количественные и качественные нарушения микробиоценоза кишечника отмечались у детей 2 группы с хронической формой лямблиоза. Снижение количества кишечной палочки с нормальной ферментативной активностью и бифидобактерий до lg6, лактобацилл до lg5 сопровождалось повышением уровня эшерихий с измененной ферментативной активностью у 12 (31,6%), высевом микроорганизмов рода Клебсиелла у 5 (13,2%), Энтеробактера – у 10 (26,3%), Протея – у 9 (23,7%), грибов рода Кандида – у 5 (13,2%) детей.
Для оценки местного иммунитета, отражающего общую иммунологическую резистентность организма на уровне слизистых оболочек, у детей с лямблиозом использовали уровень секреторного IgA в секрете кишечника (фекалиях). Средний уровень секреторного IgA в фекалиях у детей с лямблиозной инвазией составил 355,9 ± 123,8 мкг/г и был выше, чем в группе здоровых – (61,39 ± 3,2 мкг/г). У 15 (39,5%) детей отмечалось повышение уровня секреторного IgA (среднее значение 880,7 ± ± 264,3 мкг/г, диапазон колебаний 263,7–4225 мкг/г), по сравнению с группой здоровых. У остальных 32 (60,5%) детей, в основном с хроническим лямблиозом, были выявлены низкие уровни секреторного IgA (среднее значение 2,1 ± 0,5 мкг/г, диапазон колебаний 0,3–9,47 мкг/г, р Оценку эффективности терапии, как уже было сказано, проводили со 2 дня приема нифуратела. Определение антигена лямблий в пробах фекалий в процессе лечения показало, что на 2-й день после его начала концентрация антигена заметно возрастает, затем постепенно снижается и после 4-го дня антиген не определяется. При контрольном паразитологическом обследовании цисты лямблий в пробах фекалий не обнаруживались с 3 дня приема препарата (рисунок).
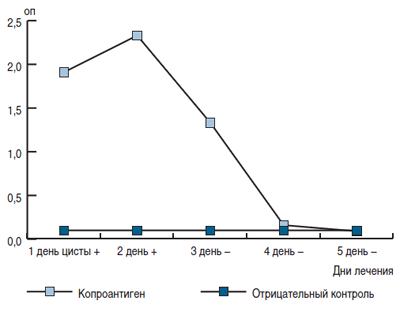
Рисунок. Оценка эффективности нифуратела у детей (n = 38) с лямблиозом
по результатам выявления копроантигена (ИФА) и цист лямблий (микроскопия) в пробах фекалий.
В ходе исследования было выявлено положительное влияние нифуратела на состояние биоценоза кишечника у детей. У 24 (85,7%) из 28 пациентов отмечалось санирующее действие препарата по отношению к представителям условно-патогенной микрофлоры: полностью редуцировались микроорганизмы рода Протея, Клебсиеллы, грибы рода Кандида. У 4 детей снизилось количество эшерихий с измененными свойствами и микроорганизмов рода Энтеробактер. Нормализация количественного содержания бифидобактерий и лактобацилл отмечалась у 15 (39,5%) из 38 детей на фоне снижения уровня секреторного IgA в фекалиях с 880,7 ± 264,3 до 97,5 ± 54,3 мкг/г (р 0,05) по сравнению с исходными данными. Группа детей с низкими уровнями sIgA в кишечнике требовала дальнейшего углубленного иммунологического исследования с последующим проведением иммунокоррекции.
На фоне проводимого комплексного лечения у детей отмечалась положительная динамика основного заболевания: к 5 дню купировались болевой и диспепсический синдромы. Контрольные анализы проб фекалий на присутствие цист лямблий и/или специфического антигена, проведенные через 2 нед после приема препарата, у всех детей были отрицательными.
Существенным моментом в оценке эффективности нифу-ратела при лечении лямблиоза в нашем исследовании являлась его хорошая переносимость. В течение всего курса лечения побочные и/или нежелательные реакции были отмечены нами всего у 1 (2,6%) ребенка в виде абдоминальной боли, возникшей на 3 день приема препарата.
Выводы
1. Эффективность Нифуратела (Макмирора) при лечении лямблиоза у детей по результатам контрольных исследований проб фекалий и выявления специфического антигена достигает 100%.
2. Нифурател не подавляет облигатную флору кишечника и в большинстве случаев оказывает санирующий эффект по отношению к представителям условно-патогенной микрофлоры.
3. Нифурател можно считать препаратом выбора для лечения лямблиоза у детей в связи с его высокой эффективностью и хорошей переносимостью. Литература 1. Swartz, Morton N., MD: Intestinal Protozoan Infections. Scientific American Medicine, 1994.
2. Авдюхина Т.И., Константинова Т.Н., Кучеря Т.В. и др. Лямблиоз. Учебное пособие. М., РМАПО. 2003; 32.
3. ВОЗ. Доклад Комитета экспертов. Профилактика кишечных паразитарных инвазий и борьба с ними. Сер. Техн. Докл. 1988; 90.
4. Соловьев М.М. Строение и биология лямблий и их взаимоотношения с организмом хозяина. Автореф. дисc. ... д.б.н. 1973, М. 38–9.
5. WHO Expert Committee. Intestinal protozoan and helminthic infections. WHO Tech. Rep. Ser. 1981; 58: 666–71.
6. Райните-Аудинене А.Б. Основные клинические синдромы и функциональное состояние печени при лямблиозе у детей. Автореф. дисc. ... к.м.н. 1969; 5–18.
7. Wolfe M.S. Clinical symptoms and diagnosis by traditional methods. Meyer E.A. eds. Giardiasis 1990; 175–85. Elsevier Amsterdam.
8. Куимова И.В. Клинико-патогенетические аспекты патологии органов пищеварения и аллергодерматозов у детей с лямблиозной инвазией. Автореф. дисc. ... д.м.н. 2003: 5–21.
9. Стебенева С.А., Лизько Н.Н., Виха Г.В. Секреторный иммуноглобулин А – показатель нарушений микрофлоры желудочно-кишечного тракта. Биотехнология 1998; 2: 85–7.
10. Hiatt R.A., Markell E.K., Ng E. How many stool examinations are necessary to detect pathogenic intestinal protozoa? Am. J. Trop. Med. Hyg. 1995; 53: 36–9.
11. Thompson R.C.A., Reynoldson J.A., Mendis A.H. Giardia and giardiasis. Adv. Parasitol. 1993; 32: 71–160.
12. Aldeen W.E., Carroll K., Robison A., Morrison M., Hale D. Comparison of nine commercially available enzyme-linked immunosorbent assays for the detection of Giardia lamblia in fecal specimens. J. Clin. Microbiol. 1998; 36: 1338-40.
13. Конаныхина С.Ю., Сердюк О.А., Степанова И.И. Моноклональные антитела к антигену лямблий для копродиагностики лямблиоза. Вопросы современной педиатрии 2005; 4, прил. 1: 648.
14. Rosales-Borjas D.M., Diaz-Rivadeneyra J., Dona-Leyva S.A., et al. Secretory immune response to membrane antigens during Giardia lamblia infection in humans. Infect. Immun. 1998; 66: 756–9.
15. Zaat J.O., Mank T.G., Assendelft W.J. A systematic review on the treatment of gia-rdiasis. Trop. Med. Int. Health. 1997; 2: 63–82
16. Upcroft P. Drug resistance in Giardia: clinical versus laboratory isolates. Drug. Resist. Updates 1998; 1: 166–8.
17. Регистр лекарственных средств России. 2005; 527.
