Жидкая лекарственная форма эргоферона — эффективное и безопасное средство лечения острых респираторных инфекций у детей. Промежуточные итоги многоцентрового двойного слепого плацебо-контролируемого рандомизированного клинического исследования
Статьи Опубликовано в журнале:
« АНТИБИОТИКИ И ХИМИОТЕРАПИЯ » , 2014, 59. Н. А. ГЕППЕ1, Е. Г. КОНДЮРИНА2, А. Н. ГАЛУСТЯН3, Т. Е. ПАК4, Н. Б. БАЛЬЦЕРОВИЧ5, O.В. ЖИГЛИНСКАЯ6, А. В. КАМАЕВ7, С. Г. ЛАЗАРЕВА8, С. Л. ЛАЛЭКО9, И. М. МЕЛЬНИКОВА10, О. А. ПЕРМИНОВА11, А. У. САБИТОВ12
1 Кафедра детских болезней Первого Московского Государственного Медицинского Университета им. И. М. Сеченова Министерства здравоохранения Российской Федерации
2 Новосибирский государственный медицинский университет Министерства здравоохранения Российской Федерации
3 Санкт-Петербургский государственный педиатрический медицинский университет Министерства здравоохранения Российской Федерации
4 Санкт-Петербургская государственная педиатрическая медицинская академия Министерства здравоохранения Российской Федерации
5 Детская городская поликлиника № 45 Невского района, Санкт-Петербург
6 Городская поликлиника № 44, Санкт-Петербург
7 Городская детская поликлиника № 44, Санкт-Петербург
8 Альянс Биомедикал-Русская группа, Санкт-Петербург
9 Детская городская больница № 22, Санкт-Петербург
10 Ярославская государственная медицинская академия Министерства здравоохранения Российской Федерации, на базе: Клинической больницы № 8, Ярославль
11 Городская детская клиническая поликлиника № 5, Пермь
12 Детская городская больница № 11, Екатеринбург
Детская лекарственная форма Эргоферона — препарата для лечения гриппа и острых респираторных инфекций (ОРИ) — разработана с учётом широкого спектра патогенов (большинство из которых вирусы) и возрастных особенностей реагирования иммунной системы (отсутствие специфического иммунитета и иммунологической памяти, относительная «незрелость» иммунных реакций, сниженная интерферон-продуцирующая активность иммунокомпетентных клеток и др.). Эргоферон оказывает воздействие на универсальные механизмы противовирусной защиты, обеспечивающие развитие иммунного ответа независимо от типа вируса (систему интерферона и CD4+ клеток), а также на вирус-индуцированную либерацию гистамина и опосредованные им воспалительные реакции.
За четыре года применения в клинической практике препарат показал высокий профиль эффективности и безопасности в лечении гриппа и ОРИ у взрослых пациентов. Целью многоцентрового двойного слепого плацебо-контролируемого рандомизированного исследования была оценка клинической эффективности и безопасности новой жидкой лекарственной формы Эргоферона в лечении ОРИ у детей.
В публикации представлены результаты завершённого в соответствии с планом первого этапа исследования и промежуточного анализа (Interim analysis). Методы. Обследовано 162 пациента от 3 до 17 лет (средний возраст 8,2±3,9 лет) с типичными проявлениями ОРИ (температура >38,0°C, измеренная электронным инфракрасным термометром в области височной артерии; выраженность симптомов >4 баллов по балльной шкале) в период сезонной заболеваемости из 13 исследовательских центров России. Эргоферон по лечебной схеме в течение 5 дней был назначен 82 пациентам; 80 детей получали плацебо. Длительность наблюдения составила 6 дней. Эффективность терапии анализировали на основании утренних, вечерних и суммарных за день оценок симптомов ОРИ, включая лихорадку, общие симптомы и симптомы со стороны верхних дыхательных путей подсчитывали суммарный индекс (СИ) ОРИ; для анализа тяжести течения ОРИ применяли математическую модель «площадь под кривой». Результаты. Начиная со второго дня, количество пациентов с выздоровлением нарастало с 6% (утром) и 14% (вечером), до 20 и 29% — на 3-й, 58 и 61% — на 4-й дни. Эффективность лечения Эргофероном была существенно выше, чем плацебо-терапия (критерий χ2 в модификации Cochran-Mantel-Haenszel: Χ2=21,7; p 2=10,6; p=0,012), на третий — 83% утром и 84% вечером (против 60 и 54% в группе плацебо соответственно; χ2=16,7; p=0,001). Метод обобщённых линейных моделей (GENMOD) подтвердил достоверность различий между группами Эргоферона и плацебо по следующим позициям:
1) Эргоферон значимо эффективнее (до более низких цифр), чем плацебо, снижал температуру тела;
2) Эргоферон быстрее, по сравнению с плацебо, оказывал влияние на лихорадку (основной маркёр виремии);
3) превосходство Эргоферона над плацебо-терапией было значимо и по утренним, и по вечерним показателям в течение всех пяти дней терапии.
Начиная со второго дня лечения Эргофероном, СИ значимо уменьшался: с 13,0±4,5 до 7,9±4,8 на 2-й день, до 4,5±2,9 — на 3-й день (по данным дневника пациента), с 14,3±4,2 до 4,9±3,0 на 3-й день (по оценкам врача). Наиболее заметно снижалась тяжесть интоксикационных проявлений ОРИ, в том числе на 3-й день лечения по результатам объективного осмотра врача (GENMOD: фактор Препарат — χ2=147,8; p 2=6,1; p=0,013; пост-хок анализ Tukey-Kramer: z=–3,09; p=0,024). Средняя продолжительность лихорадочного периода на фоне применения Эргоферона составила 1,9±0,8 дней (р 2=4,1; p=0,043), особенно в первый день болезни. Мониторинг нежелательных явлений, общеклинических и биохимических анализов крови и мочи показал, что Эргоферон является безопасным лекарственным средством. Сочетанное использование Эргоферона с антипиретиками, деконгестантами, экспекторантами, ингаляционными кортикостероидами, препаратами кромоглициевой кислоты, антагонистами лейкотриеновых рецепторов, бета-2-агонистами короткого действия и местными антисептиками не приводило к проявлениям фармакологической несовместимости, антагонистическому или взаимно усиливающему действию. Не зарегистрировано случаев развития бактериальных осложнений, ухудшения течения заболевания, обострений сопутствующей аллергической и хронической ЛОР патологии. Дети хорошо переносили препарат и продемонстрировали 100% приверженность терапии. Выводы. Жидкая форма Эргоферона — эффективное и безопасное средство для лечения ОРИ у детей.
Результаты исследования доказали эффективность препарата в отношении главных, ассоциированных с вирусемией и развивающихся вследствие неё синдромов — лихорадочного и общеинтоксикационного. Быстрый эффект препарата помогал выздоравливать пациентам в более короткие сроки, а также снижал тяжесть течения ОРИ, особенно на ранних этапах болезни.
Ключевые слова: Эргоферон, острая респираторная инфекция, лечение, дети.
Введение
По данным Всемирной организации здравоохранения (ВОЗ), «лишь незначительное число лекарственных средств существует в специально разработанных для детей формах» [1]. В связи с этим одной из «Целей тысячелетия в области охраны здоровья детей» ВОЗ объявила «необходимость обеспечения доступа детей к надлежащим лекарственным средствам», представив в декабре 2007 года «Инициативу по производству лекарств в детских формах». К детским препаратам, как известно, предъявляются особые требования: помимо соответствия всем стандартам безопасности и эффективности, они должны обладать характеристиками, которые бы учитывали анатомо-физиологические особенности маленьких пациентов и обеспечивали высокую комплаентность терапии [2].
Принимая во внимание, что наиболее распространёнными в детской популяции являются острые инфекции дыхательных путей, частота которых составляет 672,1 на 1000 детского населения [3], разработка лекарственных средств для их лечения весьма актуальна. Препараты, при создании которых учитывались такие факторы, как разнообразие респираторных патогенов, вызывающих заболевание (большинство из них — вирусы), широкий спектр клинических симптомов, которыми оно проявляется, а также возрастные особенности реагирования иммунной системы ребёнка, значительно помогают врачу-педиатру решить целый комплекс стоящих перед ним терапевтических задач.
К таким лекарственным средствам относится специально разработанная для детей жидкая форма Эргоферона («Материа Медика Холдинг»). Этот релиз-активный препарат содержит три компонента, созданных в результате технологической обработки исходных антител к интерферону-гамма (анти-IFNγ), CD4 (анти-CD4) и гистамину (анти-Н). За четыре года применения в клинической практике Эргоферон, выпускавшийся ранее только в одной «твердой» форме (в виде сублингвальных таблеток), показал высокий профиль эффективности и безопасности в лечении гриппа и ОРИ у взрослых пациентов [4—14]. Таргетное воздействие на эндогенный интерферон гамма (IFN-γ) и мишень-ассоциированные рецепторы, модуляция их функциональной активности – отличительное свойство первого компонента Эргоферона (анти-IFNγ), который более 12 лет широко применяется в педиатрии в качестве релиз-активного препарата «Анаферон детский» [15—20]. Увеличение числа CD4+ и IFNγ рецепторов, усиление интерферон-зависимой активации CD4+ клеток, участвующих в развитии адекватного противовирусного ответа, — результат использования второго компонента Эргофе-рона — анти-CD4 в комбинации с анти-IFNγ [21, 22]. Снижение вирус-индуцированного высвобождения гистамина и выраженности гистамин-опосредованных реакций при ОРИ — итог применения анти-Н [8, 22—24]. Таким образом, три компонента Эргоферона оказывают сочетанное влияние на различные этапы иммунного ответа и инфекционно-воспалительного процесса, что клинически проявляется в снижении тяжести течения гриппа/ОРИ и ускорении выздоровления пациентов, по сравнению со стандартной либо плацебо-терапией [4—14].
С учётом российских, а также разработанных ВОЗ, руководящих принципов по клиническим испытаниям с участием детей, проведено регистрационное многоцентровое двойное слепое плацебо-контролируемое рандомизированное исследование, цель которого продемонстрировать безопасность и клиническую эффективность новой жидкой лекарственной формы Эргоферона в лечении ОРИ у детей. Результаты завершенного в соответствии с планом первого этапа исследования и промежуточного анализа (Interim analysis) представлены в данной публикации.
Материал и методы
В исследовании приняли участие 162 пациента от 3 до 17 лет (средний возраст 8,2±3,9 лет), с типичными проявлениями ОРИ, в период сезонной заболеваемости, из 13 исследовательских центров России. Для того чтобы обеспечить равномерное участие пациентов различных возрастных групп, было включено 20% пациентов от 3 до 6 лет (n=32), 40% — от 6 до 12 лет (n=65) и 40% — старше 12 лет (n=65).
После подписания родителем/усыновителем, а также пациентом (если он достиг 14 лет) формы информированного согласия на участие в клиническом исследовании, проводилось обследование пациента, регистрировалась сопутствующая терапия.
Включались пациенты, обратившиеся к врачу в течение 24 ч от начала заболевания, выраженность которого соответствовала следующим критериям: температура тела не менее 38,0°C на момент осмотра врачом; выраженность симптомов ОРИ >4 баллов (наличие, как минимум, 1 общего симптома >2 баллов и 1 симптома со стороны верхних дыхательных путей >2 баллов либо большего количества симптомов выраженностью >1 балла). Термометрию проводили в области височной артерии при помощи электронного инфракрасного термометра, предоставленного спонсором исследования для каждого пациента [25]. Тяжесть симптомов ОРИ, включая температуру тела, общие симптомы (головная боль, озноб, потливость, слабость, мышечная боль, сонливость), симптомы со стороны носа (выделения из носа, заложенность носа, чихание), горла (боль в горле, хрипота/охриплость голоса) и грудной клетки (кашель, боль/тяжесть в груди при локализации воспаления в трахее) оценивали по 4-балльной шкале, где 0 — отсутствие симптома; 1 — лёгкая степень; 2 — средняя степень; 3 — тяжёлая степень. На основании выраженности каждого из симптомов при последующей статистической обработке данных подсчитывался суммарный индекс (СИ) ОРИ.
Пациент не включался в исследование при наличии клинических проявлений ОРИ нижних дыхательных путей, бронхообструктивного синдрома, острой дыхательной недостаточности; подозрении на инвазивную бактериальную инфекцию, обострении или декомпенсации хронических заболеваний, включая хронические заболевания органов дыхания; наличии в анамнезе воспалительных, дегенеративных, демиелинизирующих заболеваний центральной нервной системы, полиневропатии, эпилепсии, злокачественных новообразований, сахарного диабета, наследственной непереносимости фруктозы (вследствие наличия в составе исследуемого препарата мальтитола), аллергии/непереносимости любого из компонентов лекарственных препаратов, используемых в лечении, а также в случаях курения, употребления родителями/усыновителями/пациентом наркотиков, алкоголя, беременности/нежелания соблюдать методы контрацепции сексуально активными пациентами, психических заболеваний пациента/родителей/усыновителей, участия в других клинических исследованиях в течение 3 предшествующих месяцев.
За 1 месяц до включения в исследование, а также в ходе его проведения не разрешался приём противовирусных и антибактериальных средств; иммунных сывороток и иммуноглобулинов, вакцин; иммуностимуляторов и иммунодепрессан-тов; антигистаминных препаратов, фенспирида, омализумаба; комбинированных препаратов для симптоматической терапии ОРИ; антипиретиков, за исключением парацетамола и ибупрофена, предоставленных спонсором для применения с учётом показаний для проведения жаропонижающей терапии [26]. Пациенты могли получать не включенные в список запрещённые средства для симптоматической терапии ОРИ и лечения сопутствующих заболеваний [27, 28].
Длительность исследования составила 6 дней, в ходе которых пациенты трижды осматривались врачом (Дни 1, 3 и 6). В течение 5 дней родитель/усыновитель пациента и/или пациент старше 14 лет вели дневник, в котором отмечали выраженность симптомов заболевания, используя 4-балльную шкалу. По завершении курса лечения (День 6) проводилось заключительное обследование, контролировалась назначенная и сопутствующя терапия, её безопасность, проверялся дневник пациента.
Эффективность терапии по первичному критерию анализировали на основании утренних, вечерних и суммарных за день оценок выраженности всех симптомов ОРИ, включая лихорадку, общеинтоксикационные и катаральные симптомы. Критерием полного выздоровления было снижение температуры тела В качестве вторичных критериев эффективности анализировали несколько показателей, включая динамику лихорадки, суммарный индекс тяжести симптомов ОРИ [(1) по данным объективного осмотра врача и (2) по мнению ухаживающего за больным взрослого/пациента старше 14 лет], продолжительность основных симптомов, тяжесть течения ОРИ, наличие/отсутствие вторичных бактериальных осложнений, потребовавших назначения антибактериальных препаратов либо госпитализации пациента. Для объективной оценки тяжести течения ОРИ и сравнения её в обеих группах использовали математическую модель — построение «площади под кривой» для СИ выраженности всех симптомов. На основании оценок, сделанных в дневнике пациента на протяжении всех 5 дней лечения (значений температуры тела и выраженности всех симптомов ОРИ), подсчитывался СИ; поэтому «кривая СИ» по данным дневника пациента включала 5 значений, а «площадь под кривой» СИ рассчитывалась как произведение «СИ х n», где n=5 дней. Объективный осмотр пациента врачом в ходе исследования проводился в общей сложности 3 раза (на 1, 3 и 6 дни), поэтому «кривая СИ» по данным осмотра врача включала 3 значения, «площадь под кривой» СИ высчитывалась как произведение «СИ х n», где n=3 дня, и она была объективно меньше, чем первая площадь.
Оценка безопасности и переносимости исследуемой терапии проводилась на основании наличия и характера нежелательных явлений, их связи с лечением и других характеристик, а также динамики лабораторных показателей (общеклинических и биохимических анализов крови и мочи). В случае проведения визита на дому, взятие образца крови осуществлялось с помощью вакутейнера с последующей транспортировкой в локальную лабораторию в термоконтейнере.
Размер выборки для промежуточного анализа эффективности рассчитывали с учетом следующих правил и допущений: мощность статистических критериев принималась равной 80%; вероятность ошибки первого рода — менее 5%; используемые статистические критерии являлись двусторонними; на основании предполагаемого эффекта минимально необходимый размер выборки для промежуточного анализа составил 160 пациентов. В связи с запланированным промежуточным анализом по методу Haybittle-Peto, величина ошибки первого рода (а) вместо стандартного p=0,05 была установлена на более консервативном уровне в размере p=0,0294; все результаты рассматривались как значимые лишь в том случае, если величина «p» была равна или меньше этой величины.
Применялись стандартные методы частотного анализа: критерий χ2 и модификация Cochran-Mantel-Haenszel критерия χ2 для множественных сравнений (CMH χ2); анализ непрерывных переменных осуществлялся с использованием двух-выборочного t-критерия Стъюдента с учётом равных или неравных дисперсий; многофакторный анализ непрерывных и полиномиальных переменных проводился с использованием обобщённых линейных моделей (GENMOD, generalized linear models).
Обработка данных и все статистические расчёты производились с использованием статистического пакета SAS-9.3.
Группы пациентов. По окончании процедур скрининга пациент рандомизировался в одну из двух групп: пациенты 1 группы (n=82) получали Эргоферон; пациенты 2 группы (n=80) — плацебо. Схема приёма Эргоферона/плацебо: внутрь, вне приёма пищи; на один приём — 1 мерную ложку (5 мл); в первые 2 часа препарат принимали каждые 30 минут, затем в течение первых суток осуществляли ещё три приёма через равные промежутки времени; со 2-х по 5-е сутки — по 1 мерной ложке 3 раза в день.
Распределение пациентов в ту или иную группу терапии проводилось случайным образом с помощью специальной Интерактивной Голосовой Системы с возможностью Веб-доступа; пациенту присваивался рандомизационный номер в целях сохранения конфиденциальности; каждый пациент был рандомизирован только один раз в ходе исследования. Обе группы участников исследования исходно были сопоставимы по основным демографическим и клинико-лабораторным характеристикам. 35% участников имели различные сопутствующие заболевания, в том числе, бронхиальную астму и аллергический ринит в периоде ремиссии (всего 8%); хроническую патологию ЛОР-органов и аденоидные вегетации (4%); болезни костно-мышечной системы (9%), болезни органов пищеварения (4%), кровообращения (3%), мочевыделения (2%), кожи (3%). Исходно средний суммарный балл ОРИ, по оценкам врача, был 14,3±4,2 баллов в группе Эргоферона и 15,5±4,2 баллов в группе плацебо; по данным дневника пациента — 13,0±4,5 и 14,8±4,6 баллов соответственно. Разрешенные жаропонижающие препараты в первый, реже второй, день ОРИ принимали 61% пациентов; сосудосуживающие назальные капли и спреи — 94%, местные антисептические растворы и пастилки — 59%; экспекторанты — 29%. Пять детей (3%; 3 из группы Эргоферона и 2 из группы плацебо) получали ингаляционные препараты базисной терапии бронхиальной астмы (топические глюкокортикостероиды, кромоны, β2-агонисты).
Результаты проведённого теста на беременность среди сексуально активных девочек-подростков (n=4; 2,5%) были отрицательными у всех пациенток. Один пациент из группы плацебо использовал барьерный метод контрацепции во время участия в исследовании и в течении 30 дней после его завершения (в соответствии с требованиями протокола).
В ходе исследования не выбыло ни одного пациента, 2 пациента были исключены из анализа эффективности (оба из группы Эргоферона в связи с приемом препаратов комбинированного состава для симптоматической терапии ОРИ, относящихся к списку запрещенных). Полностью завершили участие в исследовании в соответствии с процедурами протокола 160 пациентов, их данные вошли в окончательный анализ эффективности (Per Protokol-анализ), в том числе 80 — группы Эргоферона и 80 — группы плацебо.
Оценку безопасности и переносимости исследуемой терапии проводили у всех пациентов, включённых в исследование и получивших хотя бы одну дозу исследуемого препарата (n=162).
Результаты и обсуждение
В результате лечения Эргофероном на второе утро количество пациентов с выздоровлением/значимым улучшением составило 6%, на 3-е — 20% и на 4-е — 58% (против 1, 14 и 35% в группе плацебо соответственно) (рис. 1). Частотный анализ (CMH χ2), проведённый для пяти пар утренних измерений, подтвердил, что процент выздоровевших пациентов на фоне применения Эргоферона был существенно выше, чем в группе плацебо ( Χ2=9,7; р=0,002). Оценка выраженности симптомов ОРИ в вечернее время показала сходную динамику. Начиная с вечера второго дня, количество реконвалесцентов прогрессивно нарастало и составило на 2 сутки 14%, на 3-и — 29% и на 4-е — 61% (против 5, 14 и 44% на фоне плацебо-терапии). Частотный анализ пяти пар вечерних измерений также подтвердил значимое превосходство эффективности терапии Эргофероном (Χ2=12,0; p=0,001). Оценка суммарных значений в течение дня, то есть процента пациентов с окончательным купированием всей симптоматики ОРИ по данным анализа критерия CMH, дала ещё более убедительный вывод: χ2=21,7; p=0,0001. Сравнение итогов лечения на третий (Χ2=5,8; p=0,016) и четвертый (Χ2=12,8; р=0,0004) дни подтвердило значимость различий между группами. Таким образом, после трёх дней применения Эргоферона, на 4-й день от начала болезни более чем у половины детей (61%) отмечалась ликвидация симптомов заболевания. Полученные результаты позволяют утверждать, что лечение Эргофероном приводило к более быстрому, по сравнению с плацебо, выздоровлению детей, изначально имевших выраженную симптоматику ОРИ.
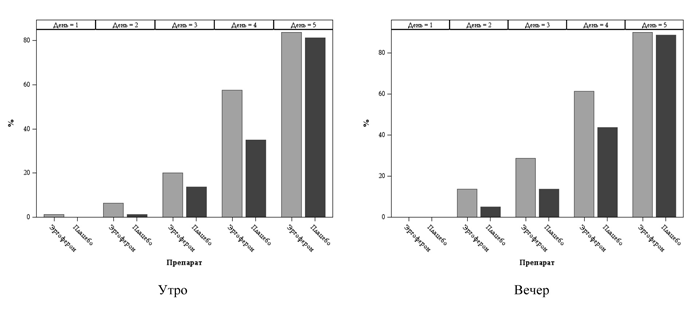
Рис. 1. Число пациентов (в %) с выздоровлением/улучшением на фоне лечения Эргофероном.
Оценка вторичных критериев эффективности включала несколько конечных точек. Принимая во внимание, что лихорадка — значимый клинический маркёр при ОРИ, был проведён анализ динамики температурной реакции на 2—5 дни лечения. Уже на второй день лечения Эргофероном у большинства детей фебрильная температура снизилась до субфебрильной (средние значения утром и вечером — 37,4±0,6°С); утром второго дня четвертая часть пациентов имела температуру тела 2=9,2; p-=0,002); вечером — 66% (Χ2=17,9; p=0,001), средние значения — 36,9±0,4°С и 37,0±0, соответственно. В группе плацебо динамика лихорадки была менее отчетливой, средние значения температуры на 3 и 4 сутки были выше, чем в группе Эргоферона, а полная нормализация наступила на 4-й день (средние значения: утром —36,7±0,3; вечером — 36,8±0,3°С).
С учётом конечной точки 2=10,6; p=0,012), на третий — 83% утром и 84% вечером (против 60 и 54% в группе плацебо соответственно; Χ2=16,7; p=0,001). Анализ динамики температурной реакции с помощью GENMOD показал, что высокодостоверными были все три исследованных фактора (Препарат [2 уровня] —Χ2=14,4; p2=16,5; p2 =153,7; p2=16,7; p2=23,6; p 1) в группе Эргоферона значимо эффективнее (до более низких цифр), чем в группе плацебо, снижалась температура тела;
2) Эргоферон быстрее, по сравнению с плацебо, оказывал влияние на лихорадку — основной маркёр виремии;
3) превосходство Эргоферона над плацебо-терапией было значимо и по утренним, и по вечерним показателям в течение всех пяти дней терапии.
Пост-хок анализ (метод Бонферони) выявил достоверные различия между группами Эргоферона и плацебо на второй (Χ2=3,7; p=0,009) и третий (Χ2=4,2; p=0,001) дни лечения, что дополнительно подтверждало быстрый эффект препарата.
Анализ изменений СИ на фоне лечения свидетельствовал о том, что мнения и взрослого, ухаживающего за ребенком (либо самого пациента >14 лет), и врача о выраженности симптомов ОРИ практически совпадали в те дни, когда была возможность их сравнить (на 1 и 3 дни наблюдения). Начиная со второго дня лечения Эргофероном, выраженность симптомов заболевания прогрессивно снижалась. По данным дневника пациента, СИ от исходного в 13,0+4,5 баллов снизился до 7,9+4,8 на второй день и до 1,1+1,2 на пятый; эта динамика снижения была значимо лучшей, чем в группе плацебо; двухфакторный анализ GENMOD выявил значимость обоих факторов (День лечения: χ2=144,7; p2=9,3; p=0,002), а также значимое их взаимодействие (День лечения и Препарат: χ2=11,0; p2=146,9; pПо данным осмотра врача на 6 день от начала болезни все пациенты группы Эргоферона не имели симптомов заболевания и были признаны здоровыми. Таким образом, анализ динамики СИ подтвердил терапевтическую эффективность Эргоферона; наиболее выраженный эффект лечения отмечался на 2 и 3 сутки лечения, что свидетельствовало о максимальном действии препарата в ранние сроки, в период наиболее тяжелого течения болезни.
Анализ влияния Эргоферона на длительность течения симптомов ОРИ доказал выраженную эффективность препарата, прежде всего, в отношении лихорадки и других проявлений синдрома интоксикации. Продолжительность лихорадочного периода у детей на фоне приёма Эргоферона в среднем составила 1,9±0,8 дня, что было существенно меньше, чем в группе плацебо (2,5±0,8 дня; pСравнение тяжести течения ОРИ с помощью математической модели «площадь под кривой» для СИ выявило значимые различия в двух группах. По данным дневника пациента, площадь под кривой в группе Эргоферона составила 21,9±10,9 СИ х Дни, и она была достоверно меньше, чем аналогичный показатель в группе плацебо (28,0±13,0 СИ х Дни; p 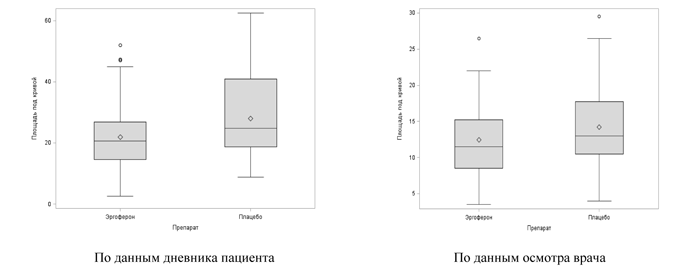
Рис. 2. Влияние Эргоферона на тяжесть течения ОРИ
(площадь под кривой для суммарного индекса).
Условные обозначения на графиках: ромб внутри прямоугольника — среднее арифметическое в группе; горизонтальная черта внутри прямоугольника — медиана; верхняя и нижняя стороны прямоугольника — границы 1-го и 3-го квартилей; нижние и верхние горизонтальные отрезки — минимум и максимум значения; круг вне прямоугольника — статистический выброс.
Следствием снижения тяжести лихорадки и общеинтоксикационных проявлений на фоне лечения Эргофероном было уменьшение частоты приёма жаропонижающих препаратов. Антипиретики в первый день лечения были назначены 68% детей группы Эргоферона; в группе плацебо таких детей было на 21% больше (89%). На второй день процент детей, нуждавшихся в антипиретиках, составил 9% и 12% соответственно.
В ходе исследования ни у одного пациента не было зарегистрировано ни одного случая ухудшения заболевания либо развития осложнений, требующих антибактериальной терапии или госпитализации. Все пациенты закончили участие в исследовании выздоровлением от ОРИ. Таким образом, итоги исследования подтвердили полученные ранее и широко опубликованные данные многочисленных исследований об эффективности Эргоферона в лечении пациентов с инфекционными заболеваниями дыхательных путей [4—14].
Результаты данного клинического испытания свидетельствуют о терапевтической эффективности жидкой лекарственной формы Эргоферона в лечении детей с ОРИ различной этиологии. Известно, что большинство острых респираторных заболеваний в период подъёма сезонной заболеваемости вызываются вирусами, подавляющими защиту клетки от инфекции [29, 30]. Эргоферон обеспечивает воздействие на универсальные механизмы противовирусной защиты, которые играют ключевую роль в развитии иммунного ответа независимо от типа вируса, а именно, систему интерферона и CD4+ клеток. Комбинация анти-IFNγ+анти-CD4 индуцирует продукцию эндогенного IFNγ, активирует функциональное состояние рецепторов IFNγ и CD4+ и лиганд-рецептороное взаимодействие, активность CD4+ клеток, в том числе антигенпрезентирующих (макрофагов и дендритных клеток) и Т-хелперов (Th1 и Th2) [17—22, 30—32]. Неспецифическая противовирусная активность первых двух компонентов Эргоферона, дополненная эффектами анти-Н, обеспечивает эффективность препарата, прежде всего, в отношении главных, ассоциированных с вирусемией и развивающихся вследствие неё, синдромов — лихорадочного и общеинтоксикационного. Быстрый эффект препарата помогает выздоравливать пациентам в более короткие сроки, а также снижает тяжесть течения ОРИ, особенно на ранних этапах болезни.
Результаты исследования подтвердили высокий уровень безопасности Эргоферона в виде раствора для приёма внутрь, используемого по лечебной схеме у детей с ОРИ. Всего в течение периода лечения и наблюдения было зарегистрировано 3 нежелательных явления (НЯ) у двух пациентов (по одному из каждой группы). Все НЯ были лёгкой степени. 2 НЯ в группе Эргоферона (кратковременные ушная боль при глотании и незначительное головокружение в момент приема препарата) и 1 НЯ в группе плацебо (однократный разжиженный стул на фоне погрешности в питании) не имели связи с исследуемой терапией и не потребовали отмены препарата. Мониторинг биохимических и общеклинических показателей крови и мочи не выявил отклонений от нормальных значений. Сочетанное использование Эргоферона с препаратами для симптоматической терапии ОРИ (антипиретиками, деконгестантами, экспекторантами), а у некоторых пациентов — с ингаляционными глюкокортикостероидами, препаратами кромоглициевой кислоты, антагонистами лейкотриеновых рецепторов, бета-2-агонистами короткого действия, не приводило к проявлениям фармакологической несовместимости, антагонистическому или взаимно усиливающему действию. Оценка комплаентности, проведённая на последнем визите, продемонстрировала 100% уровень приверженности пациентов к назначенной терапии.
Заключение
Применение Эргоферона способствовало выздоровлению значимо большего процента детей с ОРИ в более короткие сроки, по сравнению с плацебо-терапией, что подтверждено результатами статистического анализа с применением консервативных (наиболее строгих) критериев оценки. Наиболее отчётливые эффекты были продемонстрированы в отношении лихорадки и других проявлений общеинтоксикационного синдрома. В условиях двойного слепого плацебо-контроля доказано, что Эргоферон значимо эффективнее (до более низких цифр) и быстрее снижал температуру тела.
Средняя продолжительность лихорадочного периода на фоне применения Эргоферона составила 1,9±0,8 дней. Максимальное действие препарата проявлялось в ранние сроки от начала применения Эргоферона — период максимальной выраженности симптомов. Начиная со второго дня, суммарный клинический индекс ОРИ существенно снижался, а средняя длительность заболевания у пациентов, получавших Эргоферон, была значимо меньше, чем в группе плацебо. Быстрый эффект Эргоферона не только помогал выздоравливать пациентам в более короткие сроки, но и снижал тяжесть течения ОРИ на протяжении всего периода лечения, особенно на ранних этапах, что подтверждалось результатами анализа «площади под кривой» для суммарного индекса заболевания. Следствием снижения тяжести лихорадки и общеинтоксикационных проявлений на фоне лечения Эргофероном было уменьшение частоты приёмов жаропонижающих препаратов, особенно в первый день терапии Эргофероном. На фоне применения препарата не зарегистрировано случаев развития бактериальных осложнений или ухудшения течения заболевания, а также обострений сопутствующей аллергической и хронической ЛОР патологии. Все пациенты закончили участие в исследовании выздоровлением. Высокий уровень безопасности Эргоферона подтверждён отсутствием зарегистрированных нежелательных явлений, имеющих связь с исследуемой терапией. Мониторинг биохимических и общеклинических показателей крови и мочи не выявил отклонений от нормальных значений. Эргоферон хорошо сочетался с лекарственными средствами различных классов.
Пациенты детского возраста хорошо переносили препарат и продемонстрировали высокую приверженность лечению. Таким образом, новая жидкая лекарственная форма Эргоферона, разработанная специально для детей, является эффективным и безопасным препаратом для лечения острых респираторных инфекций.
ЛИТЕРАТУРА
1. Лекарственные средства для детей. ВОЗ. Информационный бюллетень ¹ 341. Июнь 2010 г
2. ICH Harmonised Tripartite Guideline. Clinical Investigation of Medicinal Products in the Pediatric Population (E11). Current Step 4 version, July 2000; 12.
3. Геппе Н.А., Волков И.К. Актуальные вопросы детской пульмонологии в России. Вест Росс акад мед наук 2008; 10: 32—34.
4. Аверьянов А.В., Бабкин А.П., Барт Б.Я. и др. Эргоферон и Осельтамивир в лечении гриппа — результаты многоцентрового сравнительного рандомизированного клинического исследования. Антибиотики и химиотер 2012; 57: 7—8: 23—30.
5. Веревщиков В.К., Борзунов В.М., Шемякина Е.К. Оптимизация этио-патогенетической терапии гриппа и ОРВИ у взрослых при применении эргоферона. Антибиотики и химиотер 2011; 56: 9—10: 23—26.
6. Княжеская Н.П., Баранова И.А., Фабрика М.П., Белевский А.С. Новые возможности лечения и профилактики ОРВИ у пациентов с хроническими обструктивными заболеваниями лёгких. Атмосфера. Пульмонол аллергол 2012; 3: 46: 37—40.
7. Княжеская Н.П., Баранова И.А., Фабрика М.П., Татарский А.Р. Релиз-активные антитела в борьбе с простудой и гриппом. Фармате-ка 2013; 4: 257: 27—31.
8. Костинов М.П. Новый препарат для лечения гриппа и острых респираторных вирусных инфекций. Инфекц бол 2011; 9: 4: 29—34.
9. Орлова Н.В. Современные подходы к лечению гриппа. Фарматека 2012; 17: 250: 72—74.
10. Пескова Ю. В поисках новых препаратов для лечения гриппа и ОРВИ. Арх внутр мед 2013; 6: 14: 46—46.
11. Сидорова Л.Д., Бабанова С.А. Клиническая фармакология современного противовирусного препарата Эргоферон и его место в лечении острых респираторно-вирусных инфекций и гриппа. Справ поликлин врач 2013; 12: 38—41.
12. Шестакова Н.В., Загоскина Н.В., Самойленко Е.В., Минакова Е.Ю., Судакова А.П., Нургалиева Р.Н. Эффективность и безопасность применения Эргоферона в комплексной терапии внебольничных пневмоний. Доктор.ру, 2012; 8: 76: 44—47.
13. Шиловский И.П., Корнилаева Г.В., Хаитов М.Р. Новые возможности в терапии респираторно-синцитиальной вирусной инфекции: данные доклинического исследования препарата «Эргоферон». Иммунология 2012; 33: 3: 144—148.
14. Sergeeva S.A., Martyushev-Poklad A.V., Petrov V.I. et al. Anaferon, oral anti-interferon gamma antibodies for treatment and prophylaxic of viral infections. Clin Exper Pharmacol Psychol 2004; 31, Suppl 1: 114—14.
15. Волков И.К., Геппе Н.А. Применение релиз-активных препаратов на основе антител к интерферону гамма в лечении и профилактике респираторных инфекций у детей. Трудный пациент 2014; 2: 5: 10—16.
16. Кондюрина Е.Г. Анаферон детский в лечении и профилактике гриппа и ОРВИ у детей в современных условиях. Обоснование и существующие возможности. Поликлиника 2009; 6:118—119.
17. Эпштейн О.И., Бельский Ю.П., Шерстобоев Е.Ю., Агафонов В.И., Мартюшев А.В. Механизмы иммунотропных свойств потенцированных антител к человеческому интерферону-γ. Бюл экспер би-ол. Приложение ¹ 3, 2001: 34—36.
18. Эпштейн О.И., Дугина Ю.Л., Качанова М.В., Тарасов С.А., Хейфец И.А., Белопольская М.В. Противовирусная активность сверхмалых доз антител к гамма-интерферону. Вест международ акад наук (Русская Секция) 2008; 2: 20—23.
19. Tarasov S., Dugina Y., Sergeeva S., Epstein O. Oral antibody to interfer-on gamma in ultra low doses: clinical efficacy and interferon stimulation in patients with upper respiratory viral infections. Fundament Clin Pharmacol 2008; 22, Suppl 2: 37—37.
20. Tarasov S.A., Zarubaev V.V., Gorbunov E.A. Activity of ultra-low doses of antibodies to gamma-interferon against lethal influenza A(H1N1)2009 virus infection in mice. Antiviral Res 2012; 93: 2: 219—224.
21. Эпштейн О.И. Феномен релиз-активности и гипотеза «пространственного» гомеостаза. Успех физиол наук 2013, 44: 3: 54—76.
22. Эпштейн О.И., Штарк М.Б., Дыгай А.М. и др. Фармакология сверхмалых доз антител к эндогенным регуляторам функций. М.: Издательство РАМН. — 2005.
23. Жавберт Е.С., Дугина Ю.Л., Эпштейн О.И. Противовоспалительные и противоаллергические свойства антител к гистамину в релиз-активной форме: обзор экспериментальных и клинических исследований. Дет инфекц 2014; 1: 40—43.
24. Зак М.С. Экспериментальное исследование противокашлевой активности сверхмалых доз антител к морфину и медиаторам воспаления (брадикинин, серотонин, гистамин). Автореф. дисс. ... канд. мед. наук. М.: 2003; 24.
25. Carleton E., Fry B., Mulligan A., Bell A., Brossart C. Temporal artery thermometer use in the prehospital setting. CJEM 2012; 14: 1: 7—13.
26. Aindow A., Brook L. Essential Medicines List for Children (EMLc); Palliative Care. Consultation document. World Health Organisation. 2008; 116.
27. Лихорадочные синдромы у детей. Рекомендации по диагностике и лечению / Под ред. А.А. Баранова, В.К. Таточенко, М.Д. Бак-радзе. М.: Союз педиатров России, 2011; 228.
28. Клинические рекомендации. Педиатрия. Лихорадка / Под ред. А.А. Баранова. М.: ГЭОТАР-Медиа, 2007. 272 с.
29. Tecu C., Mihai M.E., Alexandrescu V.I. et al. Single and multipathogen viral infections in hospitalized children with acute respiratory infections. Roum Arch Microbiol Immunol 2013; 72: 4: 242-9.
30. Ершов Ф.И., Киселев О.И. Интерфероны и их индукторы. М.: Гэо-тар-Медиа 2005; 356.
31. Ellis T.N., Beaman B.L. Interferon-gamma activation of polymor-phonuclear neutrophil function. Immunology. 2004; 112: 2—12.
32. Chapman, T. J., M. R. Castrucci, R. C. Padrick, L. M. Bradley, and D. J. Topham. Antigen-specific and non-specific CD4 T cell recruitment and proliferation during influenza infection. Virology 2005; 340: 296—306.


