Вакцинация в профилактике обострений бронхиальной астмы у детей и подростков
Статьи

Пневмо 23
|
№2 (32) март - апрель 2004 г.
Вакцинация в профилактике обострений бронхиальной астмы у детей и подростков А.Б. Малахов Аллергические заболевания являются одной из наиболее важных проблем современной медицины [1]. За последние годы в России в целом и во Владимирской области, в частности, наблюдается отчетливый рост числа аллергических заболеваний с тенденцией к их более тяжелому течению, что нередко приводит к ухудшению качества жизни детей. В структуре аллергической патологии ведущее место принадлежит бронхиальной астме, заболеваемость которой в указанном регионе за последние десятилетие увеличилась более чем в 2 раза и составила 2,7%. Несмотря на достигнутые успехи в медикаментозном лечении, связанные с внедрением современных противовоспалительных и бронхолитических средств, сохраняется значительное число больных (7-14%), имеющих неконтролируемое течение заболевания. Факторами, способствующими обострению в детском возрасте, наиболее часто являются острые респираторные заболевания верхних и/или нижних дыхательных путей [1]. В этой связи, постоянный поиск средств доступной и эффективной профилактики обострений астмы представляется актуальной задачей. С точки зрения доказательной медицины наиболее эффективной профилактической мерой является вакцинация [4, 5, 7]. Следовательно, хроническая патология органов дыхания должна рассматриваться сегодня как показание для прививок, которые не только защитят ребенка от инфекции, но и, что особенно важно, предупредят обострение и прогрессирование основного заболевания, в конечном итоге, став надежным фактором профилактики формирования инвалидизирующих форм бронхиальной астмы [3]. Рисунок 1.
Цель настоящего исследования - оценка влияния вакцинации на течение бронхиальной астмы и профилактику ее обострений у детей и подростков. Под наблюдением находилось 82 ребенка в возрасте от 2 до 18 лет. Основную группу составили 60 пациентов с установленным диагнозом бронхиальной астмы не менее 1 года, из них с легким персистирующим течением - 22, со средней тяжестью - 21, с тяжелым - 17. Все дети имели неконтролируемое течение заболевания ввиду частых респираторных инфекций, повторяющихся бронхитов и\или пневмонии, которые провоцировали обострение основного патологического процесса. Группу сравнения составили 22 ребенка с бронхиальной астмой, идентичные по возрастно-демографическим и клинико-функциональным показателям, родители которых отказались от прививок. Вакцинация проводилась в соответствии с утвержденным дизайном исследования (рис. 1) поливалентной пневмококковой вакциной "Пневмо 23" и инактивированной гриппозной сплит-вакциной "Ваксигрип" (обе - производства Авентис Пастер, Франция) в виде моно- или сочетанного режима иммунизации. Вакцинация проводилась в спокойном от обострения периоде (ремиссии) на фоне базисной противовоспалительной терапии, соответствующей степени тяжести течения заболевания. Для определения влияния вакцинации на течение патологического процесса учитывались анамнестические данные за предыдущий и последующий иммунизации год. Оценивались следующие клинические критерии: количество обострений заболевания, длительность их течения, частота интеркуррентных инфекций и обострений очагов хронической инфекции. При мониторинге клинических симптомов обращали внимание на выраженность дневных и ночных симптомов по балльной системе, потребность в дополнительной терапии, величину пиковой скорости выдоха (ПСВ) и суточной лабильности бронхов. Активность течения патологического процесса оценивали также по объективным маркерам: уровень сывороточного IgE (в ИФА) и нитратов в конденсате выдыхаемого воздуха (спектрофотометрическим методом в реакции с реактивом Грисса). Дыхательный конденсат (КВВ) собирали, используя метод последовательного выдоха через рот в отсутствии носового дыхания, в S-образную трубку, помещенную в пробирку, опущенную в стакан со льдом [6]. Статистическую обработку полученных данных осуществляли при помощи программы Statistica for Windows 5.0. Рисунок 2.
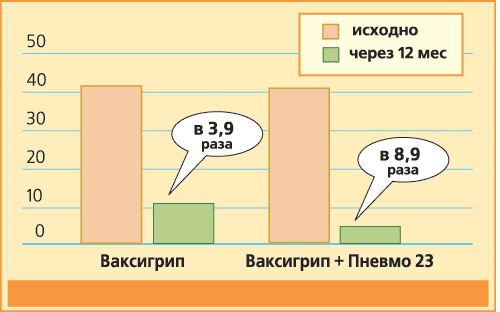
При оценке влияния вакцинации подтверждено, что иммунизация не стимулирует выработку общего IgE, показатель которого к концу первого месяца после иммунизации имел тенденцию к снижению по сравнению с исходным уровнем. Обращает внимание, что достоверно значимое снижение IgE происходило в подгруппе пациентов, не получавших антигистаминные препараты. При исследовании метаболитов оксида азота в КВВ выявлено их динамическое изменение: незначительное повышение в течение первого месяца и последующее достоверное снижение к 3 месяцу поствакцинального периода. Выявленный динамический феномен в уровне нитратов, по-видимому, лишь отражает несоответствие клинических и морфологических изменений в течение основного патологического процесса на фоне вакцинации. Подобные изменения были установлены нами ранее при использовании комбинированной противовоспалительной терапии у больных тяжелой бронхиальной астмой [2]. Важным моментом в оценке влияния вакцинации является анализ характера течения поствакцинального периода. Результаты исследования не выявили статистически значимых отклонений в группе привитых вне зависимости от варианта вакцинации (моно- или сочетанная) и тяжести течения бронхиальной астмы [2, 6]. Реакция на прививку в виде общих (субфебрильная температура тела) или местных (гиперемия в месте введения, болезненность) проявлений была слабой или умеренной и не требовала проведения медикаментозной коррекции (рис. 2). Эффективность вакцинации подтверждается также явным регрессом клинических проявлений болезни в течение последующего после вакцинации года. Так установлено достоверное снижение числа дней с явлениями обструкции, уменьшение длительности обострений в среднем на 3,7 дня. Уменьшение кратности обострений было различным и зависело от варианта вакцинации (рис. 3). Таким образом, проведенные исследования показывают, что вакцинация при бронхиальной астме, независимо от степени тяжести ее течения, не стимулирует активности аллергического воспаления в респираторной системе и атопических проявлений в целом. Наблюдается благоприятное течение поствакцинального периода, с уменьшением риска возникновения интеркуррентных заболеваний верхних и/или нижних дыхательных путей. Так заболеваемость ОРЗ среди привитых вакциной "Ваксигрип" снизилась в 13,3 раза по сравнению с непривитыми, среди привитых "Пневмо 23" - в 7,6 раза, среди привитых обеими вакцинами - в 21,2 раза. Вакцинация способствует более эффективному контролю над астмой при том же уровне базисной терапии, что в конечном итоге улучшает качество жизни больных и прогноз течения болезни. Рисунок 3.
Литература
© А.Б. Малахов, Н.Ю. Снегирева, М.А. Малахова-Капанадзе, Т.М. Пивикина, 2004 |