Применение высоких доз N-ацетилцистеина у пациентов со стабильным течением ХОБЛ
Статьи Опубликовано в издании:
CHEST 2013; 144 (1):106–118
Двойное слепое, рандомизированное плацебо-контролируемое исследование HIACE
Hoi Nam Tse , MBChB, FCCP ; Luca Raiteri , MD ; King Ying Wong , MBBS ; Kwok Sang Yee , MBBS ;
Lai Yun Ng , MBChB ; Ka Yan Wai , MBBS Ching Kong Loo , MBBS ; and Ming Houng Chan, MBBS
Состояние проблемы: Муколитические и антиоксидантные свойства N-ацетилцистеина (NAC) могут оказать благоприятный эффект при лечении ХОБЛ. Однако, в клинических исследованиях этот эффект не был подтвержден, что, возможно, объясняется или недостаточными дозами NAC, или использованием неадекватных параметров оценки. Целью настоящего исследования было изучение эффекта высоких доз NAC в дополнении к комплексной терапии у пациентов со стабильным течением ХОБЛ.
Методы: В двойном слепом, рандомизированном, плацебо контролируемоемконтролируемом исследовании HIACE, длившемся в течение 1 года и проводившемся в госпитале Kwong Wah в Гонконге, пациенты в возрасте от 50 до 80 лет со стабильным течением ХОБЛ после 4-х недельного вводного периода рандомизировались на две группы: группу, получавшую 600 мг NAC 2 р/день и группу плацебо. Оценка параметров: легочная функция, клинические симптомы, степень выраженности одышки по шкале mMRC (Medical Research Council), качество жизни по опроснику больницы Св. Георгия (SGRQ), данные теста 6-минутной ходьбы, частота обострений и частота госпитализаций проводилась в начале исследования и в дальнейшем каждые 16 недель в течение 1 года.
Результаты: Из 133 пациентов в исследование были включены 120 (93.2% мужчин; средний возраст 70.8±0.74 лет, FEV1 (%) =53.9±2.0%). Исходные характеристики в обеих группах были сопоставимы. Через 1 год в группе NAC было зарегистрировано достоверное увеличение FEF25%-75% (p=0.037), значимое снижение частоты обострений (0.96 /год против 1.71/год, p=0.196), значимое снижение частоты госпитализаций (0.5/год против 0.8 раз/год, p=0.196) в сравнении с группой плацебо. Не было получено значимых различий между группами по таким параметрам, как степень выраженности одышки по шкале mMRC, качество жизни по опроснику больницы Св. Георгия и результатам теста 6-минутной ходьбы. Серьезные побочные эффекты лечения в исследовании не отмечались.
Вывод: В настоящем исследовании лечение в течение года с применением высоких доз NAC привело к достоверному улучшению функции мелких дыхательных путей и снижению числа обострений у пациентов с ХОБЛ стабильного течения.
Регистр исследования: ClinicalTrials.gov; No.: NCT01136239; URL: www.clinicaltrials.gov
CHEST 2013; 144 (1):106–118
Обозначения: 6MWD- тест 6-минутной ходьбы; FDep-частотная зависимость; FEF25%-75% — средняя объемная форсированная скорость выдоха в интервале 25–75% FVC; МФО — метод форсированных осцилляций; Fres — резонансная частота; GSH-восста-новленный глутатион; IC-емкость вдоха; mMRC — модифицированная шкала одышки Медицинского исследовательского совета; NAC — N-ацетилцистеин; RCT — рандомизированное контролируемое исследование; RV/TLC — отношение остаточный объем/ общая емкость легких; SGRQ — респираторный опросник больницы Святого Георгия.
Дисбаланс в системе оксиданты/антиоксиданты играет ключевую роль в патогенезе ХОБЛ. Табакокурение — основной источник оксидантов и основная экзогенная причина окислительного стресса при ХОБЛ — стимулирует активность эластазы и индуцирует апоптоз, что приводит к повреждению паренхимы легких и развитию эмфиземы.1 Кроме того, оксиданты также активируют молекулярные механизмы — ряд факторов транскрипции и передачу клеточного сигнала, что вызывает экспрессию провоспалительных генов и запускает воспалительный каскад в легочной ткани и также системное воспаление2.
NAC для перорального приема — муколитическое средство, обладающее прямыми и непрямыми антиоксидантными свойствами, что может оказать благоприятный эффект при ХОБЛ.3 Прямое антиоксидантное действие NAC связано с нейтрализацией свободных радикалов, а непрямое действие обусловлено тем, что NAC выступает в роли предшественника глутатиона (GSH). NAC может восстанавливать нарушенный баланс в клеточной системе оксиданты-антиоксиданты и прерывает воспалительный каскад при ХОБЛ за счет ингибирования передачи клеточного сигнала и подавления экспрессии провоспалительных генов. 4–6
Тем не менее, в предыдущих исследованиях не было продемонстрировано клинического эффекта стандартных доз NAC у пациентов с хроническим бронхитом и ХОБЛ. Системные обзоры 7,8 показали, что NAC может снижать частоту обострений ХОБЛ по сравнению с плацебо. Однако, в рандомизированном плацебо-контролируемом двойном слепом 3-х летнем исследовании BRONCUS9 (Bronchitis Randomized on NAC Cost-Utility Study) не был продемонстрирован благоприятный эффект NAC на FEV1 и частоту обострений. Данное несоответствие, возможно, объясняется недостаточной дозой NAC (≤600 мг/день) 3 и/или применением неадекватных параметров оценки — как, например, FEV1 — маркера, не чувствительного к поражению мелких дыхательных путей и легочной гиперинфляции, и плохо коррелирующего с такими симптомами, как одышка и переносимость физической нагрузки. 10
В нашем исследовании для изучения возможного дозо-зависимого антиоксидантного и противовоспалительного эффекта NAC на течение ХОБЛ и легочную функцию, были использованы более высокие дозы NAC и более чувствительные к состоянию мелких дыхательных путей параметры — такие, как FEF25%-75% (средняя объемная форсированная скорость выдоха в интервале 25–75% FVC) и параметры метода форсированных осцилляций (МФО). Оба метода являются простыми, неинвазивными инструментами оценки функции мелких дыхательных путей. Определение FEF25%-75% — это недорогой метод 11,12 измерения среднего потока в интервале средней порции FVC. МФО — доступный метод оценки параметров респираторной механики (резистивного сопротивления — резистанса — и реактивного сопротивления — реактанса) посредством воздействия источника внешних колебаний воздуха во время спокойного дыхания. 13 В отличие от традиционной спирометрии (например, FEV1 ), которая преимущественно выявляет ограничение потока в крупных дыхательных путях, МФО способен дифференцировать поток в мелких и крупных дыхательных путях путем изменения частоты осцилляций (мультичастотный МФО). 13,14 Кроме того, показано, что МФО является более чувствительным методом оценки эффективности терапии по сравнению со спирометрией. 15
По нашим данным, это первое исследование, выполненное с участием Китайских пациентов, страдающих ХОБЛ, в котором состояние малых дыхательных путей оценивалось с помощью МФО на фоне приема высоких доз NAC (600 мг 2р/день).
МАТЕРИАЛЫ И МЕТОДЫ
Дизайн исследования и Методы
Данное двойное слепое, рандомизированное, плацебо-контролируемое исследоваиеисследование HIACE проводилось в госпитале Kwong Wah, Гонконг. 16 Проведение исследования было согласовано с Этическим комитетом (Kowloon-West-Cluster Clinical Research Ethical Committee, Hospital Authority, Hong Kong, KWC-REC reference: KW/EX-09–140).
Набор пациентов в исследование проводился на базе клини-ки ХОБЛ с 1 марта 2010 года по 28 февраля 2011 года. Включались пациенты в возрасте от 50 до 80 лет, со стабильным течением ХОБЛ и индексом FEV1 /FVCВ случае обострения у включенных в исследование пациентов они получали необходимое соответствующее лечение и вступали в исследование через 4 недели после разрешения обострения. Включенные пациенты подписывали информированное согласие и проходили 4-х недельный вводный период перед рандомизацией. Стандартная муколитическая терапия, в том случае, если она проводилась до этого, прекращалась во время этого 4-х недельного вводного периода. Пациенты с низкой комплаентностью и нежеланием участвовать исключались из исследования. Дизайн исследования представлен на рис. 1.
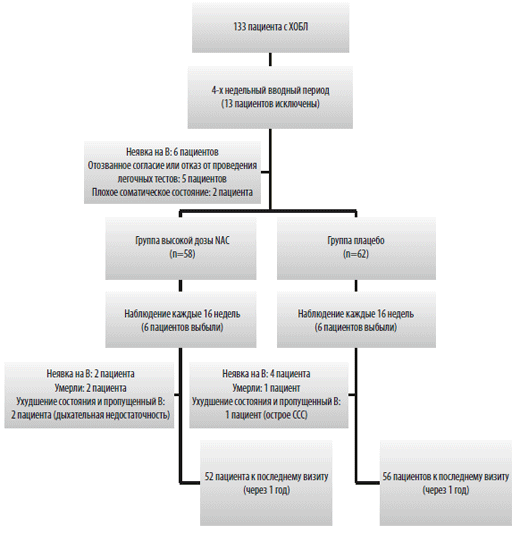
Рис. 1. Схема дизайна исследования. ССС-сердечно-сосудистое событие;
В-визит, NAC – N-ацетилцистеин
Рандомизация и ослепление
После 4-х недельного вводного периода, пациенты с ХОБЛ были рандомизированы на 2 группы: группу 600 мг NAC 2 р/день и группу плацебо. Для заослепления NAC и плацебо имели одинаковый внешний вид (шипучая таблетка 600 мг). Пациенты и врачи-исследователи не обладали информацией о лечении. Детали рандомизации и ветках терапии были известны только третьей стороне. Включенные в исследование пациенты находились под наблюдением своего лечащего врача, а NAC или плацебо назначались в дополнение к стандартному лечению ХОБЛ (в соответствии с рекомендациями GOLD (Global Initiative for Obstructive Lung Disease). 17
Оценка результатов
Исследователи проводили оценку процесса лечения каждые 16 недель в амбулаторных условиях. Первичными конечными точками в исследовании были показатели функции мелких дыхательных путей: FEF 25%-75% и параметры МФО. Также оценивались и другие показатели функции внешнего дыхания: емкость вдоха (IC), объем форсированного выдоха за 1 секунду (FEV1 ), жизненная емкость легких (FVC).
Вторичными конечными точками в исследовании были: частота обострений (обострение фиксировали при наличии двух из трех следующих симптомов: усиление одышки, увеличение объема или степени «гнойности» мокроты); частота госпитализаций по причине обострения ХОБЛ, степень выраженности одышки (по шкале mMRC — modifed Medical Research Council) и качество жизни (по респираторному опроснику больницы Святого Георгия SGRQ). Для использования опросника SGRQ в исследовании получали разрешение.
Перед началом исследования также фиксировалась следующая информация: демографические характеристики (возраст, пол), текущая терапия, сопутствующие заболевания (по опроснику), степень одышки по шкале mMRC, параметры легочной функции, качество жизни по опроснику SGRQ, результаты теста 6-минутной ходьбы.
Симптомы регистрировались во время каждого визита (каждые 16 недель). Врач оценивал приверженность к лечению путем подсчета оставшихся таблеток. Приверженность к лечению считалась хорошей в том случае, если пациент принимал более 70% назначений. Во время визитов регистрировались побочные эффекты, эпизоды обострений, и изменения в текущей терапии. Спирометрия, МФО, оценка качеству по опроснику SGRQ и тест 6-минутной ходьбы проводились на 0-й, 16-й и 52-й неделе.
Легочные тесты
Для оценки легочной функции во время исследования использовались спирометрия и МФО. Обе методики выполнялись прошедшим обучение средним медперсоналом. Спирометрия: Методика спирометрии выполнялась с использованием Spirobank-G (Medical Internetional Research USA Inc). Спирометрические параметры (FEV1, FVC, FEV1/FVC, %FEV1, FEF25%-75% и IC) измерялись в соответствии со стандартами Aмериканского Торакального Общества для легочных тестов. В качестве диапазона нормальных значений использовались референсные значения для Китая. Для оценки функции внешнего дыхания перед началом исследования проводили спирометрию и бодиплетизмографию (MedGraphics Elite Series Pletismograph; Medical Graphics Corp). Согласованность между методиками спирометрии и плетизмографии (FEV1 , FVC, FEF25%-75% и IC) проводили с использованием корелляционного анализа и анализа Бланда-Альтмана. Метод форсированных осцилляций. МФО выполняли с использованием 12m (Chess mt NV) с применением носового зажима и загубника для стабилизации положения языка пациента. Параметры механики дыхания измерялись с использованием мультичастотных (4–48 Гц), волн синусоидальной формы, при этом пациент находился в положении сидя и обеими руками поддерживал щеки, чтобы воздух не уходил. Перед каждым исследованием проводилась калибровка прибора прошедшим обучение средним медперсоналом в соответствии с рекомендациями Европейского респираторного общества. Считались воспроизводимыми значения с когерентной функцией минимум 95%. Рассчитывалось среднее из трех воспроизводимых измерений. Использовали следующие параметры МФО: резонансная частота (Fres), частота, при которой реактивное сопротивление равно нулю, частотная зависимость (Fdep), наклон кривой резистивное сопротивление-частота осцилляций, резистивное сопротивление при частоте 6 Гц, и реактивное сопротивление при частоте 6 Гц.
Статистические методы.
Размер выборки рассчитывался таким образом, чтобы получить 20% увеличение параметров МФО (резистивного и реактивного сопротивления) в группе NAC по сравнению с группой плацебо, с ошибкой α=0.05 и мощностью исследования=0.8. Стандартные отклонения для реактивного и резистивного сопротивления из предыдущего исследования 21 были взяты в качестве референсных значений. Необходимый минимальный объем выборки 86 пациентов был соблюден в нашем исследовании.
Статистический анализ проводился с использованием программы SPSS, версия 20.0 (IBM). Данные представлены в виде среднее значение±стандартная ошибка среднего. Все статистические тесты были двусторонними. Различия считались достоверными при p2-теста. Анализ изменения параметров функции легких и других параметров проводили с помощью парного t-теста и анализа вариативности повторных измерений для выявления статистически достоверных различий между группами по исследованным параметрам легочной функции в различные временные точки.
РЕЗУЛЬТАТЫ
Выборка
Из 133 набранных в исследование пациентов с ХОБЛ, 13 были исключены во время вводного периода (рис. 1): восемь пациентов отозвали свое согласие, четыре пациента выпали из-под наблюдения, и один пациент отказался от проведения легочных тестов. Из оставшихся 120 пациентов, 58 были распределены в группу NAC высокой дозы, и 62 — в группу плацебо. В течение года наблюдения 12 пациентов вышли из-под наблюдения и 108 завершили исследование (NAC, n=52; плацебо, n=56).
Исходные характеристики пациентов
Демографические характеристики пациентов суммированы в таблице 1: исходно между группами не было значимых различий. Частота обострений ХОБЛ и госпитализаций за предшествующий год также были сопоставимы. Большинство пациентов были люди старшего возраста, в основном мужчины, курильщики, страдающие ХОБЛ средней и тяжелой степени (Таблица 1,2). Сопоставимыми в обеих группах были также процент пациентов, получавших иГКС, агонисты мускариновых рецепторов длительного действия и комбинацию β2-агонисты длительного действия +иГКС.
Таблица 1.
Исходные демографические характеристики больных ХОБЛ в группе NAC и в группе плацебо
| Демографические характеристики | Группа высокой дозы NAC (n=58) | Группа плацебо (n=62) | Р |
|---|---|---|---|
| Возраст, средн±станд.ошибка | 71.0±1.08 | 70.8±1.05 | 0.89(НД) |
| Пол Мужчины | 93.1 (54/58) 6.9 (4/58) | 93.5 (58/62) 6.5 (58/62) | 1.0 (НД)... |
| Вес, средн±станд.ошибка, кг | 59.5±1.55 | 58.3±1.51 | 0.58(НД) |
| Рост, средн±станд.ошибка, см | 161.2±0.88 | 159.8±0.78 | 0.49(НД) |
| ИМТ, средн±станд.ошибка, кг/м2 | 22.8±0.52 | 22.8±0.52 | 0.94 (НД) |
| Статус курения | |||
| Курильщики | 25.9 (15/58) | 21.0 (13/62) | 0.56(НД) |
| Некурящие | 74.1 (43/58) | 79.0 (49/62) | … |
| Одышка по шкале mMRC, a мед. | 2 (1.2) | 2 (1.2) | 0.14(НД) |
| 0 | 3.4 (2/58) | 0 (0/62) | |
| 1 | 17.2 (10/58) | 11.3 (7/62) | |
| 2 | 44.8 (26/58) | 62.9 (39/62) | |
| 3 | 34.5 (20/58) | 25.8 (16/62) | |
| 4 | 0 (0/58) | 0 (0/62) | |
| Стадия ХОБЛ по GOLD, мед.(разброс) | 2 (2.3) | 2 (2.3) | |
| 1 | 17.2 (10/58) | 19.4 (12/62) | 0.65(НД) |
| 2 | 41.4 (24/58) | 38.7 (24/62) | |
| 3 | 31.1 (18/58) | 37.1 (23/62) | |
| 4 | 10.3 (6/58) | 4.8 (3/62) | |
| Сопутствующие заболевания | 41.4 (24/58) | 51.6 (32/62) | 0.35(НД) |
| Обострения ХОБЛ за последний год, мед. (разброс) | 2 (1.4) | 2 (1.4) | 0.84(НД) |
| Госпитализации в связи с ХОБЛ за последний год, мед. (разброс) | 1 (0.3) | 1 (0.2) | 0.13(НД) |
| Медикаментозная терапия, % | |||
| КДБА | 98.3 | 95.2 | 0.66(НД) |
| КДМА | 51.7 | 41.9 | 0.37(НД) |
| иГКС | 74.1 | 83.9 | 0.28(НД) |
| ДДМА | 41.4 | 48.4 | 0.56(НД) |
| ДДБА+иГКС | 36.2 | 33.9 | 0.94(НД) |
| Данные представлены в процентном отношении, если не указано другое. GOLD — Глобальная инициатива по ХОБЛ; иГКС — ингаляционные глюкокортикостероиды; ДДБА — β-агонисты длительного действия; ДДМА — агонисты мускариновых рецепторов длительного действия; mMRC- модифицированная шкала Мedical Research Council; NAC — N-ацетилцистеин; НД — не достоверно; КДБА — β-агонисты короткого действия; КДМА — агонисты мускариновых рецепторов короткого действия. * Параметры легочной функции измерялись с помощью плетизмографии. | |||
Визиты
Легочные тесты: Спирометрия (Spirobank-G) — результаты FEV1 , FVC, FEF25%-75% , IC удовлетворяли критериям по методу Бланда-Альтмана. Была также получена высокая линейная корреляция между величинами FEV1 , FVC, FEF (R2>0,9), измеренными с помощью спирометрии и плетизмографии. Линейная зависимость между измерениями IC методами спирометрии и плетизмографии, была не такой высокой (R2=0.55).
Исходно между группами не было достоверных различий по параметру FEF25%-75% . В течение года наблюдения, получено достоверное увеличение FEF25%-75% в группе NAC (с 0.72±0.07 л/с до 0.8±0.07 л/с, тогда как в группе плацебо этот показатель остался неизменным (с 0.679±0.07 л/с до 0.677±0.07 л/с) (анализ вариативности повторных измерений, P=0.037) (Рис. 2А). Как показано на рис. 2В, в группе NAC получено значимое увеличение параметра FEF25%-75% относительно исходных значений по сравнению с группой плацебо как на 16-й неделе (+0.08 л [11.6%] против +0.008 л [1.2%]), так и на 52-й неделе (+0.08 л [11.6%] против — 0.002 л [-2.9%]). Статистически достоверных различий других спирометрических показателей (FEV1 , FVC, IC) между группами за период наблюдения не было выявлено. (Таблица 3).
A. 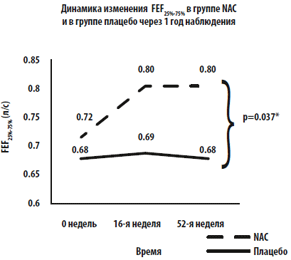 B.
B.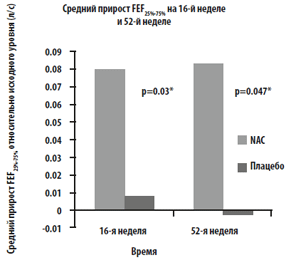
Рис. 2. А. Динамика FEF25%-75% (л/с) в обеих группах за год наблюдения.
B. Средний прирост FEF25%-75% относительно исходного уровня в обеих группах на 16-й и 52-й неделе.
FEF25%-75% - средняя объемная форсированная скорость выдоха в интервале 25-75% FVC.
См. обозначения к рис.1 для остальных аббревиатур.
МФО: Через 1 год наблюдения показатель реактивного сопротивления значимо улучшился в группе NAC по сравнению с группой плацебо: реактивное сопротивление при 6 Гц увеличилось в группе NAC, тогда как в группе плацебо этот показатель ухудшился: (+0.48 [+22.3%] против –0.22 [-10.7%]; P=0.04), также резонансная частота FRes достоверно снизилась в группе NAC по сравнению с группой плацебо: (–5.86 [-21.7%] против –1.03 [-3.7%]; P=0.02) (Рис. 3).
A.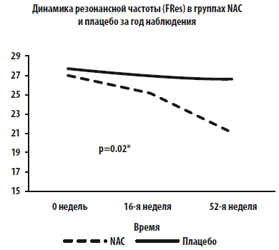 B.
B.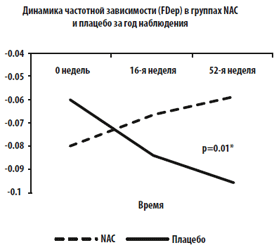 C.
C.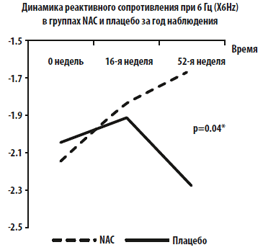 D.
D.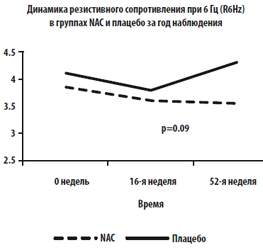
Рис. 3 А-D. Тренд и динамика параметров метода форсированных осцилляций (МФО) за год наблюдения в группе NAС и группе плацебо.
На рисунках отображены изменения: (А) Fres (P=0.02), (B) FDep (P=0.01), (C) реактивного сопротивления
при 6 Гц (P=0.04) и (D) резистивного сопротивления при 6 Гц (Р=0.09).
*P
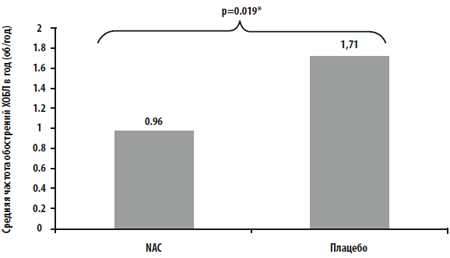
Рис. 4. Частот обострений ХОБЛ в группе NAC и группе плацебо за год наблюдения.
*Р
Частота обострений ХОБЛ: Из 146 зарегистрированных во время исследования эпизодов обострения ХОБЛ, 50 произошли в группе NAC и 96 — в группе плацебо. Средняя частота обострений ХОБЛ течение года в группе NAC была достоверно ниже (0.96/год в группе NAC и 1.71/год в группе плацебо, P=0.019). (Рис. 4). Более того, на момент завершения исследования в группе NAC была больше доля пациентов без обострений по сравнению с группой плацебо (53.8% против 37.5%), хотя эти различия не достигли уровня статистической значимости (P=0.088) (Рис. 5).
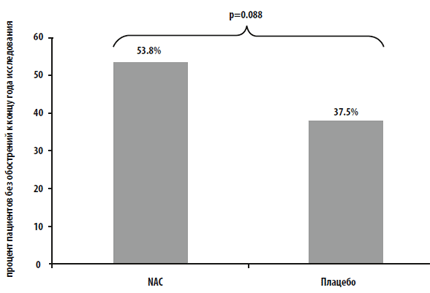
Рис. 5. Доля пациентов без обострений ХОБЛ на момент окончания исследования
Частота госпитализаций вследствие обострения ХОБЛ: Аналогичные результаты были получены и для частоты госпитализаций вследствие обострений ХОБЛ во время исследуемого периода, хотя они и не достигли уровня статистической значимости: всего 71 случаев госпитализации (26 в группе NAC и 45 в группе плацебо). Среднее число госпитализаций было меньше в группе NAC (0.5/год против 0.8/год; P=0.196), а также в группе NAC была меньше длительность госпитализаций (1.8 дней/год против 4.2 дней/год; P=0.08). (Рис. 6). Кроме того, между группами не было значимых различий по степени выраженности респираторных симптомов (по шкале одышки mMRC), качеству жизни (SGRQ), и толерантности к физическим нагрузкам (тест 6-минутной ходьбы) (P-не достоверно) (Таблица 4).
A.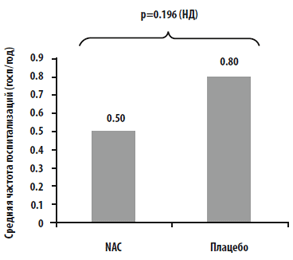 B.
B. 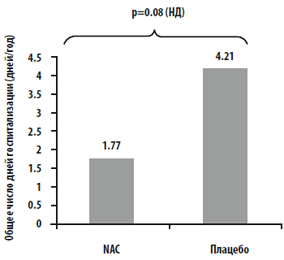
Рис. 6. A, B Сравнение (А) частоты госпитализаций в связи с обострениями ХОБЛ и (В)
общей продолжительности госпитализации в связи с обострениями ХОБЛ между группами NAC и группой плацебо за 1 год наблюдения.
НД — не достоверно. См. обозначения к рис. 1 для объяснения аббревиатур
Таблица 2.
Исходные параметры легочной функции больных ХОБЛ в группе NAC и в группе плацебо
| Параметр | Группа высокой дозы NAC (n=58) | Группа плацебо (n=62) | P |
|---|---|---|---|
| Пре-БД FEV1 , л | 1.17±0.08 | 1.16±0.07 | 0.94 (НД) |
| Пре-БД %FEV1 | 53.4±3.0 | 54.3±0.07 | 0.83 (НД) |
| Пре-БД FVC, л | 2.31±0.09 | 2.32±0.08 | 0.92 (НД) |
| Пре-БД %FVC | 78.3±2.4 | 81.3±2.3 | 0.36 (НД) |
| Пре-БД FEV1 / FVC | 49.6±1.8 | 49.1±1.7 | 0.83 (НД) |
| Пост-БД FEV1 , л | 1.32±0.08 | 1.25±0.07 | 0.56 (НД) |
| Пост-БД %FEV1 | 60.6±3.2 | 58.6±2.7 | 0.64 (НД) |
| Пост-БД FVC, л | 2.51±0.09 | 2.52±0.08 | 0.93 (НД) |
| Пост-БД %FVC | 85.6±2.41 | 88.0±2.36 | 0.47(НД) |
| Пост-БД FEV1 /FVC | 51.1±1.82 | 49.0±1.59 | 0.38 (НД) |
| FEF25%-75% , л/с | 0.54±0.06 | 0.54±0.05 | 0.99 (НД) |
| % FEF 25%-75% | 29.2±2.76 | 29.4±2.47 | 0.97 (НД) |
| IC, л | 1.55±0.07 | 1.55±0.06 | 0.99 (НД) |
| %1С | 56.7±2.20 | 58.0±2.16 | 0.66 (НД) |
| RV, л | 3.58±0.25 | 3.56±0.17 | 0.94 (НД) |
| %RV | 167.1±12 | 167.4±8.4 | 0.99 (НД) |
| TLC, л | 6.02±0.23 | 6.02±0.17 | 0.99 (НД) |
| %TLC | 104.9±4.6 | 113.2±6.0 | 0.28 (НД) |
| RV/TLC | 0.57±0.02 | 0.58±0.02 | 0.77 (НД) |
| Данные представлены в виде среднее±стандартная ошибка, если не указано другое. БД — бронходилататор; FEF25%-75% — средняя объемная форсированная скорость выдоха в интервале 25–75% FVC; IC-емкость вдоха; RV- остаточный объем; TLC-жизненная емкость легких. См. обозначения к табл. 1 для остальных аббревиатур. | |||
Побочные эффекты
Серьезных побочных эффектов не было зарегистрировано ни в одной из групп. Не наблюдалось увеличения частоты незначительных побочных эффектов в группе NAC (3 из 58 [5.2%] по сравнению с группой плацебо (5 из 62 [8%]) (Таблица 5). Три пациента умерли за год наблюдения: один, получавший плацебо (вследствие острой почечной недостаточности) и два, получавшие NAC (острый ишемический инсульт и пневмония); все случаи не имели связи с лечением.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Дозо-зависимый эффект NAC: применение высоких доз NAC
В нашем исследовании показано достоверное улучшение показателей FEF25%-75% и реактивного сопротивления (реактивного сопротивления при 6 Гц и резонансной частоты FRes) при применении высоких доз NAС по сравнению с плацебо. Малые дыхательные пути (обычно определяемые как дыхательные пути с внутренним диаметром менее 2 мм, не имеющие хрящевой основы) являются основным местом ограничения воздушного потока при астме и ХОБЛ. 22 Сопротивление воздушному потоку обратно пропорционально четвертой степени радиуса. Поэтому утолщение стенки дыхательных путей, так же как и внутрипросветная закупорка слизисто-воспалительным экссудатом, уменьшающая внутренний радиус дыхательных путей, являются независимыми факторами, вызывающими ограничение воздушного потока. 23 Закупорка малых дыхательных путей слизисто-воспалительным экссудатом выявлялась и ранее при аутопсии, но только недавно у лиц с ХОБЛ, подвергшихся резекции легких, была доказана непосредственная связь ограничения воздушного потока и закупорки слизисто-воспалительным экссудатом, 24 и у пациентов с ХОБЛ при жизни был обнаружен экссудат в малых дыхательных путях.25
Таблица 3.
Изменение параметров легочной функции (по методу спирометрии) относительно исходных значений на 16-й и 52-й неделе в группе NAC и группе плацебо
| Параметр | Лечение | Изменение на 16-й неделе | P | Изменение на 52-й неделе | P |
|---|---|---|---|---|---|
| FEF 25%-75% л/с | NAC Плацебо | +0.080±0.03 +0.080±0.02 | … 0.03 | +0.082±0.03 -0.002±0.03 | … 0.47а |
| FEV1 , л | NAC Плацебо | +0.12±0.06 +0.04±0.03 | … 0.2 | +0.07±0.33 +0.05±0.04 | … 0.7 |
| FVC, л | NAC Плацебо | +0.14±0.06 +0.10±0.05 | … 0.59 | +0.13±0.05 +0.06±0.06 | … 0.42 |
| IC, л | NAC Плацебо | -0.10±0.07 -0.03±0.59 | … 0.83 | +0.13±0.07 +0.49±0.08 | … 0.73 |
См. обозначения к табл. 1 и табл. 2 для объяснения аббревиатур.
* Статистически достоверное значение (р≤0.05).
Обычно определение обструкции дыхательных путей требует, что бы индекс FEV1 /F VC бы л менее 70%.26 На самом деле, индекс FEV1 /FVC не очень хорошо отражает состояние малых дыхательных путей,27 и поэтому в качестве маркеров повреждения дистальных отделов дыхательных путей обычно оценивают другие параметры спирометрии и бодиплетизмографии. FEF25%-75% — один из наиболее часто применяемых для выявления обструкции малых дыхательных путей спирометрических показателей23, он тесно коррелирует с индексом FEV1 /FVC, однако у больных с легкой степенью заболевания при возрастании обструкции наблюдается более резкое его снижение по сравнению с FEV1 /FVC. Другие проблемы при применении FEF25%-75% связаны с тем, что его значение зависит от усилий пациента, отмечается его вариабельность при измерениях, и кроме того, поскольку при бронхо-дилатациии и легочной инфляции возможны изменения FVC, меняется диапазон легочного объема, относительно которого рассчитывается FEF25%-75%23.
МФО является методом, позволяющим оценить ограничение экспираторного потока — ключевого момента в патогенезе ХОБЛ, поскольку именно это вызывает динамическую гиперинфляцию28. Метод представляет собой подачу внешних периодических колебаний воздуха во время спокойного дыхания пациента, что приводит к изменению респираторного потока.23 По соотношению изменений давления подаваемого воздуха и колебаний респираторного потока вычисляется резистивное и реактивное сопротивление. 23 Реактивное сопротивление определяется как эластическими свойствами дыхательных структур (при низких частотах вклад этой составляющей максимален), и также инерционного сопротивления аппарата вентиляции, которое увеличивается с частотой. 23
Ранее было показано, что резистивное сопротивление при низкой частоте осцилляций и FDep являются чувствительными индикаторами проходимости малых дыхательных путей, 13,14 и была доказана их высокая корреляция с результатами теста вымывания азо-та. 29 В настоящее время получены доказательства того, что FDep высоко коррелирует с рядом клинических параметров — например, выраженностью одышки при физической нагрузке у пациентов с ХОБЛ30 и достаточно чувствителен для выявления ранних стадий респираторных заболеваний у пациентов группы риска — курильщиков — даже в тех случаях, когда стандартные параметры легочной функции еще остаются в пределах нормальных значений. 31,32
На настоящий момент нет опубликованных данных о влиянии противовоспалительного лечения (например, иГКС) на изменение параметров осциллометрии у больных ХОБЛ, хотя имеются данные о влиянии воспаления на реактивное сопротивление у больных с ХОБЛ при обострении. 23 По нашим сведениям, это первое исследование, в котором проводилась подобная оценка и доказана эффективность высокой дозы NAC в улучшении функции малых дыхательных путей у больных ХОБЛ. Хотя в большинстве проведенных ранее исследований не была доказана эффективность NAC 600 мг/день у больных ХОБЛ, 9, 33, 34 наше исследование продемонстрировало, что прием высокой дозы NAC (600 мг 2 р/день) в течение года улучшает функцию дистальных дыхательных путей у пациентов, страдающих ХОБЛ.
Различия в результатах между нашим и предыдущими исследованиями может быть обусловлено более высокими дозами NAC, поскольку известно, что антиоксидантный эффект NAC является дозозависи-мым.3 В исследованиях in vitro было показано, что муколитический эффект NAC проявляется и при низких дозах, тогда как антиоксидантный эффект начинает проявляться только при высоких дозах (1.200–1.800 мг в день). Действительно, у человека биодоступность NAC составляет лишь 6%-10%, поэтому, если требуется антиоксидантный эффект, нужны более высокие дозы NAC.
Кроме того, есть данные, свидетельствующие о том, что увеличение дозы NAС может приводить к увеличению его биодоступности и снижению времени достижения максимальной концентрации в плазме. 39
Недостаточность «низких доз» NAC была продемонстрирована в исследовании Cotgreave5: доза 600 мг в день не приводила к изменению уровней цистеина и GSH в жидкости бронхоальвеолярного лаважа у здоровых лиц. Аналогичные результаты были получены в исследовании Bridgeman и соавт. 40, подтвердивших, что через 5 дней применения высоких доз NAC (600 мг 2 р/день) увеличивается уровень GSH у пациентов с ХОБЛ, а при низкой дозе (600 мг в день) такой эффект не наблюдался. Кроме того, показано, что высокая доза NAC (1200 мг/день) снижает содержание пероксида водорода в выдыхаемом воздухе (источник окислительного стресса) у пациентов со стабильным течением ХОБЛ, 41 тогда как через 6 месяцев терапии низкими дозами NAC (600 мг/день) такого эффекта не наблюдалось. 42 Эти данные подтверждают наше предположение о том, что для достижения ан-тиоксидантного эффекта нужны высокие дозы NAC (≥1200 мг/день). Kasielski и соавт. 42 показали, что низкие дозы NAC (600 мг/день) могут снижать содержание пероксида водорода в выдыхаемом воздухе через 9–12 месяцев лечения, но не через 6 месяцев. Это может означать, что для достижения эффекта от низких доза NAC требуется более долгосрочная терапия. Кроме того, данные о более высокой эффективности высокой дозы NAC были получены в исследовании IFIGENIA (Study of the Efects of High-Dose N-Acetylcysteine in Idipathic Pulmonary Fibrosis), в котором применение высокой дозы NAC (1800 мг/день) в течение года в дополнение к стандартной терапии у пациентов с идиопатическим легочным фиброзом приводило к достоверному и клинически значимому улучшению диффузионной способности легких и жизненной емкости.
Влияние высокой дозы NAC на функцию легких
Механизм действия высокой дозы NAC на малые дыхательные пути: NAC непосредственно нейтрализует свободные радикалы и, кроме того, выступает предшественником глутатиона — основного тиольного внутиклеточного антиоксиданта. Следовательно, NAC может восстанавливать нарушенный окислительно-восстановительный статус клетки, модифицировать каскад воспалительных реакций за счет ингибирования редокс-чувствительных факторов передачи сигнала в клетках и экспрессии провоспалительных генов.4–6 Действительно, исследования in vitro показали, что NAC снижает вызванное пероксидом водорода повреждение эпителиальных клеток. 44 Высокие дозы NAC также уменьшают толщину стенок эпителия дыхательных путей и снижают гиперплазию бокаловидных клеток у крыс, вызванную табачным дымом. 45,46 Более того, у человека NAС увеличивает содержание GSH в жидкости БАЛ47 и снижает содержание пероксида водорода в выдыхаемом воздухе. 41,42 Этими противовоспалительными эффектами можно объяснять улучшение функции малых дыхательных путей на фоне приема NAC.
Влияние высоких доз NAC на гиперинфляцию: Положительное влияние высоких доз NAC на гиперинфляцию легких показано в предыдущих исследованиях. Анализ данных крупного, 3-х летнего исследования BRONCUS 9 показал, что NAC уменьшает гиперинфляцию даже при низких дозах. Другое рандомизированное, контролируемое исследование 48 доказало, что NAC в дозе 1200 мг/день уменьшал гиперинфляцию через 12 недель: было продемонстрировано увеличение постнагрузочных значений IC и FRC, а также снижение соотношения остаточный объем/общая емкость легких (RV/TLC) по сравнению с плацебо. Это единственное исследование 48, в которое включались пациенты со стабильным течением ХОБЛ (степень тяжести от умеренной до тяжелой, FEV1Существует несколько предполагаемых механизмов положительного влияния антиоксидантов (в частности, высоких доз NAC) на гиперинфляцию при ХОБЛ. Во-первых, антиоксиданты могут непосредственно предотвращать развитие эмфиземы: в доклинических исследования на крысах было показано, что пероральный прием NAC снижал индуцированное эластазой повреждение. 49,50 Во-вторых, положительное воздействие на гиперинфляцию может объясняться антиоксидантным и противовоспалительным действием NAC на дистальные дыхательные пути при ХОБЛ.
Это предположение согласуется с полученными нами результатами: применение NAC в высокой дозе (600 мг 2 р/ день) уменьшало сопротивление в мелких дыхательных путях больных ХОБЛ, что выражалось значимым повышением FEF25%-75% и улучшением параметров МФО при ХОБЛ стабильного течения. Это снижение сопротивления приводило к уменьшению гиперинфляции в группе пациентов ХОБЛ с эмфиземой. Тем не менее, в нашем исследовании не получено достоверного увеличения IC и FVC на фоне приема NAC. В отличие от описанных выше рандомизированных контролируемых иссле-дований, 48 показавших благоприятный эффект NAC у пациентов с преимущественно эмфиземой (среднее значение RV/TLC=137% долж.), в нашем исследовании была гетерогенная выборка пациентов с различной степенью гиперинфляции. Эта гетерогенность, возможно, и послужила причиной отсутствия увеличения IC.
Таблица 4.
Динамика качества жизни по опроснику SGRQ, теста 6-минутной ходьбы и степени выраженности одышки по шкале mMRC на фоне приема NAС и плацебо
| Параметр | NAC | Плацебо | P |
|---|---|---|---|
| Баллы по SGRQ | |||
| Симптомы | |||
| Исходно, 0 неделя | 36.6±3.3 | 30.7±3.1 | 0.20 (НД) |
| 52 неделя | 30.2±3.3 | 24.1±2.9 | 0.18 (НД) |
| Изменение, 52 нед – 0 нед | -6.4±3.4 | -8.3±3.7 | 0.72 (НД) |
| Активность | |||
| Исходно, 0 неделя | 44.4±3.6 | 46.1±3.0 | 0.73 (НД) |
| 52 неделя | 46.3±4.4 | 40.5±3.5 | 0.31 (НД) |
| Изменение, 52 нед – 0 нед | +0.8±3.6 | -5.5±3.4 | 0.21 (НД) |
| Влияние | |||
| Исходно, 0 неделя | 21.0±2.1 | 24.4±2.2 | 0.27 (НД) |
| 52 неделя | 18.8±1.8 | 17.0±1.9 | 0.50 (НД) |
| Изменение, 52 нед – 0 нед | -3.5±2.1 | -8.4±2.0 | 0.10 (НД) |
| Общая оценка | |||
| Исходно, 0 неделя | 30.9±2.5 | 32.0±2.2 | 0.74 (НД) |
| 52 неделя | 28.4±2.3 | 25.3±2.2 | 0.34 (НД) |
| Изменение, 52 нед – 0 нед | -3.3±2.1 | -7.4±2.2 | 0.19 (НД) |
| Тест 6-минутной ходьбы, м | |||
| Исходно, 0 неделя | 327.9±11.6 | 338.7±9.9 | 0.47 (НД) |
| 52 неделя | 339.4±12.4 | 348.6±12.5 | 0.61 (НД) |
| Изменение, 52 нед – 0 нед | +15.8±7.3 | +6.4±6.6 | 0.34 (НД) |
| Баллы по шкале mMRC | |||
| Исходно, 0 неделя, мед. (разброс) | 2 (1.3) | 2 (2.3) | 0.47 (НД) |
| 52 неделя | 2 (1.2) | 2 (1.2) | 0.26 (НД) |
| Изменение, 52 нед – 0 нед | 0 (-1.0) | 0 (-1.0) | 0.49 (НД) |
| Данные представлены в виде среднее±стандартная ошибка, если не указано другое. SGRQ — респираторный опросник госпиталя Святого Георгия. См. обозначения к рис. 1 для объяснения остальных аббревиатур. | |||
Влияние высоких доз NAC на частоту обострений
На фоне применения высоких доз NAC наблюдалось достоверное снижение частоты обострений ХОБЛ (снижение составило 0.75/год), что согласуется с данными системного обзора7 по применению муколитической терапии при ХОБЛ/бронхите, на основании которого был сделан вывод, что пероральный прием муколитиков снижает частоту обострений в 2 раза по сравнению с плацебо. Более того, крупномасштабное рандомизированное плаце-бо контролируемое исследование PEACE51 (Efect of Carbocisteine on Acute Exacerbations of COPD), в котором изучалось длительное применение муколитиков (карбоцистеина) при ХОБЛ показало, что карбоцистеин в дозе 1500 мг достоверно снижал частоту обострений у Китайских пациентов, страдающих ХОБЛ.
Таблица 5.
Побочные эффекты в группе NAC и группе плацебо
| Эффект | Группа высокой дозы NAC | Группа плацебо |
|---|---|---|
| Серьезные осложнения | 0 | 0 |
| Симптомы ГЭРБ | 1 | 3 |
| Диарея | 1 | 0 |
| Сухость во рту | 1* | 1 |
| Боль в суставах и мышцах | 1* | 0 |
| Усиление кашля | 0 | 1 |
| Общее число, доля (%) | 3/58 (5.2) | 5/62 (8.0) |
| Данные представлены в виде количественного значения, если не указано другое. ГЭРБ — гастроэзофагальная рефлюксная болезнь. См. обозначения к табл. 1 для объяснения других аббревиатур. * Один человек пожаловался на сухость глаз и боль в мышцах | ||
Мы предполагаем, что подобное снижение частоты обострений ХОБЛ может быть обусловлено антиоксидантным и противовоспалительным действием высоких доз NAC, в результате чего улучшается функция малых дыхательных путей, что и продемонстрировало наше исследование (улучшение показателя FEF25%-75% и параметров МФО). Это улучшение функции малых дыхательных путей может снижать гиперинфляцию48 и снижать частоту обострений ХОБЛ.
Более того, поскольку слизь и воспаленный эпителий являются благоприятной средой для присоединения бактериальной инфекции, 52, возможно, NAC снижает частоту обострений за счет подавления адгезии бактерий к клеткам реснитчатого эпителия. Кроме этого, муколитическое действие NAC может снижать вязкость слизи и мокроты в дыхательных путях, что также препятствует связыванию рецепторов клеток эпителия с бактериями. Исследования in vitro подтверждают эти предположения, свидетельствуя о том, пероральный прием муколитиков снижает адгезию бактерий к клеткам фарингеального эпителия у здоровых лиц. 52, 53
Влияние высоких доз NAC на частоту госпитализаций, степень выраженности одышки, качество жизни и толерантность к физическим нагрузкам
Кроме снижения частоты обострений ХОБЛ, на фоне приема NAC по сравнению с плацебо наблюдалась тенденция к снижению числа госпитализаций в связи с ХОБЛ (0.5 р/год против 0.8 р/год; P=0.196) и средней длительности госпитализации (1.8 дней/год против 4.2 дней/год, P=0.8), хотя различия не достигли уровня статистической достоверности. Эти результаты согласуются с данными системного обзора7, показавшего, что пероральный прием муколитиков может снижать число дней нетрудоспособности (–0.56, 96% ДИ; от –0.77 до –0.35) и риск госпитализации.
Ретроспективные исследования показали, что прием NAC ассоциировался с 30%-ным снижением риска повторной госпитализации в связи с ХОБЛ, и это снижение было дозоза-висимым.54
Мы полагаем, что различия частоты госпитализаций не достигли уровня достоверности в нашем исследовании из-за недостаточного размера выборки. Для оценки соотношения стоимость-эффективность высоких доз NAC в плане снижения частоты госпитализаций, уменьшения числа обращений за медицинской помощью и снижения затрат на госпитализации, необходимы дальнейшие исследования с бо?льшим размером выборки.
Наше исследование не показало значимого улучшения симптомов ХОБЛ, толерантности к физической нагрузке и параметров качества жизни на фоне приема высоких доз NAC. Этому может быть несколько возможных объяснений. Во-первых, маленький объем выборки не обеспечивает адекватной статистической мощности исследования, и поэтому изменение этих клинических параметров не достигло уровня достоверности. Во-вторых, NAC, как и бронходилататоры, воздействуют на течение ХОБЛ благодаря антиоксидантным, противовоспалительным и муколитическим свойствам. Следовательно, NAC могут не оказывать прямого воздействия на одышку у пациентов с ХОБЛ, несмотря на то, что благоприятное влияние NAC на функцию мелких дыхательных путей было доказано в нашем исследовании.
Безопасность длительной терапии NAC
В нашем исследовании была продемонстрирована безопасность и хорошая переносимость длительного применения NAC в дозе 600 мг 2р/день. Не было выявлено достоверных различий в частоте побочных эффектов между группами NAC и плацебо (5.2% против 8%). Наиболее часто в нашем исследовании отмечались побочные явления со стороны ЖКТ: диарея и гастроэзофагальный рефлюкс. Серьезные побочные эффекты не отмечались. Существуют данные о длительном применении более высоких доз NAC (1800 мг/день) при интерстициальном легочном фи-брозе43. В этом исследовании была показана хорошая переносимость высоких доз NAC с минимальными побочными эффектами.
Значимость и ограничения
По нашим данным, это первое исследование, продемонстрировавшее c применением МФО благоприятный эффект высоких доз NAC на функцию малых дыхательных путей у пациентов со стабильным течением ХОБЛ. В нашем исследовании показано улучшение функции малых дыхательных путей, снижение частоты обострений ХОБЛ, и показана безопасность длительного лечения высокими дозами NAC больных со стабильной ХОБЛ.
Размер выборки в нашем исследовании был недостаточно большим для того, чтобы можно было выявить улучшение параметров функции легких (например, параметров МФО) и исследование не обладало достаточной статической мощностью для выявления динамики других клинических параметров. Поэтому требуются дальнейшие исследования длительной терапии высокими дозами NAC с увеличением объема выборки.
ЗАКЛЮЧЕНИЕ
Высокие дозы NAC (600 мг 2 р/день) — хорошо переносимая терапия, достоверно снижающая сопротивление малых дыхательных путей, что видно по улучшению показателя FEF25%-75% и параметров МФО, уменьшающая частоту обострений у пациентов со стабильным течением ХОБЛ.
СПИСОК ЛИТЕРАТУРЫ
1. Evans MD, Pryor WA. Cigarette smoking, emphysema, and damage to alpha 1-proteinase inhibitor. Am J Physiol. 1994; 266 (6 pt 1): L593-L611.
2. Rahman I, MacNee W. Oxidative stress and regulation of glutathione in lung infammation. Eur Respir J. 2000; 16 (3): 534– 554.
3. Sadowska AM, Manuel-Y-Keenoy B, De Backer WA. Antioxidant and anti-inf ammatory efcacy of NAC in the treatment of COPD: discordant in vitro and in vivo dose-efects: a review. Pulm Pharmacol Ter. 2007; 20 (1): 9–22.
4. Aruoma OI, Halliwell B, Hoey BM, Butler J. Te antioxidant action of N-acetylcysteine: its reaction with hydrogen peroxide, hydroxyl radical, superoxide, and hypochlorous acid. Free Radic Biol Med. 1989; 6 (6): 593–597.
5. Cotgreave IA. N-acetylcysteine: pharmacological considerations and experimental and clinical applications. Adv Pharmacol. 1997;38: 205–227.
6. Moldeus P, Cotgreave IA, Berggren M. Lung protection by a thiol-containing antioxidant: N-acetylcysteine. Respiration. 1986; 50 (Suppl 1): 31–42.
7. Poole P, Black PN. Mucolytic agents for chronic bronchitis or chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2010; (2): CD001287.
8. Grandjean EM, Berthet P, Rufmann R, Leuenberger P. Efcacy of oral long-term N-acetylcysteine in chronic bronchopulmonary disease: a meta-analysis of published double-blind, placebo-controlled clinical trials. Clin Ter. 2000; 22 (2): 209–221.
9. Decramer M, Rutten-van Molken M, Dekhuijzen PN, et al. Efects of N-acetylcysteine on outcomes in chronic obstructive pulmonary disease (Bronchitis Randomized on NAC Cost-Utility Study, BRONCUS): a randomised placebo-controlled trial. Lancet. 2005; 365 (9470): 1552–1560.
10. Antonelli-Incalzi R, Imperiale C, Bellia V, et al; SaRA Investigators. Do GOLD stages of COPD severity really correspond to diferences in health status? Eur Respir J. 2003; 22 (3): 444–449.
11. McFadden ER Jr, Linden DA. A reduction in maximum midexpiratory fow rate. A spirographic manifestation of small airway disease. Am J Med. 1972; 52 (6): 725–737.
12. Gelb AF, Zamel N. Simplifed diagnosis of small-airway obstruction. N Engl J Med. 1973; 288 (8): 395–398.
13. Goldman MD, Saadeh C, Ross D. Clinical applications of forced oscillation to assess peripheral airway function. Respir Physiol Neurobiol. 2005; 148 (1–2): 179–194.
14. Grimby G, Takishima T, Graham W, Macklem P, Mead J. Frequency dependence of fow resistance in patients with obstructive lung disease. J Clin Invest. 1968; 47 (6): 1455–1465.
15. Evans TM, Rundell KW, Beck KC, Levine AM, Baumann JM.Airway narrowing measured by spirometry and impulse oscillometry following room temperature and cold temperature exercise. Chest. 2005; 128 (4): 2412–2419.
16. US National Institutes of Health. Te efect of high dose n-acetylcysteine on airtrapping and airway resistance of chronic obstructive pulmonary disease — a double-blinded, randomized, placebo-controlled trial. NCT01136239. ClinicalTrials.gov. Bethesda, MD: National Institutes of Health; 2010. http://www. clinicaltrials.gov/ct2/show/NCT01136239. Updated June 2, 2010.
17. Global Initiative for Chronic Obstructive Lung Disease. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. Global Initiative for Chronic Obstructive Lung Disease website. goldcopd.org uploads/users/f les/GOLD_Report_2011_Feb21.pdf. Accessed December 7, 2012.
18. American Toracic Society. Standardization of spirometry, 1994 update. Am J Respir Crit Care Med. 1995; 152 (3): 1107–1136.
19. Ip MS, Ko FW, Lau AC, et al; Hong Kong Toracic Society; American College of Chest Physicians (Hong Kong and Macau Chapter). Updated spirometric reference values for adult Chinese in Hong Kong and implications on clinical utilization. Chest. 2006; 129 (2): 384–392.
20. Oostveen E, MacLeod D, Lorino H, et al; ERS Task Force on Respiratory Impedance Measurements. Te forced oscillation technique in clinical practice: methodology, recommendations and future developments. Eur Respir J. 2003; 22 (6):1026–1041.
21. Crim C, Celli B, Edwards LD, et al; ECLIPSE investigators. Respiratory system impedance with impulse oscillometry in healthy and COPD subjects: ECLIPSE baseline results. Respir Med. 2011; 105 (7): 1069–1078.
22. Macklem PT, Mead J. Resistance of central and peripheral airways measured by a retrograde catheter. J Appl Physiol.1967; 22 (3): 395–401.
23. Burgel PR, Bourdin A, Chanez P, et al. Update on the roles of distal airways in COPD. Eur Respir Rev. 2011; 20 (119): 7–22.
24. Hogg JC, Chu F, Utokaparch S, et al. Te nature of small-airway obstruction in chronic obstructive pulmonary disease. N Engl J Med. 2004; 350 (26): 2645–2653.
25. Caramori G, Di Gregorio C, Carlstedt I, et al. Mucin expression in peripheral airways of patients with chronic obstructive pulmonary disease. Histopathology. 2004; 45 (5): 477–484.
26. Rabe KF, Hurd S, Anzueto A, et al; Global Initiative for Chronic Obstructive Lung Disease. Global strategy for the Downloaded From: journal.publications.chestnet.org by a Zambon Group User on 07/02/2013 27. Bourdin A, Burgel PR, Chanez P, Garcia G, Perez T, Roche N. Recent advances in COPD: pathophysiology, respiratory physiology and clinical aspects, including comorbidities. Eur Respir Rev. 2009; 18 (114): 198–212.
28. Calverley PM, Koulouris NG. Flow limitation and dynamic hyperinfation: key concepts in modern respiratory physiology. Eur Respir J. 2005; 25 (1): 186–199.
29. King GG, Downie SR, Verbanck S, et al. Efects of methacholine on small airway function measured by forced oscilation technique and multiple breath nitrogen washout in normal subjects. Respir Physiol Neurobiol. 2005; 148 (1–2): 165–177.
30. Mahut B, Caumont-Prim A, Plantier L, et al. Relationships between respiratory and airway resistances and activity-related dyspnea in patients with chronic obstructive pulmonary disease. Int J Chron Obstruct Pulmon Dis. 2012; 7: 165–171.
31. Brochard L, Pelle G, de Palmas J, et al. Density and frequency dependence of resistance in early airway obstruction. Am Rev Respir Dis. 1987; 135 (3): 579–584.
32. Faria AC, Costa AA, Lopes AJ, Jansen JM, Melo PL. Forced oscillation technique in the detection of smoking-induced respiratory alterations: diagnostic accuracy and comparison with spirometry. Clinics (Sao Paulo). 2010; 65 (12): 1295–1304.
33. Black PN, Morgan-Day A, McMillan TE, Poole PJ, Young RP.Randomised, controlled trial of N-acetylcysteine for treatment of acute exacerbations of chronic obstructive pulmonary disease [ISRCTN21676344] [ISRCTN21676344]. BMC Pulm Med. 2004; 4:13.
34. Poole PJ, Black PN. Oral mucolytic drugs for exacerbations of chronic obstructive pulmonary disease: systematic review. BMJ. 2001; 322 (7297): 1271–1274.
35. Benrahmoune M, Terond P, Abedinzadeh Z. Te reaction of superoxide radical with N-acetylcysteine. Free Radic Biol Med. 2000; 29 (8): 775–782.
36. Gressier B, Cabanis A, Lebegue S, et al. Decrease of hypochlorous acid and hydroxyl radical generated by stimulated human neutrophils: comparison in vitro of some thiol-containing drugs. Methods Find Exp Clin Pharmacol. 1994; 16 (1): 9–13.
37. Kharazmi A, Nielsen H, Schiotz PO. N-acetylcysteine inhibits human neutrophil and monocyte chemotaxis and oxidative metabolism. Int J Immunopharmacol. 1988; 10 (1): 39–46.
38. Stolarek R, Bialasiewicz P, Nowak D. N-acetylcysteine efect on the luminol-dependent chemiluminescence pattern of reactive oxygen species generation by human polymor phonuclear leukocytes. Pulm Pharmacol Ter. 2002; 15 (4): 385–392.
39. Borgstrom L, Kagedal B. Dose dependent pharmacokinetics of N-acetylcysteine afer oral dosing to man. Biopharm Drug Dispos. 1990; 11 (2): 131–136.
40. Bridgeman MM, Marsden M, Selby C, Morrison D, MacNee W. Efect of N-acetyl cysteine on the concentrations of thiols in plasma, bronchoalveolar lavage fuid, and lung tissue. Torax. 1994; 49 (7): 670–675.
41. De Benedetto F, Aceto A, Dragani B, et al. Long-term oral n-acetylcysteine reduces exhaled hydrogen peroxide in stable COPD. Pulm Pharmacol Ter. 2005; 18 (1): 41–47.
42. Kasielski M, Nowak D. Long-term administration of N-acetylcysteine decreases hydrogen peroxide exhalation in subjects with chronic obstructive pulmonary disease. Respir Med. 2001; 95 (6): 448–456.
43. Demedts M, Behr J, Buhl R, et al; IFIGENIA Study Group. High-dose acetylcysteine in idiopathic pulmonary fbrosis. N Engl J Med. 2005; 353 (21): 2229–2242.
44. Cotgreave IA, Moldeus P. Lung protection by thiol-containing antioxidants. Bull Eur Physiopathol Respir. 1987; 23 (4): 275–277.
45. Jefery PK, Rogers DF, Ayers MM. Efect of oral acetylcysteine on tobacco smoke-induced secretory cell hyperplasia. Eur J Respir Dis Suppl. 1985; 139: 117–122.
46. Rubio ML, Sanchez-Cifuentes MV, Ortega M, et al. N-acetylcysteine prevents cigarette smoke induced small airways alterations in rats. Eur Respir J. 2000; 15 (3): 505–511.
47. Bridgeman MM, Marsden M, MacNee W, Flenley DC, Ryle AP. Cysteine and glutathione concentrations in plasma and bronchoalveolar lavage fuid afer treatment with N-acetylcysteine. Torax. 1991; 46 (1): 39–42.
48. Stav D, Raz M. Efect of N-acetylcysteine on air trapping in COPD: a randomized placebo-controlled study. Chest. 2009; 136 (2): 381– 386.
49. 4Hanaoka M, Droma Y, Chen Y, et al. Carbocisteine protects against emphysema induced by cigarette smoke extract in rats. Chest. 2011; 139 (5): 1101–1108.
50. Rubio ML, Martin-Mosquero MC, Ortega M, Peces-Barba G, Gonzalez-Mangado N. Oral N-acetylcysteine attenuates elastase-induced pulmonary emphysema in rats. Chest. 2004; 125 (4): 1500–1506.
51. Zheng JP, Kang J, Huang SG, et al. Efect of carbocisteine on acute exacerbation of chronic obstructive pulmonary disease (PEACE Study): a randomised placebo-controlled study. Lancet. 2008; 371 (9629): 2013–2018.
52. Niederman MS, Raferty TD, Sasaki CT, Merrill WW, Matthay RA, Reynolds HY. Comparison of bacterial adherence to ciliated and squamous epithelial cells obtained from the human respiratory tract. Am Rev Respir Dis. 1983; 127 (1): 85–90.
53. Suer E, Sayrac S, Sarinay E, et al. Variation in the attachment of Streptococcus pneumoniae to human pharyngeal epithelial cells afer treatment with S-carboxymethylcysteine. J Infect Chemother. 2008; 14 (4): 333–336.
54. Gerrits CM, Herings RM, Leufens HG, Lammers JW. N-acetylcysteine reduces the risk of re-hospitalisation among patients with chronic obstructive pulmonary disease. Eur Respir J. 2003; 21 (5): 795–798.
