Cумамед в лечении осложненных острых респираторных инфекций у детей
СтатьиОпубликовано в журнале:
ДЕТСКИЕ ИНФЕКЦИИ »» 2 * 2003
В. Ф. УЧАЙКИН, ф. С. ХАРЛАМОВА, О. В. КЛААОВА, В. Ю. КРЫЛАТЫХ, Т. П. ЛЕГКОВА
РОССИЙСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ,
МОРОЗОВСКАЯ ДЕТСКАЯ ГОРОДСКАЯ КЛИНИЧЕСКАЯ БОЛЬНИЦА, МОСКВА
Резюме
С целью оценки терапевтической эффективности и безопасности коротких курсов сумамеда в суспензии при ОРЗ, 10 больных с острым средним отитом получали препарат в дозе 30 мг/кг однократно (1 группа), 10 больных — 10 мг/кг в сутки в течение 3-х дней (2 группа), 10 больных с этим осложнением получали ампициллин в дозе 100 мг/кг 3 раза в сутки в течение 7 дней (группа контроля); 10 больных с тонзиллофарингитом получали сумамед в дозе 30 мг/кг однократно (1 группа), 10 больных — в дозе 10 мг/кг в сутки в течение 3 дней (2 группа) и 10 больных с этой патологией получали ампициллин в дозе 100 мг/кг в сутки в течение 7 дней (группа контроля).
Результаты исследований свидетельствуют о преимуществе однократного и короткого режимов дозирования сумамеда с большей эффективностью и безопасностью по сравнению с общепринятой тактикой лечения антибиотиком пенициллинового ряда, что обеспечивает максимальный комплаенс при минимальной нагрузке на медицинский персонал и позволяет сократить длительность заболевания.
Ключевые слова: сумамед, ампициллин, острый средний отит, тонзиллофарингит, микрофлора ротоглотки и слухового прохода, максимальный комплаенс.
Антибактериальная терапия является ведущей в лечении острых респираторных заболеваний с бактериальными осложнениями. Принято считать, что абсолютными показаниями для проведения антибактериальной терапии являются пневмония, синусит, вирусно-бактериальный обструктивный ларингит, тонзиллофарингит, эпиглоттит [1—5]. Особенно часто к назначению антибактериальных средств прибегают у детей первых месяцев и лет жизни, в связи с возникновением острого среднего отита (ОСО). Около 90% детей к 5-летнему возрасту переносят острый средний отит и примерно 30 млн. из них при этом ежегодно получают антибактериальную терапию [6]. Вопрос о безусловной необходимости применения антибиотиков при данной патологии остается дискутабельным [3—5].
Результаты метаанализа 33 рандомизированных исследований (у 5400 детей) показывают, что назначение антибиотиков только на 13,7% повышает частоту разрешения ОСО. Вместе с тем, сравнительные данные у получавших антибиотики и плацебо, указывают на большую продолжительность сохранения выпота в среднем ухе у детей без антибиотикотерапии и поэтому большинство клиницистов приходят к выводу о необходимости применения антибиотикотерапии при ОСО [3, 5].
Наиболее часто бактериальные осложнения при ОРВИ вызываются пневмококками, гемофильной палочкой, моракселлой катарралис, стафилококками, стрептококками, клебсиеллой. У детей, ранее получавших антибиотики, ведущую роль в этиологии бактериальных осложнений играют моракселла и стафилококки, которые приобретают лекарственную устойчивость к р-лактамазе. В последние годы все возрастающее значение в патологии носоглотки и верхних дыхательных путей приобретают внутриклеточные и мембранные атипичные возбудители (хлами-дии и микоплазмы), как правило, нечувствительные к антибиотикам, но несмотря на это они широко применяются, поскольку природные и полусинтетические пенициллины, цефалоспорины или сульфаниламидные препараты принято считать препаратами первого ряда при всех заболеваниях ротоглотки и респираторного тракта [1, 2, 5, 7, 8].
Теоретически для эффективного лечения и сдерживания роста резистентных штаммов бактерий необходимо определять чувствительность возбудителей болезни к антибактериальным препаратам, но поскольку практически такой подход реализовать не представляется возможным, выбор антибиотика на начальном этапе лечения проводится эмпирически, при этом не учитываются возникшие региональные изменения в структуре возбудителей и их свойствах, рост антибиотикорезистентных форм, а также способность причинно-значимых патогенов разрушать антибиотики (3-лактамазами. Известно, что за последние 10—15 лет во многих странах мира распространилась устойчивость пневмококков к пенициллином и цефалоспоринам, а гемофильной палочки — к аминопенициллинам и т. д. [9, 10]. Поэтому, в настоящее время нельзя, например, рассчитывать на хороший эффект монотерапии пенициллинами и его производными, а также цефалоспоринами 1—2 поколения [9—11]. С учетом высказанных положений вполне оправдан устойчивый интерес клиницистов в нашей стране и за рубежом к использованию макролидных антибиотиков. Современные макролиды обладают рядом привлекательных свойств и антибиотики этого ряда можно считать определенной альтернативой пенициллином и цефалоспоринам в лечении бактериальных осложнений при ОРЗ у детей, особенно с учетом того, что макролиды обладают активностью в отношении атипичных возбудителей, способны создавать в тканях при воспалении концентрации, превышающие таковые в сыворотке крови, не разрушаются Р — лактамазами моракселл, гемофильной палочки и др. По способности проникать через гистогематические барьеры, макролиды превосходят B-ЛаКТОМЫ и аминогликозиды [2, 3, 6, 12—15].
Согласно данным литературы, представитель группы макролидов-азалидов Сумамед® (азитромицин) выгодно отличается широтой антимикробного спектра, имеет клинически значимую активность в отношении наиболее частых патогенов, вызывающих инфекции
респираторного тракта, включая гемофильную палочку, моракселлу катарралис, нейсерии, в том числе и ампициллинрезистентные штаммы, а также имеет высокую активность против внутриклеточных патогенов [6, 10, 16]. Тканевые концентрации азитромицина (сумамеда) в 10—100 раз выше плазменных, что позволяет ему наиболее интенсивно накапливаться в миндалинах, лимфоузлах, полости среднего уха, придаточных пазухах носа, легких, бронхиальном секрете, плевральной жидкости, органах малого таза, а также проникать в фагоцитирующие клетки и транспортироваться с их помощью в очаги воспаления. Концентрации азитромицина в тканях длительно сохраняются на терапевтическом уровне в результате медленного высвобождения его из клеток [13]. Особая, уникальная фармакокинетика с пролонгированным периодом полувыведения из тканей дает возможность применять Сумамед® перорально короткими режимами дозирования, даже в однократной дозе, без ущерба для клинического эффекта и без опасения выработки резистентj ных штаммов. Перечисленные особенности препарата и наличие специальных педиатрических лекарственных форм позволяют применять препарат в лечении респираторной бактериальной инфекции у детей, однако до настоящего времени применение коротких режимов дозирования антибиотиков вызывает определенное скепти- ческое отношение, что делает целесообразным углубленное изучение эффективности и безопасности этого антибиотика в широкой клинической практике.
Цель исследования: оценить терапевтическую эффективность и безопасность различных режимов дозирования педиатрической лекарственной формы Сумамеда® в суспензии (200 мг/5 мл) при ОРЗ бактериальной этиологии, сопровождающихся острым средним отитом, а также поражением ротоглотки и (или) верхних дыхательных путей у детей.
Дизайн исследования: открытое (незамаскированное), сравнительное, группы больных подбирали по случайному алфавитному признаку.
Материалы и методы
В исследование были включены 60 детей в возрасте от 3 мес. до 12 лет, госпитализированных в боксы 18 инфекционного отделения Морозовской городской детской клинической больницы, в связи с наличием осложненного течения ОРВИ тонзиллофарингитом, острым средним отитом. В преморбидном фоне у 21 (35%) из этих детей регистрировался атонический дерматит и рецидивирующий обструктивный ларингит и бронхит, у 7 (12%) — пищевая аллергия, у 14 (23%) — дисбиоз кишечника, у 9 (15%) — хронический тонзиллит, у 3 (5%) — гипертензионный синдром, у 3 (5%) — фебрильные судороги и у 3 (5%) — инфекция мочевыводящих путей. Большинство больных поступали в первые 4 дня от начала заболевания. У всех больных отмечались различной степени выраженности симптомы интоксикации (от легкой до умеренной). Лихорадка регистрировалась у 80% больных.
Среди 30 больных с тонзиллофарингитом на фоне отека, гиперемии слизистой ротоглотки и миндалин, болей в горле в 75% случаев выявлялся слизисто-гнойный секрет на задней стенке глотки, а в 25% — имели место гнойные наложения в лакунах миндалин или гнойные фолликулы в области миндалин либо на задней стенке глотки. У всех больных этой группы фиксировались признаки регионарной лимфаденопатии.
У 30 детей с острым средним отитом на фоне выраженных катаральных явлений в носоглотке, при отоскопии выявлялись воспалительные изменения барабанной перепонки без признаков перфорации и гноетечения. У 12 детей диагностировали 2-х-сторонний острый средний отит, а у остальных — односторонний. Все больные осматривались ЛОР-врачом при первичном обследовании и в динамике.
Данные клинико-лабораторного обследования больных регистрировались в виде балльной оценки, которая в сумме всех баллов отражала общее состояние пациента в течение всего срока наблюдения. У больных, выписанных из стационара на 5—7 сутки от начала терапии, на 10—12 день проводилось катамнестическое амбулаторное обследование с указанием оценки общего состояния в баллах.
Учитывались данные лабораторных исследований: показатели общего анализа периферической крови и общего анализа мочи. Из исследования исключались дети, имевшие: аллергию к антибиотикам в анамнезе, в том числе к макролидам; тяжелые заболевания печени, почек, сердца и кроветворных органов; инфекционный мононуклеоз; симптомы и признаки системных осложнений инфекции; расстройства ЖКТ, которые могли повлиять на всасывание препарата; ревматизм в анамнезе (для больных тонзиллофарингитом); хронический отит; антимикробную терапию (более одной дневной дозы) за 72 часа до включения в испытание или инъекции пролонгированных пенициллинов в течение последних 4 недель; иммунодефицит.
Состав микрофлоры ротоглотки и слухового прохода оценивали до назначения терапии, спустя 72 часа от начала антибактериальной терапии и по окончании курса лечения. Количественные исследования аэробной грамположительной и грамотрицательной микрофлоры проводили в бактериологической лаборатории НИИЭМ им. Н. ф. Гамалеи (зав. лабораторией — профессор, д. м. н. А. ф. Мороз).
При количественном исследовании материала секрет из ротоглотки и наружного слухового прохода, взятого стерильным тампоном, помещали в пробирку с 1 мл тиогликолевого бульона с целью активации микробных клеток, которую доставляли в лабораторию не позже 2 часов после забора мазков. В дальнейшем, из последовательных десятикратных разведении, для идентификации выделенного возбудителя делали посевы на селективные питательные среды: кровяной агар, Эндо-, Сабуро-, желточно-солевой-, эктон-энтерик-, конго-, клебсиеллезный-, ЦПХ- и висмутовый агары. Антибиотикограммы выделенных бактериальных культур определяли методом дисков, импрегнированных антибиотиками, на агаре Мюллер-Хинтона, а грибов рода Кандида — на кандида-агаре. Патогенность золотистого стафилококка определяли в тесте плазмокоагуляции. На конго-агаре идентифицировали весь спектр бактериальной флоры из мазка. Штаммы стрептококков определяли по типу а- и р-гемолиза, гидролизу эскулина, разжижению желатина и гидролизу гиппурата. По виду гемолиза на кровяном агаре стрептококки делили на мукоидные, гемолитические и шероховатые. Зеленящие стрептококки (Str. viridans) дифференцировали по образующемуся на кровяном агаре a-гемолизу в виде полупрозрачной зоны зеленоватого оттенка, которая обуславливает превращение гемоглобина в метгемоглобин.
Таблица 1.
Продолжительность клинических проявлений у больных ОРЗ, осложненным отитом

Основная группа больных (40 детей) получала Сумамед®-форте (azythromicin) в суспензии (200 мг/ 5 мл) — препарат фирмы PLIVA (Хорватия). Эта группа больных подразделялась на следующие подгруппы:
1 — Острый средний отит (ОСО) — 10 больных получали лечение Сумамедом® в дозе 30 мг/кг однократно (1а) и 10 больных получали Сумамед® в суспензии по 10 мг/кг один раз в день на протяжении 3 дней (16).
2 — Тонзиллофарингит — 10 больных получали лечение Сумамедом® в дозе 30 мг/кг однократно (2а) и еще 10 больных получали Сумамед® в дозе 10 мг/кг в сутки 3-х дневным курсом (26).
Контрольную группу больных (3) составили пациенты с острым средним отитом (10 детей) и тонзиллофарингитом (10 детей), получавшие стандартную антибактериальную терапию антибиотиком пенициллинового ряда — ампициллин в дозе 100 мг/кг 3 раза в сутки в течение 7 дней.
В течение исследования больные не принимали других антимикробных препаратов, но могли получать симптоматические и патогенетические средства.
Эффективность препарата определялась на основании сравнительного анализа динамики купирования основных клинических симптомов заболевания в основной и контрольной группах, а также результатами обследования клинического анализа крови, мочи, микрофлоры ротоглотки и уха в течение всего срока пребывания в стационаре и после выписки, в среднем, до 10—12 дня. Критерии оценки эффективности: выздоровление — хороший результат — при значительном клиническом улучшении в течение первых 3-х дней лечения с последующим полным исчезновением признаков и симптомов инфекции; улучшение — удовлетворительный результат — при значительном клиническом улучшении в течение первых 3-х дней, с неполным исчезновением признаков и симптомов инфекции в течение периода последующего наблюдения, но без необходимости дополнительного лечения антибиотиками; отсутствие успеха — неудовлетворительный результат — при наличии персистенции или усилении признаков и симптомов инфекции, спустя как минимум, 72 часа лечения, требующее назначения другой антимикробной терапии. Кроме того, учитывались возможные симптомы побочного действия препарата.
Результаты и их обсуждение
Результаты исследований до назначения антибактериальной терапии свидетельствовали о дисбиозе ротоглотки у 25 из 30 (83,3%) больных тонзиллофарингитом, обусловленном колонизацией слизистой ротоглотки преимущественно золотистым и гемолитическим стафилококком — у 14, а-гемолитическим стрептококком — у 2, лактозонегативной E.coli — у 3, клебсиеллой пневмонии — у 3, энтерококком — у 3 больных.
У больных острым средним отитом у 20 из 30 (67%) обследованных выявлено нарушение нормального состава микрофлоры слухового прохода, обусловленного колонизацией стафилококками (золотистым — у 4, гемолитическим — у 4, эпидермальным и сапрофитирующим — у 6), моракселлой катарралис — у 2, Е. coli и энтерококками — у 4 больных. У большинства больных, у которых в области ротоглотки отмечена колонизация преимущественно стафилококками, сопутствовал кандидоз.
Среди больных острым средним отитом, получавших терапию Сумамедом® однократно в дозе 30 мг/кг достоверно короче, чем в группе контроля, регистрировалась продолжительность лихорадки, что в среднем составило 0,9 + 0,3 дня против 2,0 + 0,3 дней, соответственно (р < 0,05). Аналогично сокращалась продолжительность симптомов интоксикации, что достоверно составило, в среднем, 1,0 + 0,2 день в испытуемой группе, а в группе контроля таковые сохранялись, в среднем, до 3,4 + 0,4 дней (р < 0,001). Симптомы отита у получавших однократную дозу сумамеда, в среднем, продолжались 3,5 + 0,5 дней, в то время как достоверно продолжительнее их проявления были у больных, получавших ампициллин, что в среднем составило 5,8 + 0,3 дней (р < 0,001). Аналогичными и достоверными были различия в продолжительности лихорадки, симптомов интоксикации и отита у больных, получавших сумамед 3-х-дневным курсом относительно больных, получавших 7-дневный курс ампициллина (таблица 1, рисунки 1,2).
Рисунок 1.
Динамика интоксикации у больных ОРЗ, осложненным средним отитом, леченых сумамедом в течение 3-х дней (I), сумамедом в течение 1-го дня (II) и ампициллином (III)
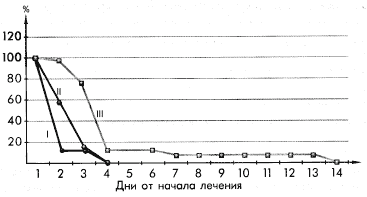
Рисунок 2.
Динамика отоскопических изменений у больных ОРЗ, осложненным средним отитом, леченых сумамедом в течение 3-х дней (I), сумамедом в течение 1-го дня (II) и ампициллином (III)
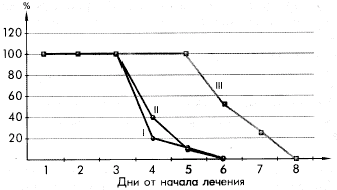
Средний показатель эрадикации выделенных патогенов у больных отитом на обоих режимах дозирования сумамеда составил 92,3%. В то же время у больных, получавших ампициллин была достигнута эрадикация только 80% выделенных патогенов.
Выздоровление на обоих режимах дозирования сумамеда с хорошим результатом наступило у 80% детей и с удовлетворительным — у 20% детей, страдавших острым средним отитом на фоне ОРЗ. В группе контроля эти показатели составили только 65 и 35% соответственно.
В результате проведенной терапии однократной дозой сумамеда (30 мг/кг) у больных тонзиллофарингитом, продолжительность лихорадки, в среднем, составила 1,3 + 0,5 дня, в то время как в группе контроля — 2 + 0,3 дня; симптомы интоксикации продолжались, в среднем, 1,5 + 0,4 дня, по срокам достоверно отличаясь от таковых в группе контроля, где, в среднем, регистрировались в течение 2,9 + 0,3 дней (р < 0,01). Симптомы тонзиллофарингита также достоверно были менее продолжительными среди получавших сумамед, относительно группы контроля, что в среднем, составило 4,3 i 0,2 дня против 6,3 i + 0,3 дней, соответственно (р < 0,001). Аналогично достоверно сокращалась продолжительность симптомов интоксикации и лихорадки у больных подгруппы, получавших сумамед 3-х дневным курсом в дозе 10 мг/кг в сутки. Несколько продолжительнее, чем в предыдущей подгруппе, но достоверно короче, чем в группе контроля, продолжались симптомы тонзиллофарингита, что, в среднем, составило 5 i 0,6 дней, против 6,3 + 0,3 дней, соответственно (р < 0,05) (таблица 2, рисунки 3,4). У больных тонзиллофарингитом, получавших сумамед однократно и в течение 3-х-дневного курса, достигнуто выздоровление с хорошим результатом эффективности терапии у 80 и 90% больных, соответственно, и удовлетворительным — у 20 и 10%, соответственно.
Таблица 2. Продолжительность клинических проявлений у больных ОРЗ, осложненным тонзиллофарингитом
|
Продолжительность , в днях . |
|||
|
Симптомы |
Сумамед — |
Сумамед — |
Ампициллин — |
|
1 день, n=10 |
3 ДНЯ, n=10 |
7 дней,n = 10 |
|
|
Повышение t |
1,3 ± 0,5 |
1,4 + 0,5 |
2,0 ± 0,3 |
|
Интоксикация |
1,5 ± 0,4* |
1,6 ± 0,3* |
2,9 + 0,3 |
|
Тонзилло- фарингит |
4,3 + 0,2** |
5,0 ± 0,6*** |
6,3 ± 0,3 1 |
* — р < 0,01, ** — р < 0,001, *** — р < 0,05
В подгруппе больных, получавших терапию сумамедом, достигнута эрадикация 80% патогенов. В то же время у больных, получавших ампициллин, наступила эрадикация только 50% выделенных патогенов.
Принципиально важным является тот факт, что ни в одном случае лечения Сумамедом не было выявлено отрицательного влияния препарата на нормальную микрофлору полости рта и уха. А в контрольной группе у половины больных тонзиллофарингитом отмечено нарастание количественных показателей кандидоза ротоглотки.
В группе контроля выздоровление с хорошим результатом достигнуто лишь у 70% и удовлетворительным — у 30% больных.
Из побочных эффектов терапии Сумамедом® мы не выявили значительных нарушений в состоянии больных, лишь у 3-х детей отмечено учащение стула без нарушения его качества при однократном приеме в дозе 30 мг/кг, что расценено как усиление моторики кишечника в течение одних суток, с дальнейшей нормализацией его частоты. Ни в одном случае побочные эффекты не являлись причиной отмены лечения.
Таким образом, полученные нами данные подтверждают данные зарубежных исследователей об уровне безопасности Сумамеда®. Практически ценным является и то, что Сумамед® относится к препаратам с минимальным количеством нежелательных реакций, включая и эффекты аллергического плана. Отсутствие метаболизма через систему цитохрома Р-450 у сумамеда обеспечивает низкий процент лекарственного взаимодействия, и в отличие от других макролидов таковой может применяться одновременно с другими антибактериальными препаратами [17, 18].
Рисунок 3.
Динамика интоксикации у больных ОРЗ, осложненным тонзиллофарингитом, леченых сумамедом в течение 3-х дней (I), сумамедом в течение 1-го дня (II) и ампициллином (III)
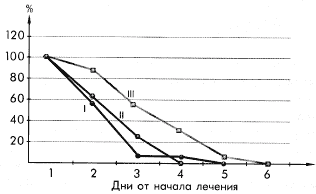
Рисунок 4.
Динамика фарингоскопических изменений у больных ОРЗ, осложненным тонзиллофарингитом, леченых сумамедом в течение 3-х дней (I), сумамедом в течение 1-го дня (II) и ампициллином (III)
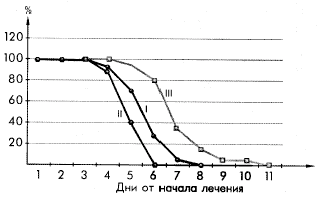
В группе контроля отмечено у 5 больных с 3—4 дня терапии ампициллином изменение характера стула с появлением патологических примесей, что требовало введения ферментативных и пробиотических препаратов, а у 3-х больных к 7 дню терапии ампициллином появилась аллергическая сыпь.
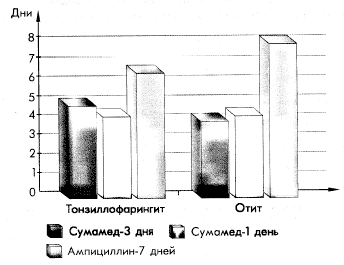
Среднее количество койко-дней в испытуемой группе больных достоверно сокращалось относительно таковых в группе контроля (рисунок 5), что среди больных тонзиллофарингитом составило на однодневном курсе сумамеда, в среднем, 4,4 ± 0,6 дня (р < 0,01), у больных отитом — 4,3 ± 0,5 дня (р < 0,01), а на 3-х дневном курсе — 4,9 ± 0,7 (р < 0,05) и 4,0± 0,4 дня (р < 0,001), соответственно; в то время как у получавших ампициллин, в среднем, составило 6,6± 0,4 и 8± 0,6 дней, соответственно.
Заключение
Полученные нами результаты позволяют высказаться о преимуществе нового режима дозирования Сумамеда® перед традиционной терапией антибиотиком пенициллинового ряда, способствующего созданию высокой терапевтической концентрации препарата в очаге инфекции в короткие сроки в самом начале развития осложненного ОРЗ, что, во-первых, способствует сокращению продолжительности симптомов болезни и сроков пребывания в стационаре, а во-вторых — более эффективной эрадикации возбудителей в очаге воспаления. Наши данные косвенно подтверждают, что фармакокинетические и фармакодинамические преимущества этого антибиотика имеют свое клиническое подтверждение и при лечении осложненного течения острой вирусной инфекции у детей. Хорошо известно, что концентрации азитромицина в тканях длительно сохраняются на терапевтическом уровне в очаге воспаления в результате медленного высвобождения его из фагоцитирующих клеток [13], что и позволяет добиться эрадикации возбудителя и быстрой положительной динамики в течении заболевания. Особая, уникальная
Рисунок 5.
Среднее количество койко-дней у больных в основной и контрольной группах
фармакокинетика с пролонгированным периодом полувыведения из тканей дает возможность применять сумамед (азитромицин) перорально короткими режимами дозирования, даже в однократной дозе, без ущерба для клинического эффекта и без опасения выработки резистентных штаммов.
Наш опыт применения Сумамеда® показал, что его эффективность равна, а в ряде случаев и превышает таковую по сравнению с антибиотиком пенициллинового ряда, что также согласуется с данными литературы. Так, Cohen R. с соавторами [19] лечили 500 детей в возрасте от 2 до 12 лет с тонзиллофарингитом коротким 3-х-дневным курсом (10 мг/кг массы тела) азитромицина. Была показана равнозначная степень эффективности Сумамеда® в сравнении с 10-дневным курсом орального пенициллина V, с клиническим успехом выше 90%. При сравнительном исследовании эффективности лечения острого среднего отита амоксициллином — 30 дозами, цефаклором — 30 дозами, цефуроксимом — 20 дозами, азитромицином — 3 дозами (10 мг/кг — 3-х дневным курсом) и однократной дозой (30 мг/кг массы тела) выявлены преимущества укороченных курсов сумамеда, как в обеспечении терапевтической концентрации препарата в очаге в самом начале развития инфекции, так и в достижении максимального комплаенса [20—22].
В ноябре 2001 года FDA была рекомендована оральная суспензия азитромицина для лечения острого среднего отита у детей как в режиме 3-х-дневного курса, так и в режиме однократного приема в дозе 30 мг/кг массы тела [23].
Терапия однократной дозой азитромицина (30 мг/кг) была апробирована у 480 детей с острым средним отитом в возрасте от 6 мес. до 12 лет с эффективностью, равной лечению аугментином при низкой частоте побочных проявлений. О высокой эффективности терапии однократной дозой азитромицина при тонзиллофарингите, развившемся как осложнение ОРВИ сообщают S. Schonwald с соавт. [23].
Таким образом, современные данные о препарате группы азалидов Сумамед® (азитромицин) и наш собственный опыт позволяют шире использовать его уникальные возможности для обеспечения целенаправленной антибактериальной терапии, достижения комплаентности применения антибиотика и сокращения сроков госпитализации ребенка.
Выводы:
Короткие режимы дозирования Сумамеда® имеют равную или даже большую эффективность по сравнению с общепринятой тактикой лечения антибиотиком пенициллинового ряда. Режим однократного приема Сумамеда® столь же эффективен и безопасен, как и режим 3-х дневного применения этого антибиотика и превосходит по своей эффективности и безопасности препарат группы сравнения (ампициллин). Сумамед® обеспечивает максимальный комплаенс при минимальной нагрузке на медицинский персонал.
Сумамед® высокоэффективен и безопасен в качестве стартового антибиотика и позволяет сократить длительность пребывания больного ребенка в стационаре.
Литература:
1. Яковлев С. В. Современная антимикробная терапия / С. В. Яковлев, В. П. Яковлев // Consilium medicum. — 2001. — С. 23—27.
2. Страчунский Л. С. Макролиды в современной клинической практике / Л. С. Страчунский, С. Н. Козлова. — Смоленск, 1998.
3. Страчунский Л. С. Антибактериальная терапия острого среднего отита у детей / Л. С. Страчунский, М. Р. Богомильский // Детский доктор. — 2001. — № 1. — С. 6—9.
4. Антибактериальная терапия острых респираторных заболеваний у детей. — Пособие для врачей: Под ред. Л. К. Баженовой. — Москва, 2002.
5. Каманин Е. И. ОСО у детей: клиническое значение и антибактериальная терапия /Е. И. Каманин, О. А. Егорова // Российский медицинский журнал. — 2001. — 6: 1—7.
6. Богомильский М. Р. Место макролидов в антибактериальной терапии среднего отита у детей /М. Р. Богомильский, Т. И. Гаращенко // Вестник оториноларингологии. — 2000. — № 2. — С. 34—36.
7. Bisno A. L. Acute pharyngitis // N. Engl. J. Med. — 2001, January. — V. 344 — № 3. — P. 205—211.
8. Esposito S. Emerging Pathogens in Acute Pharyngitis / 41st ICAS, Chicago, Illinois — 2001, Desember. — P. 1—3.
9. Клейн Д. Терапия острого среднего отита в эру изменения чувствительности к антибактериальным препаратам. — Новости МСРПА. — 1999. — 2: 46.
10. Самсыгина Г. А. Антибактериальная терапия респираторных заболеваний у детей / Г. А. Самсыгина, М. Р. Богомильский, Т. И. Гаращенко // Consilium medicum (Педиатрия)— 2002. — № 2. — вып. № 3. — С. 3—7.
11. Retsema J. A. Susceptibility ad resistance emergence studies with macrolides // Int. J. of Antimicr. Agents. — 1999 — 11 (Suppl.l). — P. 15—21.
12. Amsden G. W. Pharmacokinetics in serum and leucocyte exposures of oral azythromicin, 1500 mg, given a 3 or 5-day period in healthy subjects / G. W. Amsden, A. N. Nafziger and Foulds // Antimicrobial Agents and Chemotherapy .—
1999. — 43. — P. 163—165.
13. Amsden G. W. ICNAS-KO 6. — 2002. — 4.13.
14. Cuzzolin L. Use of Macrolides in Children: A Review of the Literature /L Cuzzolin, V. Fanos // Infect. Med. — 2002. — 19(6). — P. 279—285.
15. Pichichero М. Е. Acute otitis media: Part 2. Treatment in an Era of Increasing Antibiotic Resistance // Am. Fam. Physician. —
2000. — 61. — P. 2416.
16. Hof H. Intracellular microorganisms: a particular problem for hemotherapy // Introduction. — 1991: 19 (Suppl.4). — P. 193—194.
17. Rubinstein E. Comparative safety of the different macrolides // Intern. J. of Micr. Agents. — 2001. — 18. — P. 71—76.
18. Williams J. D. Ewaluation of safety of Macrolides // Intern. J. of Antimicr. Agents. — 2001. — 18 (Suppl.l). — P. 77—81.
19. Comparison of two dosages ofazithromicin for three days versus penicillin V for ten days in acute group A streptococcal tonsillopharyngitis / Cohen R. et al. // The Pediatric infectious disease journal. — 2002 .— 21. — P. 297—303.
20. Treadway G. Tolerability of 3-day, once-daily azythromicin suspension versus standard treatments for community-acqired pediatric infectious disease / G. Treadway, A. Reisman // Intern. J. of antimicr. Agents. — 2001. — 18. — P. 427—431.
21. Mohs E. A comparative study of azythromicin and amoxycillin in pediatric patients with acute otitis media. / E. A. Mohs, A. Rodriqez — Solares, E. Rivas and Z. El. Hoshy // J. of Antimicr. Chemother. — 1993. — 31 (Suppl. E). — P. 73—79.
22. Use and Complaience with oral Antibiotics treatment in children / T. Cuchi et al. // ICMASK Poster Book — Barselona, Spain. — 1998. — 21—23 January. — P. 34—35.
23. S. Schonwald et al./ ICMAS Ко 6 — 2002, 23—26 January, Bologna, Italy. — 12.
