| 1. Гепатоцеллюлярная карцинома (ГЦК) - одна из самых часто встречающихся злокачественных опухолей. Ее распространенность в западных странах в последние десятилетия также значительно возросла и составляет 10-30 новых случаев заболевания на 100 000 жителей в год. На территории России смертность от ГЦК достаточно высока и составляет менее 5,8*105 случаев. Достичь уменьшения смертности от ГЦК возможно при проведении ранней диагностики данного заболевания. Пациенты зачастую не проходят регулярного медицинского контроля в связи с отсутствием симптомов ГЦК на начальном этапе, поэтому проблема ранней диагностики ГЦК остро стоит во всех странах. | 1. Смертность от гепатоцеллюлярной карциномы в различных регионах
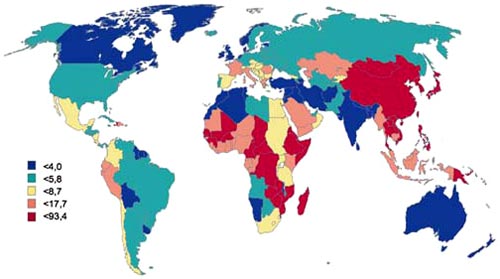 |
|
| 2. На графике представлены данные исследования, в котором участвовало 417 больных циррозом печени, но без ГЦК. В течение 5 лет наблюдения ГЦК была выявлена у 112 пациентов, заболеваемость составила 3,4% в год. Благодаря совершенствованию оборудования и приобретению опыта лечения данной группы больных, в III периоде наблюдения (1997-2001 гг.) стало возможным выявление опухолей все более мелкого размера (до 2,2 см). Ранее пациенты, не подлежащие лечению, составляли до 50% больных ГЦК, тогда как при ранней диагностике терапевтические возможности имеются у гораздо большей когорты больных. Ранняя диагностика ГЦК и ее скрининг основываются на 3 главных составляющих: методах лучевой диагностики, результатах лабораторных исследований и гистологических данных. | 2. Частота развития ГЦК у пациентов с циррозом печени
- 417 пациентов с циррозом без ГЦК три 5-летних периода
- Период наблюдения 148 мес (1-213 мес), УЗИ каждые 6 или 12 мес 1
- ГЦК: 112 пациентов, 3,4% в год
- Размер опухоли: 3,7 см против 3,0 см против 2,2 см (р<0,02 против III)
- Неоперабельность: 46% против 38% против 26%
- Ежегодная смертность: 45% против 37% против 10% (р<0,02 против III)
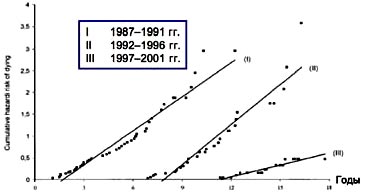
Sangiovanni et al., GE 2004; 126: 1005.
|
|
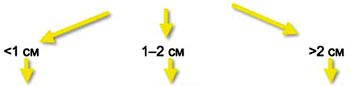
| 3. Всем пациентам с подозрением на ГЦК должно регулярно проводиться ультразвуковое исследование (УЗИ) печени. По результатам УЗИ выделяются группы больных с малыми (менее 1 см), средними (1-2 см) и большими (более 2 см) образованиями. При наличии малого образования трудно с уверенностью диагностировать опухоль и затруднительно произвести биопсию данного образования, в связи с чем у данной группы пациентов рекомендовано проведение УЗИ с более короткими промежутками - каждые 3 мес с целью оценки динамики роста образования. В случае роста опухоли более 1 см для диагностики ГЦК требуется совпадение результатов по меньшей мере 2 лучевых методов исследования: компьютерной томографии (КТ), цветной допплер-сонографии с контрастным усилением или магнитно-резонансной томографии (МРТ). При опухоли более 2 см достаточного одного результата. При получении сомнительных результатов необходимо проведение биопсии образования печени. | 3. Алгоритм диагностики ГЦК
УЗИ печени
|
УЗИ 1 раз в
3-6 мес |
КТ в динамике, цветная
допплер-сонография с контрастным усилением, МРТ
2 исследования
При сомнительных результатах - биопсия |
КТ в динамике, цветная
допплер-сонография с контрастным усилением, МРТ
1 исследования
При сомнительных результатах - биопсия |
Типичный признак ГЦК - гиперваскуляризация
образования в артериальную фазу |
|
|
| J.M.Llovet и соавт. представили в Барселоне классификацию ГЦК, так называемую классификацию BCLC. На ее основании рекомендуется проводить выбор метода лечения в зависимости от характеристик самой опухоли и фоновых заболеваний печени. В соответствии с данной классификацией выделяют 3 группы пациентов с различным подходом к лечению и различным прогнозом. Пациенты со стадией 0 достаточно сохранны соматически, имеют небольшое образование в печени, нормальные лабораторные показатели и являются кандидатами на резекцию ГЦК. Ранняя стадия (А) ГЦК характеризуется наличием 1-3 образований в печени менее 3 см в диаметре. Этой группе пациентов при отсутствии внепеченочных проявлений возможно проведение трансплантации печени, чрескожных инъекций этанола (ЧИЭ) или радиочастотной абляции (РЧА). Лечение на первых двух стадиях позволяет достичь 50-70% 5-летней выживаемости. Пациентам с промежуточной стадией (В), имеющим множественные образования в печени, по классификации BCLC рекомендуется проведение трансартериальной химиоэмболизации (ТАХЭ). Для прогрессирующей стадии (С) характерна яркая клиническая симптоматика, имеется инвазия опухоли в воротную вену, регионарные и отделенные метастазы. Именно в этой стадии рекомендуется назначение сорафениба. У пациентов с терминальной стадией (D) ожидаемая продолжительность жизни не превышает 3 мес, им рекомендовано паллиативное лечение. | 4. Классификация и лечение ГЦК (BCLC)
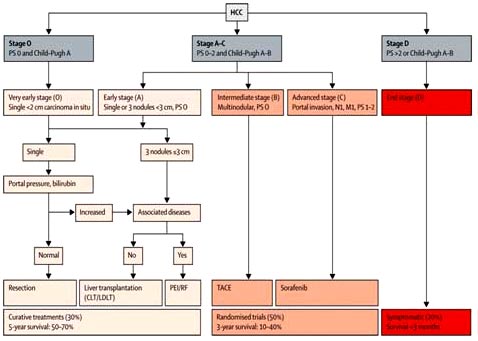
|
|
| 5. Трансплантация печени представляет собой, бесспорно, самый эффективный метод лечения, поскольку при этом устраняется прокарциногенное поле, каким является цирроз печени. При соблюдении строгих критериев отбора (1 очаг опухоли размером менее 5 см или 3 очага опухоли размером менее 3 см) и в случае отсутствия внепеченочных проявлений, а также инвазии сосудов 5-летняя выживаемость после трансплантация печени достигает 70% при частоте рецидивов 15% | 5. Трансплантация печени при ГЦК |
- 48 пациентов со статусом по Чайлд-Пью А (28) и В (20)
- ТАХЭ/ ЧИЭ I резекция до проведения трансплантации
- Критерии для ТП: одиночная опухоль <5 см <3 опухоли <3 см
|
| Palienls at Risk |
| | Criteria met | 35 | 34 | 31 | 24 | 21 | 16 | 13 | 6 | 3 | | Criteria not met | 13 | 13 | 11 | 8 | 6 | 6 | 4 | 4 | 3 |
|
|
| 6. В качестве альтернативы ЧИЭ получил распространение метод РЧА. Этот метод также применяют чрескожно, он эффективен и редко оказывает побочные действия. В отличие от ЧИЭ для достижения полной абляции обычно бывает достаточно его однократного применения. Долгосрочные результаты по применению РЧА обнадеживают. В исследовании на 206 пациентах 5-летняя выживаемость у пациентов, перенесших РЧА, составила 41%. При этом стоит отметить, что в группе пациентов, имеющих статус А по Чайлд-Пью результаты лучше, чем в группе В. Также при одиночных опухолях выживаемость выше, чем при множественных. | 6. РЧА: долгосрочные результаты
- 1996-2003 гг.: 206 пациентов (187 получали лечение)
- Чайлд-Пью А, В; отсутствие показаний для хирургического лечения
- 1 ГЦК<5 см или <3 <3 см, или диаметр 2,8 см
- Медиана выживаемости 57 мес, 5 летняя выживаемость 41%
 |
|
| 7. ТАХЭ подлежат пациенты, находящиеся в группе В по Барселонской классификации. ТАХЭ или трансартериальная эмболизация (ТАЭ) относятся к методам местного интервенционного воздействия. Учитывая преимущественно артериальный тип снабжения ГЦК, после селективной катетеризации ветви A. hepatica, снабжающей опухоль, вводится липиодол - масляный контрастный препарат, накапливающийся большей частью опухолевыми клетками, смешанный с химиотерапевтическими средствами. При хорошей переносимости курсы терапии в зависимости от ответа на лечение могут быть проведены повторно с интервалами в несколько месяцев. В настоящий момент ТАХЭ является стандартом лечения пациентов с промежуточной стадией ГЦК. Представленный метаанализ демонстрирует эффективность ТАХЭ в сравнении с контрольной группой (ТАЭ). Следует, однако, учитывать, что результаты данной процедуры зависят от опыта рентгенолога. | 7. BCLC B: метаанализ ТАХЭ по сравнению с контролем
| Study |
Number of patients |
| Lin et al, 1988104 |
63 |
| GETCH, 1995106 |
96 |
| Bruix et al., 1998107 |
80 |
Pelletier et al.,
1998105 |
73 |
| Lo et al. 2002109 |
79 |
| Llovel et al., 2002110 |
112 |
Overall 503
Heterogeneity p=0,14 |
 |
- Метаанализ, 7 РКИ ТАХЭ/ТАЭ, 545 пациентов
- ТАХЭ с докоорубицином или циллатином, 2-годичные результаты
- Выживаемость ТАХЭ (4 исследования, 323 пациента): OR 0,42 (95% CI 0,2-0,88)
- Нет преимущества ТАЭ (3 исследования, 215 пациентов): OR 0,59 (95% CI 0,3-1,2)
- Клинический ответ: 35% (16-51%)
Примечание- OR - относительный риск, СI - доверительный интервал. |
|
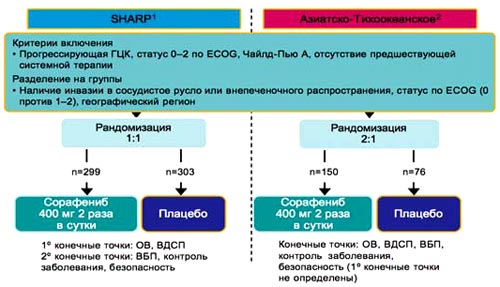
| 8. У пациентов с прогрессирующей стадией (С) по BCLC на различных популяциях проводились исследования SHARP и Азиатско-Тихоокеанское исследование. Критериями включения были статус 0-2 по классификации ECOG, стадия А по Чайлд-Пью, отсутствие предшествующей системной терапии. Стратегия лечения в двух испытаниях была одинаковой: после рандомизации пациентов 1 группа получала сорафениб в дозе 400 мг дважды в день, вторая группа получала плацебо. Оценивались конечные точки: общая выживаемость (ОВ), время до симптоматического прогрессирования (ВДСП), время без прогрессирования (ВБП), контроль заболевания (частичная ремиссия и стабилизация), а также безопасность терапии. | 8. Дизайн исследования SHARP (III фаза) и Азиатско-Тихоокеанского исследования
1 Lioirer JM et al. N Engl J Med 2008; 359: 378-90;
2Cheng A et el. J Clin Oncol 2006; 26; abstract 4509.
|
|
| 9. По результатам исследования SHARP, применение сорафениба позволило улучшить показатель общей выживаемости у пациентов с ГЦК по сравнению с плацебо (10,7 мес против 7,9 мес). Данные по Азиатско-Тихоокеанскому исследованию аналогичны, однако эффективность лечения сорафенибом не столь выраженная, так как пациенты находились на более поздней стадии заболевания (медиана ОВ 6,5 мес против 4,2 мес). | 9. Сорафениб увеличивает общую выживаемость по сравнению с плацебо
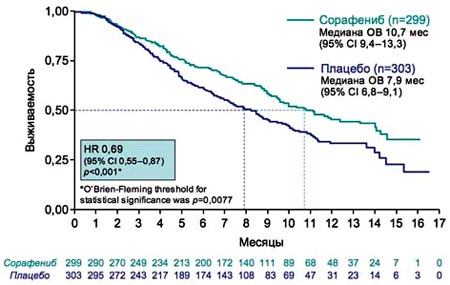
ОВ – общая выживаемость.
Liovet JM et al, N Engl J Med 2008г 359:370-90
|
|
| 10. В исследовании SHARP также удалось достичь увеличения ВБП при применении сорафениба (5,5 мес против 2,8 мес). Таким образом, сорафениб является новым стандартом лечения у пациентов с прогрессирующей стадией ГЦК, имеющих инвазию опухоли в сосудистое русло и внепеченочные проявления. Комбинировать сорафениб с другими методами терапии не рекомендуется, так как не накоплено достаточно данных по их совместному применению. | 10. SHARP: сорафениб остонавливает прогрессию

HR - hazard ratio.
Liovet JM et al, N Engl J Med 2008г 359:370-90
|
|
| 11. Официальных рекомендаций по последующему контролю состояния пациентов не существует. По рекомендациям нашей клиники после резекции печени, трансплантации, инъекции этанола в 1-й год проводится УЗИ с контрастным усилением, КТ или МРТ каждые 3 мес. Начиная со 2-го года визуализирующие методы обследования проводятся раз в 6 мес. При применении паллиативного лечения (ТАХЭ, сорафениб) проведение УЗИ с контрастным усилением, КТ или МРТ рекомендовано 1 раз в 3 мес. | 11. Контроль состояния пациентов в период наблюдения
- Отсутствие рекомендаций в руководствах
- Наблюдение после лечения
- 1 год: визуализация (УЗИ с контрастным усилением/КТ/МРТ) 1 раз в 3 мес
- 2 год и далее: визуализация 1 раз в 6 мес
- Наблюдение после паллиативной терапии
- Визуализация (УЗИ с контрастным усилением/КТ/МРТ /КТ/МРТ) 1 раз в 3 мес
|
|










