Лабораторное обеспечение регистра пациентов, получающих препарат ритуксимаб (Мабтеру)
СтатьиОпубликовано в журнале:
«Научно-практическая ревматология» 2008, приложение к № 1, С. 21-28
Е.Н. Александрова
В настоящее время в клинических исследованиях продемонстрирована высокая эффективность ритуксимаба для лечения ревматоидного артрита (РА), системной красной волчанки (СКВ), синдрома Шегрена (СШ), АНЦА-ассоциированных васкулитов, антифофсолипидного синдрома (АФС) и многих других аутоиммунных и хронических воспалительных заболеваний, относящихся к числу наиболее распространенных и тяжелых форм патологии человека.
В основе аутоиммунитета лежит нарушение толерантности к собственным антигенам, приводящее к развитию иммунного ответа против нормальных тканей, как если бы они были чужеродными для организма. Иммунный ответ, направленный против ограниченного числа аутоантигенов, присутствующих в определенных тканях, приводит к локальному органоспецифическому воспалению, характерному для аутоиммунных эндокринопатий и заболеваний нервной системы. Иммунный ответ против множества аутоантигенов, присутствующих во всех тканях (нуклеиновые кислоты, нуклеопротеиды, белки плазмы), индуцирует генерализованное (системное) воспаление. Аутоиммунные заболевания характеризуются наличием аутореактивных лимфоцитов в пораженных тканях и циркулирующих аутоантител - иммуноглобулинов, направленных против собственных антигенов. Наряду с нарушением иммунорегуляции важную роль в патогенезе аутоиммунных заболеваний играют генетические и внешнесредовые факторы.
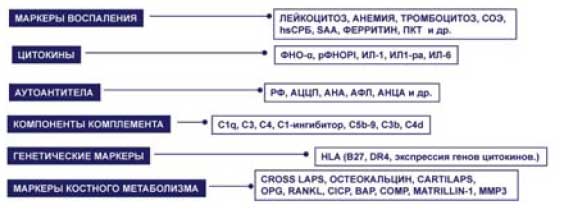
Лабораторная диагностика аутоиммунных и системных воспалительных заболеваний включает определение маркеров воспаления (лейкоцитоз, анемия, тромбоцитопения, СОЭ; белки острой фазы воспаления - С-реактивный белок, сывороточный амлоидный белок А, ферритин, прокальцитонин), аутоантител (ревматоидный фактор - РФ, анттела к циклическому цитрулинированному пептиду -АЦЦП, антинуклеарные антитела - АНА, антитела к фосфолипидам - аФЛ, антинейтрофильные цитоплазматические антитела - АНЦА), компонентов комплемента, провоспалительных цитокинов и их растворимых рецепторов (фактор некроза опухоли - ФНО и рФНОР, интерлейкин - ИЛ-1 и антагонист рецептора ИЛ-1, ИЛ-6), субпопуляций лимфоцитов, генетических маркеров, маркеров костного метаболизма. Эти лабораторные биомаркеры имеют важное значение для диагностики аутоиммунных заболеваний, мониторирования активности патологического процесса, оценки прогноза болезни и эффективности проводимой терапии.
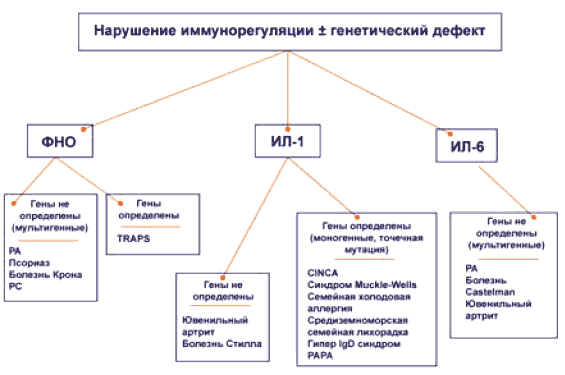
В настоящее время выделяют три группы цитокинзависимых иммуновоспалительных заболеваний с преимущественной гиперпродукцией ФНО, ИЛ-1 или ИЛ-6, патогенез которых обусловлен нарушением Т-клеточной иммунорегуляции. Данная медицинская концепция является основанием для применения генно-инженерных биологических препаратов, блокирующих активность соответствующих цитокинов.
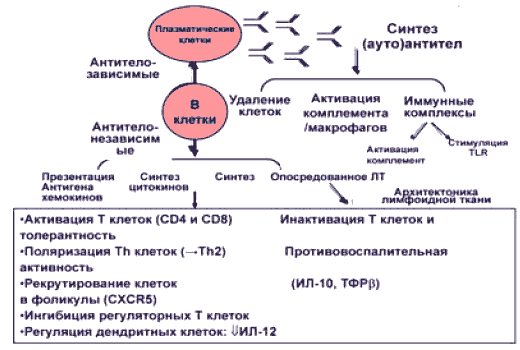
В последние годы установлено, что наряду с Т клетками важную роль в развитии аутоиммунных заболеваний играют аутореактивные В-клетки. В-клетки синтезируют аутоантитела (РФ, АЦЦП и др.), участвуют в презентации антигена Т-клеткам, являются продуцентами провоспалительных цитокинов.
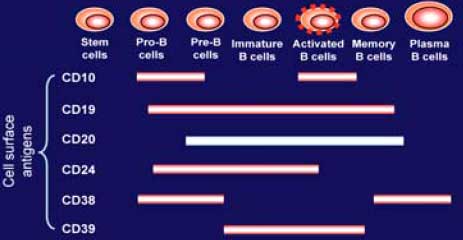
Выбор CD20 антигена в качестве мишени для моноклональных антител связан с особенностями дифференцировки В-клеток, которые в процессе созревания от стволовых клеток в плазматические клетки проходят несколько последовательных стадий, для каждой из которых характерна экпрессия определенных мембранных молекул. Экспрессия CD20 наблюдается на мембране ранних и зрелых В клеток, но не на стволовых, про В-клетках, дендритных клетках и плазматических клетках. Поэтому применение ритуксимаба приводит к истощению зрелых В-клеток, но не отменяет регенерацию пула В-клеток и синтез иммуноглобулинов плазматическими клетками. Для оценки эффективности терапии ритуксимабом в измеряют количество CD19 клеток в периферической крови и синовиальной ткани методом проточной цитофлюорометрии.
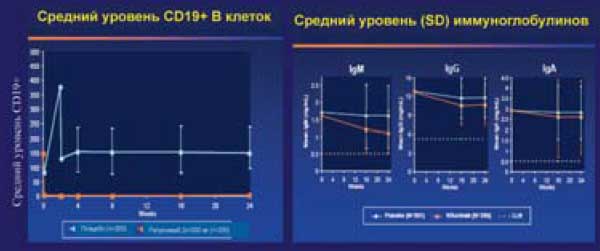
Имеются данные о резком снижении числа В-лимфоцитов в крови больных РА в течение 24 недель после введения ритуксимаба при незначительном снижении уровня иммуноглобулинов в сыворотке крови.
При использовании высокочувствительного метода проточной цитофлюорометрии выявлено неполное удаление В-клеток на 2-ой неделе после введения ритуксимаба и более раннее восстановление их количества (через 9 месяцев) по сравнению с обычным методом цитофлюорометрии.
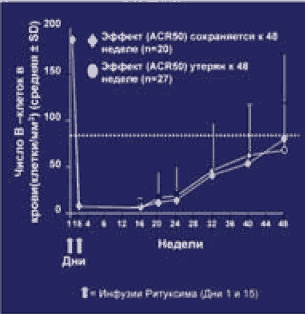
Восстановление В-клеток начинается через 16 недель после назначения мабтеры и к 24 неделе достигает одинакового уровня как у пациентов с сохранением, так и у пациентов с утратой клинического эффекта, т.е. удаление В-клеток не отменяет эффект ритуксимаба.
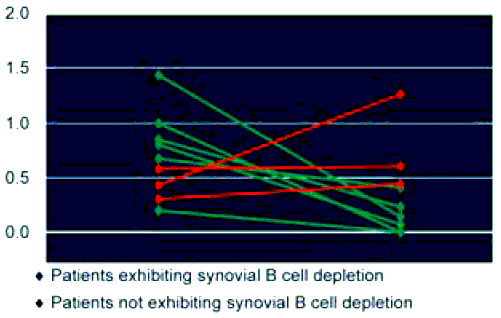
Отмечается корреляция между уровнем деплеции В-клеток в периферической крови (на 15 день после введения Мабтеры) и в синовиальной ткани (через 6 месяцев после введения Мабтеры). В большинстве случаев при РА наблюдается снижение числа В клеток в синовиальной мембране через 6 мес. после введения препарата, однако у некоторых больных деплеции синовиальных В-лимфоцитов не наблюдается.
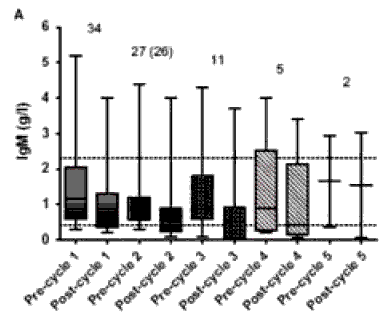
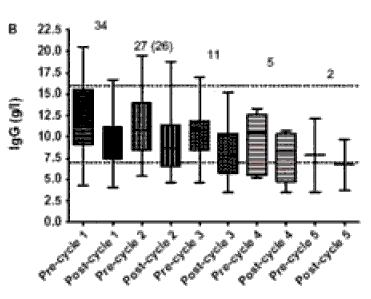
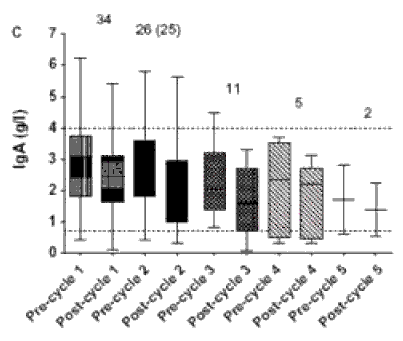
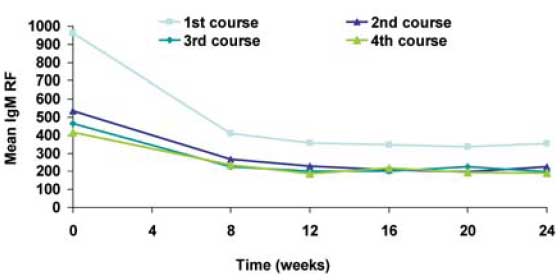
Наиболее часто у больных РА отмечается уменьшение концентрации IgM ниже нормы, которое однако не ассоциируется с нарастанием частоты инфекционных осложнений. При повторных введениях ритуксимаба значительное снижение сывороточного уровня IgM наблюдалось у 12, IgG - у 7, IgA - у 1 из 22 больных РА. Эти данные свидетельствуют о необходимости мониторировать уровень сывороточных иммуноглобулинов при лечении ритуксимабом.
Аутоантитела, как известно, являются основными диагностическими маркерами ревматических аутоиммунных заболеваний. Наиболее важными серологическими маркерами РА являются РФ и АЦЦП. Ревматоидные факторы -IgG, IgM, IgA антитела к Fc фрагменту IgG, определяемые методами латекс-агглютинации, иммуноферментного анализа и нефелометрии. Наибольшее клиническое значение имеет IgМ-РФ (чувствительность 60-80%, специфичность-80-93%). Увеличение титров РФ является диагностическим критерием РА.
АЦЦП - новый высокоспецифичный и чувствительный серологический маркер РА (чувствительность 41-80%, специфичность 93-99%), определяемый методом иммуноферментного анализа. Определение АЦЦП очень полезно для диагностики раннего РА, подтверждения диагноза серонегативного РА и дифференциальной диагностики с другими РЗ, для прогнозирования тяжелого эрозивного поражения суставов.
Выраженное и стойкое снижение концентрации РФ наблюдается к 8 неделе после введения ритуксимаба и продолжается в течение 24 недель.
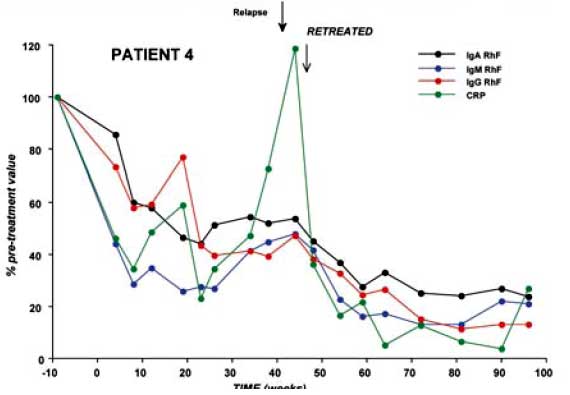
Как показано на слайде, к 30 неделе у пациента произошло нарастание уровня РФ и СРБ, развилось обострение заболевания, что явилось основанием для назначения повторного курса ритуксимаба.
Данные о влиянии ритуксимаба на уровень АЦЦП противоречивы.
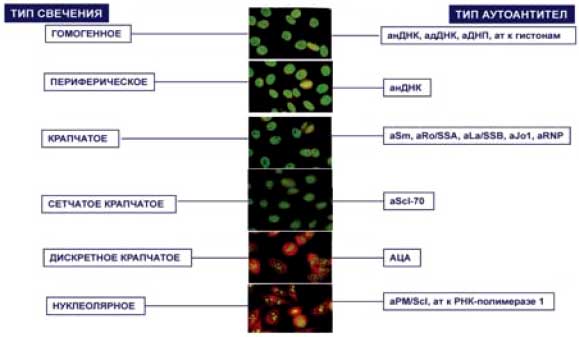
Антинуклеарные антитела - гетерогенная группа антител, реагирующих с различными компонентами ядра. Стандартным скрининговым тестом для определения антинуклеарных антител (в этом случае их обозначают как АНФ) является метод непрямой иммунофлюоресценции с использованием в качестве субстрата криостатных срезов мышиной печени и НЕр-2 клеток человека. Использование НЕр-2 леток предпочтительнее, т.к. позволяет повысить чувствительность метода и выявлять некоторые типы свечения, которые не обнаруживаются на криостатных срезах (антитела к центромере, аRo). Клиническое значение АНФ зависит от титра и типа свечения. Гомогенное свечение характерно для антител к нДНК, ДНП, гистонам; периферическое - для анДНК; крапчатое - для аSm, aRo/La, aRNP, aJo1; сетчатое крапчатое - для aScl 70; дискретное крапчатое - для антител к центромере; нуклеолярное - для аPM/Scl, аРНК-полимеразе 1. С целью подтверждения диагноза у АНФ положительных пациентов рекомендуется определение специфических АНА к отдельным компонентам ядра, используя подтверждающие тесты (иммуноферментный анализ, иммуноблот, двойная иммунодиффузия и др.).
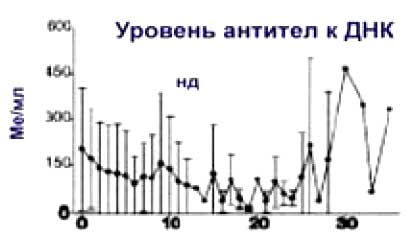
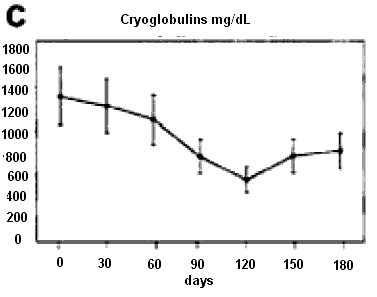
Данные о влиянии ритуксимаба на уровень антител к ДНК противоречивы. Одни исследователи не отмечали достоверного снижения титров аДНК на протяжении 30 недель после деплеции В-лимфоцитов, другими авторами показано уменьшение сывороточной концентрации аДНК у большинства больных СКВ. В частности, через 6 месяцев после деплеции В-клеток ритуксимабом у больных СКВ наблюдалось достоверное снижение уровня антител к ДНК и гистонам, в то время как уровень антимикробных антител (к столбнячному токсину и пневмококковому полисихариду) не изменялся.
В недавнем исследовании показано, что повышение уровня антител к экстрагируемым ядерным антигенам является предиктором обострения СКВ и индикатором необходимости повторного введения препарата.
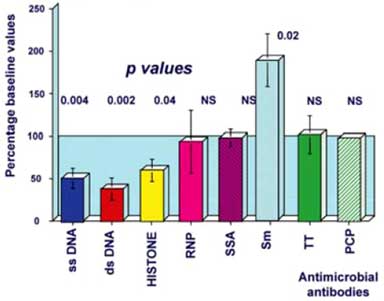
Получены также интересные данные о снижении уровня криоглобулинов на фоне терапии ритуксимабом.
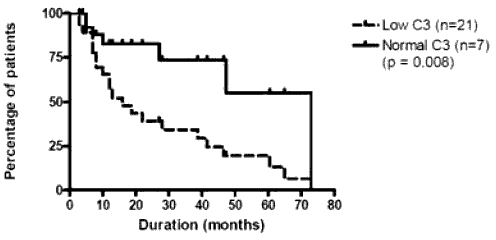
При СКВ у большинства больных показано увеличение концентрации С3 компонента комплемента после приема препарата. Получены данные о повышении уровня С4 на фоне лечения ритуксимабом. Снижение уровня С3 рассматривается как предиктор обострения СКВ и является основанием для повторного введения препарата.
Среди маркеров воспаления наибольшее клиническое значение для оценки эффективности мабтеры имеют СОЭ и СРБ.
У больных РА установлено выраженное снижение СОЭ на фоне лечения мабтерой. При этом эффект снижения СРБ сохраняется после начала восстановления числа В клеток в периферической крови. Имеются данные, что СРБ остается сниженным на 75% по сравнению с его базальным уровнем в течение 5 циклов лечения ритуксимабом.
Согласно рекомендациям Эдвардса при РА оптимальными лабораторными маркерами для мониторирования терапии ритуксимабом являются CD19+В-клетки, IgG, СРБ и IgM РФ. Определение этих маркеров следует проводить до введения препарата, через 1 месяц после введения, далее 1 раз в 2 месяца. Наилучшим предиктором обострения является РФ
Учитывая потенциальную возможность реактивации гепатита В на фоне лечения ритуксимабом консенсус 2006 года по использованию ритуксимаба у больных РА рекомендует наряду с выполнением рутинных лабораторных тестов (общий и биохимический анализ крови, анализ мочи) и определением уровня иммуноглобулинов обязательное исследование маркеров гепатита В до начала терапии ритуксимабом. Наряду с этим большинством экспертов указывается на неэффективность мониторирования В-клеток в обычной клинической практике.
Таким образом, важнейшими лабораторными биомаркерами для обеспечения регистра больных, получающих ритуксимаб, являются: маркеры воспаления (СОЭ, СРБ), аутоантитела (РФ, АЦЦП, аДНК, аЭЯА, АНЦА), иммуноглобулины, криоглобулины, С3 и С4 -компоненты комплемента,
CD19+В-клетки, тесты на гепатит В, а также прокальцитониновый тест для дифференциальной диагностики бактериальной инфекции и сепсиса от обострения аутоиммунного заболевания.
Лабораторными индикаторами обострения заболевания, которые могут служить основанием для повторного введения ритуксимаба, являются: при РА - восстановление количества В клеток в периферической крови и синовиальной ткани при достаточном уровне IgG, повышение концентрации СРБ более, чем на 50% от исходного уровня непосредственно после предшествующего введения препарата, увеличение титров IgM РФ; при СКВ - наряду с восстановлением числа В-клеток - увеличение концентрации антител к экстрагируемым ядерным антигенам и снижение уровня С3-компонента комплемента.
ЛАБОРАТОРНОЕ ОБЕСПЕЧЕНИЕ РЕГИСТРА ПАЦИЕНТОВ ПОЛУЧАЮЩИХ ПРЕПАРАТ РИТУКСИМАБ (МАБТЕРУ)
Е.Н. Александрова, А.А. Новикова, Е.Л. Насонов
ГУ Институт ревматологии РАМН
Москва
2007
Заболевании, при которых продемонстрирована эффективность Ритуксимаба
| Аутоиммунные Ревматоидный артрит (суставы) Системная красная волчанка (системность) Синдром Шегрена (железы внешней секреции) АНЦА-ассоциированные васкулиты (сосуды) Антифосфолипидный синдром (сосуды) Идиопатическая тромбоцитопения (тромбоциты) Аутоиммунная гемолитическая анемия (эритроциты) Синдром Гийена Барре (периферическая нервная система) Хроническая иммунная полинейропатия (периферическая нервная система) Аутоиммунный тиреоидит (щитовидная железа) Сахарный диабет типа I (поджелудочная железа) Болезнь Адисона (надпочечники) Мембранозная нефропатия (почки) Болезнь Гудпасчера (почки, лёгкие) Аутоиммунный гастрит (желудок) Пернициозная анемия (желудок) Пузырчатка (кожа, слизистые) Первичный билиарный цирроз (печень) Дерматомиозит, полимиозит (скелетная мускулатура) Миастения (скелетная мускулатура) Целиакия (тонкий кишечник) |
Воспалительные IgA нефропатия (почки) Другие
|
АУТОИММУНИТЕТ
Нарушение толерантности к собственным антигенам, приводящее к развитию иммунного ответа против нормальных тканей, как если бы они были чужеродны для организма.
- Иммунный ответ против небольшого числа аутоантигенов, присутствующих в определенных тканях, приводит к локальному (органоспецифическому) воспалению, особенно характерному для аутоиммунных эндокринопатии и заболевании нервной системы.
- Иммунный ответ против множества аутоанти генов, присут¬ствующих во всех тканях (нуклеиновые кислоты, нуклеопротеиды, белки плазмы и др), приводит к развитию генерали¬зованного (системного) воспаления.
ПАТОГЕНЕЗ АУТОИМУННЫХ ЗАБОЛЕВАНИЙ
Primer: the practical use of biological markers of rheumatic and systemic inflammatory diseases
РОЛЬ В КЛЕТОК В РАЗВИТИИ АУТОИММУННЫХ БОЛЕЗНЕЙ
В клетки
REFLEX: ДИНАМИКА ЛАБОРАТОРНЫХ ПОКАЗАТЕЛЕЙ
HIGH SENSITIVITY FLOW CYTOMETRY REVEALS INCOMPLETE DEPLETION AND EARLIER RETURN OF В CELLS AFTER THERAPY
| Patients with detectable В cells | |
| At 2 weeks, highly sensitive methods reveal large differences in В cell depletion. High sensitivity also identified return of В cells earlier than standard techniques | 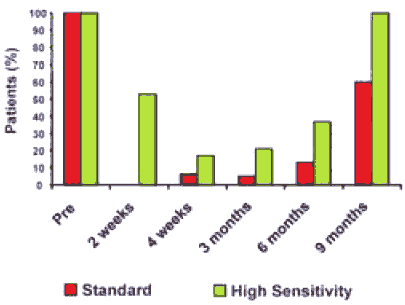 |
КЛИНИЧЕСКИЙ ЭФФЕКТ В ЗАВИСИМОСТИ ОТ УРОВНЯ B-КЛЕТОК
|
Число В-клеток к 24 неделе в зависимости от эффекта (ACR50) терапии |
|
| - Фармакокинетика ритуксимаба не меняется при совместном введении с циклофосфаном (ЦФ) или метотрексатом (МТ) - Восстановление В-клеток начинается через 16 недель - Удаление В-клеток не определяет клинический эффект ритуксимаба - Восстановление В-клеток не отменяет эффект ритуксимаба - Решение о необходимости повторных курсов должно основываться на оценке клинических данных |
 |
LEVEL OF INITIAL В CELL DEPLETION (DAY 15) IN PB CORRELATES WITH LATER SYNOVIAL В CELL EXPRESSION
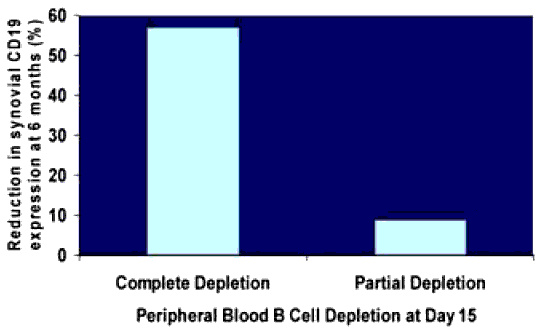
SYNOVIAL B CELL SCORES PRE- AND 6 MONTHS POST-TREATMENT WITH RTX
УРОВЕНЬ IgM В СЫВОРОТКАХ БОЛЬНЫХ РА ПРИ ПОВТОРНЫХ ЦИКЛАХ ТЕРАПИИ РИТУКСИМАБОМ (МАБТЕРОЙ)
УРОВЕНЬ IgG В СЫВОРОТКАХ БОЛЬНЫХ РА ПРИ ПОВТОРНЫХ ЦИКЛАХ ТЕРАПИИ РИТУКСИМАБОМ (МАБТЕРОЙ)
ПОВТОРНЫЕ КУРСЫ РИТУКСИМАБА
суммарный анализ безопасности
|
Число пациентов с низкой концентрацией Ig в период лечения |
|||
| Курс 1 (n=1039) | Курс 2 (n=570) | Курс З (n=191) | |
| Общий Ig <НГН | 0,1% | 0,7% | - |
| IgG <НГН | 1,4% | 4,3% | 5,9% |
| IgM <НГН | 10,3% | 18,5% | 23,5% |
|
Частота тяжелых инфекций до и после снижения |
||
| Всего (n=207) | До снижения IgM <НГН | После снижения IgM <НГН |
| Тяжелые инфекции*/ 100 пациентов-год | 5,1 | 5,9 |
| 95% ДИ | (2,6-10,2) | (3,4-10,2) |
| *Тяжелые или требующие антибактериальной терапии (в/в) | ||
УРОВЕНЬ IgA В СЫВОРОТКАХ БОЛЬНЫХ РА ПРИ ПОВТОРНЫХ ЦИКЛАХ ТЕРАПИИ РИТУКСИМАБОМ (МАБТЕРОЙ)
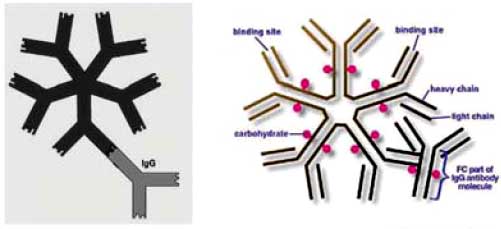
РЕВМАТОИДНЫЙ ФАКТОР (РФ)
IgM антитела к Fc-IgG
Методы определения: латекс-агглютинация (>1/40), ИФА (>15 МЕ/мл), нефелометрия (>15 МЕ/мл), чувствительность 60-80%, специфичность 80-93%.
АНТИТЕЛА К ЦИКЛИЧЕСКОМУ ЦИТРУЛЛИНИРОВАННОМУ ПЕПТИДУ (АЦЦП)
| АЦЦП представляют собой аутоантитела, взаимодействующие с синтетическими пептидами, содержащими атипичную (unusual) аминокислоту - цитруллин. | 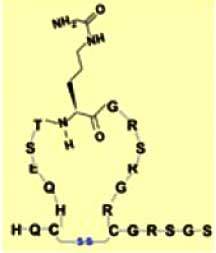 |
IGM RF LEVELS OVER TIME BY TREATMENT COURSE
INFLAMMATION FOLLOWS AUTOANTIBODIES (NOT В CELL LEVELS)
АНТИНУКЛЕАРНЫЙ ФАКТОР (АНФ) ГЕТЕРОГЕННАЯ ГРУППА АУТОАНТИТЕЛ, РЕАГИРУЮЩИХ С КОМПОНЕНТАМИ ЯДРА
Метод определения: НИФ с использованием криостатных срезов мышиной печени (>1/40) и HEp-2 клеток человека (>1/100)
ДИНАМИКА ЛАБОРАТОРНЫХ ПОКАЗАТЕЛЕЙ
SLE: ANTIBODY LEVELS 6 MONTHS AFTER В CELL DEPLETION
Efficacy and safety of rituximab in type II mixed cryoglobulinemia
В Lymphocyte Depletion Therapy in Children With Refractory Systemic Lupus Erythematosus
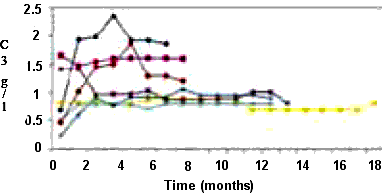
Efficacy and safety of rituximab in type II mixed cryoglobulinemia
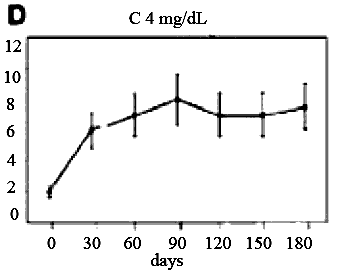
Baseline serum C3 and time to flare after BCDT
ЛАБОРАТОРНЫЕ ПРЕДИКТОРЫ ОТВЕТА НА ТЕРАПИЮ РУТИКСИМАБОМ (МАБТЕРОЙ)
| CD19+ В клетки |
| IgG |
| hsCPБ |
| IgM РФ |
| ENA |
| СЗс |
Safety and Efficacy of Rituximab in Patients with Rheumatoid Arthritis Refractory to Disease Modifying Antirheumatic Drugs and Anti-Tumor Necrosis Factor-a Treatment
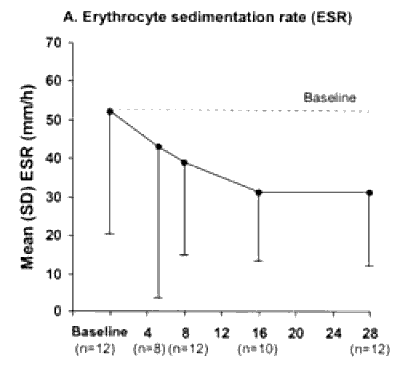
Currently our impression is that monitoring оf CDl9+ В cells, IgG, CRP and IgM RF titre pre-treatment. 1 month post-treatment, then bi-monthly, with clinical state often assessable by telephone or email, is optimal for intelligent re-treatment.
ОБСЛЕДОВАНИЯ ДО НАЗНАЧЕНИЯ ТЕРАПИИ
Consensus statement on the use or rituximab in patients with rheumatoid arthritis
J S Smolen, E C Keystone, P Emery, F C Breedveld, N Betteridge, G R Burmester, M Dougados, G Ferraccioli, U Jaeger, L Klareskog, T K Kvien, E Martin-Mola, K Pavelka The Working Group on the Rituximab Consensus Statement
Annals of the Rheumatic Diseases 2007;66:143-150
Лабораторные тесты
- Рутинные лабораторные тесты
- Уровень иммуноглобулинов (IgG, IgA, IgM)
- Маркеры вируса гепатита В
ИНФЕКЦИЯ ВИРУСАМИ ГЕПАТИТА В, С И ВИЧ
Данные, касающиеся применения ритуксимаба, у пациентов с РА, являющихся носителями гепатита В, С и ВИЧ отсутствуют
В онкологии
- успешное применение у носителей гепатита С без прояилактики (Уровень доказательности IV)
- успешное применение у носителей гепатита В на фоне профилактики ламивудином (Уровень доказательности IV)
- развитие фулминантного гепатита на фоне реактивации инфекции вирусом гепатита В
- не увеличивает риск обострения ВИЧ (Уровень доказательности lib)
ОСНОВНЫЕ ЛАБОРАТОРНЫЕ БИОМАРКЕРЫ ДЛЯ ОБЕСПЕЧЕНИЯ РЕГИСТРА ПАЦИЕНТОВ ПОЛУЧАЮЩИХ ПРЕПАРАТ РИТУКСИМАБ (МАБТЕРА)
| СОЭ СРБ |
IgM, IgG. IgA. Криоглобулины, СЗ,С4 |
| Аутоантитела: IgM РФ АЦЦП |
CD19+ В клетки |
| AHA: анти-ДНК Антитела к нуклеосомам Антитела к гистонам Анти-RNP Анти-Sm Анти-SSA АНЦА |
Прокальцитониновый тест HBS-Ag |
Комментарии
ПРАКТИКА ПЕДИАТРА
