Антигистаминные препараты: мифы и реальность
СтатьиОпубликовано в журнале:
«ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ»; № 5; 2014; стр. 50-56.
Т.Г. Федоскова
ГНЦ Институт иммунологии ФМБА России, Москва
К основным препаратам, воздействующим на симптомы воспаления и контролирующим течение заболеваний аллергического и неаллергического генеза, относятся антигистаминные средства.
В статье проанализированы дискуссионные моменты, касающиеся опыта применения современных антигистаминных препаратов, а также их некоторых основных характеристик. Это позволит дифференцированно подходить к выбору оптимального препарата при проведении комплексной терапии различных заболеваний.
Ключевые слова: антигистаминные препараты, аллергические заболевания, цетиризин, Цетрин
ANTIHISTAMINES: MYTHS AND REALITY
T.G. Fedoskova
State Science Center Institute of Immunology, Federal Medical and Biological Agency, Moscow
Antihistamines belong to main drugs influencing symptoms of inflammation and controlling course both of allergic and non-allergic diseases. In this paper debatable issues regarding experience of using current antihistamines as well as some of their characteristics are analyzed. It may let to make a differential choice to administer appropriate drugs for a combination therapy of different diseases.
Key words: antihistamines, allergic diseases, cetirizine, Cetrine
Антигистаминные препараты 1-го типа (Н1-АГП), или антагонисты гистаминовых рецепторов 1-го типа, широко и успешно применяются в клинической практике уже более 70 лет. Их используют в составе симптоматической и базисной терапии аллергических и псевдоаллергических реакций, комплексном лечении острых и хронических инфекционных заболеваний различного генеза, в качестве премедикации при проведении инвазивных и рентгеноконтрастных исследований, оперативных вмешательствах, для профилактики побочных эффектов вакцинации и т.д. Иными словами, Н1-АГП целесообразно применять при состояниях, обусловленных высвобождением активных медиаторов воспаления специфического и неспецифического характера, основным из которых является гистамин.
Гистамин обладает широким спектром биологической активности, реализуемой путем активации клеточных поверхностных специфических рецепторов. Основным депо гистамина в тканях являются тучные клетки, в крови - базофилы. Он также присутствует в тромбоцитах, слизистой оболочке желудка, эндотелиальных клетках и нейронах головного мозга. Гистамин обладает выраженным гипотензивным действием и представляет собой важный биохимический медиатор при всех клинических симптомах воспаления различного генеза [1]. Именно поэтому антагонисты данного медиатора остаются наиболее востребованными фармакологическими средствами.
В 1966 г. была доказана гетерогенность гистаминовых рецепторов. В настоящее время известно 4 типа гистаминовых рецепторов - Н1, Н2, Н3, Н4, относящихся к суперсемеиству рецепторов, связанных с G-белками (G-protein-coupled receptors -GPCRs [2]). Стимуляция Н1-рецепторов приводит к высвобождению гистамина и реализации симптомов воспаления в основном аллергического генеза. Активация Н2-рецепторов способствует повышению секреции желудочного сока и его кислотности. Нз-рецепторы представлены преимущественно в органах центральной нервноИ системы (ЦНС). Они выполняют функцию чувствительных к гистамину пресинаптических рецепторов в головном мозге, регулируют синтез гистамина из пресинаптических нервных окончаний. Недавно был идентифицирован новый класс гистаминовых рецепторов, экспрессируемых преимущественно на моноцитах и гранулоцитах, - Н4. Эти рецепторы представлены в костном мозге, тимусе, селезенке, легких, печени, кишечнике [3]. Механизм действия Н1-АГП основан на обратимом конкурентном ингибировании гистаминовых Н1-рецепторов: они предупреждают или сводят к минимуму воспалительные реакции, предупреждая развитие индуцируемых гистамином эффектов, причем их эффективность обусловлена способностью конкурентно ингибировать влияние гистамина на локусы специфических Н1-рецепторных зон в эффекторных структурах тканей [4].
В настоящее время в России зарегистрировано свыше 150 наименований противогистаминных препаратов. Это не только Н1-АГП, но и препараты, повышающие способность сыворотки крови связывать гистамин, а также препараты, тормозящие высвобождение гистамина из тучных клеток [1, 5]. Из-за многообразия антигистаминных средств сделать выбор между ними для их максимально эффективного и рационального использования в конкретных клинических случаях достаточно сложно. В связи с этим возникают дискуссионные моменты, а зачастую рождаются мифы о применении широко используемых в клинической практике Н1-АГП. В отечественной литературе представлено множество работ по указанной теме [1, 2, 5-7], однако единого мнения о клиническом использовании указанных лекарственных средств (ЛС) не существует.
Миф о трех поколениях антигистаминных препаратов
Многие заблуждаются, думая, что существует три поколения антигистаминных средств. Некоторые фармацевтические компании представляют новые препараты, появившиеся на фармацевтическом рынке, как АГП третьего - новейшего - поколения. К третьему поколению пытались отнести метаболиты и стереоизомеры современных АГП. В настоящее время считается, что эти ЛС - АГП второго поколения, поскольку между ними и предыдущими препаратами второго поколения существенной разницы нет. Согласно Консенсусу по антигистаминным препаратам название «третье поколение» решено зарезервировать для обозначения синтезируемых в будущем АГП, которые по ряду основных характеристик скорее всего будут отличаться от известных соединений [8].
Различий между АГП первого и второго поколения много. Это прежде всего наличие или отсутствие седативного эффекта. Седативное действие при приеме АГП первого поколения субъективно отмечают 40-80% больных. Его отсутствие у отдельных пациентов не исключает объективного отрицательного действия этих средств на когнитивные функции, на которые пациенты могут не жаловаться (способность к управлению автомобилем, обучению и др.). Нарушение функции ЦHС наблюдается даже при использовании минимальных доз этих средств. Влияние АГП первого поколения на ЦHС такое же, как при использовании алкоголя и седативных препаратов (бензодиазепины и др.) [5].
Препараты второго поколения практически не проникают через гематоэнцефалический барьер, поэтому не снижают умственную и физическую активность пациентов. Кроме того, АГП первого и второго поколений отличаются наличием или отсутствием побочных эффектов, связанных со стимуляцией рецепторов другого типа, длительностью действия, развитием привыкания [5].
Первые АГП - фенбензамин (Антерган), пириламина малеат (Нео-Антерган) начали применять еще в 1942 г. [4]. Впоследствии появились новые АГП для использования в клинической практике. До 1970-х гг. были синтезированы десятки соединений, относящихся к препаратам данной группы.
С одной стороны, накоплен большой клинический опыт применения АГП первого поколения, с другой - эти препараты не проходили экспертизы в клинических исследованиях, соответствующих современным требованиям доказательной медицины.
Сравнительная характеристика АГП первого и второго поколений представлена в табл. 1 [5].
Таблица 1.
Сравнительная характеристика АГП первого и второго поколений
| Свойства | Первое поколение | Второе поколение |
| Седативный эффект и влияние на когнитивные функции | Есть (в минимальных дозах) | Нет (в терапевтических дозах) |
| Селективность в отношении Н1-рецепторов | Нет | Да |
| Фармакокинетические исследования | Мало | Много |
| Фармакодинамические исследования | Мало | Много |
| Научные исследования различных доз | Нет | Да |
| Исследования у новорожденных, детей, пожилых пациентов | Нет | Да |
| Использование у беременных | FDA категория B (дифенгидрамин, хлорфенирамин), категория C (гидроксизин, кетотифен) | FDA категория B (лоратадин, цетиризин, левоцетиризин), категория C (дезлоратадин, азеластин, фексофенадин, олопатадин) |
С 1977 г. фармацевтический рынок пополняется новыми Н1-АГП, имеющими явные преимущества перед ЛС первого поколения и отвечающими современным требованиям к АГП, изложенным в согласительных документах EAACI (European Academy of Allergology and Clinical Immunology -Европейская академия аллергологии и клинической иммунологии).
Миф о пользе седативного эффекта АГП первого поколения
Даже в отношении ряда побочных эффектов АГП первого поколения существуют заблуждения. С седативным эффектом Н1-АГП первого поколения связан миф о том, что их применение предпочтительно при лечении пациентов с сопутствующей бессонницей, а если этот эффект нежелателен, его можно нивелировать, применяя препарат на ночь. При этом следует помнить, что АГП первого поколения угнетают фазу быстрого сна, благодаря чему нарушается физиологический процесс сна, не происходит полноценной обработки информации во сне. При их использовании возможно нарушение дыхания, сердечного ритма, что повышает риск развития апноэ во сне. Кроме того, в ряде случаев применение высоких доз указанных ЛС способствует развитию парадоксального возбуждения, что также негативно влияет на качество сна. Необходимо учитывать различие в длительности сохранения противоаллергического эффекта (1,5-6 часов) и седативного эффекта (24 часа), а также тот факт, что длительная седация сопровождается нарушением когнитивных функций [6].
Наличие выраженных седативных свойств развенчивает миф о целесообразности использования Н1-АГП первого поколения у пациентов пожилого возраста, которые применяют указанные ЛС, руководствуясь сложившимися стереотипами привычного самолечения, а также рекомендациями врачей, недостаточно информированных о фармакологических свойствах препаратов и противопоказаниях к их назначению. Из-за отсутствия избирательности воздействия на альфа-адренорецепторы, мускариновые, серотониновые, брадикининовые и другие рецепторы противопоказанием к назначению указанных ЛС является наличие достаточно распространенных среди пожилого контингента пациентов заболеваний - глаукомы, доброкачественной гиперплазии предстательной железы, бронхиальной астмы, хронической обструктивной болезни легких и др. [2, 6].
Миф об отсутствии в клинической практике места для АГП первого поколения
Несмотря на то что Н1-АГП первого поколения (большинство из них разработано в середине прошлого века) способны вызывать известные побочные эффекты, они и сегодня широко применяются в клинической практике. Поэтому миф о том, что с появлением АГП нового поколения не осталось места для АГП предыдущего поколения, неправомочен. У Н1-АГП первого поколения имеется одно неоспоримое преимущество - наличие инъекционных форм, незаменимых при оказании экстренной помощи, премедикации перед проведением некоторых видов диагностического обследования, хирургических вмешательствах и т.д. Кроме того, некоторые препараты обладают противорвотным действием, снижают состояние повышенной тревожности, эффективны при укачивании. Дополнительный антихолинергический эффект ряда препаратов указанной группы проявляется в значительном снижении зуда и кожных высыпаний при зудящих дерматозах [9], острых аллергических и токсических реакциях на пищевые продукты, лекарственные препараты, укусы и ужаления насекомых [6, 7]. Однако назначать указанные ЛС необходимо со строгим учетом показаний, противопоказаний, тяжести клинических симптомов, возраста, терапевтических дозировок, побочных эффектов. Наличие выраженных побочных эффектов и несовершенство Н1-АГП первого поколения способствовало разработке новых антигистаминных ЛС второго поколения. Основными направлениями совершенствования препаратов стало повышение избирательности и специфичности, устранение седативности и толерантности к препарату (тахифилаксия).
Современные Н1-АГП второго поколения обладают способностью к селективному воздействию на Н1-рецепторы, не блокируют их, а, будучи антагонистами, переводят в «неактивное» состояние, не нарушая их физиологических свойств [10], оказывают выраженное антиаллергическое действие, быстрый клинический эффект, действуют продолжительно (24 часа), не вызывают тахифилаксии. Указанные ЛС практически не проникают через гематоэнцефалический барьер, поэтому не вызывают седативного эффекта, нарушения когнитивных функций.
Современные Н1-АГП второго поколения обладают значимым противоаллергическим эффектом - стабилизируют мембрану тучных клеток, подавляют индуцированное эозинофилами выделение интерлейкина-8, гранулоцитарно-макрофагального колониестимулирующего фактора (Granulocyte Macrophage Colony-Stimulating Factor. GM-CSF) и растворимой молекулы межклеточной адгезии 1 (Soluble Intercellular Adhesion Molecule-1, sICAM-1) из эпителиальных клеток, что способствует большей эффективности по сравнению с Н1-АГП первого поколения при проведении базисной терапии аллергических заболеваний, в генезе которых значительную роль играют медиаторы поздней фазы аллергического воспаления [2, 6].
Кроме того, важной характеристикой Н1-АГП второго поколения является их способность оказывать дополнительный противовоспалительный эффект за счет ингибирования хемотаксиса эозинофилов и нейтрофильных гранулоцитов, уменьшения экспрессии на эндотелиальных клетках молекул адгезии (ICAM-1), ингибирования IgE-зависимой активации тромбоцитов и выделения цитотоксических медиаторов [1, 4]. Многие врачи не уделяют этому должного внимания, однако перечисленные свойства обусловливают возможность применения таких ЛС при воспалении не только аллергической природы, но и инфекционного генеза.
Миф об одинаковой безопасности всех АГП второго поколения
Среди врачей существует миф о том, что все Н1-АГП второго поколения сходны по своей безопасности. Однако в этой группе ЛС существуют отличия, связанные с особенностью их метаболизма. Они могут зависеть от вариабельности экспрессии фермента CYP3A4 системы цитохрома Р 450 печени. Такая вариабельность может быть обусловлена генетическими факторами, заболеваниями органов гепатобилиарной системы, одновременным приемом ряда ЛС (антибиотики макролидного ряда, некоторые антимикотические, противовирусные препараты, антидепрессанты и др.), продуктов (грейпфрут) или алкоголя, оказывающих ингибирующее воздействие на оксигеназную активность CYP3A4 системы цитохрома Р450 [2, 6].
Cреди Н1-АГП второго поколения выделяют:
Рис. 1. Особенности метаболизма Н1-АГП второго поколения 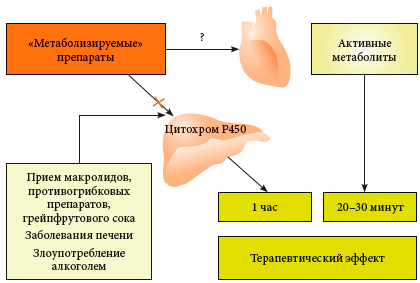
Преимущества активных метаболитов, прием которых не сопровождается дополнительной нагрузкой на печень, очевидны: быстрота и предсказуемость развития эффекта, возможность совместного приема с различными ЛС и пищевыми продуктами, подвергающимися метаболизму с участием цитохрома P450.
Миф о более высокой эффективности каждого нового АГП
Миф о том, что появившиеся в последние годы новые Н1-АГП средства заведомо эффективнее предыдущих, также не нашел подтверждения. Работы зарубежных авторов [10-12] свидетельствуют о том, что Н1-АГП второго поколения, например цетиризин, обладают более выраженной противогистаминной активностью, чем ЛС второго поколения, появившиеся значительно позже (рис. 2).
Рис. 2. Противогистаминная сравнительная активность цетиризина и дезлоратадина по действию на кожную реакцию, вызванную введением гистамина, в течение 24 часов [10]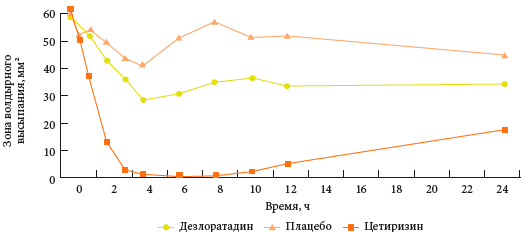
Следует отметить, что среди Н1-АГП второго поколения цетиризину исследователи отводят особое место. Разработанный в 1987 г., он стал первым оригинальным высокоизбирательным антагонистом Н1-рецепторов, полученным на основе фармакологически активного метаболита ранее известного антигистаминного средства первого поколения - гидроксизина. До настоящего времени цетиризин остается своеобразным эталоном противогистаминного и противоаллергического действия, используемым для сравнения при разработке новейших антигистаминных и противоаллергических средств [4]. Бытует мнение, что цетиризин -один из наиболее эффективных антигистаминных Н1-препаратов, он чаще использовался в клинических исследованиях, препарат предпочтителен для пациентов, плохо отвечающих на терапию другими антигистаминными средствами [4].
Высокая противогистаминная активность цетиризина обусловлена степенью его сродства к Н1-рецепторам, которое выше, чем у лоратадина [10]. Следует также отметить значимую специфичность препарата, поскольку даже в высоких концентрациях он не оказывает блокирующего воздействия на серотониновые (5-НТ2), допаминовые (D2), М-холинорецепторы и альфа-1-адренорецепторы [4].
Цетиризин отвечает всем требованиям, предъявляемым к современным АГП второго поколения, и обладает рядом особенностей. Среди всех известных АГП активный метаболит цетиризин имеет наименьший объем распределения (0,56 л/кг) и обеспечивает полную занятость Н1-рецепторов и наивысшее противогистаминное действие [4, 13]. Препарат характеризуется высокой способностью проникновения в кожу. Через 24 часа после приема однократной дозы концентрация цетиризина в коже равна или превышает концентрацию его содержания в крови. При этом после курсового лечения терапевтический эффект сохраняется до 3 суток [11]. Выраженная противогистаминная активность цетиризина выгодно выделяет его в ряду современных антигистаминных средств (рис. 3).
Рис. 3. Эффективность одной дозы Н1-АГП второго поколения в подавлении вызванной введением гистамина волдырной реакции на протяжении 24 часов у здоровых мужчин [11]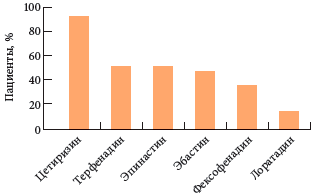
Миф о высокой стоимости всех современных АГП
Любое хроническое заболевание не сразу поддается даже адекватной терапии. Как известно, недостаточный контроль над симптомами любого хронического воспаления приводит не только к ухудшению самочувствия пациента, но и к повышению общих затрат на лечение, обусловленных увеличением потребности в медикаментозной терапии. Выбранный препарат должен оказывать наиболее эффективное терапевтическое воздействие и быть приемлемым по цене. Врачи, сохраняющие приверженность назначению Н1-АГП первого поколения, объясняют свой выбор, ссылаясь на очередной миф о том, что все АГП второго поколения значительно дороже препаратов первого поколения. Однако помимо оригинальных препаратов на фармацевтическом рынке имеются дженерики, стоимость которых ниже. Например, в настоящее время из препаратов цетиризина помимо оригинального (Зиртек) зарегистрировано 13 дженериков [14]. Результаты фармакоэкономического анализа, представленные в табл. 2, свидетельствуют об экономической целесообразности применения Цетрина - современного АГП второго поколения.
Таблица 2.
Результаты сравнительной фармакоэкономической характеристики Н1-АГП первого и второго поколений
| Препарат | Супрастин 25 мг № 20 | Диазолин 100 мг №10 | Тавегил 1 мг № 20 | Зиртек 10 мг № 7 | Цетрин 10 мг № 20 |
| Средняя рыночная стоимость 1 упаковки | 120 руб. | 50 руб. | 180 руб. | 225 руб. | 160 руб. |
| Кратность приема | 3 р/сут | 2 р/сут | 2 р/сут | 1 р/сут | 1 р/сут |
| Стоимость 1 дня терапии | 18 руб. | 10 руб. | 18 руб. | 32 руб. | 8 руб. |
| Стоимость 10 дней терапии | 180 руб. | 100 руб. | 180 руб. | 320 руб. | 80 руб. |
Миф об одинаковой эффективности всех дженериков
Вопрос о взаимозаменяемости дженериков актуален при выборе оптимального современного противогистаминного ЛС. Из-за разнообразия дженериков, представленных на рынке фармакологических средств, возник миф о том, что все дженерики действуют примерно одинаково, поэтому можно выбирать любой, ориентируясь прежде всего на цену.
Между тем дженерики отличаются друг от друга, причем не только фармакоэкономическими характеристиками. Стабильность лечебного эффекта и терапевтическая активность воспроизведенного препарата определяются особенностями технологии, упаковки, качеством активных субстанций и вспомогательных веществ. Качество активных субстанций препаратов разных производителей может существенно отличаться. Любое изменение в составе вспомогательных веществ может способствовать снижению биодоступности и возникновению побочных эффектов, в том числе гиперергических реакций различной природы (токсическая и др.) [6, 15]. Дженерик должен быть безопасным в применении и эквивалентным оригинальному препарату. Два лекарственных препарата считают биоэквивалентными, если они фармацевтически эквивалентны, имеют одинаковую биодоступность и после назначения в одинаковой дозе являются сходными, обеспечивая должную эффективность и безопасность [15]. Согласно рекомендациям Всемирной организации здравоохранения, биоэквивалентность дженерика следует определять по отношению к официально зарегистрированному оригинальному лекарственному препарату [15]. Изучение биоэквивалентности - один из этапов исследования терапевтической эквивалентности. FDA (Food and Drug Administration - Управление по контролю качества пищевых продуктов и лекарственных препаратов (США)) ежегодно издает и публикует «Оранжевую книгу» с перечнем препаратов, которые считаются терапевтически эквивалентными оригинальным. Таким образом, любой врач может сделать оптимальный выбор безопасного антигистаминного препарата с учетом всех возможных характеристик данных ЛС.
Одним из высокоэффективных дженериков цетиризина является Цетрин. Препарат действует быстро, продолжительно, обладает хорошим профилем безопасности. Цетрин практически не метаболизируется в организме, максимальная концентрация в сыворотке достигается через час после приема, при продолжительном применении не накапливается в организме. Цетрин выпускается в таблетках по 10 мг, показан для взрослых и детей с 6 лет [13, 16]. Цетрин полностью биоэквивалентен оригинальному препарату (рис. 4) [12].
Рис. 4. Усредненная динамика концентрации цетиризина после приема сравниваемых препаратов [12]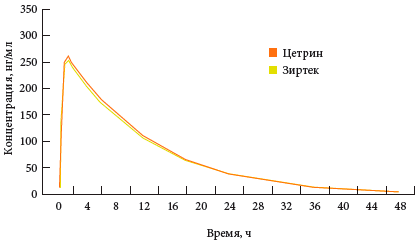
Цетрин успешно применяется в составе базисной терапии пациентов с аллергическим ринитом, имеющих сенсибилизацию к пыльцевым и бытовым аллергенам [7], аллергическим ринитом, ассоциированным с атопической бронхиальной астмой [16], аллергическим конъюнктивитом, крапивницей, в том числе хронической идиопатической [6, 9, 15], зудящими аллергодерматозами [17], ангионевротическим отеком, а также в качестве симптоматической терапии при острых вирусных инфекциях у пациентов с атопией [13]. При сравнении показателей эффективности дженериков цетиризина у больных хронической крапивницей при применении Цетрина отмечены наилучшие результаты (рис. 5) [15].
Рис. 5. Сравнительная оценка клинической эффективности препаратов цетиризина у пациентов с хронической крапивницей [15]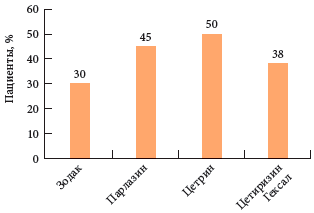
Отечественный и зарубежный опыт использования Цетрина свидетельствует о его высокой терапевтической эффективности в клинических ситуациях, когда показано применение Н1-антигистаминных препаратов второго поколения.
Таким образом, при выборе оптимального Н1-антигистаминного препарата из всех ЛС, представленных на фармацевтическом рынке, следует основываться не на мифах, а на критериях выбора, включающих соблюдение разумного баланса между эффективностью, безопасностью и доступностью, наличие убедительной доказательной базы, высокого качества производства.
СПИСОК ЛИТЕРАТУРЫ:
1. Лусс Л.В. Выбор антигистаминных препаратов в лечении аллергических и псевдоаллергических реакций // Российский аллергологический журнал. 2009. № 1. С. 78-84.
2. Гущин И.С. Потенциал противоаллергической активности и клиническая эффективность Н1-антагонистов // Аллергология. 2003. № 1. C. 78-84.
3. Takeshita K., Sakai K., Bacon K.B., Gantner F. Critical role of histamine H4 receptor in leukotriene B4 production and mast cell-dependent neutrophil recruitment induced by zymosan in vivo // J. Pharmacol. Exp. Ther. 2003. Vol. 307. № 3. P. 1072-1078.
4. Гущин И.С. Разнообразие противоаллергического действия цетиризина // Российский аллергологический журнал. 2006. № 4. С. 33.
5. Емельянов А.В., Кочергин Н.Г., Горячкина Л.А. К 100-летию открытия гистамина. История и современные подходы к клиническому применению антигистаминных препаратов // Клиническая дерматология и венерология. 2010. № 4. С. 62-70.
6. Татаурщикова Н.С. Современные аспекты применения антигистаминных препаратов в практике врача-терапевта // Фарматека. 2011. № 11. С. 46-50.
7. Федоскова Т.Г. Применение цетиризина (Цетрин) в лечении больных круглогодичным аллергическим ринитом // Российский аллергологический журнал. 2006. № 5. C. 37-41.
8. Holgate S. T., Canonica G. W., Simons F.E. et al. Consensus Group on New-Generation Antihistamines (CONGA): present status and recommendations // Clin. Exp. Allergy. 2003. Vol. 33. № 9. P. 1305-1324.
9. Grundmann S.A., Stander S., Luger T.A., Beissert S. Antihistamine combination treatment for solar urticaria // Br. J. Dermatol. 2008. Vol. 158. № 6. P. 1384-1386.
10. Brik A., Tashkin D.P., Gong H. Jr. et al. Effect of cetirizine, a new histamine H1 antagonist, on airway dynamics and responsiveness to inhaled histamine in mild asthma // J. Allergy. Clin. Immunol. 1987. Vol. 80. № 1. P. 51-56.
11. Van De Venne H., Hulhoven R., Arendt C. Cetirizine in perennial atopic asthma // Eur. Resp. J. 1991. Suppl. 14. P. 525.
12. Открытое рандомизированное перекрестное исследование сравнительной фармакокинетики и биоэквивалентности препаратов Цетрин, таблетки 0,01 («Д-р Редди'с Лабораторис ЛТД», Индия) и Зиртек таблетки 0,01 (UCB Pharmaceutical Sector, Германия). СПб., 2008.
13. Федоскова Т.Г. Особенности лечения ОРВИ у больных круглогодичным аллергическим ринитом // Российский аллергологический журнал. 2010. № 5. С. 100-105.
14. Лекарственные препараты в России, Справочник Видаль. М.: АстраФармСервис, 2006.
15. Некрасова Е.Е., Пономарева А.В., Федоскова Т.Г. Рациональная фармакотерапии хронической крапивницы // Российский аллергологический журнал. 2013. № 6. С. 69-74.
16. Федоскова Т.Г. Применение цетиризина в лечении больных круглогодичным аллергическим ринитом, ассоциированного с атопической бронхиальной астмой // Российский аллергологический журнал. 2007. № 6. C. 32-35.
17. Елисютина О.Г., Феденко Е.С. Опыт использования цетиризина при атопическом дерматите // Российский аллергологический журнал. 2007. № 5. С. 59-63.
