Гетерогенность мигрени: роль нестероидной противовоспалительной терапии
Статьи Табеева Г.Р.Мигрень является хроническим заболеванием, которое характеризуется повторяющимися приступами односторонней пульсирующей головной боли, сопровождающимися вегетативными и эмоциональными нарушениями. Несмотря на пароксизмальное течение заболевания и относительно благоприятный прогноз, мигрень существенно нарушает качество жизни пациентов. Причинами значительной дезадаптации пациентов, страдающих мигренью является высокая интенсивность боли и сопровождающих ее симптомов, высокая частота и длительность мигренозных атак, симптомы предшествующие мигрени (продромальный период) и резкое снижение работоспособности в последующие несколько дней.
Мигрень - заболевание, которое сопровождает человека большую часть жизни, причем пик заболеваемости приходится на наиболее трудоспособный возраст. Согласно данным широкомасштабного исследования American Migraine Study II (9) около 53% пациентов тяжело переносят приступы мигрени, когда полностью утрачивается трудоспособность. В среднем на каждого пациента мигренью приходится потеря 3.2 рабочих дней в год (13). Часть пациентов, которые вынуждены продолжать трудовую деятельность в момент приступа ГБ характеризуются снижением трудовой активности более чем на 46%.
Несмотря на то, что мигрень является распространенным и хорошо изученным заболеванием, его диагностика является крайне низкой. В большом эпидемиологическом популяционном исследовании, проведенном во Франции FRAMIG-3 (11) проводилось интервью 10.352 человек с целью диагностики мигрени в соответствии с критериями МКГБ-2 (85). У 1.179 (21.3%) была диагностирована мигрень. Из них 60% впервые узнали о своем диагнозе. В этом исследовании также отмечается крайне низкий процент больных, которые находятся под наблюдением специалистов - только 20% больных мигренью наблюдаются врачами. Подавляющее большинство больных мигренью находятся вне поля зрения специалистов и предпочитают самостоятельное лечение головных болей, используя доступные безрецептурные лекарственные средства (9).
Гетерогенность ведущих проявлений мигрени
Спектр клинических проявлений мигрени чрезвычайно широк. Это касается многих ее проявлений, как количественных, так и качественных: частоты приступов и их длительности, тяжести основных симптомов приступа, прежде всего, боли, но и многих сопровождающих симптомов. Но это в одинаковой мере относится и проявлениям межприступного периода. Наряду с тем, что существуют две клинически разные формы - мигрень с аурой и без, существует крайняя вариабельность представленности симптомов продромального и постдромального периода (1). У некоторых пациентов отмечается очевидная связь с провоцирующими факторами, включающими пищевые и алкогольные триггеры, связь с менструальным циклом или наличие исключительно ассоциированных с менструацией приступов (катамениальная мигрень). У значительного числа пациентов развиваются клинические симптомы кожной аллодинии, которая проявляется болевыми ощущениями при причесывании, ношении головного убора. Развитие феномена аллодинии (болевое ощущении в ответ на неболевой раздражитель) считают ответственным за развитие резистентности к специфической антимигренозной терапии. У некоторых пациентов уже при первых признаках боли в приступе мигрени возникает нарастающая тошнота и симптомы гастростаза, что крайне затрудняет прием пероральных средств купирования боли. Эти и многие другие свойства гетерогенности мигрени обусловливают и различия терапевтических ответов. Примечательно, что даже в случае успешного купирования мигренозной боли выбранное средство может оказаться эффективном не в каждом приступе у одного и того же пациента.
Крайней вариабельностью отличается мигрень в отношении степени дезадаптации вследствие повторяющихся приступов мигрени. Вариабельность наблюдается как в отношении различий между пациентами (межиндивидуальные), так и внутрииндивидуальные, т.е. у одного пациенты могут наблюдаться приступы мигрени с аурой и без нее. При этом приступы могут быть как длительные, так и короткие, как тяжелые, так и легкие.
Гетерогенность мигрени хорошо известна практическим врачам и активно изучается специалистами. Так, в исследовании Stewart с соавт. (14) показана чрезвычайная вариабельность основных параметров приступов мигрени: у 17% больных наблюдаются редкие приступы (менее 1 раза в месяц); у 32% - 1 раз в месяц; в 40% случаев атаки возникают с частотой 2-4 раза в месяц; у 10% пациентов наблюдаются крайне частая мигрень - чаще 1 раза в неделю. Согласно критериям Международной классификации головной боли (7) установлены жесткие временные рамки длительности приступа от 4 до 72 часов. Но на практике хорошо известно, что наряду с тем, что большинство атак мигрени продолжаются около 24 часов, на самом деле атаки по длительности могут варьировать от 2 часов до 3 дней.
Фазовые характеристики мигрени также широко варьирует. Продромальный период и аура далеко не всегда предшествуют собственно приступу мигрени. А у некоторых пациентов постдромальный период бывает наиболее дезадаптирующей фазой приступа. Аура, которая в целом наблюдается у менее, чем трети пациентов мигренью, возникает далеко не во всех приступах и может протекать самостоятельно в отсутствии собственно болевого приступа. Частота приступов также отличается чрезвычайной вариабельностью. Около 49 % пациентов переносят редкие приступы с частотой менее 1 раза в месяц, 40% пациентов - 2-4 раза в месяц и около 10% больных испытывают частые приступы мигрени более 1 раза в неделю (14).
Важнейшей характеристикой мигрени является тяжесть собственно приступа. Понятие тяжести приступа обусловлено не столько интенсивностью боли, сколько степенью влияния болевых и неболевых проявлений мигрени на степень дезадаптации и уровень повседневного функционирования пациента. Последние могут быть связаны как с интенсивной, так и с умеренной болью, как короткими, так и с длительными приступами. Являясь, таким образом, интегративным понятием тяжесть приступа как наиболее вариабельный параметр мигрени имеет важное значение не только с позиций дезадаптации пациента, но и с точки зрения выбора оптимального способа ее купирования. С целью стратификации и для количественной оценки тяжести приступов мигрени принято использование специальной шкалы MIDAS (Migraine Disability Assessment Questionnaire), которая позволяет количественно оценить степень дезадаптации вследствие приступов мигрени(15).
ОПРОСНИК MIDAS
За последние 3 месяца:
- Сколько рабочих дней Вы пропустили из-за головной боли?____дней
- Сколько дней Ваша работоспособность была снижена наполовину и более из-за головной боли?____дней
- В течение скольких дней Вы не занимались домашними делами из-за головной боли?____дней
- Сколько дней продуктивность Вашей домашней работы была снижена наполовину и более из-за головной боли? ____дней
- В течение скольких дней Вы не участвовали в семейных и общественных мероприятиях, активном проведении досуга из-за головной боли? ____дней
| Сумма баллов | Степень тяжести |
| 0-5 | I |
| 6-10 | II |
| 11-20 | III |
| 21 и более | IV |
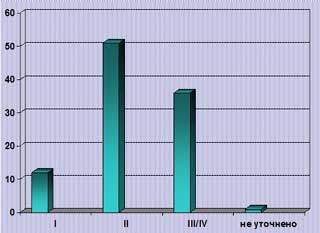
Изучение гетерогенности мигрени в терминах "тяжесть приступов и степень ограничения повседневной активности" (14) выявило, что около 36% пациентов характеризуются тяжелыми приступами мигрени, 51% переносят умеренной тяжести приступы и примерно у 12% больных приступы протекают достаточно легко, без значительного влияния на повседневную активность (рис. 1).
Рис. 1. Гетерогенность уровня дезадаптации вследствие мигрени (% пациентов).
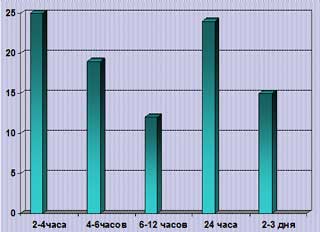
Еще одним важным показателем, характеризующим степень дезадаптации пациентов, является длительность атак мигрени. Показатель длительности приступа варьирует в широких пределах у различных пациентов и может существенно различаться у одного и того же больного. Однако в целом при анализе средней длительности приступов мигрени выявлено (14), что у 25% пациентов приступы чрезвычайно короткие (2-4-часа), в 19% случаев они длятся 4-6 часов, в 12% случаев - 6-12 часов, 24% пациентов отмечают приступы длительностью около 24 часов и лишь 15% больных переносят длительные приступы (2-3 дня) (рис. 2).
Рис. 2. Гетерогенность продолжительности приступов мигрени (% пациентов).
Гетерогенность терапевтических стратегий мигрени
Лечение мигренозного приступа представляет крайне сложную задачу, что связано, прежде всего, с чрезвычайной вариабельностью основных ее проявлений, но и с различием терапевтических ответов. Среди средств, традиционно используемых для купирования мигрени, выделяют фармакологические средства нескольких групп: 1. Простые и комбинированные аналгетики (ацетаминофен, кафергот и др.); 2. Нестероидные противовоспалительные средства (ибупрофен, напроксен, кетопрофен, индометацин и др.); 3. Неселективные агонисты 5-НТ1 рецепторов (эрготамин, дигидроэрготамин); 4. Селективные агонисты 5-НТ ?B\1D рецепторов (суматриптан, золмитриптан, элетриптан и др.); 5. Вспомогательные средства (метоклопрамид, домперидон).
В выборе оптимального способа купирования мигрени учитывается совокупность множества факторов, среди которых наряду с частотой приступов и их длительностью важнейшим и определяющим являются тяжесть и степень дезадаптации, влияние на повседневную активность пациентов, а также учет предшествующего опыта успешного купирования приступов. Выбор между неспецифическими и специфическими антимигренозными средствами зависит от характеристик мигренозных атак; не все атаки даже у одного и того же пациента могут успешно купироваться одними и теми средствами. Так, легкие и умеренные по тяжести приступы могут эффективно купироваться аналгетикми и НПВП, возможно в комбинации со средствами, которые улучшают их абсорбцию (метоклопрамид). Исходя из тяжести основных проявлений мигрени используют два методических подхода: ступенчатый и стратифицированный. В соответствии со ступенчатым подходом (рис. 3) предполагается начало терапии с применения простых аналгетиков или НПВП, а при их низкой эффективности возможно использование комбинированный препаратов, агонистов 5-НТ рецепторов.
Рис.3. Ступенчатый подход к лечению приступов мигрени (10).
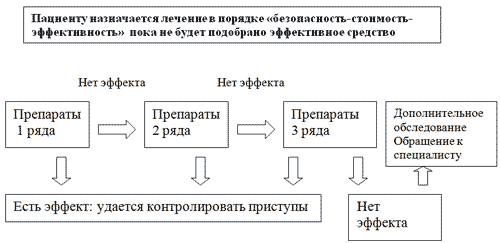
В соответствии со ступенчатым подходом, пациенту первоначально назначается простой аналгетик, а в случае его неэффективности следует использовать возможности более высокого уровня. Ступенчатый подход может быть применим и к купированию мигренозной боли в течение одного приступа, т.е. при отсутствии эффекта простого аналгетика или при низкой его эффективности пациент может перейти к приему НПВП в течение данного приступа мигрени.
Ступенчатый подход является оптимальным для лечения больных с вариабельностью различных приступов: наличием, прежде всего легких и умеренных по тяжести атак. Однако для больных, страдающих преимущественно тяжелыми приступами с высокой интенсивностью боли и выраженной дезадаптацией более адекватным является применение стратифицированного подхода (рис. 4). Понятие стратификации тяжести мигрени подразумевает количественную оценку степени ее влияния на повседневную активность пациента, в соответствии с которой применяется дифференцированный подход в выборе фармакологического средства.
Рис. 4. Стратифицированный подход к лечению приступов мигрени (10).
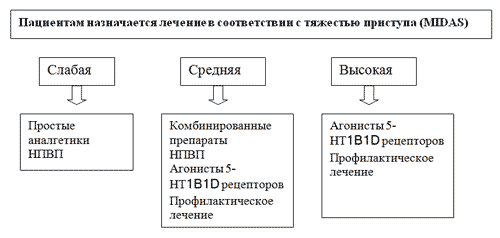
Для эффективного лечения приступов мигрени важно соблюдение некоторых общих принципов практического использования вышеупомянутых фармакологических средств. Среди них важнейшим с практической точки зрения является наиболее раннее применение выбранного препарата при первых признаках мигренозной боли, поскольку более позднее использование любого класса купирующих средств связано с меньшей его эффективностью.
ПРИНЦИПЫ КУПИРОВАНИЯ ПРИСТУПОВ МИГРЕНИ
- Использование общепринятых эффективных доз
- Раннее применение купирующих средств при умеренной головной боли
- Исключение средств, потенциально способных вызывать злоупотребление ими: кофеина, комбинаций ацетаминофен\аспирин, буталбитал\кофеин\ацетаминофен\аспирин с или без кофеина
- Использование стратифицированного подхода в выборе купирующего средства
- Купирование ассоциированных симптомов (тошноты, головокружения)
- Учет предшествующего опыта эффективного купирования приступов
- Использование оптимального способа применения препарата
- Учет противопоказаний
- Применение комбинаций триптан\НПВП и НПВП\метоклопрамид (при необходимости)
Нестероидные противовоспалительные средства в купировании мигренозных атак
НПВП являются наиболее широко распространенным классом фармакологических препаратов, которые используются пациентами для облегчения мигренозной боли (2). Это связано не только с простотой применения и дозировки большинства безрецептурных препаратов, но и с относительно высокой их эффективностью, что показывает многолетний опыт их применения. Антимигренозная активность НПВП обусловлена несколькими механизмами. Прежде всего, они связаны с блокированием синтеза простагландинов из арахидоновой кислоты, которая наряду с другими провоспалительными агентами участвует в инициации механизмов вазодилатации и стерильного нейрогенного воспаления в мигренозном приступе. Эти два фактора, как известно, играют ключевую роль в сенситизации болевых рецепторов к нормальным механическим и химическим стимулам и в снижении порогов восприятия боли. Наряду с периферическими, НПВП имеют и центральные механизмы действия при мигрени (3,4), которые предположительно связаны не только с ингибированием синтеза простагландина в центральной нервной системе, но и с усилением высвобождения норадреналина, активацией нисходящей серотонинергической системы. А основной механизм НПВП в ингибировании тромбоцитарной циклооксигеназы с последующим подавлением образования тромбоксана А2, потенциального агента агрегации, может иметь значение и для профилактической терапии мигрени.
Терапевтические эффекты НПВП при мигрени хорошо изучены в 38 рандомизированных двойных слепых исследованиях. Так, ибупрофен в дозах 800-1200 мг\сут показал эффективность, превышающую плацебо в трех исследованиях (6,8,12) по показателю уровня обезболивающего действия. Более низкие дозы (400 мг) также превышают эффективность плацебо, однако существенно отличаются от низкой дозы (200 мг). Схожая эффективность антимигренозного действия ибупрофена продемонстрирована у детей в купировании приступов мигрени (5).
Нурофен, оригинальный ибупрофен, обладает способностью блокировать рецепторы ЦОГ-1 и ЦОГ-2, снижая синтез простагландинов, при этом до 80% активного вещества воздействует на ЦОГ-2 и лишь 20% на ЦОГ-1. Таким образом Нурофен имеет выраженный анальгетический и противовоспалительный эффект с одной стороны и относительную безопасность - с другой.
Нурофен Форте, новая форма препарата, содержит 400 мг ибупрофена, оптимальную дозировку для купирования головной боли при мигрени, что можно с успехом использовать в повседневной практике.
ЛИТЕРАТУРА
