Валсартан: центральное место в лечении кардиологического больного
СтатьиОпубликовано в журнале:
« АтмосферА. Новости кардиологии » 2, 2014г.
Ю.А. Карпов
профессор, первый заместитель генерального директора, заместитель генерального директора по науке ФГБУ "РКНПК" Министерства здравоохранения Российской Федерации, Москва.
Ключевые слова:антагонисты к рецепторам ангиотензина II, валсартан.
С точки зрения фармакологии препараты из группы АРАП можно классифицировать по механизму их связывания с рецепторами (конкурентные и неконкурентные антагонисты ангиотензина II) и степени сродства (аффинности) к АТ1-рецепторам. Обратимо связывающиеся с рецепторами лозартан и эпросартан являются конкурентными антагонистами, а валсартан, ирбесартан, кандесартан и телмисартан связываются с рецепторами необратимо и действуют как неконкурентные антагонисты. По возрастанию аффинности (селективности) к АТ1-рецепторам эти лекарства выстраиваются в такой ряд: лозартан, эпросартан, телмисартан, ирбесартан, кандесартан, олмесартан, валсартан. Таким образом, валсартан отличается самым оптимальным соотношением фармакологических характеристик. Он обладает самостоятельной фармакологической активностью, не имеет активных метаболитов. Эффект валсартана поддерживается в течение 24 ч после однократного приема (период полувыведения примерно 9 ч), что позволяет назначать его 1 раз в сутки [3]. Основной путь элиминации валсартана из организма - выведение с желчью (70-86%), в основном в неизмененном виде. Лишь 14-30% валсартана выводится с мочой, что делает безопасным его применение у больных с хронической почечной недостаточностью [4].Ренин-ангиотензиновая система (РАС) - одна из важнейших гуморальных систем, регулирующих гемодинамику, электролитный и водный обмен. Ее активация является универсальным компенсаторным механизмом, позволяющим пережить кратковременные гемодинамические нарушения. Однако хроническая гиперактивация РАС, наблюдаемая на всех этапах сердечно-сосудистого континуума, становится основным самостоятельным звеном патогенеза заболеваний сердечно-сосудистой системы и, следовательно, важнейшей мишенью фармакотерапии - от факторов риска через развитие функциональных нарушений (артериальной гипертонии (АГ), эндотелиальной дисфункции и нефропатии) к тяжелым поражениям органов-мишеней и смертельному исходу (развитию сердечной недостаточности). В настоящий момент в арсенале практического врача имеются три последовательно разработанных способа противостояния гиперактивации РАС: ингибирование ангио тензинпревращающего фермента, блокада рецепторов ангиотензина II и ингибирование ренина [1, 2]. Последний вариант пока не получил широкого распространения из-за относительно малой доказательной базы. Поэтому в практической деятельности выбор в основном стоит между использованием ингибиторов ангиотензинпревращающего фермента (ИАПФ) и антагонистов рецепторов ангиотензина II (АРАП). Многие годы лидирующие позиции занимали ИАПФ, однако в последнее время, с появлением доступных генерических препаратов из группы АРАП, всё больше врачей в мире отдают им предпочтение из-за более полного подавления негативных эффектов ангиотензина II, переносимости, сравнимой с таковой у плацебо, и, как результат, самой лучшей приверженности больных к лечению.
Доказательная база эффективности и безопасности валсартана огромна (более 150 клинических исследований, в том числе с жесткими конечными точками, приблизительно 100 тыс. пациентов) и касается практически всех звеньев сердечно-сосудистого континуума.
Большое количество исследований проведено в популяции больных АГ. В конце 1990-х годов было доказано сходное с таковым у эналаприла гипотензивное действие валсартана при значительно лучшей переносимости последнего [5, 6]. Десять лет назад были опубликованы результаты крупнейшего (15 245 пациентов из 31 страны) исследования сартанов при АГ - VALUE (Valsartan Antihypertensive Long-term Use Evaluation) [7]. Помимо двойного слепого сравнения гипотензивного действия валсартана и амлодипина в этом исследовании сопоставлялось их влияние на частоту развития сердечно-сосудистых осложнений и летальность. За 3,2 года наблюдения артериальное давление у пациентов обеих групп сопоставимо снизилось, таким образом, было отмечено сходное влияние препаратов на прогноз при лучшей переносимости валсартана.
Важным преимуществом валсартана, выявленным в этом исследовании, был несколько меньший риск прогрессирования сердечной недостаточности и достоверно меньшая (на 23%, p<0,001), чем в группе амлодипина, частота развития новых случаев сахарного диабета. В крупном метаанализе доказано, что блокаторы РАС в отличие от других антигипертензивных классов снижают риск развития сахарного диабета у больных АГ, причем сартаны превосходят ИАПФ [8]. Кроме того, при анализе данных 14 588 больных было установлено, что валсартан предупреждает развитие новых случаев сахарного диабета эффективнее лозартана [9]. Помимо этого была продемонстрирована возможность снижения инсулинорезистентности при применении валсартана у пациентов с АГ и обнаружены возможные механизмы этого воздействия [10, 11].
Возвращаясь к теме АГ, нельзя не отметить результаты исследования Val-Syst. В нем также была выявлена одинаковая гипотензивная эффективность валсартана и амлодипина (при лучшей переносимости валсартана), но у более сложного контингента пациентов - у пожилых с изолированной систолической АГ [12]. Согласно российским рекомендациям по диагностике и лечению АГ, валсартан как сартан наряду с тиазидными диуретиками и антагонистами кальция является препаратом первого выбора у пожилых больных АГ [13].
Надо отметить, что протоколы исследований VALUE и Val-Syst предусматривали титрование дозы изучаемого препарата и в случае необходимости добавление второй группы гипотензивных лекарств - тиазидных диуретиков. В исследовании Val-MARC (Valsartan-Managing Blood Pressure Aggressively and Evaluating Reductions in hs-CRP) было продемонстрировано более выраженное снижение как систолического, так и диастолического артериального давления при использовании именно такой комбинации в сравнении с монотерапией валсартаном [14]. При этом комбинированная терапия валсартаном в сочетании с низкими дозами гидрохлоротиазида (до 25 мг) не влияет на показатели углеводного и липидного обмена, что подтверждает ее безопасность [15].
Важно, что валсартан может тормозить поражение всех органов-мишеней АГ, так, например, доказана его способность уменьшать выраженность гипертрофии левого желудочка (ЛЖ) [16, 17]. При этом регресс гипертрофии ЛЖ на фоне приема валсартана обусловлен не просто снижением периферического сопротивления и постнагрузки, описан механизм прямого кардиопротективного действия, реализуемого через влияние на клеточные структуры кардиомиоцитов [18]. Всё изложенное объясняет важное место, занимаемое валсартаном в последних рекомендациях европейских экспертов по ведению пациентов с АГ [19].
Во многих исследованиях отмечено заметное снижение выраженности альбуминурии на фоне применения валсартана, что подтверждает его нефропротективный эффект [20]. Считается, что нефропротективное действие АРА11 связано преимущественно с их способностью снижать артериальное давление, однако есть предположения о прямом воздействии некоторых препаратов этой группы на нефрон [21]. Так, в исследовании SMART (Shiga Microalbuminuria Reduction Trial) более выраженное снижение отношения альбумин/креатинин наблюдалось в группе валсартана, а не амлодипина, несмотря на то что контроль над АГ был лучше во второй группе [22].
Валсартан уже около 10 лет применяется для лечения ишемической болезни сердца (ИБС). Первые доказательные данные в этом отношении были получены в исследовании VALIANT (VALsartan In Acute myocardial iNfarcTion), в котором сравнивали эффективность валсартана, каптоприла и их комбинации у больных с острым и перенесенным инфарктом миокарда, сердечной недостаточностью и/или систолической дисфункцией ЛЖ [23]. За 2 года наблюдения (14 703 пациента) была продемонстрирована равная эффективность этих стратегий в отношении прогноза. При этом переносимость валсартана была достоверно лучше, чем переносимость ИАПФ. На основании этих данных валсартан - единственный сартан, который внесен в российские и международные рекомендации по диагностике и лечению больных с острым и перенесенным инфарктом миокарда с подъемом сегмента ST на ЭКГ как один из важных компонентов лечения таких пациентов [24-26].
В плацебоконтролируемом исследовании ValPREST (Valsartan for Prevention of Restenosis after Stenting of Type B2/C lesions) применение валсартана у больных, перенесших стентирование по поводу острого коронарного синдрома, приводило к достоверному снижению частоты рестенозов и повторного стентирования [27]. При дальнейшем изучении этого вопроса в исследовании VALVACE (VALsartan Versus ACE inhibition after bare metal stent implantation) была продемонстрирована большая эффективность полугодового приема валсартана, чем ИАПФ, в предотвращении рестеноза стента, что подтверждает более выраженное анти-пролиферативное действие валсартана [28].
Применение валсартана при хронической сердечной недостаточности (ХСН) также имеет твердую доказательную базу. В многоцентровом двойном слепом плацебоконтролируемом исследовании Val-HeFT (Valsartan Heart Failure Trial) у пациентов с ХСН II-IV функционального класса и фракцией выброса менее 40% валсартан достоверно снижал частоту событий комбинированной первичной конечной точки (рисунок) [29, 30]. Не менее важен тот факт, что даже при добавлении валсартана к ИАПФ снижалась частота госпитализаций, а у пациентов, не получавших ИАПФ ранее, препарат достоверно улучшал выживаемость. Валсартан наряду с кандесартаном и лозартаном рассматривается в рекомендациях отечественных экспертов по диагностике и лечению ХСН как одна из основных альтернатив ИАПФ. У этой категории пациентов крайне важное значение имеет правильное титрование дозы лекарства - стартовая доза валсартана составляет 40 мг 2 раза в сутки, терапевтическая - 80 мг 2 раза в сутки, максимальная - 160 мг 2 раза в сутки [31].
Мощное терапевтическое действие валсартана при ХСН обусловило создание нового комбинированного препарата на его основе - валсартан + сакубитрил (ингибитор неприлизина). В недавно завершившемся исследовании PARADIGM-HF (Prospective comparison of ARNI with ACEI to Determine Impact on Global Mortality and morbidity in Heart Failure) было выявлено достоверное снижение риска смерти и госпитализации по поводу сердечной недостаточности при использовании этой комбинации в сравнении с показателями пациентов, принимавших эналаприл.
Результаты недавних исследований свидетельствуют о наличии у валсартана чрезвычайно важных для кардиологических пациентов свойств - положительного влияния на свертывающую систему. Так, в работе E. Gavriilaki et al. 3-месячное лечение валсартаном у пациентов с АГ привело к нормализации показателей коагуляции и фибринолиза (комплекса тромбин-антитромбин и ингибитора-1 активатора человеческого плазминогена), измеренных после высокоинтенсивной физической нагрузки [32].
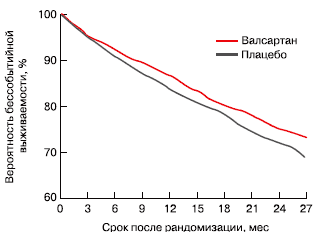
Вероятность выживания без развития событий комбинированной конечной точки
(смерть по любой причине, остановка сердца или успешная реанимация,
госпитализация из-за декомпенсации ХСН или внутривенное введение инотропных
препаратов или вазодилататоров) - кривые Каплана-Мейера (p=0,009) [30].
В экспериментальной работе продемонстрировано положительное влияние валсартана при сахарном диабете на регуляцию аденозинмонофосфат-активируемой киназы и фактора транскрипции Egr1 (центрального медиатора в патофизиологии сосудов), что приводит к снижению уровня тканевого фактора и Toll-подобных рецепторов 2 и 4. Эти эффекты валсартана не зависели от его влияния на АТ1-рецепторы и, как считается, объясняют снижение вероятности атеротромботических событий при его применении [33].
Огромное значение придается воздействию АРАП, и особенно валсартана, на функцию эндотелия, играющую центральную роль в развитии сердечно-сосудистых заболеваний. Даже на небольших группах больных удается продемонстрировать положительное влияние 12-месячного использования этого препарата после стентирования каротидных артерий на толщину комплекса интима-медиа, оцениваемую с помощью ультразвукового дуплексного сканирования, и на уровень маркеров оксидативного стресса, воспаления и эндотелиальной дисфункции (С-реактивный белок, фактор Виллебранда) [34].
Таким образом, валсартан можно назвать универсальным кардиологическим инструментом, обладающим мощным и длительным антигипертензивным эффектом, имеющим доказанные органопротективные свойства, доказавшим свою эффективность на всем протяжении сердечно-сосудистого континуума и при этом отличающимся благоприятным метаболическим профилем. Особенно важно его доказанное положительное влияние на прогноз и продолжительность жизни пациентов с сердечно-сосудистыми заболеваниями.
На протяжении нескольких лет эти данные делают валсартан одним из наиболее популярных у врачей и пациентов гипотензивных лекарств в мире. По данным, опубликованным на сайте medscape.com в августе 2014, наиболее часто выписываемым и наиболее продаваемым в США препаратом для лечения сердечно-сосудистых заболеваний стал валсартан [35].
Далеко не всегда в реальной клинической практике доступны оригинальные лекарственные средства. Во всем мире приемлемой практикой становится широкое использование качественных генерических препаратов. В случае с валсартаном качественным генериком можно назвать препарат Валз (компания "Актавис") с доказанной биоэквивалентностью и терапевтической эквивалентностью, что позволяет ему занять достойное место в повседневной практике российских кардиологов и терапевтов [4, 36, 37].
Литература
- Осадчий К.К., Подзолков В.И. Сердечно-сосудистый континуум: могут ли ингибиторы АПФ разорвать "порочный круг"? // Рус. мед. журн. 2008. Т. 16. № 17. С. 1102-1109.
- Шилов А.М. Сартаны в практике врача первичного звена при лечении артериальной гипертонии // Фарматека. 2014. № 9. С.39-44.
- Шилов А.М., Еремина И.В. Селективные ингибиторы рецепторов ангиотензина II (Валсартан) в практике лечения ССЗ // Трудный пациент. 2011. Т. 9. № 7. С. 26-32.
- Барышникова А.Г. Роль блокаторов рецепторов ангиотензина. Фокус на валсартан. М.: Медиком, 2012.
- Holwerda N.J., Fogari R., Angeli P. et al. Valsartan, a new angiotensin II antagonist for the treatment of essential hypertension: efficacy and safety compared with placebo and enalapril // J. Hypertens. 1996. V. 14. № 9. P. 1147-1151.
- Mallion J.M., Boutelant S., Chabaux P. et al. Valsartan, a new angiotensin II antagonist; blood pressure reduction in essential hypertension compared with an angiotensin converting enzyme inhibitor, enalapril // Blood Press. Monit. 1997. V. 2. № 4. P. 179-184.
- Julius S., Kjeldsen S.E., Weber M. et al.; VALUE trial group. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial // Lancet. 2004. V. 363. № 9426. P. 2022-2031.
- Elliott W.J., Meyer P.M. Incident diabetes in clinical trials of antihypertensive drugs: a network meta-analysis // Lancet. 2007. V. 369. № 9557. P. 201-207.
- Weycker D., Falvey H., Edelsberg J., Oster J. Risk of diabetes in hypertensive patients receiving valsartan versus losartan // J. Clin. Hypertens. 2007. V. 9. Suppl. A. P. 448.
- Hasan A.U., Ohmori K., Hashimoto T. et al. Valsartan ameliorates the constitutive adipokine expression pattern in mature adipocytes: a role for inverse agonism of the angiotensin II type 1 receptor in obesity // Hypertens. Res. 2014. V. 37. № 7. P. 621-628.
- Satirapoj B., Leelasiri K., Supasyndh O., Choovichian P. Short-term administration of an angiotensin II receptor blocker in patients with long-term hemodialysis patients improves insulin resistance // J. Med. Assoc. Thai. 2014. V. 97. № 6. P. 574-581.
- Palatini P., Mugellini A., Spagnuolo V. et al.; Investigators Group. Comparison of the effects on 24-h ambulatory blood pressure of valsartan and amlodipine, alone or in combination with a low-dose diuretic, in elderly patients with isolated systolic hypertension (Val-syst Study) // Blood Press. Monit. 2004. V. 9. № 2. P. 91-97.
- Диагностика и лечение артериальной гипертензии. Российские рекомендации (четвертый пересмотр) // Систем. гипертен. 2010. № 3. С. 5-26.
- Benz J., Black H., Graff A. et al. Valsartan and hydrochlorothiazide in patients with essential hypertension. A multiple dose, double-blind, placebo controlled trial comparing combination therapy with monotherapy // J. Hum. Hypertens. 1998. V. 12. № 12. P. 861-866.
- Zappe D.H., Sowers J.R., Hsueh W.A. et al. Metabolic and antihypertensive effects of combined angiotensin receptor blocker and diuretic therapy in prediabetic hypertensive patients with the cardiometabolic syndrome // J. Clin. Hypertens. (Greenwich). 2008. V. 10. № 12. P. 894-903.
- Kucukler N., Kurt I.H., Topaloglu C. et al. The effect of valsartan on left ventricular myocardial functions in hypertensive patients with left ventricular hypertrophy // J. Cardiovasc. Med. (Hagerstown). 2012. V. 13. № 3. P. 181-186.
- Suzuki K., Kato K., Soda S. et al. The effect of valsartan on regression of left ventricular hypertrophy in type 2 diabetic patients // Diabetes Obes. Metab. 2004. V. 6. № 3. P. 195-199.
- Zhang X., Li Z.L., Crane J.A. et al. Valsartan regulates myocardial autophagy and mitochondrial turnover in experimental hypertension // Hypertension. 2014. V. 64. № 1. P. 87-93.
- Mancia G., Fagard R., Narkiewicz K. et al.; Task Force Members. 2013 ESH/ESC Guidelines for the management of arterial hypertension: the Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) // J. Hypertens. 2013. V. 31. № 7. P. 1281-1357.
- Viberti G., Wheeldon N.M.; MicroAlbuminuria Reduction With VALsartan (MARVAL) Study Investigators. Microalbuminuria reduction with valsartan in patients with type 2 diabetes mellitus: a blood pressure-independent effect // Circulation. 2002. V. 106. № 6. P. 672-678.
- Casas J.P., Chua W., Loukogeorgakis S. et al. Effect of inhibitors of the renin-angiotensin system and other antihypertensive drugs on renal outcomes: systematic review and meta-analysis // Lancet. 2005. V. 366. № 9502. P. 2026-2033.
- Shiga Microalbuminuria Reduction Trial (SMART) Group; Uzu T., Sawaguchi M., Maegawa H., Kashiwagi A. Reduction of microalbuminuria in patients with type 2 diabetes: the Shiga Microalbuminuria Reduction Trial (SMART) // Diabetes Care. 2007. V. 30. № 6. P. 1581-1583.
- McMurray J., Solomon S., Pieper K. et al. The effect of valsartan, captopril, or both on atherosclerotic events after acute myocardial infarction: an analysis of the Valsartan in Acute Myocardial Infarction Trial (VALIANT) // J. Am. Coll. Cardiol. 2006. V. 47. № 4. P. 726-733.
- Диагностика и лечение больных острым инфарктом миокарда с подъемом сегмента ST ЭКГ. Рекомендации ВНОК // Кардиоваск. тер. и профилакт. 2007. Т. 6. № 8. Прилож. 1.
- Task Force on the management of ST-segment elevation acute myocardial infarction of the European Society of Cardiology (ESC); Steg P.G., James S.K., Atar D. et al. ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation // Eur. Heart J. 2012. V. 33. № 20. P. 2569-2619.
- American College of Emergency Physicians; Society for Cardiovascular Angiography and Interventions; O'Gara P.T., Kushner F.G., Ascheim D.D. et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines // J. Am. Coll. Cardiol. 2013. V. 61. № 4. P. е78-140.
- Peters S., Gotting B., Trummel M. et al. Valsartan for prevention of restenosis after stenting of type B2/C lesions: the VAL-PREST trial // J. Invasive Cardiol. 2001. V. 13. № 2. P. 93-97.
- Peters S., Trummel M., Meyners W. et al. Valsartan versus ACE inhibition after bare metal stent implantation - results of the VALVACE trial // Int. J. Cardiol. 2005. V. 98. № 2. P. 331-335.
- Maggioni A.P., Latini R., Carson P.E. et al.; Val-HeFT Investigators. Valsartan reduces the incidence of atrial fibrillation in patients with heart failure: results from the Valsartan Heart Failure Trial (Val-HeFT) // Am. Heart J. 2005. V. 149. № 3. P. 548-557.
- Cohn J.N., Tognoni G.; Valsartan Heart Failure Trial Investigators. A randomized trial of the angiotensin-receptor blocker valsartan in chronic heart failure // N. Engl. J. Med. 2001. V. 345. № 23. P. 1667-1675.
- Национальные рекомендации ОССН, РКО и РНМОТ по диагностике и лечению ХСН (четвертый пересмотр) // Сердечн. недостат. 2013. Т. 14. № 7(81).
- Gavriilaki E., Gkaliagkousi E., Nikolaidou B. et al. Increased thrombotic and impaired fibrinolytic response to acute exercise in patients with essential hypertension: the effect of treatment with an angiotensin II receptor blocker // J. Hum. Hypertens. 2014. V. 28. № 10. P. 606-609.
- Suzuki H., Sano T., Umeda Y. et al. Valsartan prevents neointimal hyperplasia after carotid artery stenting by suppressing endothelial cell injuries // Neurol. Res. 2014. Jun 18. 1743132814Y0000000408. [Epub ahead of print].
- Ha YM., Park E.J., Kang Y.J. et al. Valsartan independent of AT1 receptor inhibits tissue factor, TLR-2 and -4 expression by regulation of Egr-1 through activation of AMPK in diabetic conditions // J. Cell. Mol. Med. 2014. V. 18. № 10. P. 2031-2043.
- medscape.com/viewarticle/829246
- Маянская С.Д., Малышева Е.В. Суточный профиль артериального давления на фоне приема валсартана компании "Актавис" по сравнению с оригинальным валсартаном и монотерапией эналаприлом // Практ. мед. 2011. № 4(52). С. 201-202.
- Марцевич С.Ю., Лукина Ю.В., Дмитриева Н.А. и др. Сравнительное изучение эффективности и переносимости дженерического и оригинального препаратов валсартана в виде монотерапии или в комбинации с гидрохлоротиазидом и бисопрололом у больных артериальной гипертонией 1-2 степени и метаболическим синдромом // Рац. фармакотер. в кардиол. 2012. №8(1). С. 17-22.
