Противовоспалительная терапия хронической обструктивной болезни легких: настоящее и будущее
СтатьиС.Н. Авдеев, ФБГУ «НИИ пульмонологии» ФМБА России
Сегодня хроническая обструктивная болезнь легких представляет собой значительную экономическую и социальную проблему и является единственной болезнью, при которой смертность продолжает увеличиваться [4, 5]. По данным ряда недавно выполненных исследований, распространенность хронической обструктивной болезни легких в мире у людей старше 40 лет составляет 10,1% (11,8% у мужчин и 8,5% у женщин) [3].
Ключевые слова: хроническая обструктивная болезнь легких, Т-лимфоциты, мокрота, рофлумиласт
Значение воспаления в патогенезе хобл
Хроническая обструктивная болезнь легких (ХОБЛ) -заболевание, характеризующееся ограничением воздушного потока с развитием не полностью обратимой бронхиальной обструкции; ограничение воздушного потока прогрессирует и связано с усиленным патологическим воспалительным ответом дыхательных путей на повреждающие частицы или газы [1, 2]. Курение и другие ингаляционные ирританты инициируют развитие воспалительного ответа в дыхательных путях и легочной паренхиме. Воспаление у «здоровых» курильщиков по составу клеточных элементов, медиаторов и протеаз очень похоже на воспаление у пациентов с ХОБЛ, но менее выражено [6, 7]. Поэтому полагают, что воспаление в дыхательных путях и паренхиме при ХОБЛ представляет собой усиленный хронический воспалительный ответ на ирританты (такие как табачный дым) [8]. Механизм такого усиления или амплификации пока остается до конца не изученным, он может детерминироваться генетическими факторами [9], латентными вирусными инфекциями [10] и нарушением активности деацетилазы гистонов [11].
Основное место локализации характерной для ХОБЛ дыхательной обструкции - это малые дыхательные пути (ЦП) диаметром менее 2 мм [12]. Но картина воспалительного инфильтрата в крупных и малых дыхательных путях, а также в легочной паренхиме и стенке легочных сосудов в целом довольно сходная [8]. Данное воспаление может разрешаться или приводить к фиброзу, протеолизу и ремоделированию. Hogg и колл. показали, что по мере возрастания тяжести ХОБЛ происходит прогрессирующее утолщение стенки бронха, вызванное аккумуляцией клеток воспаления, а также накопление избытка слизи в просвете бронха [7]. Воспалительный инфильтрат состоит из нейтрофилов, макрофагов и Т-лимфоцитов (CD4+ и CD8+) и других клеток (рис. 1).
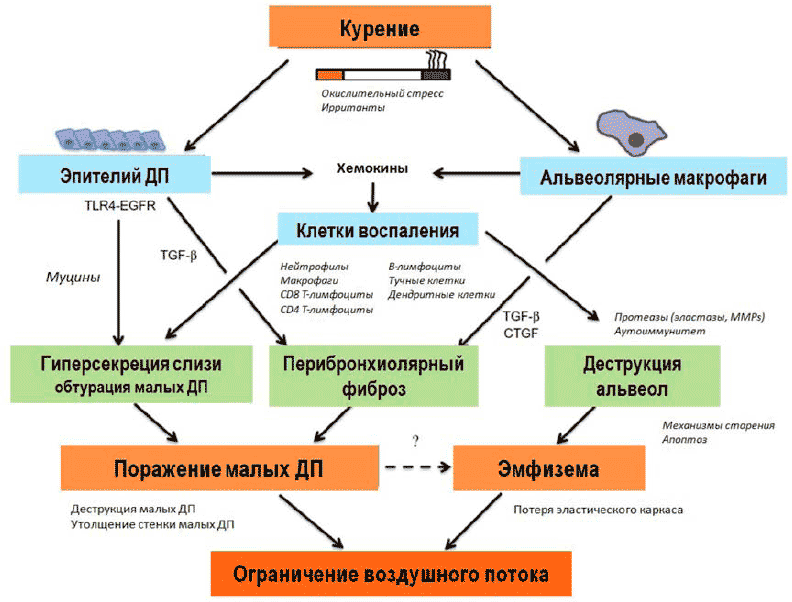
Рисунок 1. Патогенез ХОБЛ (Martin et al. Int J COPD 2013)
Одну из ведущих ролей в воспалении при ХОБЛ играют нейтрофилы. O'Donnell et al. показали, что число нейтрофилов в индуцированной мокроте хорошо коррелирует с тяжестью поражения малых ДП по данным КТВР (отношение средних плотностей легких во время выдоха и вдоха), но не с тяжестью эмфиземы [13]. Нейтрофильное воспаление ДП связано с гиперпродукцией секрета в проводящих ДП [14].
У пациентов с ХОБЛ обнаруживают повышенное содержание макрофагов в ДП, и эти макрофаги могут демонстрировать различные фенотипические черты [15]. Frankenberger и колл. показали, что среди макрофагов, изолированных из индуцированной мокроты пациентов ХОБЛ, 46% были малыми макрофагами, в то время как у здоровых добровольцев обнаруживали лишь 1% малых макрофагов [16].
Повышенное содержание Т-лимфоцитов при ХОБЛ обнаруживают в проксимальных ДП, в малых ДП и в альвеолах [15]. Saetta и колл. выявили у пациентов с ХОБЛ в эпителии малых ДП CD8+ Т-лимфоциты, экспрессирующие CXCR3, хемокиновый рецептор и его лиганд-интерферон-индуцированный протеин 10/CXCL10 [17]. Аккумуляция активированных CD8+ Т-лимфоцитов в дистальных ДП у больных ХОБЛ была ассоциирована с различными структурными изменениями, что говорит о важной роли этих клеток в патогенезе ХОБЛ [18].
Пока недостаточно изучена роль в воспалительной реакции ДП таких клеток, как тучные клетки и эозинофилы. Grashoff et al. показали значительное повышение числа интраэпителиальных тучных клеток у пациентов с ХОБЛ, что не исключает их роль в патогенезе структурных изменений, приводящих к бронхиальной обструкции [19]. Эозинофильную инфильтрацию проксимальных ДП обнаруживают у больных ХОБЛ во время обострений [20], особенно вызванных вирусной инфекцией [21], и в т. ч. у больных ХОБЛ с хроническим кашлем и выраженной продукцией мокроты [22].
Анализ бронхиальных биопсий и индуцированной мокроты у бросивших курить пациентов демонстрирует схожий воспалительный процесс, что предполагает персистенцию воспаления даже после прекращения действия ингаляционных ирритантов (курения) [23].
С учетом такой важной роли воспаления ДП в патогенезе ХОБЛ неудивительно, что противовоспалительной терапии при данном заболевании сегодня уделяют огромное внимание. К числу противовоспалительных препаратов для терапии ХОБЛ сегодня относятся ингаляционные глюкокортикостероиды (ИГКС), а новые перспективы противовоспалительной терапии ХОБЛ связывают с препаратами из класса ингибиторов фосфодиэстеразы-4 (рофлумиласт) [24], с новыми макролидами [25] и статинами [26].
Ингаляционные глюкокортикостероиды
Согласно современным руководствам, терапия ИГКС рекомендована больным с тяжелыми и крайне тяжелыми стадиями ХОБЛ при наличии частых обострений; терапия ИГКС добавляется к терапии длительно действующими (ДД) бронходилататорами [1]. Важное место среди лекарственных средств (ЛС), использующихся для длительной поддерживающей терапии ХОБЛ, занимают комбинированные препараты - ИГКС плюс длительно действующие β2-агонисты (ДДБА) [27-29]. Так же как и ИГКС, комбинированная терапия ИГКС/ (ДДБА) в настоящее время рекомендована для применения больным с III—IV стадиями (по классификации GOLD) и с частыми обострениями [1]. Научное обоснование комбинации ИГКС/ДДБА вытекает из комплементарных эффектов препаратов: ИГКС повышают экспрессию гена β2-рецептора и уменьшают потенциал для развития десенситизации β2-рецептора, в то время как β2-агонисты активируют неактивные ГКС-рецепторы, делая их более чувствительными для стероидзависимой активации [30].
Данные об эффективности ИГКС у больных ХОБЛ довольно противоречивы. В некоторых краткосрочных исследованиях терапия ИГКС не приводила к значимой модификации воспалительной реакции у больных ХОБЛ (рис. 2) [31-33]. Однако в ряде работ показано, что терапия ИГКС в сочетании с ДДБА и без них может не оказать влияния на маркеры воспаления в мокроте, но может повлиять на воспаления в стенке бронха по данным биопсий [34]. Краткосрочная терапия ИГКС (в течение 2-3 месяцев) у больных со среднетяжелой ХОБЛ приводила к уменьшению числа тучных клеток, не влияла на СD8+-лимфоциты, нейтрофилы и макрофаги [35]. Комбинированная терапия ИГКС/ДДБА в течение 3 месяцев оказалась более эффективной по влиянию на бронхиальное воспаление по сравнению с плацебо [36] и, в сравнении с ИГКС, приводила к снижению числа СD8+-клеток и макрофагов [33]. По данным исследования GLUCOLD, терапия флутиказоном в течение 30 месяцев приводила к стойкому уменьшению числа Т-лимфоцитов и тучных клеток в слизистой бронхов, однако после прекращения терапии ИГКС в течение 6 месяцев вновь наблюдалось усиление воспалительной реакции [34], т. е. данные этого исследования указывают на то, что противовоспалительные эффекты терапии ИГКС не «закрепляются» надолго [34].
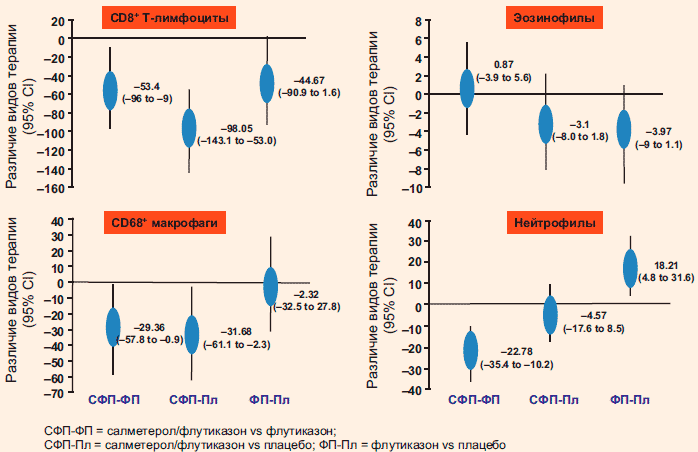
Рисунок 2. Влияние терапии на ИГКС и ИГКС/ДДБА на клетки воспаления в дыхательных путях больных ХОБЛ (по данным бронхобиопсии) (Bourbeau J. et al. Thorax 2007)
Jen и колл. провели метаанализ на основе 8 рандомизированных исследований, посвященных изучению эффектов ИГКС на маркеры воспаления дыхательных путей по данным бронхоальвеолярного лаважа (БАЛ) (n = 102) и данным эндобронхиальных биопсий (n = 309) [37]. По сравнению с пациентами контрольной группы, у больных, принимавших ИГКС, стандартизованное среднее различие (ССР) по числу нейтрофилов в жидкости БАЛ составило -0,64 ед. (р = 0,003). ИГКС также снижали число лимфоцитов в жидкости БАЛ (ССР -0,64 ед., р = 0,01). Терапия ИГКС не оказывала никакого эффекта на эозинофилы БАЛ, но приводила к повышению числа альвеолярных макрофагов (ССР 0,68 ед., р = 0,002). ИГКС не влияли на число нейтрофилов в бронхиальных биоптатах (ССР 0,61 ед., р = 0,10). Однако терапия ИГКС приводила к достоверному снижению числа CD8-лимфоцитов (ССР -0,66 ед., р = 0,002) и СD4-лимфоцитов (ССР -0,52 ед., р = 0,001) в препаратах эндобронхиальных биопсий. ИГКС не оказывали никакого влияния на число тканевых CD68-макрофагов и эозинофилов. Основные результаты метаанализа схематично представлены в таблице [37].
Таблица.
Влияние терапии ИГКС на маркеры воспаления дыхательных путей по данным БАЛ (n = 102) и данным эндобронхиальных биопсий (n = 309) [37]
|
Клетки воспаления |
Данные эндобронхиальных биопсий | Данные БАЛ |
| Нейтрофилы | = | ↓ |
| Макрофаги | = | ↑ |
| Эозинофилы | = | = |
| СD8-лимфоциты | ↓ | ↓ |
| СD4-лимфоциты | ↓ |
Менее выраженная эффективность ИГКС при ХОБЛ, по сравнению с бронхиальной астмой, может быть объяснена с позиции снижения экспрессии и активности одного из ключевых ядерных ферментов - деацетилазы гистонов-2 (HDAC-2), который необходим для «выключения» активированных воспалительных генов [11, 38]. Снижение активности HDAC-2 и относительная резистентность воспаления при ХОБЛ к ИГКС являются следствием выраженного окислительного и нитративного стресса в дыхательных путях пациентов ХОБЛ [38].
Согласно ряду исследований регулярная противовоспалительная терапия ИГКС у больных ХОБЛ улучшает симптомы, функциональные показатели, качество жизни и снижает число обострений у пациентов с ХОБЛ [39,40]. Отмена ИГКС (под прикрытием ДДБА) приводит к снижению ОФВ1, нарастанию симптомов, ухудшению качества жизни и повышению числа обострений [41].
В одном из самых масштабных исследований, проведенных в последнее время (наблюдение за 6 000 больными ХОБЛ на протяжении 3 лет) - TOwards a Revolution in COPD Health (TORCH), было продемонстрировано, что длительная поддерживающая терапия ИГКС (флутиказоном), ДДБА (салметеролом) и ИГКС/ДДБА (салметеролом/флутиказоном) приводит к замедлению скорости снижения OФB1 на 13,13 и 16 мл/год соответственно [42]. Согласно результатам недавно выполненного метаанализа, основанного на 27 исследованиях (30 495 пациентов с ХОБЛ), комбинированная терапия ИГКС/ДЦБА приводит к снижению общей летальности больных на 20% (ОР 0,80; р = 0,005) [43].
При терапии больных ХОБЛ необходимо помнить о возможных нежелательных реакциях со стороны ИГКС. По данным когортных исследований, применение ИГКС сопровождается определенным риском развития остеопороза и катаракты [44, 45]. Пневмония чаще осложняет терапию ИГКС и ИГКС/ДЦБА по сравнению с ЦЦ бронхолитиками и плацебо [42], но в то же время на фоне терапии ИГКС/ДЦБА отмечен более низкий уровень летальности и меньшее число обострений ХОБЛ. По данным крупного когортного исследования, терапия ИГКС была ассоциирована с повышением на 34% риска развития сахарного диабета и риском прогрессирования диабета [46].
Ингибиторы фосфодиэстеразы-4
Ингибиторы фосфодиэстеразы-4 (ФДЭ-4) пока представлены всего одним препаратом — рофлумиластом, который оказывает разнообразное противовоспалительное действие и специфически влияет на основные механизмы воспаления при ХОБЛ. Практически все клетки, участвующие в воспалении дыхательных путей при ХОБЛ, содержат изофермент ФДЭ-4 [24].
Противовоспалительная активность рофлумиласта в модели астмы на мышах и in vitro в легочных фибробластах эмбриона человека проявлялась в уменьшении ремоделирования дыхательных путей и в антифибротическом эффекте, сравнимом с эффектом дексаметазона при хроническом аллергическом воспалении [24]. В животных моделях ХОБЛ рофлумиласт снижал число нейтрофилов в БАЛ и гиперсекрецию слизи, однако при хроническом воздействии табачного дыма противовоспалительный эффект рофлумиласта проявлялся только при высоких дозах препарата и заключался в уменьшении макрофагального воспаления и уменьшении площади эмфиземы без влияния на гиперплазию бокаловидных клеток [24]. Данные, полученные на различных животных моделях, свидетельствуют о способности рофлумиласта уменьшать содержание нейтрофилов дыхательных путей, но в то же время - о неэффективности таких средств, как метилпреднизолон и дексаметазон [24].
Grootendorst и колл. в рандомизированном плацебо-контролируемом перекрестном исследовании изучали эффекты рофлумиласта на цитологический профиль индуцированной мокроты у больных ХОБЛ [47]. Терапия рофлумиластом в течение 4 недель привела к улучшению функциональных показателей, а также снижению количества воспалительных клеток в мокроте, таких как нейтрофилы (рис. 3), лимфоциты и эозинофилы [47]. Кроме того, на фоне терапии рофлумиластом отмечено уменьшение концентрации воспалительных маркеров - нейтрофильной эластазы, IL-8, эозинофильного катионного белка и α2-макроглобулина - маркера микроваскулярной проницаемости [47].
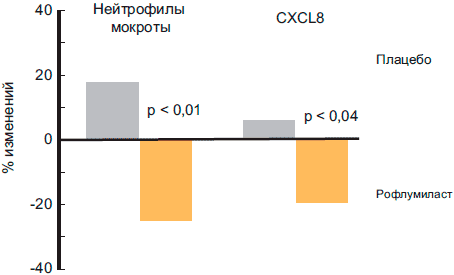
Рисунок 3. Рофлумиласт уменьшает уровни маркеров воспаления в мокроте больных ХОБЛ (Grootendorst et al. Thorax 2007)
Клиническая эффективность рофлумиласта у пациентов с ХОБЛ среднетяжелого и тяжелого течения была продемонстрирована в серии крупных рандомизированных плацебо-контролируемых исследований. Рофлумиласт не обладает прямым бронхорасширяющим действием, но благодаря своим противовоспалительным эффектам способен улучшить функциональные показатели у пациентов с ХОБЛ [48]. В исследовании Rabe и колл. рофлумиласт улучшил постбронходилатационный OФB1 на 74 мл в минимальной (250 мг/сут) и на 97 мл в максимальной дозировках (500 мг/сут) по сравнению с плацебо [49].
В двух исследованиях среднее число тяжелых и среднетяжелых обострений ХОБЛ на одного пациента в год значительно снизилось у больных, получавших рофлумиласт, по сравнению с плацебо: отношение риска (ОР; 0,83) независимо от одновременного приема ДДБА [50].
Rennard и колл. выполнили совокупный post-hoc-анализ исследований, изучавших эффективность рофлумиласта у пациентов с тяжелой и очень тяжелой ХОБЛ (стадии III и IV по классификации GOLD), и показали значительное снижение числа обострений ХОБЛ в подгруппе больных с бронхитическим вариантом ХОБЛ (т. е. с хроническим кашлем и продукцией мокроты) — на 26,2% (р = 0,001), в то время как в целом по группе ХОБЛ снижение числа обострений составило 14,3% (р = 0,026) (рис. 4) [51]. Bateman и колл. на основе двух других исследований проанализировали влияние рофлумиласта на число обострений у пациентов с ХОБЛ с частыми (≥ 2 в год) и нечастыми (< 2 в год) обострениями (рис. 5) [52]. У больных с нечастыми обострениями терапия рофлумиластом приводила к достоверному снижению числа обострений по сравнению с плацебо на 16,5% (р = 0,006). Но у больных с частыми обострениями различие с плацебо оказалось еще более выраженным — 22,3% (р = 0,002).
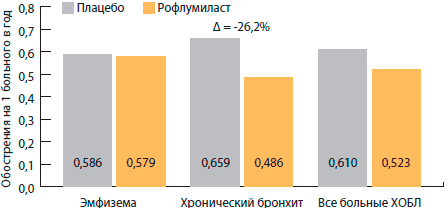
Рисунок 4. Терапия рофлумиластом приводит к наибольшему снижению числа обострений у больных с бронхитическим типом ХОБЛ
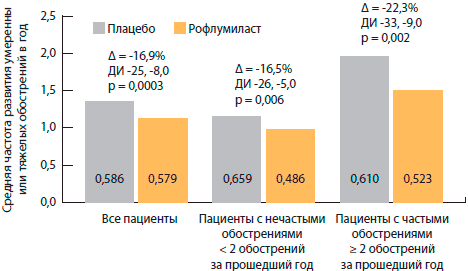
Рисунок 5. Терапия рофлумиластом приводит к наибольшему снижению числа обострений у больных ХОБЛ с частыми обострениями
В соответствии с современными рекомендациями GOLD рофлумиласт рассматривается как терапия, назначаемая дополнительно к приему комбинации ИГКС и ДДБА или к приему ДД антихолинергических препаратов у пациентов с выраженными симптомами, тяжелой или очень тяжелой бронхиальной обструкцией и высоким риском обострений [1].
Из наиболее частых нежелательных явлений можно отметить диарею, тошноту, снижение аппетита, снижение массы тела и головную боль [48]. Большинство нежелательных явлений носили легкий и умеренный характер. Нежелательные явления при приеме рофлумиласта появлялись чаще всего в первые недели приема препарата и разрешались в ходе его дальнейшего приема [55]. У пациентов ХОБЛ, получавших терапию рофлумиластом, было отмечено более частое, по сравнению с плацебо, снижение массы тела. После отмены рофлумиласта масса тела большинства пациентов восстановилась в течение 3 месяцев.
Длительная терапия макролидами
В настоящее время накапливается все больше и больше данных (причем не только в экспериментальных, но и в клинических исследованиях) о том, что макролидные антибиотики обладают важными иммуномодулирующими и противовоспалительными свойствами, которые могут быть использованы для контроля воспаления при хронических заболеваниях дыхательных путей [25].
Противовоспалительные свойства макролидов тесно связаны с их структурным строением - иммуномодулирующая активность была выявлена только у 14-членных (эритромицин, кларитромицин и ротроксимицин) и 15-членных макролидов (азитромицин), но не у 16-членных макролидов (спирамицин, джозамицин). Сегодня в клинической практике для терапии хронических воспалительных бронхолегочных заболевании используются преимущественно макролиды нового поколения - азитромицин или кларитромицин [25].
Потенциальными механизмами действия макролидов при хронических воспалительных бронхолегочных заболеваниях могут быть ингибиторные эффекты на секрецию в дыхательных путях [56], на аккумуляцию нейтрофилов и лимфоцитов в дыхательных путях [57] и антипролиферативное воздействие на активноделящиеся клетки (рис. 6) [58].
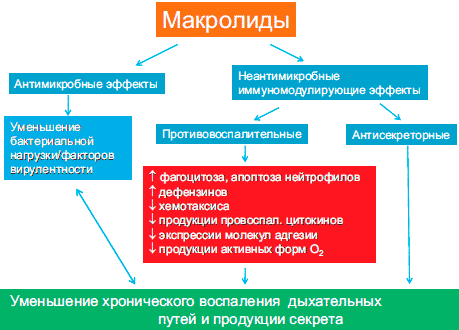
Рисунок 6. Потенциальные механизмы действия макролидов при хронических воспалительных бронхолегочных заболеваниях
Эффективность терапии макролидами воспалительных заболеваний малых дыхательных путей, уже продемонстрированная во многих исследованиях, может быть связана со способностью макролидов подавлять нейтрофильное воспаление [59]. Принципиальным различием между терапией ГКС/иммуносупрессантами и макролидами является ингибирование различных митоген-активированных протеинкиназ, таких как р38-МАРК, экстрацеллюлярно регулируемой киназы и Janus-N-концевой киназы, а также уменьшение окислительного стресса макролидами, но не ГКС/иммуносупрессантами [60].
Возможным механизмом положительного влияния макролидов на воспалительный процесс при патологии дыхательных путей является их способность модулировать бактериальную вирулентность. Кроме того, макролиды способны уменьшить формирование биопленок [61].
Относительно недавно было опубликовано самое масштабное на сегодня исследование, посвященное изучению влияния длительной терапии азитромицином на развитие обострений ХОБЛ [62]. В исследование было включено 1 142 больных ХОБЛ (средний OФB1 40 ± 16%), которые в течение 1-го года принимали либо азитромицин в дозе 250 мг/сут ежедневно (570 пациентов), либо плацебо (572 пациента). Число обострений ХОБЛ оказалось существенно ниже у больных, принимавших азитромицин: 741 против 900 в группе плацебо, т. е. риск развития обострений составил 0,73 (р < 0,001). Частота обострений на одного человека в год составила 1,48 и 1,83, а среднее время до следующего обострения — 266 против 174 дней (р < 0,001) соответственно в группах азитромицина и плацебо (рис.7). Не было отмечено различий между группами пациентов по числу госпитализаций в стационар, однако число незапланированных визитов оказалось меньше среди больных, принимавших азитромицин: 2,46 против 2,57 на одного пациента в год (р = 0,048).
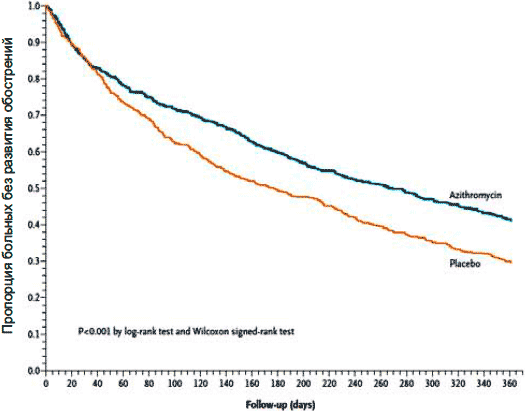
Рисунок 7. Развитие обострений ХОБЛ при терапии азитромицином и плацебо (Alberts et al. N Engl J Med, 2011) обострений ХОБЛ [62]. В исследование было включено
Несмотря на полученные обнадеживающие данные о возможности использования макролидов у больных с хроническими воспалительными заболеваниями легких, нельзя не обсудить проблему безопасности длительной терапии данными препаратами. Продолжительная терапия макролидами может привести к селекции штаммов микроорганизмов, резистентных к данному классу антибиотиков, что особенно актуально для S. pneumoniae [63]. Кроме того, известны случаи, когда терапия макролидами приводила к развитию побочных явлений со стороны желудочно-кишечного тракта [64], кардиотоксичным (нарушение внутрисердечной проводимости) [65] и ототоксичным эффектам [62].
Статины
Довольно неожиданно хорошо изученные «нереспираторные» препараты - статины (ингибиторы ГМГ-КоА-редуктазы) недавно привлекли внимание и с точки зрения терапии ХОБЛ. Статины обладают универсальными противовоспалительными эффектами, в т. ч. они способны уменьшить выраженность воспаления дыхательных путей, индуцированного табачным дымом [26, 66]. Статины уменьшают экспрессию поверхностных молекул адгезии на эндотелиальных клетках, макрофагах и эозинофилах, а также хемокиновых рецепторов, что приводит к снижению рекрутирования и миграции таких клеток воспаления, как нейтрофилы [67]. Кроме того, статины подавляют продукцию провоспалительных цитокинов.
Согласно результатам когортных исследований статины могут уменьшить число обострений и летальность больных ХОБЛ [68-70]. Также на фоне приема статинов отмечено уменьшение выраженности тяжести обострений, числа интубаций трахеи и потребности использования респираторной поддержки во время обострений [71-73]. По данным двух исследований, статины способны замедлить прогрессирование ХОБЛ [74, 75]. Lee и колл. показали, что у пациентов с ХОБЛ на фоне приема статинов наблюдается снижение сывороточного уровня СРБ и повышение физической выносливости [76].
Антагонисты медиаторов
В формировании воспалительного ответа при ХОБЛ участвуют многие медиаторы [77], и антагонисты некоторых из них теоретически могут быть использованы для контроля воспаления у пациентов с ХОБЛ. Уже сегодня можно привести несколько примеров использования таких препаратов в пилотных исследованиях.
Фактор некроза опухоли (TNF-α) является универсальным цитокином, принимающим участие в хемотаксисе и активации макрофагов и нейтрофилов. Повышенные уровни TNF-a способствуют развитию апоптоза миоцитов поперечно-полосатых мышц и их атрофии [78]. Rennard и колл. провели многоцентровое РКП, в котором изучали эффективность терапии инфликсимабом — человеческим моноклональным антителом к TNF-a — у пациентов с ХОБЛ [79]. Препарат хорошо переносился пациентами, однако не снижал число обострений и не улучшал качество жизни больных. В данном исследовании была отмечена недостоверная тенденция к повышению числа опухолей и пневмоний на фоне приема инфликсимаба [79].
Цитокин IL-8 также играет большую роль в воспалительном каскаде, приводя к повышенной миграции и активации нейтрофилов [80]. В единственном на сегодня РКП человеческий моноклональный IgG2 к IL-8 (ABX-IL8) назначали пациентам с ХОБЛ в виде 3 инфузий в течение 3 месяцев [81]. По сравнению с плацебо терапия ABX-IL8 привела к статистически значимому улучшению одышки (по шкале Transitional Dyspnea Index), но не было различий по другим показателям эффективности (функциональные параметры, качество жизни и 6-минутный тест). Была отмечена хорошая переносимость препарата.
Лейкотриен В4 (LTB4), дериват арахидоновой кислоты, является хемоаттрактантом и активатором нейтрофилов [80]. Эффективность ингибитора синтеза лейкотриенов BAYx1005 была изучена в небольшом исследовании II фазы у больных ХОБЛ [82]. Терапия препаратом в течение 14 дней приводила к значительному снижению концентрации LTB4 в мокроте по сравнению с плацебо [82]. Так как подавление синтеза лейкотриенов может быть важным методом влияния на нейтрофильное воспаление, обсуждается вопрос о проведении дальнейших исследований с подобными препаратами при ХОБЛ [83].
Заключение
Воспаление у «здоровых» курильщиков по составу клеточных элементов, медиаторов и протеаз очень похоже на воспаление у пациентов с ХОБЛ, но менее выражено. Поэтому полагают, что воспаление в дыхательных путях и паренхиме при ХОБЛ представляет собой усиленный хронический воспалительный ответ на ирританты (такие как табачный дым). К числу широко используемых противовоспалительных препаратов при ХОБЛ относятся ИГКС, как правило, в виде комбинаций с ДДБА. Новые перспективы противовоспалительной терапии ХОБЛ связывают с препаратами из класса ингибиторов фосфодиэстеразы-4 (рофлумиласт), с макролидами, статинами и новыми антагонистами медиаторов.
ЛИТЕРАТУРА
1. Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for diagnosis, management, and prevention of chronic obstructive pulmonary disease. NHLBI/WHO workshop report. Last updated 2011.
2. Celli B.R., MacNee W. ATS/ERS Task Force. Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J 2004; 23: 932-946.
3. Buist A.S., McBurnie M.A., Vollmer W.M. et al. International variation in the prevalence of COPD (the BOLD Study): a population-based prevalence study. Lancet 2007; 370: 741-50.
4. Mannino D.M., Ноmа D.M., Akinbami L. et al. Chronic obstructive pulmonary disease surveillance - United States, 1971-2000. MMWR Surveill Summ 2002; 51: 1-16.
5. Murray C.J., Lopez A.D. Alternative projections of mortality and disability by cause 1990-2020: Global Burden of Disease Study. Lancet 1997; 349: 1498-504.
6. Barnes P.J., Shapiro S.D., Pauwels R.A. Chronic obstructive pulmonary disease: molecular and cellular mechanisms. Eur Respir J 2003; 22: 672-88.
7. HoggJ.C. Pathophysiology of airflow limitation in chronic obstructive pulmonary disease. Lancet 2004; 364: 709-21.
8. Barnes P.J. Chronic obstructive pulmonary disease. N Engl J Med 2000; 343: 269-80.
9. Barnes P.J. Molecular genetics of chronic obstructive pulmonary disease. Thorax 1999; 54: 245-52.
10. Meshi B., Vitalis T.Z., Ionescu D., Elliott W.M., Liu С., Wang X.D. et al. Emphysematous lung destruction by cigarette smoke. The effects of latent adenoviral infection on the lung inflammatory response. Am J Respir Cell Mol Biol 2002; 26: 52-7.
11. Ito K., Barnes PJ., Adcock I.M. Glucocorticoid receptor recruitment of histone deacetylase 2 inhibits interleukin- lb-induced histone H4 acetylation on lysines 8 and 12. Mol Cell Biol 2000; 20: 6891-903.
12. Hogg J.C., Macklem P.T., Thurlbeck W.M. Site and nature of airway obstruction in chronic obstructive lung disease. N Engl J Med 1968; 278: 1355-1360.
13. O’Donnell R.A., Peebles С., Ward J.A. et al. Relationship between peripheral airway dysfunction, airway obstruction, and neutrophilic inflammation in COPD. Thorax 2004; 59: 837-842.
14. Nadel J.A. Role of neutrophil elastase in hypersecretion during COPD exacerbations, and proposed therapies. Chest 2000; 117: Suppl. 2, 386S-389S.
15. Finkelstein R, Ma H.D., Ghezzo H. et al. Morphometry of small airways in smokers and its relationship to emphysema type and hyperresponsiveness. Am J Respir Crit Care Med 1995; 152: 267-276.
16. Frankenberger М., Menzel М., Betz R. et al. Characterization of a population of small macrophages in induced sputum of patients with chronic obstructive pulmonary disease and healthy volunteers. Clin Exp Immunol 2004; 138: 507-516.
17. Saetta М., Mariani М., Panina-Bordignon P. et al. Increased expression of the chemokine receptor CXCR3 and its ligand CXCL10 in peripheral airways of smokers with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2002; 165: 1404-1409.
18. Fairclough L„ Urbanowicz R.A., Corne J., et al. Killer cells in chronic obstructive pulmonary disease. Clin Sci (Lond) 2008; 114: 533-541.
19. Grashoff W.F., Sont J.K., Sterk P.J., et al. Chronic obstructive pulmonary disease: role of bronchiolar mast cells and macrophages. Am J Pathol 1997; 151: 1785-1790.
20. Saetta М., Di Stefano A., Maestrelli P., et al. Airway eosinophilia in chronic bronchitis during exacerbations. Am J Respir Crit Care Med 1994; 150: 1646-1652.
21. Papi A., Bellettato C.M., Braccioni F., et al. Infections and airway inflammation in chronic obstructive pulmonary disease severe exacerbations. Am J Respir Crit Care Med 2006; 173: 1114-1121.
22. Snoeck-Stroband JB, Lapperre TS, Gosman MM, et al. Chronic bronchitis sub-phenotype within COPD: inflammation in sputum and biopsies. Eur Respir J 2008; 31: 70-77.
23. Rutgers SR, Postma DS, ten Hacken NH, Kauffman HF, Der Mark TW, ter GH, et al. Ongoing airway inflammation in patients with COPD who do not currently smoke. Thorax 2000; 55: 12-18.
24. Antoniu S.A. New therapeutic options in the management of COPD - focus on roflumilast. Int J Chron Obstruct Pulmon Dis 2011; 6: 147-155.
25. Yamaya M, Azuma A, Takizawa H. Macrolide effects on the prevention of COPD exacerbations. Eur Respir J 2012; 40:485-494.
26. Young RP, Hopkins R, Eaton ТЕ. Pharmacological actions of statins: potential utility in COPD. Eur Respir Rev 2009; 18: 1-11.
27. Cazzola M, Dahl R. Inhaled combination therapy with long-acting β 2-agonists and corticosteroids in stable COPD. Chest 2004; 126: 220-237.
