Агомелатин в терапии большого депрессивного расстройства: Приложение
Статьи Sidney H. Kennedy , Sakina J. RizviПредыдущий раздел | Содержание | Список литературы
ПРИЛОЖЕНИЕ
Таблица I. Исследования агомелатина с плацебо-контролем и активными препаратами сравнения
| Исследование, г | Число пациентов | Доза агомелатина (мг/сут) | Препарат сравнения | Активный контроль | Длительность | Выборка | Главный показатель эффективности | Критерий эффективности | Общий результат |
| Эффективность при кратковременной терапии в сравнении с плацебо | |||||||||
| Loo et al.,[40] 2002 (исследование 1) |
711 | 1, 5 и 25 | Плацебо | Пароксетин 20мг/сут |
8 недель | БДР и биполярное расстройство II типа | HAMD-17 | HAMD-17 | Позитивный |
| Olie и Kasper,[41] 2007 (исследование 2) |
238 | 25-50 | Плацебо | Нет | 6 недель 46 недель дополнение |
БДР | HAMD-17 | HAMD-17 | Позитивный |
| Kennedy и Emsley,[42] 2006 (исследование 3) |
212 | 25-50 | Плацебо | Нет | 6 недель 46 недель дополнение |
БДР | HAMD-17 | HAMD-17 | Позитивный |
| EPAR,[43] 20 08 (CL3-022) |
419 | 25 | Плацебо | Флуоксетин 20мг/сут |
6 недель 18 недель дополнение |
БДР | HAMD-17 | HAMD-17 | Негативный |
| EPAR,[43] 2008 (CL3-023) |
418 | 25 | Плацебо | Пароксетин 20мг/сут |
6 недель 18 недель дополнение |
БДР | HAMD-17 | HAMD-17 | Неудачноеa |
| EPAR,[43] 2008 (CL3-024) |
607 | 25 | Плацебо | Флуоксетин 20мг/сут |
6 недель 18 недель дополнение |
БДР | HAMD-17 | HAMD-17 | Неудачноеa |
| Профилактика рецидивов | |||||||||
| EPAR,[43] 2008 (CL3-021) |
367 | 25 | Плацебо | Нет | 34 недели 18 недель дополнение |
БДР | HAMD-17 | HAMD-17 | Негативный |
| Goodwin et al.,[44 2009 (исследование 4) |
339 | 25-50 | Плацебо | Нет | 32-34 недели 20 недель дополнение |
БДР | HAMD-17 | HAMD-17 | Позитивный |
| Эффективность при кратковременной терапии в сравнении с активными препаратами сравнения | |||||||||
| Lemoine и Guilleminault,[45] 2007 (исследование 5) |
334b | 25-50 | Венлафаксин 75-150 мг/сут |
Нет | 6 недель 18 недель дополнение |
БДР | LSEQ | Кратковременная терапия: HAMD-17; длительная терапия: CGI |
Позитивный |
| Kasperetal.,[46] 2010 (исследование 6) |
313 | 25-50 | Сертралин 50-100 мг/сут |
Нет | 6 недель 18 недель дополнение |
БДР | Circadian rest-activity cycle |
HAMD-17 | Позитивный |
| Kennedy etal.,[47] 2008 (исследование7) |
277 | 50 | Венлафаксин XR 150 мг/сут |
Нет | 12 недель 12 недель дополнение |
БДР | SEXFX | MADRS | Позитивный |
| Симптомы отмены | |||||||||
| Montgomery et al.,[48] 2004 (исследование 8) |
335 | 25 | Плацебо Пароксетин 20 мг/сут |
Нет | 12 недель followed by 2 недель плацебо substitution period |
БДР | DESS | MADRS | Позитивный |
| Переносимость в контексте половой функции у здоровых добровольцев | |||||||||
| Montejo et al.,[49] 2008 (исследование 9) |
92 | 25-50 | Плацебо | Пароксетин 20 мг/сут |
8недель | Здоровые добровольцы | PRSEXDQ | Неприемлемо | Позитивный |
| Эффективность при кратковременной терапии ГТР в сравнении с плацебо | |||||||||
| Stein et al.,[50] 2009 | 121 | 25-50 | Плацебо | Нет | 12 недель | ГТР | HAMA | Неприемлемо | Позитивный |
a Без различий между активным контролем и плацебо.
b Два пациента не были включены в анализ эффективности.
CGI = Шкала общего клинического впечатления; DESS = Симптомы и признаки отмены; EPAR = Европейский отчет общественной оценки (European Public Assessment Report); ГТР = Генерализованное тревожное расстройство; HAMА = Шкала тревоги Гамильтона;
HAMD-17 = 17-пунктовая Шкала депрессии Гамильтона; LSEQ = Вопросник для оценки сна Leeds; MADRS = Шкала депрессии Монтгомери-Асберг; БДР = большое депрессивное расстройство; PRSEXDQ = Вопросник для оценки связанных с психотропными средствами половых дисфункций; SEXFX = Вопросник для оценки половых эффектов; XR = замедленного высвобождения.
Таблица II. Демографические и стартовые характеристики пациентов в общих выборках основных исследований
| CL3-022[43]a | CL3-023[43]a | CL3-024[43]a | CL3-021[43]b рецидив профилактика |
Исследование 1[40]a | Исследование 2[41]a | Исследование 3[42]a | Исследование 4[44]b,o профилактика рецидивов |
Исследование 5[45]a | Исследование 6[46]a | Исследование 7[47]a | Исследование 8 [48]a | |
| Число пациентов |
409 | 415 | 604 | 367 | 697 | 235 | 211 | 339 | 332 | 307 | 276 | 335 |
| Возраст, лет | 42.5±10.2 | 40.9±10.6 | 41.0±10.9 | 45.7±10.3 | 42.3±11.0 | 45.0±11.3 | 42.5±12.3 | 43.3±10.6 | 40.1 ±10.5 | 43.8±10.2 | 40.9±10.2 | 42.4± 13.4 |
| Женщины, % | 69.0 | 74.0 | 72.6 | 77.9 | 66.7 | 73.2 | 60.2 | 74.3 | 71.1 | 70.0 | 71.8 | 68.1 |
| Рекуррентный эпизод, % | 69.0 | 71.0 | 69.3 | 100 | 67.0 | 77.0 | 76.8 | 100 | 56.0 | 70.7 | 70.4 | 68.4 |
| Число эпизодов1 | 3.0 ±2.6 | 3.0 ±3.7 | 4.4±3.5 | 3.7±2.7 | 2.7±1.7 | 2.6±1.6 | 3.6±2.1 | 2.2±1.9 | 2.9±2.8 | 2.4±1.4 | 2.5±1.8 | |
| Стартовый суммарный балл | 25.9±2.8 | 26.6±3.3 | 26.2±2.9 | 27.4±3.0 | 27.3±2.7 | 26.6±2.9 | 26.8±2.6 | 26.0±3.3 | 26.3±2.9 | 27.9±4.3 (MADRS) |
23.0±2.4 (MADRS) |
|
| HAMD-17/ MADRS CGI-S |
5.0±0.6 | 4.6±0.6 | 4.7±0.7 | 4.8±0.7 | 4.9±0.7 | 4.9±0.7 | 4.8±0.7 | 4.9±0.7 | NA | 4.7±0.7 | 4.5±0.6 | 4.1 ±0.7 |
b Выборка рандомизации. c Рандомизированное исследование профилактики рецидивов.
d Включая текущий эпизод.
CGI-S = Шкала общего клинического впечатления - Тяжесть; HAMD-17 = 17-пунктовая Шкала депрессии Гамильтона; MADRS = Шкала депрессии Монтгомери-Асберг; NA= неприемлемо.
Таблица III. Эффективность агомелатина и активного препарата сравнения пароксетина в сопоставлении с плацебо по суммарным баллам 17-пунктовой Шкалы депрессии Гамильтона
| Исследование, терапевтическая группа (n) |
Стартовое значение |
Финальное значение |
Различие в сравнении с плацебо |
95% CI | p-Value |
| Исследование 1[40] (8 недель) | |||||
| Агомелатин 25 мг/сут (135) | 27.4 - 2.7 | 12.8-8.2 | 2.57 | 0.15, 4.99 | 0.034 |
| Плацебо (136) | 27.4 - 3.1 | 15.3-8.9 | |||
| Пароксетин 20мг/сут (144) | 27.3 - 3.4 | 13.1 -8.4 | 2.25 | 0.22, 4.28 | 0.030 |
| Исследование 2[41] (6 недель) | |||||
| Агомелатин 25-50 мг/сут (116) | 27.4-2.7 | 13.7-0.8 | 3.44 | 1.63, 5.26 | 0.001 |
| Плацебо (119) | 27.2-2.7 | 17.1 -0.8 | |||
| Исследование 3[42](6 недель) | |||||
| Агомелатин 25-50 мг/сут (106) | 26.5 - 2.8 | 14.1 -7.7 | 2.30 | 0.28, 4.31 | 0.026 |
| Плацебо (105) | 26.7-3.0 | 16.5-7.4 | |||
Таблица IV. Эффективность агомелатина при кратковременной и длительной терапии в сравнении с активными препаратами сравнения: доли респондеров и пациентов в ремиссии в соответствии с суммарными баллами 17-пунктовой Шкалы депрессии Гамильтона (HAMD-17) и баллами Шкалы общего клинического впечатления улучшение (CGI-I)
| Исследование 5[45] агомелатин 25-50 мг/сут (n = 165) |
Исследование 6[46] | |||
| венлафаксин 75-150 мг/сут (n = 167) |
агомелатин 25-50 мг/сут (n = 150) |
сертралин 50-100 мг/сут (n = 156) |
||
| HAMD-17 % респондеры (редукция стартового балла >50%) | ||||
| 6 недель | 76.4 | 70.6 | 70.0 | 61.5 |
| Различие | 5.8 | 8.5 | ||
| 6 месяцев | 76.0 | 63.5 | ||
| Различие | 12.5* | |||
| CGI-I % респондеров (балл = 1 или 2) | ||||
| 6 недель | 87.9 | 77.8 | 83.3 | 76.9 |
| Различие | 10.0* | 6.4 | ||
| 6 месяцев | 83.0 | 74.9 | 78.0 | 71.2 |
| Различие | 8.2 | 6.9 | ||
| HAMD-17 % пациентов в ремиссии (балл < 7) | ||||
| 6 недель | 33.3 | 29.4 | 32.7 | 28.8 |
| Различие | 3.9 | 3.8 | ||
| 6 месяцев | 55.3 | 51.3 | ||
| Различие | 4.1 | |||
| CGI-I % пациентов в ремиссии (балл = 1) | ||||
| 6 недель | 49.1 | 46.7 | 37.8 | |
| Различие | 3.6 | 8.9 | ||
| 6 месяцев | 60.0 | 50.3 | 56.7 | 56.4 |
| Различие | 9.7 | 0.3 | ||
| * p<0.05. | ||||
Таблица V. Частота (%): пациенты, обнаруживавшие связанные с терапией нежелательные явления (СТНЯ) в двойных-слепых, плацебо-контролируемых исследованиях агомелатина длительностью 6-месяцев (неопубликованные данные on file)
| Плацебо (n =998) |
Агомелатин 25-50 мг/сут (n = 1120) |
|
| Все СТНЯ | 56.4 | 58.1 |
| Тяжелые EAEa | 9.7 | 8.8 |
| Серьезные EAEb | 3.5 | 4.2 |
| СТНЯ, ставшие причиной отмены терапии | 7.4 | 8.5 |
| Наиболее частые СТНЯ (>1 % в группе агомелатина) | ||
| Головная боль | 16.7 | 17.0 |
| Тошнота | 7.3 | 8.2 |
| Головокружение | 3.5 | 5.9 |
| Диарея | 3.0 | 3.8 |
| Инсомния | 2.8 | 3.4 |
| Сонливость | 2.4 | 3.1 |
| Запор | 2.3 | 2.3 |
| Слабость | 2.2 | 2.9 |
| Абдоминальная боль, верхние отделы | 1.5 | 2.7 |
| Боль в спине | 2.2 | 2.7 |
| Тревога | 1.6 | 2.6 |
| Гипергидроз | 0.9 | 1.3 |
| Мигрень | 0.5 | 1.3 |
b Любые медицинские явления, приведшие к смерти, угрожающие жизни, требующие госпитализации или продления текущей госпитализации, приводящие к стойкой или выраженной дезадаптации/инвалидизации или представляющие собой врожденную аномалию/дефект.
Таблица VI. Частота (%): пациенты, обнаруживавшие связанные с терапией нежелательные явления (СТНЯ) и с отменой терапии вследствие нежелательных явлений в исследованиях агомелатина и активными препаратами сравнения
| Исследование 5[45] | Исследование 6[46] | Исследование 7[47] | ||||
| агомелатин 25-50 мг/сут (n = 166) |
венлафаксин 75-150 мг/сут (n = 168) |
агомелатин 25-50 мг/сут (n = 152) |
сертралин 50-100 мг/сут (n = 159) |
агомелатин 50 мг/сут (n = 137) |
венлафаксин 150 мг/сут (n = 139) |
|
| Все СТНЯ | 67.5 | 67.9 | 58.6 | 56.6 | 66.4 | 81.3 |
| Тяжелые СТНЯ | 3.6 | 10.7 | 10.5 | 7.6 | 7.3 | 8.6 |
| Серьезные СТНЯ | 3.6 | 0.6 | 2.0 | 2.5 | 3.7 | 2.9 |
| Отмена вследствие СТНЯ | 4.2 | 14.9 | 6.7 | 12.6 | 3.7 | 10.8 |
Таблица VII. Частота (%): пациенты, обнаруживавшие гастроинтестинальные связанные с терапией нежелательные явления (СТНЯ) и нежелательные явления, послужившие причиной отмены терапии: интегративный анализ безопасности за 6 месяцев (неопубликованные данные on file)
| Плацебо (n = 826) |
Агомелатин (n = 3792) |
СИОЗСa (n = 892) |
ИОЗСНb (n = 307) |
|||||
| СТНЯ | ОТСТНЯ | СТНЯ | ОТСТНЯ | СТНЯ | ОТСТНЯ | СТНЯ | ОТСТНЯ | |
| Тошнота | 8.1 | 1.0 | 6.7 | 0.6 | 12.4 | 1.7 | 20.2 | 3.9 |
| Рвота | 1.3 | 0.4 | 1.2 | 0.1 | 2.6 | 0.7 | 4.6 | 0.7 |
| Диарея | 3.0 | 0.1 | 3.2 | 0.1 | 6.6 | 0.5 | 2.9 | |
| Запор | 2.7 | 0.1 | 2.3 | 0.1 | 2.2 | 0.2 | 5.5 | |
b Венлафаксин 75-150 мг/сут.
ИОЗСН = ингибитор обратного захвата серотонина и норадреналина; СИОЗС = селективный ингибитор обратного захвата серотонина; ОТСТНЯ = СТНЯ, ставшее причиной отмены терапии.
Таблица VIII. Частота (%): ухудшение (редукция стартового значения на >1 балл в каждой категории) половой функции в соответствии с показателями Вопросника для оценки половых эффектов у пациентов с сохранной половой активностью на момент включения в исследовании 7[47]
| Категория | Агомелатин 50 мг/сут (n =103) |
Венлафаксин 150 мг/сут (n =90) |
Значение p |
| Влечение | 6.6 | 16.4 | <0.0001 |
| Возбуждение | 9.2 | 11.4 | 0.322 |
| Оргазм | 9.1 | 18.5 | 0.001 |
| Общее удовлетворение | 4.9 | 12.8 | 0.005 |
| Суммарный балл | 8.2 | 15.2 | <0.0001 |
Рисунок. 1. Время до рецидива у пациентов, получавших агомелатин (n = 165) и плацебо (n = 174) за 6 месяцев двойной-слепой терапии. Расчет выживаемости Kaplan-Meier, исследование 4.[44]
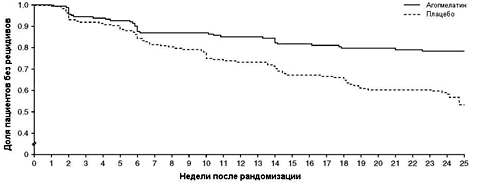
Рисунок. 2. Эффективность агомелатина при кратковременной терапии в сопоставлении с активными препаратами сравнения венлафаксином и сертралином в соответствии с суммарными баллами 17-пунктовой Шкалы депрессии Гамильтона (HAMD) и баллами Шкалы общего клинического впечатления - Улучшение (CGI-I). В исследовании 5[45] агомелатин (n = 165) сравнивался с венлафаксином (n = 167); в исследовании 6[46] агомелатин (n = 150) сравнивался с сертралином (n = 156).
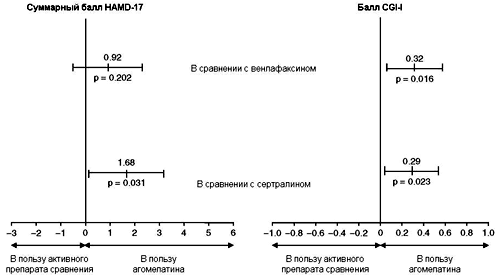
Рисунок. 3. Улучшение субъективных показателей сна при терапии агомелатином (n = 165) в сравнении с венлафаксином (n = 167) по показателям Вопросника для оценки сна Leeds (LSEQ) в исследовании 5.[45] Н = неделя.
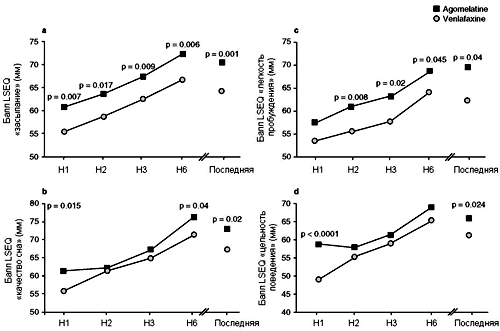
Рисунок. 4. Эффективность агомелатина в сравнении с плацебо у пациентов с «тяжелой депрессией» (стартовый суммарный балл 17-пунктовой Шкалы депрессии Гамильтона >25) в трех рандомизированных исследованиях: 1 (p = 0.024); 2(p<0.001); и 3 (p = 0.024).[40-42]
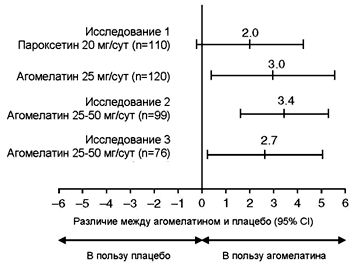
Предыдущий раздел | Содержание | Список литературы
Комментарии
ПРАКТИКА ПЕДИАТРА
