Возможности тканеселективной эстрогенной регуляции у пациенток в постменопаузе
СтатьиМ.И. Ярмолинская1,2, А.В. Колошкина1
1ФГБНУ «Научно-исследовательский институт акушерства, гинекологии и репродуктологии имени Д.О. Отта», Санкт-Петербург, Россия
2ФГБОУ ВО «Северо-Западный государственный медицинский университет имени И.И. Мечникова» Минздрава России, Санкт-Петербург, Россия
Постменопауза характеризуется снижением уровней половых стероидных гормонов, что ассоциировано с возникновением вазомоторных симптомов, генитоуринарного менопаузального синдрома (ГУМС), изменением состояния кожи и молочных желез, нарушениями липидного и углеводного профилей, эндотелиальной дисфункцией и повышением кардиометаболических рисков, снижением минеральной плотности костной ткани. На сегодняшний день наиболее эффективным методом коррекции разнообразных симптомов менопаузы является менопаузальная гормональная терапия; в качестве одного из ее вариантов в постменопаузе рассматривается применение тиболона — тканеселективного регулятора эстрогенной активности.
В обзоре представлена история изучения молекулы тиболона — синтетического стероида с эстрогенной, прогестагенной и андрогенной активностью. Механизм действия тиболона заключается в образовании трех активных метаболитов: 3-в-гидрокситиболона и 3-а-гидрокситиболона, которые отвечают за его эстрогенные эффекты и присутствуют преимущественно в неактивной сульфатированной форме, и А4-тиболона, который обладает прогестагенным и андрогенным свойствами. На фоне применения тиболона в постменопаузе отмечено эффективное устранение вазомоторных симптомов и ГУМС, повышение минеральной плотности костной ткани, наблюдались положительные эффекты в отношении сердечно-сосудистой и центральной нервной систем; при этом не отмечено стимулирующего влияния на эндометрий. Отдельно рассматривается механизм влияния тиболона на молочную железу. Таким образом, тиболон обладает избирательной эстрогенной активностью и регулирует действие в различных тканях, что делает его уникальным представителем класса STEAR.
Заключение: Тиболон является первым представителем селективных тканевых регуляторов эстрогенной активности. Разнообразные гормональные эффекты тиболона обусловлены действием нескольких ключевых метаболитов на различные ткани. На сегодняшний день тиболон может рассматриваться в качестве эффективной терапии для многих женщин в постменопаузе. Необходимо учитывать ряд особенностей действия тиболона и, исходя из этого, определять возможность назначения данной терапии для конкретной пациентки.
Ключевые слова: тиболон, STEAR, тканеселективный регулятор, постменопауза, вазомоторные симптомы, маммографическая плотность, рак молочной железы, эндометрий, минеральная плотность костной ткани.
Вклад авторов: Ярмолинская М.И. — концепция и план исследования, анализ данных и выводы; Ярмолинская М.И., Колошкина А.В. — сбор данных, подготовка рукописи.
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Работа выполнена без спонсорской поддержки.
Для цитирования: Ярмолинская М.И., Колошкина А.В. Возможности тканеселективной эстрогенной регуляции у пациенток в постменопаузе. Акушерство и гинекология. 2024; 5: 32-43 dx.doi.org/10.18565/aig.2024.117
Постменопауза и климактерический синдром
Постменопауза - это физиологический период жизни женщины, который характеризуется гипоэстрогенным состоянием, гипергонадотропной овариальной недостаточностью и связан с изменением функции лимбической системы, нарушением секреции нейрогормонов, развитием инволютивных и атрофических процессов в репродуктивных и нерепродуктивных органах-мишенях [1]. Средний возраст наступления менопаузы в мире составляет 48,8 года, в Российской Федерации - от 49 до 51 года. Диагноз менопаузы устанавливается ретроспективно, при условии аменореи не менее 12 месяцев, которая обусловлена потерей фолликулярной активности яичников и снижением количества эстрогенов, что обусловливает развитие большинства симптомов менопаузы [1].
Наиболее частым проявлением является климактерический синдром, проявляющийся приливами «жара», гипергидрозом, который встречается у 75% женщин и наиболее выражен в первые годы постменопаузы [2]. Со временем у женщин могут развиваться признаки генитоуринарного менопаузального синдрома (ГУМС), такие как вульвовагинальная атрофия, зуд, жжение, диспареуния, недержание мочи и дизурия - такие жалобы предъявляют до 80% женщин в постменопаузе. Известно, что эстрогены оказывают положительное влияние на эндотелий гладкой мускулатуры сосудов. Дефицит эстрогенов в период постменопаузы может привести к ухудшению эндотелийзависимой вазодилатации [3]. Установлено, что постменопауза характеризуется эндотелиальной дисфункцией, являющейся важным предиктором сердечно-сосудистых событий и сопровождающейся вялотекущим хроническим воспалением, потерей сосудистого тонуса и повышенной экспрессией молекул адгезии такими эндотелиальными клетками, как члены суперсемейства Ig (ICAM, VCAM), интегрины (CD11b) и селектины (CD62L и CD62E) [4]. Вышеперечисленные молекулы облегчают транспорт лейкоцитов (полиморфноядерных лейкоцитов, моноцитов, тканевых макрофагов, происходящих из моноцитов, и лимфоцитов) в интиму медиа, вызывая эндотелиальную дисфункцию и сердечно-сосудистые заболевания [5]. Другие воспалительные биомаркеры также могут прогнозировать сосудистые события, включая провоспалительные цитокины (интерлейкин (IL)-6, фактор некроза опухоли (TNF)-a), хемокины и микрочастицы, сложные везикулярные структуры, выделяемые активированными или апоптотическими эндотелиальными клетками, лейкоцитами или тромбоцитами, которые содержат фосфолипидный бислой с трансмембранными рецепторами. Активные формы кислорода (АФК) и оксид азота (NO) также участвуют в воспалении, дестабилизации бляшек, привлечении воспалительных клеток и раннем атерогенезе [6]. Воспаление и повреждение сосудов могут быть связаны с вазомоторными и эмоциональными симптомами, главным образом приливами жара и депрессивным настроением [7], которые могут быть ассоциированы с другими метаболическими нарушениями, частыми в период менопаузы, такими как увеличение веса, дислипидемия и резистентность к инсулину. У женщин в постменопаузальном периоде может быть увеличено количество циркулирующих маркеров воспаления, таких как TNF-a, что повышает чувствительность артерий к вазоконстрикции [8], а также уровни хемокина IL-8, которые вызывают расширение сосудов во время приливов [9].
Также постменопауза характеризуется сексуальной дисфункцией, эмоциональной лабильностью и склонностью к депрессивным состояниям, что часто сочетается с вазомоторными симптомами и ночной потливостью, приводит к снижению качества сна и бессоннице (встречается у 35—60% женщин в постменопаузе) и является результатом нарушения регуляции норадренергической и серотонинергической систем [1, 10]. Эти же процессы являются причиной нарушений когнитивной функции (снижение концентрации внимания и памяти), которые коррелируют с вазомоторными симптомами, депрессией и тревожными состояниями у женщин в постменопаузе [1].
Гипоэстрогенемия также оказывает негативное влияние на костный метаболизм — в период постменопаузы процессы костной резорбции преобладают над процессами формирования костной ткани. Усилению костной резорбции способствуют и снижение с возрастом абсорбции кальция в кишечнике, дефицит витамина D, нарушение образования в почках активного 1,25-дигидрокси-витамина D3. Эти изменения приводят к снижению минеральной плотности костной ткани (МПК), переломам при минимальной нагрузке на скелет (низкоэнергетические переломы). Среди женщин в возрасте 50 лет и старше в Российской Федерации остеопороз выявляется в 34% случаев, а частота остеопении составляет 43% [11].
Значение менопаузальной гормональной терапии
Главной целью менопаузальной гормональной терапии (МГТ) у пациенток в пери- и постменопаузе является частичное восполнение гормонального дефицита с помощью минимально достаточных доз гормональных препаратов, которые не сопровождаются побочными эффектами, обеспечивают профилактику поздних обменных нарушений, корректируют МПК. Показаниями для назначения МГТ являются наличие вазомоторных симптомов умеренной и тяжелой степени, существенно снижающих качество жизни, коррекция симптомов ГУМС, сексуальной дисфункции, профилактика постменопаузального остеопороза, восполнение дефицита эстрогенов при преждевременной недостаточности яичников (ПНЯ) и ранней менопаузе при двусторонней овариэктомии [12].
Согласно положениям Североамериканского общества изучения менопаузы (North American Menopause Society), старт назначения МГТ должен быть в «окне терапевтических возможностей» — женщинам в возрасте моложе 60 лет или с длительностью менопаузы менее 10 лет при отсутствии противопоказаний. Оптимальное время для старта МГТ — период пери- и ранней постменопаузы [13].
Для выявления противопоказаний необходимо провести обследование пациентки перед назначением гормональной терапии [1]. К противопоказаниям для назначения МГТ относят кровотечение из половых путей неясного генеза, рак молочной железы и эстрогензависимые злокачественные новообразования, острые и хронические заболевания печени в настоящее время или в анамнезе (до нормализации функциональных проб печени), тромбозы (артериальные и венозные) и тромбоэмболии (тромбоз глубоких вен, тромбоэмболия легочной артерии), инфаркт миокарда, ишемические или геморрагические цереброваскулярные нарушения, наличие миомы матки с субмукозным расположением узла, наличие полипа эндометрия, аллергия к компонентам МГТ, кожная порфирия (для эстрогенного компонента), прогестагензависимые новообразования (для гестагенов) [12].
Для коррекции симптомов менопаузы используются либо комбинации эстроген-прогестагенных препаратов у женщин с интактной маткой, либо изолированный прием эстрогенов, биоидентичных натуральным, у женщин без матки. МГТ назначается в циклическом режиме в перименопаузе и в непрерывном режиме — в постменопаузе [1].
Тканеселективная эстрогенная терапия
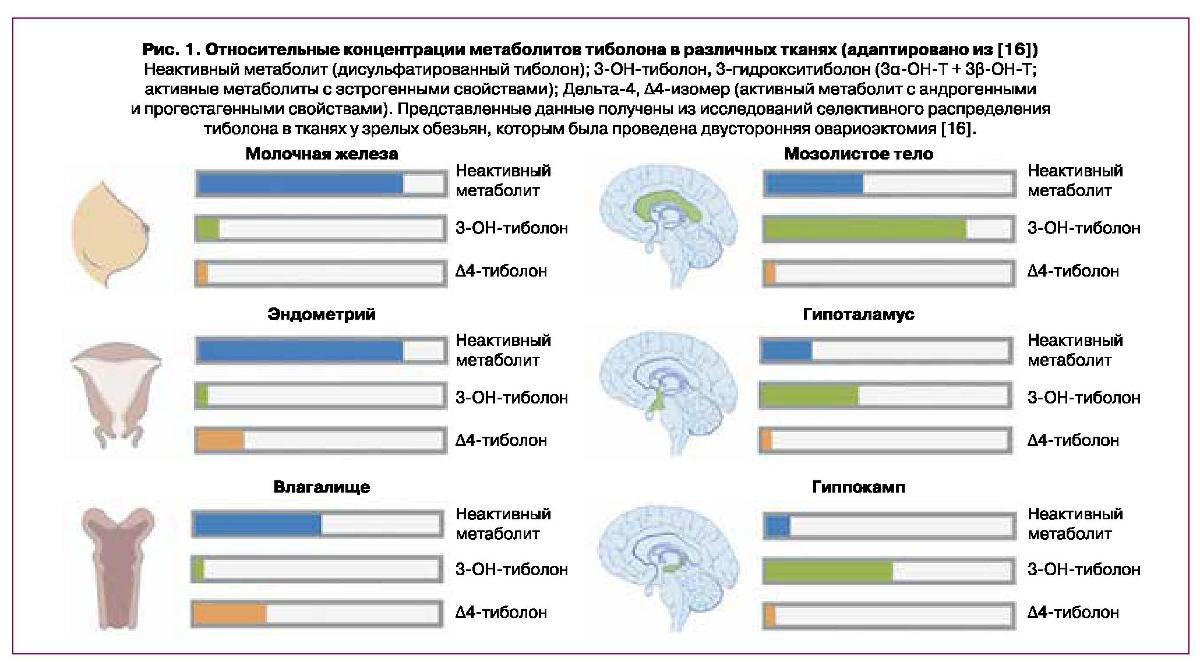
Одним из отдельных направлений МГТ для пациенток в постменопаузе является тканеселективная эстрогенная терапия. Тиболон — синтетический стероид, обладающий прогестагенной, эстрогенной и андрогенной активностью в зависимости от ткани-мишени, но не имеющий в своем составе ни эстрогенов, ни прогестагенов [14]. Механизм действия тиболона заключается в образовании трех активных метаболитов: 3-в-гидрокситиболона и 3-а-гидрок-ситиболона, которые отвечают за его эстрогенные эффекты и присутствуют преимущественно в неактивной сульфатированной форме, и Д4-тиболона, который обладает прогестагенным и андрогенным свойствами. Таким образом, тиболон снижает потерю костной массы и устраняет вазомоторные проявления, при этом не оказывая стимулирующего эстрогенного влияния на эндометрий. Эффект, оказываемый на костную ткань, головной мозг, слизистую влагалища, сердечно-сосудистую систему, центральную нервную систему, можно объяснить избирательной эстрогенной активностью тиболона, которая не распространяется на эндометрий и молочные железы, где отсутствие эстрогенного влияния обусловлено местной активностью ферментов, которые ингибируют образование активных эстрогенов (рис. 1) [15, 16]. Таким образом, эффект тиболона обусловлен не тотальным замещением половых гормонов, а избирательной регуляцией эстрогенной активности в тканях, и тиболон является единственным представителем класса STEAR (Selective Tissue Estrogenic Activity Regulator — тканеселективный регулятор эстрогенной активности) [15].
Тиболон принимается перорально, быстро и полностью всасывается из желудочно-кишечного тракта, его максимальная концентрация достигается через 1—1,5 ч. Тиболон метаболизируется в печени с образованием гидрофильных продуктов, часть из которых фармакологически активна. Выводится почками (в том числе в форме метаболитов) и через кишечник. Период полувыведения составляет примерно 7 ч, не накапливается в тканях [17].
Впервые тиболон был введен в клиническую практику в 1987 г. в Нидерландах, а сегодня данный препарат доступен в более чем 90 странах мира для лечения климактерических симптомов; а в более чем 50 странах одобрен для профилактики остеопороза [18].
Историю изучения механизмов действия тиболона можно разделить на несколько основных периодов, в ходе которых происходила трансформация представлений о механизме действия данного препарата. Первоначально его разработка была сосредоточена главным образом на лечении нейровегетативных симптомов, связанных с менопаузой; однако в ходе проведения многочисленных исследований были также рассмотрены показания для профилактики и лечения остеопороза.
Молекула тиболона - Org OD-14 - была разработана в 1964 г. и запатентована в 1965 г. компанией Organon. Его структура представляла собой модификацию прогестагенов, производных 19-нортесто-стерона [19].
Изначально эстрогенная активность молекулы тиболона составляла 10% активности этинилэстрадиола, а прогестагенная активность - всего 12% активности норэтистерона. Андрогенная активность составляла 2% активности метилтестостерона, что оказалось намного ниже, чем ожидалось при исследовании тиболона и его метаболитов; они показали относительную аффинность связывания около 30% для Д4-метаболита. Такая низкая андрогенная активность объяснялась быстрым исчезновением метаболита. Ключевым стало введение 7а-метильной группы — это привело к получению более эстрогенного соединения, при том, что проге-стагенная активность была снижена по сравнению с таковой норэтинодрела, а андрогенная активность осталась прежней. Считалось, что слабая прогестагенная активность тиболона обусловлена наличием эстрогенной активности, что впоследствии было подтверждено в исследованиях de Gooyer M.E. et al., где прогестагенная активность тиболона увеличивалась в присутствии антиэстрогенов [20].
Были проведены экспериментальные исследования на животных, которые доказывали эстрогенное действие тиболона на головной мозг. Отмечено образование β-эндорфина (наиболее важного биологически активного эндогенного опиоидного пептида, участвующего в поведении, обезболивании, терморегуляции и нейроэндокринной регуляции) у кастрированных крыс аналогично влиянию эстрогенов. Также продемонстрировано влияние тиболона на костную ткань: было проведено экспериментальное исследование на приматах, демонстрирующее, что действие тиболона на костную ткань происходит через активацию и связывание с эстрогеновыми рецепторами, так как на фоне применения антиэстрогенов данное влияние отсутствовало [21, 22].
Позже было обнаружено, что тиболон обладает не только эстрогенными, но и анаболическими свойствами, что, по-видимому, приводит к положительному балансу кальция в организме. На этом этапе было доказано, что применение тиболона предотвращает потерю костной массы, облегчает вазомоторные проявления; кроме того, отмечалось невыраженное положительное эстрогенное влияние на улучшение трофики слизистой влагалища. При этом среди пациентов отмечалась хорошая переносимость препарата (частота встречаемости таких симптомов, как изменение массы тела и вагинальные кровотечения, была низкой) и не наблюдалось гиперплазии эндометрия [18].
Отсутствие эстрогенного влияния тиболона на эндометрий потребовало дальнейших фундаментальных исследований для уточнения механизма действия. Markiewicz L. et al. продемонстрировали, что прогестагенная активность тиболона и его Д4-метаболита оказывают аналогичное прогестерону влияние на эндометрий. Несмотря на то что тиболон имеет низкое сродство к прогестероновым рецепторам, схожая прогестагенная активность тиболона свидетельствует о его возможности метаболизироваться в Д4-метаболит и уже после этого связываться с прогестагенными рецепторами, противодействуя эстрогенному эффекту 3-гидроксиметаболитов (рис. 2) [18, 23].
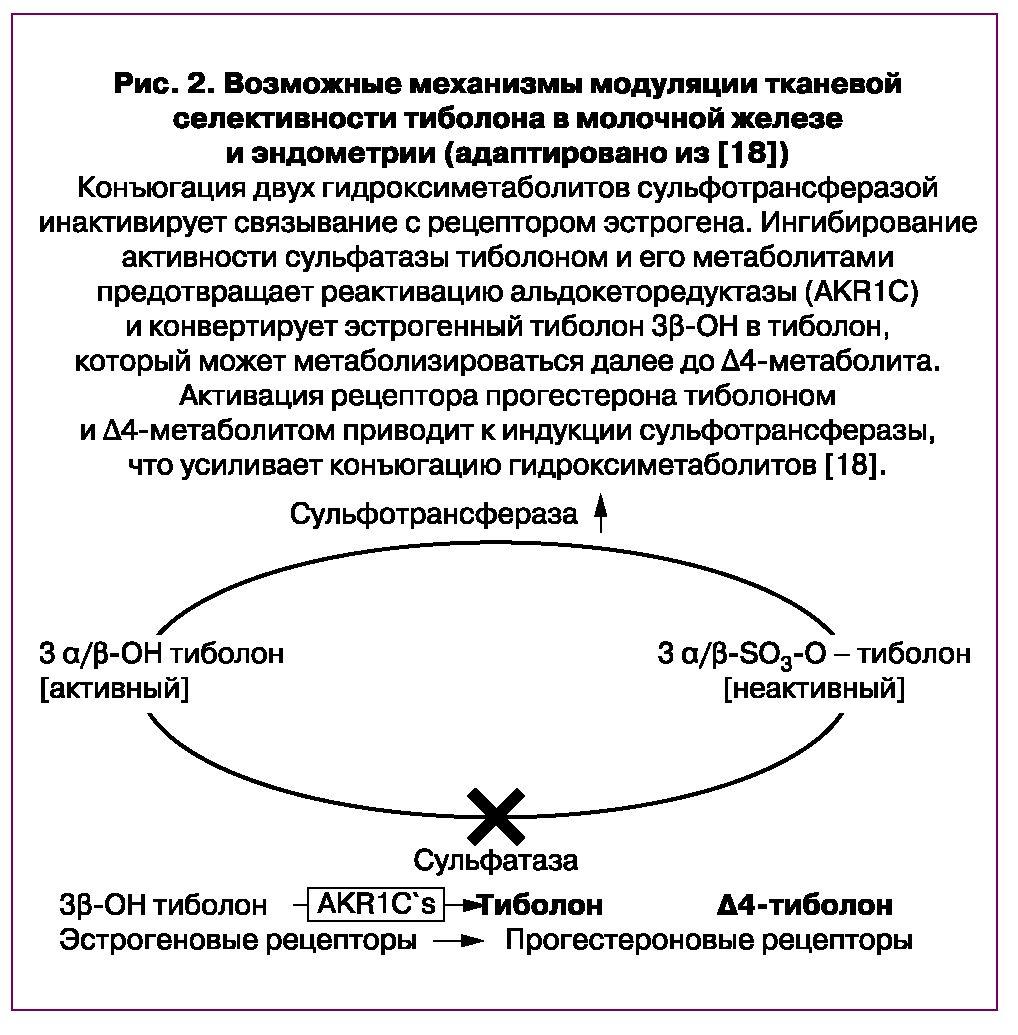
Конъюгация эстрогенных метаболитов с помощью сульфотрансферазы, которая превращает активные эстрогены в эндометрии в эстроген-неактивные метаболиты, по-видимому, играет ключевую роль в предотвращении стимуляции эстрогенными метаболитами тиболона [18].
Конъюгация двух гидроксиметаболитов сульфотрансферазой инактивирует связывание с рецептором эстрогена. Ингибирование активности сульфатазы тиболоном и его метаболитами предотвращает реактивацию альдокеторедуктазы (AKR1C) и конвертирует эстрогенный тиболон 3β-OH в тиболон, который может метаболизироваться далее до Д4-метаболита. Активация рецептора прогестерона тиболоном и Д4-метаболитом приводит к индукции сульфотрансферазы, что усиливает конъюгацию гидроксиметаболитов [18].
Два 3-гидроксиметаболита убедительно продемонстрировали эстрогенные эффекты в тесте, оценивающем эстрогенную активность. При этом было обнаружено, что 3в-гидроксильный метаболит увеличивает активность 17в-гидроксистероиддегидро-геназы (17β-HSD) 2 типа и накопление гликогена в тканях, что, как ранее предполагалось, должно контролироваться прогестагенным компонентом. Эти исследования стали первым указанием на то, что тиболон и его метаболиты могут локально метаболизироваться в ткани эндометрия и послужили объяснением, почему у женщин, принимавших данный препарат, наблюдался атрофичный эндометрий. Tang B. et al. в 1993 г. подтвердили вышеописанную гормональную конверсию с использованием меченного радиоактивным изотопом тиболона [24].
Хотя лечение эстрогенами снижает частоту остеопоротических переломов и кардиометаболических рисков (но не назначается с целью первичной или вторичной профилактики сердечно-сосудистых заболеваний) у женщин в постменопаузе, длительное лечение эстрогенами в качестве монотерапии у пациенток с интактной маткой повышает риск рака эндометрия [25].
Исследование, в которое были включены 3240 женщин в постменопаузе, продемонстрировало, что действие тиболона на пролиферацию эндометрия было сходным с действием прогестагенов [26], и, согласно опубликованным данным, тиболон в течение 24 недель оказывал протективное воздействие на эндометрий в постменопаузе благодаря более высокой экспрессии прогестероновых рецепторов и белка Bcl-2 в железистом эпителии эндометрия, тем самым создавая баланс между проапоптотическим и антиапоптотическим действием, что приводило к снижению пролиферации и атрофии эндометрия [27].
В ряде рандомизированных клинических исследований (РКИ) описана меньшая частота прорывных кровотечений среди пациенток, принимавших тиболон (кровотечения встречались у 18—27% женщин), по сравнению с пациентками, принимающими комбинированную МГТ (кровотечения наблюдались в 47% случаев). Относительно гистологической характеристики эндометрия на фоне применения тиболона первоначально были получены противоречивые данные: некоторые исследования продемонстрировали схожую гистологическую картину эндометрия у женщин, принимающих тиболон, и женщин, принимающих конъюгированные эквин-эстрогены в сочетании с медроксипрогестерона ацетатом [28]; в других работах на фоне приема препарата был отмечен слабо пролиферативный тип эндометрия [29].
Вышеописанные данные указывают на то, что метаболиты тиболона, обладающие прогестагенным действием, не полностью противодействуют эстрогенному влиянию на эндометрий. В 2011 г. были опубликованы тревожные результаты проспективного когортного исследования с участием датских женщин в возрасте от 50 до 79 лет, находившихся под наблюдением в течение 14 лет, которые показали, что по сравнению с женщинами, никогда не получавшими гормональную терапию, у пациенток, принимавших тиболон, наблюдался несколько более высокий коэффициент заболеваемости раком эндометрия, в особенности раком эндометрия 1 типа, который имеет более выраженную гормональную чувствительность. Этот риск повышался с увеличением продолжительности лечения, что указывало на причинно-следственную связь. Кроме того, в той же группе были обнаружены повышение коэффициента заболеваемости раком яичников и риск, который также увеличивался с продолжительностью использования [30].
Сообщения о повышении частоты рака эндометрия, ассоциированного с приемом тиболона, инициировали ряд исследований. Авторы когортного исследования «случай — контроль», проведенного в Великобритании, пришли к заключению, что недостаточно данных для однозначных выводов о повышении риска рака эндометрия на фоне приема тиболона (введенного в продажу в Великобритании в 1991 г.) из-за величины остаточной систематической ошибки [31]. В другом исследовании были представлены данные о том, что кратковременное лечение тиболоном в течение 21 дня приводит к небольшой стимуляции пролиферации эндометрия, а в долгосрочной перспективе наблюдается атрофичный тип эндометрия, согласно гистологическому исследованию. На основании этого авторы заключают, что стимулирующее действие тиболона приводит к незначительной стимуляции пролиферации эндометрия, однако данный эффект носит временный характер. Предполагается, что тиболон сначала проявляет более эстрогенный механизм действия, который со временем уравновешивается индукцией его прогестагенных свойств [32].
В ходе дальнейших исследований тиболона были доказаны его важные свойства: антипролиферативный эффект и ингибирующее влияние на ферменты, участвующие в синтезе активных эстрогенов в молочной железе. Тиболон и его Д4-метаболит продемонстрировали антипролиферативный эффект на клетки молочной железы здоровых женщин; тогда как 3а-ги-дроксиметаболит, напротив, оказал пролиферативный эффект, сопоставимый с влиянием эстрадиола в концентрации 10 нмоль/л. При этом метаболит 3в-ги-дрокситиболона не стимулировал пролиферацию, что может быть связано с его обратным превращением в тиболон и/или Д4-метаболит. Вскоре были проведены нерандомизированные клинические исследования, показавшие, что тиболон не повышает плотность молочных желез, согласно морфометрическому индексу роста [33]. Кроме того, Gompel A. et al. продемонстрировали, что тиболон и его метаболиты способны ингибировать пролиферацию клеток интактной молочной железы. На основании экспериментальных исследований было установлено, что экспрессия маркера пролиферации Ki-67 существенно не увеличивалась в ткани молочной железы обезьян с удаленными яичниками после 2 лет лечения тиболоном [34].
В рандомизированном проспективном двойном слепом исследовании было показано, что тиболон и плацебо не повышают уровень Ki-67 после 6-месячного применения на основании результатов тонкоигольной аспирационной биопсии; в то время как комбинация МГТ эстрадиолом 2 мг в сочетании с норэтистерона ацетатом значительно повышает уровень Ki-67 в ткани молочной железы. В том же исследовании отмечено гораздо более выраженное и значительное влияние комбинированной МГТ на повышение маммографической плотности молочных желез [35, 36].
Согласно клиническим рекомендациям «Менопауза и климактерические состояния у женщин» 2021 г., на сегодняшний день всем женщинам, начиная с 40-летнего возраста, должна выполняться маммография один раз в два года, а на фоне проведения МГТ — ежегодно. Также необходимо проводить дополнительное обследование молочных желез перед началом приема МГТ, если предыдущее обследование было проведено более полугода назад с обязательной оценкой по шкале BI-RADS для определения дальнейшей тактики ведения [1].
Известно, что большинство случаев рака молочной железы гормонально зависимы. Эстрадиол играет важную роль в генезе и эволюции рака молочной железы, а пути метаболизма эстрадиола в ткани молочной железы определяют его локальную концентрацию в тканях. Ткань молочной железы человека (неизмененная или пораженная онкологическим процессом) содержит все ферменты активации или инактивации эстрадиола: сульфатазу, 17β-HSD, ароматазу и сульфотрансферазы [37]. Линии раковых клеток MCF-7 и T-47D или клеточные линии здоровой молочной железы обычно используются для исследований in vitro. Тиболон и его метаболиты Д4 ингибируют синтез эстрадиола, блокируя активность сульфатазы и 17β-HSD 1 типа в клеточных линиях MCF-7 и T-47D, что указывает на потенциальный протективный эффект в отношении развития гиперпролиферативных заболеваний молочной железы. 3а-Гидрокси и Д4-изомеры тиболона также оказывают двойное влияние на активность сульфотрансфераз: эффект является стимулирующим при низких дозах, но ингибирование этой активности наблюдается при более высоких дозах в клетках рака молочной железы MCF-7 и T-47D. Интересно отметить, что 3а-гидроксипроизводное тиболона является наиболее сильным соединением с точки зрения стимулирующего действия на сульфотрансферазу [38].
Было выдвинуто предположение, что тиболон и гидроксиметаболиты тиболона не влияют на экспрессию мРНК фактора роста эндотелия сосудов в клетках MCF-7. Известно, что прогестерон и прогестины увеличивают экспрессию мРНК фактора роста эндотелия сосудов в клетках рака молочной железы T-47D, а Д4-тиболон менее эффективен, чем прогестагены в отношении экспрессии этого ангиогенного гена в клетках T-47D. Этот дифференциальный эффект может быть связан с возникновением рака молочной железы. Относительно влияния на ароматазную активность тиболона представлены противоречивые данные. В одном из исследований было представлено, что тиболон увеличивает активность ароматазы и, в свою очередь, местную концентрацию эстрогена в жировой ткани молочной железы [39]; в противоположность этому в другой работе было отмечено, что ни тиболон, ни его метаболиты не являются субстратами ароматазы; следовательно, этот путь не приводит к какой-либо эстрогенной активности тиболона [40].
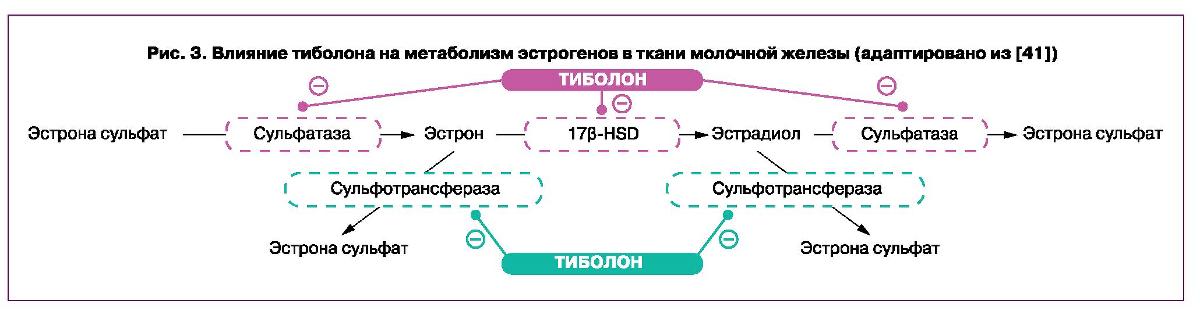
В постменопаузе у женщин преобладают неактивные эстрогены, которые в молочной железе могут трансформироваться в более активные. Этот процесс регулируется тканевыми ферментами. Как уже отмечалось ранее, в тканях молочной железы тиболон и его метаболиты подавляют сульфатазу и 17в-HSD 1 типа. Эти ферменты в молочных железах превращают эстрона сульфат, форму неактивного эстрогена, в активный эстрадиол. Кроме того, метаболит 3-ОН повышает активность сульфтрансферазы, которая, наоборот, конвертирует эстрон обратно в менее активный сульфат эстрона (рис. 3). Таким образом, на фоне терапии тиболоном эстрогены в молочной железе не активны, чем и объясняется более низкий риск развития гиперпролиферативных процессов в молочной железе [41].
Также, согласно проведенному проспективному исследованию среди 121 женщины в постменопаузе, получавших в течение 1 года тиболон либо различные формы МГТ: эстроген-прогестаген-содержащую гормональную терапию у женщин с интактной маткой или монотерапию эстрогенами у женщин с удаленной маткой, где в качестве эстрогенного компонента использовался трансдермальный эстрадиол, не было обнаружено статистически значимой разницы в повышении маммографической плотности между женщинами, принимавшими тиболон, и пациентками из контрольной группой, не получавшими лечения. При этом в группах пациенток, которые принимали ту или иную форму МГТ, увеличение маммографической плотности было статистически значимым по сравнению с группой контроля [41].
Также на фоне приема тиболона меньше выражены нагрубание молочных желез и масталгия по сравнению с использованием комбинированной МГТ [42]. Кроме того, проводились исследования, где было отмечено повышение заболеваемости раком молочной железы у женщин, принимавших эстроген-прогестагенную МГТ, однако не наблюдалось значительного увеличения заболеваемости раком молочной железы у женщин, принимавших тиболон [43].
На основании рандомизированного исследования, включившего 4538 женщин в поздней постменопаузе, отмечено достоверное снижение риска инвазивного рака молочной железы у пациенток, получавших тиболон [44].
На основании таких позитивных данных о протективном влиянии тиболона на риск рака молочной железы было проведено исследование LIBERATE у пациенток с раком молочной железы в анамнезе, на основании которого, однако, были представлены данные о повышении риска рецидива рака молочной железы при использовании тиболона [45].
Согласно клиническим рекомендациям «Менопауза и климактерическое состояние у женщин», ни один препарат для МГТ не может быть назначен для пациенток с раком молочной железы в настоящее время или в анамнезе [1].
Также были проведены исследования, сравнивающие применение тиболона и классическую эстроген-прогестагенную МГТ, в ходе которого было описано, что и тиболон, и МГТ значительно снижали количество приливов (МГТ в большей степени, чем тиболон), эпизодов потливости и проявлений ГУМС. Наблюдался более выраженный положительный эффект МГТ в отношении вазомоторных проявлений по сравнению с тиболоном; однако в группе пациенток, получающих тиболон, отмечено значительно более низкое кумулятивное число эпизодов кровотечений или кровянистых выделений в сравнении с группой МГТ. Тиболон также продемонстрировал положительное влияние на повышение либидо [18].
На сегодняшний день существует большое количество рандомизированных исследований, демонстрирующих эффективность тиболона для устранения вазомоторных симптомов в период постменопаузы. Последние данные обобщены в Кокрановском обзоре 2016 г., в котором в общей сложности приняли участие 19 976 женщин в 46 РКИ. Основное внимание было уделено эффективности и безопасности лечения тиболоном. Результаты показали, что тиболон был более эффективен, чем плацебо; при этом несколько уступил в эффективности комбинированной гормональной терапии: вазомоторные симптомы сохранялись у 7% женщин, принимавших комбинированную МГТ, и у 8—14% пациенток, получавших тиболон.
При этом отсутствуют данные о том, что тиболон увеличивает риск нежелательных явлений при длительном применении или что он отличается от классической МГТ в отношении своей долгосрочной безопасности [46].
Следующим важным этапом в истории применения тиболона стало определение оптимальной дозировки препарата с учетом эффективности и безопасности использования. Landgren M.B. et al. оценили клинически оптимальную дозу для купирования климактерических жалоб у соматически здоровых женщин. Исследовались дозы 1,5, 2,5 и 5,0 мг. Начиная с 4-й недели применения тиболон в дозе 2,5 и 5,0 мг был значительно эффективнее плацебо в отношении уменьшения частоты приливов и эпизодов потливости. Доза 1,25 мг статистически значимо отличалась от плацебо только начиная с 8-й недели применения препарата. Частота кровотечений в группе, принимавшей дозу 5,0 мг, была примерно в два раза выше, чем в группе, принимавшей дозу 2,5 мг. Таким образом, суточная доза тиболона 2,5 мг считается оптимальной и в настоящее время используется в клинической практике [47].
Однако представлены исследования, в которых используется меньшая доза тиболона исключительно для коррекции остеопоротических изменений. В исследовании «Долгосрочное вмешательство при переломах с помощью тиболона» (LIFT) приняли участие 4538 женщин в возрасте от 60 до 85 лет с остеопорозом, которые получали 1,25 мг тиболона в день или плацебо. Результаты исследования подтвердили эффективность тиболона в отношении коррекции остеопороза: через 34 месяца лечения в группе тиболона наблюдалось значительное снижение частоты позвоночных и внепозвоночных переломов [44].
Недавний метаанализ (2019 г.) также показал, что при использовании тиболона наблюдалось значительное снижение частоты вертебральных и невертебральных переломов. В этом метаанализе также рассматривалось влияние тиболона на остеопению и наблюдалось значительное повышение МПК при сравнении с терапией ралоксифеном — селективным модулятором эстрогеновых рецепторов [48].
Согласно другому исследованию, эффект тиболона на МПК аналогичен эффекту МГТ и бисфосфонатов; при этом риск переломов шейки бедра на 30% ниже при приеме тиболона [16].
Сердечно-сосудистые заболевания рассматриваются как ведущая причина смертности среди женщин старше 50 лет в развитых странах. Снижение уровня эстрогенов в постменопаузе ассоциировано с повышением кардиометаболических факторов риска. Терапия эстрогенами, биоидентичными натуральным, оказывает более благоприятный эффект на липидный профиль по сравнению с применением комбинированной МГТ эстроген-прогестагенами. Однако существуют противоречивые данные в отношении влияния тиболона на липидный профиль пациенток, что обосновывает проведение дальнейших исследований [12]. В предшествующих исследованиях не было обнаружено значимой связи между изменением показателей липидограммы и приемом тиболона [49]. При этом, согласно данным метаанализа, проведенного в 2021 г., включившего 26 РКИ, на фоне приема тиболона отмечено снижение уровня общего холестерина, липопротеидов высокой плотности и триглицеридов. Снижение концентрации липопротеидов низкой плотности наблюдается начиная с 26-й недели приема тиболона [14].
При этом представлены данные о том, что для женщин с гипертриглицеридемией более безопасной терапией является трансдермальная или низко-дозированная МГТ или тиболон [50].
Кроме того, существуют данные, что и тиболон, и его Д4-изомер обладают определенной антагонистической активностью в отношении глюкокортикоидных и, в большей степени, минералокортикоидных рецепторов, что может объяснять наблюдаемое в клинических исследованиях снижение артериального давления на фоне применения тиболона [12].
Данные субанализа РКИ и наблюдательных исследований демонстрируют повышение риска фибрилляции предсердий при применении тибо-лона в равной степени, как и на фоне приема комбинированной МГТ; поэтому у пациенток с фибрилляцией предсердий в анамнезе целесообразно рекомендовать альтернативные методы [51].
Представлены единичные данные о повышенном риске развития инсульта при использовании тиболона у пациенток в поздней постменопаузе (возраст 60-85 лет); однако данный механизм до конца не ясен и может быть связан с возрастом женщин. Рандомизированное плацебо-контролируемое исследование показало, что прием как 2,5 мг тиболона, так и конъюгированных эквинэстрогенов в сочетании с медроксипрогестерона ацетатом незначительно увеличивал толщину комплекса интима-медиа. При этом тиболон повышает уровень С-реактивного белка, фактора риска инсульта, так же, как и конъюгированные эквин-эстрогены [44].
В опубликованном крупном исследовании с использованием баз данных QResearch и CPRD, оценившем связь венозной тромбоэмболии (ВТЭ) с применением различных режимов, комбинаций и видов МГТ, отмечено, что прием тиболона не ассоциирован с увеличением риска ВТЭ [52].
Еще одними симптомами, ассоциированными с постменопаузой, являются ГУМС и сексуальная дисфункция [1, 12]. Проведены исследования, в ходе которых было представлено, что действие тиболона превосходит эффект плацебо и эстроген-прогестагенной МГТ в отношении улучшения сексуальной функции и уменьшения сухости влагалища, что позволяет его рассматривать как эффективный препарат для пациентов с сексуальной дисфункцией.
Андрогенная активность Д4-изомера в сочетании с наблюдаемым снижением уровня глобулина, связывающего половые гормоны, с соответствующим увеличением биодоступности тестостерона, эстрадиола и дегидроэпиандростерон сульфата, объясняют позитивное влияние тиболона на либидо и сексуальное здоровье женщин и слизистую оболочку влагалища и, соответственно, уменьшение симптомов вульвовагинальной атрофии в постменопаузе [46].
На основании результатов рандомизированных исследований отмечено более выраженное уменьшение сухости влагалища и жалоб на диспареунию на фоне приема тиболона по сравнению как с плацебо, так и эстроген-прогестагенной МГТ, что в результате приводило к повышению либидо и сексуальной функции [16].
Gupta B. et al. также продемонстрировали, что тиболон повышает либидо более эффективно, чем дегидроэпиандростерон и 17в-эстрадиол [53]. При этом важно отметить, что прием тиболона не сопровождался возникновением таких андроген-зависимых побочных эффектов, как акне и гирсутизм [16].
Снижение уровня половых стероидных гормонов в период перименопаузы и постменопаузы, а также после хирургической менопаузы - двусторонней овариэктомии - связано с депрессивным настроением и когнитивными нарушениями. Хотя нет никаких доказательств того, что менопауза увеличивает распространенность депрессивных состояний, риск депрессивных симптомов увеличивается во время постменопаузы, особенно при наличии в анамнезе большого депрессивного расстройства [54].
Механизмы воздействия тиболона на центральную нервную систему мало изучены. Представлены данные о влиянии тиболона на когнитивные функции: женщины в постменопаузе, получавшие тиболон в течение 6 месяцев, продемонстрировали улучшение долговременной семантической памяти аналогично женщинам, принимающим эстроген-прогестагенную МГТ [16]. Результаты исследования Fluck E. et al., в которое были включены женщины, получавшие тиболон в дозировке по 2,5 мг ежедневно в течение 10 лет, и группа контроля, никогда не получавшая гормональную терапию, показали, что в ответ на стрессовые тесты в контрольной группе пациенток наблюдались повышенное беспокойство и заторможенность в отношении принятия умственных решений, в отличие от группы женщин, получавших тиболон. Кроме того, группа, получавшая лечение, значительно лучше справилась с заданием на вспоминание категорий, которое отражает показатели семантической памяти [55]. Такое улучшение когнитивной функции у женщин в постменопаузе объясняется увеличением биодоступности эстрадиола, вызванным снижением тиболоном уровня глобулина, связывающего половые гормоны.
В отношении депрессивных состояний у женщин в постменопаузе было продемонстрировано, что тиболон в суточной дозе 2,5 мг оказывает положительное влияние на настроение по сравнению с плацебо и с эстроген-прогестагенной МГТ [54].
Несмотря на это, Berlanga C. et al. не заметили существенного улучшения симптомов депрессии у женщин в постменопаузе с большим депрессивным расстройством, у которых тиболон использовался в течение 8 недель в качестве вспомогательного средства в дополнение к антидепрессантам (флуоксетин). Важно отметить, что необходимо учитывать тяжесть депрессивных симптомов и общую длительность лечения [56]. В двойном слепом РКИ (2018 г.) 44 женщины с депрессией в постменопаузе были разделены на две группы — получавших тиболон в дозе 2,5 мг/день или получавших плацебо в течение 12 недель на фоне стандартного лечения антидепрессантами. Среди пациенток, получавших тиболон, наблюдалось значительное улучшение по шкале оценки депрессии Монтгомери—Асберга по сравнению с группой плацебо [57]. Возможные механизмы этих эффектов могут основываться на модуляции дофаминергических и серотонинергических синапсов путем активации эстрогеновых рецепторов [58]. Кроме того, показано, что тиболон оказывает влияние на ГАМКергические проопиомеланокортиновые нейроны гипоталамуса через мембранные эстрогеновые рецепторы, и эта стимуляция приводит к повышению содержания бета-эндорфинов, что обеспечивает как коррекцию депрессивных симптомов, так и общее улучшение настроения у пациенток [16].
В представленной таблице 1 отражены многообразные эффекты тиболона.
Таблица 1. Различные эффекты тиболона
|
Эстрогенные эффекты |
Прогестагенные эффекты |
Андрогенные эффекты |
|
Снижает выраженность климактерической вегетативной дисфункции |
Регулирует пролиферацию эндометрия в полости матки |
Повышает либидо |
|
Стимулирующее действие на слизистую оболочку влагалища |
Улучшает психоэмоциональное состояние |
|
|
Увеличение минеральной плотности костной ткани |
||
|
Снижение кардиометаболических рисков |
||
|
Профилактика пролиферативных процессов в молочной железе |
||
Таблица 2. Применение тиболона в зависимости от клинической картины
|
Женщины в постменопаузе с климактерическим синдромом |
Женщины в постменопаузе без климактерического синдрома |
Переход с МГТ на тиболон |
|
Снижение либидо или сексуальная дисфункция |
||
|
Изменение настроения |
||
|
Прогрессирующая потеря костной ткани (профилактика остеопороза во время раннего постменопаузального периода) |
Остеопения |
|
|
Масталгия и напряжение молочных желез в пременопаузальном периоде |
Масталгия или напряжение молочных желез |
|
|
Высокая маммографическая плотность |
Высокая плотность молочных желез, когда маммография нечитаемая или требуется повторное исследование |
|
|
Урогенитальные проблемы |
Нерегулярные вагинальные кровотечения без гистопатологических изменений |
|
В связи с тем, что патентная защита оригинального тиболона закончилась, на российском рынке появилось несколько генерических форм данной субстанции. В настоящее время на рынке имеется препарат «Леатриса» (тиболон), производимый фармацевтической компанией ООО «Аристо Фарма», гарантирующей его качество.
Наиболее перспективной группой пациенток для назначения тиболона (Леатрисы) являются женщины в постменопаузе с вазомоторными симптомами, сексуальной дисфункцией, эмоциональной лабильностью, урогенитальными жалобами, а также женщины с мастодинией или высокой маммографической плотностью молочных желез при использовании комбинированной эстроген-прогестагенной МГТ, а также для профилактики остеопороза (табл. 2). Начало приема тиболона должно совпадать с «окном терапевтических возможностей» для МГТ — возраст не старше 60 лет и длительность менопаузы не более 10 лет. Однако в настоящее время нет жестких ограничений длительности приема МГТ.
Таким образом, результаты проведенного обзора подтвердили, что тиболон может служить препаратом выбора для лечения дефицита эстрогенов у женщин в постменопаузе, а также профилактики постменопаузального остеопороза.
Заключение
Сохранение здоровья женщин, улучшение качества жизни и увеличение периода активного долголетия являются важными задачами государственной политики Российской Федерации. Согласно клиническим рекомендациям «Менопауза и климактерическое состояние у женщин», выбор оптимального эффективного и безопасного способа коррекции эстроген-дефицитных состояний у женщин должен основываться на выраженности жалоб, личном и семейном анамнезе, стадии репродуктивного старения (по STRAW+10), а также ожиданиях самой женщины для увеличения ее комплаентности. Основой для назначения МГТ является наличие показаний и отсутствие противопоказаний.
На сегодняшний день тиболон может рассматриваться в качестве эффективной терапии для многих женщин в постменопаузе. Однако необходимо учитывать ряд особенностей действия тиболона и, исходя из этого, определять возможность назначения данной терапии для конкретной пациентки. Тиболон является первым представителем класса соединений, известных как селективные тканевые регуляторы эстрогенной активности. Разнообразные гормональные эффекты тиболона обусловлены действием нескольких ключевых метаболитов на различные ткани.
Литература/References
1. Министерство здравоохранения Российской Федерации. Клинические рекомендации. Менопауза и климактерическое состояние у женщины. 2021. [Ministry of Health of the Russian Federation. Clinical guidelines. Menopause and climacteric state in women. 2021. (in Russian)].
2. Sarri G., Pedder H., Dias S., Guo Y., Lumsden M.A. Vasomotor symptoms resulting from natural menopause: a systematic review and network metaanalysis of treatment effects from the National Institute for Health and Care Excellence guideline on menopause. BJOG. 2017; 124(10): 1514-23. https:// dx.doi.org/10.1111/1471-0528.14619.
3. Ярмолинская М.И., Татарова Н.А., Касян В.Н., Петросян А.С. Эффективность негормональной терапии в лечении женщин с климактерическим синдромом. Российский вестник акушера-гинеколога. 2021; 21(2): 91-101. [Yarmolinskaya M.I., Tatarova N.A., Kasyan V.N., Petrosyan A.S. Efficacy of non-hormonal therapy for menopausal syndrome treatment. Russian Bulletin of Obstetrician-Gynecologist. 2021; 21(2): 91-101. (in Russian)]. dx.doi.org/10.17116/rosakush20212102191.
4. Figueroa-Vega N., Moreno-Frias C., Malacara J.M. Alterations in adhesion molecules, pro-inflammatory cytokines and cell-derived microparticles contribute to intima-media thickness and symptoms in postmenopausal women. PLoS One. 2015; 10(5): e0120990. dx.doi.org/10.1371 journal.pone.0120990.
5. Woollard K.J. Immunological aspects of atherosclerosis. Clin. Sci. (Lond). 2013; 125(5): 221-35. dx.doi.org/10.1042/CS20120576.
6. Vara D., Pula G. Reactive oxygen species: physiological roles in the regulation of vascular cells. Curr. Mol. Med. 2014; 14(9): 1103-25. dx.doi.org 10.2174/1566524014666140603114010.
7. Szmuilowicz E.D., Manson J.E., Rossouw J.E., Howard B.V., Margolis K.L., Greep N.C. et al. Vasomotor symptoms and cardiovascular events in postmenopausal women. Menopause. 2011; 18(6): 603-10. dx.doi.org 10.1097/gme.0b013e3182014849.
8. Novella S., Heras M., Hermenegildo C., Dantas A.P. Effects of estrogen on vascular inflammation: a matter of timing. Arterioscler. Thromb. Vasc. Biol. 2012; 32: 2035-42. dx.doi.org/10.1161/ATVBAHA.112.250308.
9. Yasui T., Uemura H., Tomita J., Miyatani Y., Yamada M., Kuwahara A. et al. Association of interleukin-8 with hot flashes in premenopausal, perimenopausal, and postmenopausal women and bilateral oophorectomized. J. Clin. Endocrinol. Metab. 2006; 91: 4805-8. dx.doi.org/10.1210/jc.2006-1100.
10. Santoro N., Epperson C.N., Mathews S.B. Menopausal symptoms and their management. Endocrinol. Metab. Clin. North Am. 2015; 44(3): 497-515. dx.doi.org/10.1016/j.ecl.2015.05.001.
11. Tremollieres F. Assessment and hormonal management of osteoporosis. Climacteric. 2019; 22(2): 122-6. dx.doi.org/10.1080/13697137.2018. 1555582.
12. Шляхто Е.В., Сухих Г.Т., Серов В.Н., Дедов И.И., Арутюнов Г.П., Сучков И.А. и др. Российские критерии приемлемости назначения менопаузальной гормональной терапии пациенткам с сердечно-сосудистыми и метаболическими заболеваниями. Согласительный документ РКО, РОАГ, РАЭ, ЕАТ, РАФ. Проблемы эндокринологии. 2023; 69(5): 11536. [Shlyakhto E.V., Sukhikh G.T., Serov V.N., Dedov I.I., Arutyunov G.P., Suchkov I.A. et al. Russian eligibility criteria prescribing menopausal hormonal hormones therapy for patients with cardiovascular and metabolic diseases. Consensus document of the Russian Cardiological Society, Russian Society of Obstetricians and Gynecologists, Russian Association of Endocrinologists, Eurasian Association of Therapists, Association of Phlebologists of Russia. Problems of Endocrinology. 2023; 69(5):115-36. (in Russian)]. dx.doi. org/10.14341/probl13394.
13. Gass M.L.S., Maki P., Shifren J.L., Schnatz P.F., Kaunitz A.M., Shapiro M. et al. NAMS supports judicious use of systemic hormone therapy for women aged 65 years and older. Menopause. 2015; 22(7): 685-6. dx.doi.org/10.1097 GME.0000000000000491.
14. Lv C., Zhang W, Tan X., Shang X., Gaman M.A., Salem H. et al. The effect of tibolone treatment on lipid profile in women: A systematic review and dose-response meta-analysis of randomized controlled trials. Pharmacol. Res. 2021; 169: 105612. dx.doi.org/10.1016 j.phrs.2021.105612.
15. Kenemans P., Speroff L.; International Tibolone Consensus Group. Tibolone: clinical recommendations and practical guidelines. A report of the International Tibolone Consensus Group. Maturitas. 2005; 51(1): 21-8. dx.doi.org/10.1016/j.maturitas.2005.02.011.
16. Del Rio J.P., Molina S., Hidalgo-Lanussa O., Garcia-Segura L.M., Barreto G.E. Tibolone as hormonal therapy and neuroprotective agent. Trends Endocrinol. Metab. 2020; 31(10): 742-59. dx.doi.org/10.1016 j.tem.2020.04.007.
17. Kloosterboer H.J. Tissue-selectivity: the mechanism of action of tibolone. Maturitas. 2004; 48 (Suppl. 1): S30-40. dx.doi.org/10.1016 j.maturitas.2004.02.012.
18. Kloosterboer H.J. Historical milestones in the development of tibolone (Livial®). Climacteric. 2011; 14(6): 609-21. dx.doi.org/10.3109 13697137.2011.580639.
19. Van Vliet N.P., Broess A.I.A., Peters J.A.M., van den Broek J.A.J., Leemhuis J.A.J., Zeelen F.J. An alternative synthesis of 17e-hydroxy-7a-methyl-19-nor-17a-pregn-5(10)-en-20-yn-3-one (Org OD14). Recl. Trav. Chim. Pays-Bas. 1986; 105(4): 111-5. dx.doi.org/10.1002/recl.19861050403..
20. de Gooyer M.E., Deckers G.H. Schoonen W.G., Verheul H.A., Kloosterboer H.J. Receptor profiling and endocrine interactions of tibolone. Steroids. 2003; 68(1): 21-30. dx.doi.org/10.1016 s0039-128x(02)00112-5.
21. Jelinek J., Kappen A., Schonbaum E., Lomax P. A primate model of human postmenopausal hot flushes. J. Clin. Endocrinol. Metab. 1984; 59(6):1224-8. dx.doi.org/10.1210/jcem-59-6-1224.
22. Genazzani A.R., Petraglia F., Facchinetti F., Genazzani A.D., Bergamaschi M., Grasso A. et al. Effects of Org OD 14 on pituitary and peripheral beta-endorphin in castrated rats and post-menopausal women. Maturitas. 1987; Suppl 1: 35-48. dx.doi.org/10.1016/0378-5122(87)90041-7.
23. Markiewicz L., Gurpide E. In vitro evaluation of estrogenic, estrogen antagonistic and progestagenic effects of a steroidal drug (Org OD-14) and its metabolites on human endometrium. J. Steroid Biochem. 1990; 35(5): 535-41. dx.doi.org/0.1016/0022-4731(90)90196-y.
24. Tang B., Markiewicz L., Kloosterboer H.J., Gurpide E. Human endometrial 3 beta-hydroxysteroid dehydrogenase/isomerase can locally reduce intrinsic estrogenic/progestagenic activity ratios of a steroidal drug (Org OD 14). J. Steroid Biochem. Mol. Biol. 1993; 45(5): 345-51. dx.doi.org/10.1016 0960-0760(93)90003-f.
25. Hanifi-Moghaddam P., Boers-Sijmons B., Klaassens A.H., van Wijk F.H., den Bakker M.A., Ott M.C. et al. Molecular analysis of human endometrium: short-term tibolone signaling differs significantly from estrogen and estrogen + progestagen signaling. J. Mol. Med. (Berl). 2007; 85(5): 471-80. dx.doi.org/10.1007/s00109-006-0146-1.
26. Archer D.F., Hendrix S., Gallagher J.C., Rymer J., Skouby S., Ferenczy A. Endometrial effects of tibolone. Clin. Endocrinol. Metab. 2007; 92(3): 911-8. dx.doi.org/10.1210/jc.2006-2207.
27. Reis B.F., Lima S.M., Silva G.M., Francisco A.M., Barbosa L.C., Archangelo S.C. et al. Effects of low dose of tibolone on steroid receptors and Bcl-2 on the postmenopausal endometrium. Histol. Histopathol. 2016; 31(6): 629-34. dx.doi.org/10.14670/HH-11-706.
28. Huber J., Palacios S., Berglund L., Hanggi W, Sathanandan S.M., Christau S. et al. Effects of tibolone and continuous combined hormone replacement therapy on bleeding rates, quality of life and tolerability in postmenopausal women. BJOG. 2002; 109(8): 886-93. dx.doi.org/10.1111 j.1471-0528.2002.01338.x.
29. Volker W., Coelingh Bennink H.J., Helmond F.A. Effects of tibolone on the endometrium. Climacteric. 2001; 4(3): 203-8.
30. McCluggage W.G. Morphological subtypes of ovarian carcinoma: a review with emphasis on new developments and pathogenesis. Pathology. 2011; 43(5): 42032. dx.doi.org/10.1097/PAT.0b013e328348a6e7.
31. de Vries C.S., Bromley S.E., Thomas H., Farmer R.D. Tibolone and endometrial cancer: a cohort and nested case-control study in the UK. Drug Saf. 2005; 28(3): 241-9. dx.doi.org/10.2165/00002018-200528030-00005.
32. Klaassens A.H., van Wijk F.H., Hanifi-Moghaddam P., Sijmons B., Ewing P.C., Ten Kate-Booij M.J. et al. Histological and immunohistochemical evaluation of postmenopausal endometrium after 3 weeks of treatment with tibolone, estrogen only, or estrogen plus progestagen. Fertil. Steril. 2006; 86(2): 352-61. https:// dx.doi.org/10.1016/j.fertnstert.2005.12.077.
33. Vos R.M., Krebbers S.F., Verhoeven C.H., Delbressine L.P. The in vivo human metabolism of tibolone. Eur. Drug Metab. Dispos. 2002; 30(2): 106-12. https:// dx.doi.org/10.1124/dmd.30.2.106.
34. Gompel A., Chaouat M., Jacob D., Perrot J.Y., Kloosterboer H.J., Rostene W. In vitro studies of tibolone in breast cells. Fertil. Steril. 2002; 78(2): 351-9. https:// dx.doi.org/10.1016/s0015-0282(02)03203-x.
35. Conner P., Christow A., Kersemaekers W., Soderqvist G., Skoog L., Carlstrom K. et al. A comparative study of breast cell proliferation during hormone replacement therapy: effects of tibolon and continuous combined estrogen-progestogen treatment. Climacteric. 2004; 7(1): 50-8. https:// dx.doi.org/10.1080/13697130310001651472.
36. Lundstrom E., Christow A., Kersemaekers W., Svane G., Azavedo E., Soderqvist G. et al. Effects of tibolone and continuous combined hormone replacement therapy on mammographic breast density. Obstet. Gynecol. 2002; 186(4): 71722. dx.doi.org/10.1067/mob.2002.121896.
37. Erel C.T., Senturk L.M., Kaleli S. Tibolone and breast cancer. Postgrad. Med. J. 2006; 82(972): 658-62. dx.doi.org/10.1136/pgmj.2005.037184.
38. Pasqualini J.R., Kloosterboer H.J. Estrone sulfatase and 17e-hydroxysteroid dehydrogenase activities in human breast cancer. Inhibitory effect by tibolone and its metabolites. Acta Obstet. Gynaecol. Scand. 1997; 76(167): 35.
39. DIPART (Vitamin D Individual Patient Analysis of Randomized Trials) Group. Patient level pooled analysis of 68 500 patients from seven major vitamin D fracture trials in US and Europe. BMJ. 2010; 340: b5463. dx.doi.org 10.1136/bmj.b5463.
40. Higgins J.P., Jackson D., Barrett J.K., Lu G., Ades A.E., White I.R. Consistency and inconsistency in network meta-analysis: concepts and models for multiarm studies. Res. Synth. Methods. 2012; 3(2): 98-110. dx.doi.org 10.1002/jrsm.1044.
41. Lee J.K., Yun H., Kim H., Yun B.H., Seo S.K. Tibolone and breast cancer. Menopausal Med. 2023; 29(3): 92-6. dx.doi.org/10.6118 jmm.23032.
42. Kenemans P., Speroff L.; International Tibolone Consensus Group. Tibolone: clinical recommendations and practical guidelines. A report of the Int. Tibolone Consensus Group. Maturitas. 2005; 51(1): 21-8. dx.doi.org/10.1016 j.maturitas.2005.02.011.
43. Lello S., Capozzi A., Scambia G., Franceschini G. Tibolone and breast tissue: a review. Reprod. Sci. 2023; 30(12): 3403-9. dx.doi.org/10.1007 s43032-023-01295-9.
44. Cummings S.R., Ettinger B., Delmas P.D., Kenemans P., Stathopoulos V., Verweij P. et al. The effects of tibolone in older postmenopausal women. N. Engl. J. Med. 2008; 14; 359(7): 697-708. dx.doi.org/10.1056 NEJMoa0800743.
45. Sismondi P., Kimmig R., Kubista E., Biglia N., Egberts J., Mulder R. et al. Effects of tibolone on climacteric symptoms and quality of life in breast cancer patients--data from LIBERATE trial. Maturitas. 2011; 70(4): 365-72. dx.doi.org/10.1016/j.maturitas.2011.09.003.
46. Formoso G., Perrone E., Maltoni S., Balduzzi S., Wilkinson J., Basevi V. et al. Short-term and long-term effects of tibolone in postmenopausal women. Cochrane Database Syst. Rev. 2016; 10(10): CD008536. dx.doi.org 10.1002/14651858.CD008536.pub3.
47. Landgren M.B., Bennink H.J., Helmond F.A., Engelen S. Dose-response analysis of effects of tibolone on climacteric symptoms. BJOG. 2002; 109(10): 1109-14. dx.doi.org/10.1111/j.1471-0528.2002.02020.x.
48. Barrionuevo P., Kapoor E., Asi N., Alahdab F., Mohammed K., Benkhadra K. et al. Efficacy of pharmacological therapies for the prevention of fractures in postmenopausal women: A Network meta-analysis. Clin. Endocrinol. Metab. 2019; 104(5): 1623-30. dx.doi.org/10.1210 jc.2019-00192.
49. Anagnostis P., Galanis P., Chatzistergiou V., Stevenson J.C., Godsland I.F., Lambrinoudaki I. et al. The effect of hormone replacement therapy and tibolone on lipoprotein (a) concentrations in postmenopausal women: A systematic review and meta-analysis. Maturitas. 2017; 99(2): 27-36. https:// dx.doi.org/10.1016/j.maturitas.2017.02.009.
50. Casanova G., dos Reis A.M., Spritzer P.M. Low-dose oral or nonoral hormone therapy: effects on C-reactive protein and atrial natriuretic peptide in menopause. Climacteric. 2015; 18(1): 86-93. dx.doi.org/10.3109 13697137.2014.940309.
51. Lee J., Kim Y., Park H., Kim C., Cho S., Kim J. Clinical impact of hormone replacement therapy on atrial fibrillation in postmenopausal women: A nationwide cohort study. Clin Med. 2021; 10(23): 5497. dx.doi.org 10.3390/jcm10235497.
52. Vinogradova Y., Coupland C., Hippisley-Cox J. Use of hormone replacement therapy and risk of venous thromboembolism: nested case-control studies using the QResearch and CPRD databases. BMJ. 2019; 2015(8): k4810. dx.doi.org/10.1136/bmj.k4810.
53. Gupta B., Mittal P., Khuteta R., Bhargava A. A comparative study of CEE, Tibolone, and DHEA as hormone replacement therapy for surgical menopause. J. Obstet. Gynaecol. India. 2013; 63(3): 194-8. dx.doi.org/10.1007 s13224-012-0297-7.
54. Gordon J., Peltier A., Grummisch J.A., Sykes Tottenham L. Estradiol fluctuation, sensitivity to stress, and depressive symptoms in the menopause transition: a pilot study. Front. Psychol. 2019; 10: 1319. dx.doi.org/10.3389 fpsyg.2019.01319.
55. Fluck E., File S.E., Rymer J. Cognitive effects of 10 years of hormone-replacement therapy with tibolone. J. Clin. Psychopharmacol. 2002; 22(1): 62-7. dx.doi.org/10.1097/00004714-200202000-00010.
56. Berlanga C., Mendieta D., Alva G., del Carmen Lara M. Failure of tibolone to potentiate the pharmacological effect of fluoxetine in postmenopausal major depression. Womens Health (Larchmt). 2003; 12(1): 33-9. dx.doi.org 10.1089/154099903321154121.
57. Kulkarni J., Gavrilidis E., Thomas N., Hudaib A.R., Worsley R., Thew C. et al. Tibolone improves depression in women through the menopause transition: A double-blind randomized controlled trial of adjunctive tibolone. Affect. Disord. 2018; 236: 88-92. dx.doi.org/10.1016/j.jad.2018.04.103.
58. Pinto-Almazan R., Segura-Uribe J.J., Farfan-Garcia E.D., Guerra-Araiza C. Effects of tibolone on the central nervous system: clinical and experimental approaches. Biomed. Res. Int. 2017; 2017: 8630764. dx.doi.org 10.1155/2017/8630764.
Поступила 15.05.2024
Принята в печать 21.05.2024
Received 15.05.2024
Accepted 21.05.2024
Сведения об авторах:
Ярмолинская Мария Игоревна, профессор РАН, д.м.н., профессор, заведующий отделом гинекологии и эндокринологии, руководитель центра «Диагностики и лечения эндометриоза», НИИ АГиР им. Д.О. Отта, 199034, Россия, Санкт-Петербург, Менделеевская линия, д. 3; профессор кафедры акушерства и гинекологии, СЗГМУ им. И.И. Мечникова Минздрава России, 191015, Россия, Санкт-Петербург, ул. Кирочная, д. 41, m.yarmolinskaya@gmail.com, SPIN-код: 3686-3605, Researcher ID: P-2183-2014, Scopus Author ID: 7801562649, orcid.org/0000-0002-6551-4147
Колошкина Анастасия Владимировна, ординатор, НИИ АГиР им. Д.О. Отта, 199034, Россия, Санкт-Петербург, Менделеевская линия, д. 3, nastyasalukhova@gmail.com, orcid.org/0000-0002-5200-7672.
TISSUE-SELECTIVE ESTROGEN REGULATION CAPABILITIES IN POSTMENOPAUSAL WOMEN
M.I. YARMOLINSKAYA1`2, A.V. KOLOSHKINA1
1D.O. Ott Research Institute of Obstetrics, Gynecology and Reproductology, St. Petersburg, Russia
2I.I. Mechnikov North-Western State Medical University, Ministry of Health of Russia, St. Petersburg, Russia
Postmenopause is a physiological period in a woman’s life characterized by a decrease in levels of sex steroid hormones. Estrogen deficiency is associated with the development of vasomotor symptoms, genitourinary syndrome of menopause (GSM), skin and breast tissue changes, lipid and carbohydrate disorders, endothelial dysfunction, and increased cardiometabolic risks, as well as decreased bone mineral density. To date, the most effective method for correcting various symptoms of menopause is menopausal hormone therapy; one of its options that can be used in postmenopause is considered to be tibolone, a tissue-selective regulator of estrogenic activity. The review presents the history of studying the molecule of tibolone, which is a synthetic steroid with estrogenic, progestogenic, and androgenic activity. The mechanism of action of tibolone involves the formation of three active metabolites: 3-P-hydroxytibolone and 3-a-hydroxytibolone, which are responsible for estrogenic effects of tibolone and mainly present in an inactive sulfated form, and A4-tibolone, which has progestogenic and androgenic activity. Tibolone use in postmenopausal women has demonstrated effective alleviation of vasomotor symptoms, GSM, increase in bone mineral density, and positive effects on the cardiovascular and central nervous systems; stimulating effect on the endometrium was absent. There is also a discussion of mechanism of tibolone impact on breast tissue. Thus, tibolone exhibits selective estrogenic activity and regulates actions in different tissues, making it a unique representative of the STEAR class.
Conclusion: Tibolone is the first representative of tissue selective regulators of estrogenic activity. The diverse hormonal effects of tibolone are due to the action of several key metabolites on various tissues. Tibolone can currently be considered as an effective therapy for many postmenopausal women. It is necessary to take into account a number of characteristics of tibolone action and determine the possibility ofprescribing the therapy for a specific patient on the basis of this information.
Keywords: tibolone, STEAR, tissue-selective regulator, postmenopause, vasomotor symptoms, mammographic density, breast cancer, endometrium, bone mineral density.
Author’s contributions: Yarmolinskaya M.I. - developing the concept of the study and research plan, data analysis and conclusions; Yarmolinskaya M.I., Koloshkina A.V. - collecting data, preparing the manuscript.
Conflicts of interest: The authors declare no possible conflicts of interest.
Funding: The study was conducted without sponsorship.
For citation: Yarmolinskaya M.I., Koloshkina A.V. Tissue-selective estrogen regulation capabilities in postmenopausal women. Akusherstvo i Ginekologiya/Obstetrics and Gynecology. 2024; (5): 32-43 (in Russian). dx.doi.org/10.18565/aig.2024.117
Authors’ information:
Maria I. Yarmolinskaya, Dr. Med. Sci., Professor of the Russian Academy of Sciences, Head of the Department of Gynecology and Endocrinology, Head of the Center of Diagnostics and Treatment of Endometriosis, D.O. Ott Research Institute of Obstetrics, Gynecology and Reproductology, 199034, Russia, St. Petersburg, Mendeleevskaya line, 3; Professor, Department of Obstetrics and Gynecology, I.I. Mechnikov North-Western State Medical University, Ministry of Health of Russia, 191015, Russia, Saint-Petersburg, Kirochnaya str., 4 1, m.yarmolinskaya@gmail.com, SPIN-код: 3686-3605, Researcher ID: P-2 183-2014, Scopus Author ID: 7801562649, orcid.org/0000-0002-6551-4147
Anastasiya V. Koloshkina, Resident, D.O. Ott Research institute of Obstetrics, Gynecology and Reproductology, 199034, Russia, St. Petersburg, Mendeleevskaya line, 3, nastyasalukhova@gmail.com, orcid.org/0000-0002-5200-7672.