Роль тиболона в устранении симптомов климактерического синдрома
СтатьиИ.Ю. Ильина, Ю.Э. Доброхотова, М.Р. Нариманова
ФГАОУ ВО «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова», Минздрава России, Москва, Россия
Актуальность: Период менопаузы характеризуется постепенным снижением, а затем и «выключением» функции яичников. Физиологические изменения в организме женщины сопровождаются развитием нейропсихических, вегетативно-сосудистых, нейроэндокринных симптомов. Менопауза является важным периодом, связанным с интенсивными гормональными изменениями, которые могут быть причиной снижения когнитивных функций, развития тревожных и депрессивных состояний, сексуальных расстройств, нарушений сна.
Цель: Провести сравнительный анализ применения различных фармакологических препаратов для коррекции менопаузальных симптомов.
Материалы и методы: На базе ГКБ №1 им. Н.И. Пирогова в период с сентября 2024 г. по июнь 2025 г. проведено исследование, в котором приняли участие 62 женщины в постменопаузе. Участницы были разделены на 3 группы: 1-я группа (n=21) — женщины, получавшие тиболон (препарат «Леатриса») в течение 6 месяцев; 2-я группа (n=17) — женщины, получавшие препарат, содержащий эстрадиол 1 мг и дидрогестерон 5 мг (E2/DYD); 3-я группа (n=24) — женщины в постменопаузе, не получавшие МГТ. Помимо общепринятых методов исследования, проводили анкетирование (шкала Грина, краткая шкала оценки психического статуса (MMSE), госпитальная шкала тревоги и депрессии (HADS), шкала женского сексуального дистресса (FSDS), анкета качества сна).
Результаты: Было выявлено, что действие тиболона сопоставимо с действием препарата E2/DYD, который рекомендован к применению пациентками через 12 месяцев после наступления менопаузы, в плане исчезновения симптомов климактерического синдрома, облегчения его степени тяжести. Тиболон эффективен для терапии сексуальной дисфункции у женщин в постменопаузе за счет метаболита, обладающего андрогенным эффектом. По результатам исследования у тиболона отсутствует пролиферативное действие на эндометрий.
Заключение: Применение тиболона значительно улучшает сексуальную функцию, снижает тревожность и депрессию, облегчает симптомы менопаузы, способствует стабилизации веса, при этом отсутствует пролиферативное влияние на эндометрий. По нашему мнению, тиболон может рассматриваться в качестве эффективной терапии для многих женщин в постменопаузе.
Ключевые слова: тиболон, менопаузальная гормональная терапия, менопауза, климактерический синдром, нарушения сна, нарушение сексуальной функции, шкала тревоги и депрессии.
Вклад авторов: Ильина И.Ю., Доброхотова Ю.Э., Нариманова М.Р. - концепция и дизайн исследования, сбор и обработка материала, написание текста, редактирование.
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Работа выполнена без спонсорской поддержки.
Согласие пациентов на публикацию: Пациенты подписали информированное согласие на публикацию своих данных. Обмен исследовательскими данными: Данные, подтверждающие выводы этого исследования, доступны по запросу у автора, ответственного за переписку, после одобрения ведущим исследователем.
Для цитирования: Ильина И.Ю., Доброхотова Ю.Э., Нариманова М.Р. Роль тиболона в устранении симптомов климактерического синдрома. Акушерство и гинекология. 2025; 9: dx.doi.org/10.18565/aig.2025.248
Менопауза - это не одномоментное событие, ему предшествует длительный процесс, связанный с завершением фертильной функции и адаптацией организма к новому состоянию [1, 2]. Данный период нередко сопровождается нейропсихическими, вегетативно-сосудистыми, нейроэндокринными симптомами, которые составляют основу климактерического синдрома (КС) и в последующем могут привести к развитию сердечно-сосудистых заболеваний, обменно-метаболических и неврологических нарушений [1].
Одним из основных проявлений КС являются приливы, наличие которых значительно снижает качество жизни пациенток, особенно при выраженном течении. Следует отметить, что приливы являются индикатором тяжести сердечно-сосудистых заболеваний, возможной причиной развития болезни Альцгеймера, способствуют повышению уровня прокоагулянтных факторов, развитию дислипопротеинемии [3]. Кроме того, дефицит эстрогенов ассоциирован с возникновением генитоуринарного менопаузального синдрома (ГУМС), изменением состояния кожи и молочных желез, снижением минеральной плотности костной ткани [4].
Менопауза является важным физиологическим периодом, связанным с интенсивными гормональными изменениями, которые могут быть причиной снижения когнитивных функций. Известно, что женщины в большей степени подвержены риску развития деменции, так как нейропротекторное действие эстрогенов снижается в период постменопаузы. Эти изменения проявляются ухудшением работоспособности, снижением скорости переключения с одного вида деятельности на другой и ослаблением памяти [5]. Кроме того, когнитивная дисфункция является своеобразным показателем развивающегося неблагополучия в головном мозге, выявление которого позволяет предвидеть развитие цереброваскулярного события и интеллектуально-мнестических расстройств, длительно протекающих бессимптомно [6].
Также, согласно данным литературы, менопаузальный переход и ранняя постменопауза связаны с повышенным риском возникновения и развития аффективных расстройств у женщин [7]. Распространенность депрессии у женщин в данный период составляет 45-68%. При этом в перименопаузе депрессивная симптоматика наблюдается в 2 раза чаще, чем в постменопаузе [8]. Результаты многочисленных крупномасштабных исследований указывают на связь между симптомами депрессии и такими проявлениями менопаузы, как приливы, ночная потливость, генитоуринарные расстройства [9-11].
Очевидно, что физиологические изменения в организме женщины на фоне дефицита эстрогенов часто сопровождаются сексуальными расстройствами, психологическими проблемами [12]. Многие женщины в постменопаузе испытывают негативные эмоции, связанные со старением, изменением внешности, утратой привлекательности. Нередко возникают соматические расстройства, депрессия и тревога, связанные с негативными возрастными трансформациями, которые влияют на сексуальную функцию [13, 14].
С возрастом у пациенток наблюдаются изменения в цикле «сон - бодрствование», которые могут происходить под действием различных факторов и связаны в первую очередь с дегенерацией нейронов головного мозга. Данные изменения обусловлены гормонально-метаболической перестройкой в период менопаузы. Известно, что частота проблем со сном в данном возрастном периоде увеличивается и составляет в пременопаузе 16-42%, в постменопаузе - 35-60%, а наличие вазомоторных симптомов в постменопаузе в 1,85 раза увеличивает риск ночных пробуждений [15, 16].
Менопаузальная гормональная терапия (МГТ) -патогенетически обоснованный метод лечения вазомоторных, психосоматических симптомов, расстройств сна, а также метод профилактики обменных нарушений и их отдаленных последствий [17, 18].
Известно, что среди женщин старше 45 лет в постменопаузе комбинированные препараты МГТ продемонстрировали большую эффективность в отношении снижения приливов у женщин в возрасте менее 55 лет при длительности менопаузы менее 5 лет и при ИМТ >30 кг/м2 [2, 19].
Однако свою эффективность продемонстрировал и относящийся к тканеселективному регулятору эстрогеновых рецепторов синтетический стероид тиболон (препарат «Леатриса»). После приема препарат метаболизируется в печени и тонком кишечнике с образованием биологически активных метаболитов, обладающих эстрогенными, прогестагенными и андрогенными свойствами [1, 2, 4].
Тиболон (7а-метилнорэтинодрел) является синтетическим веществом стероидной структуры, прогормоном, превращающимся в три активных метаболита, обладающих эстрогенным, прогестагенным и андрогенным свойствами (За- и 3в-гидроксиме-таболиты связываются с рецепторами эстрогенов, а 4-Д-изомер — преимущественно с андрогенными и гестагенными рецепторами) [2, 4].
Учитывая все вышеизложенное, целью нашего исследования явилось проведение сравнительного анализа применения различных фармакологических препаратов для коррекции менопаузальных симптомов.
Материалы и методы
Было проведено исследование на базе ГКБ №1 им. Н.И. Пирогова в период с сентября 2024 г. по июнь 2025 г. Все пациентки, принимавшие участие в исследовании, подписали информированное добровольное согласие.
В исследовании приняли участие 62 женщины в постменопаузе от +1а до +1с стадии в соответствии с критериями классификации репродуктивного старения STRAW+10, то есть пациентки, у которых отсутствовали менструации от 1 до 3 лет. Критериями включения также были: наличие менопаузальных симптомов; отсутствие абсолютных противопоказаний к назначению МГТ; отсутствие тяжелой экстра-генитальной патологии; готовность принять участие в исследовании.
В рамках исследования проводились анкетирование, детальный сбор анамнеза, включающий данные о длительности менопаузы, перенесенных заболеваниях, проводимой на момент исследования лекарственной терапии и других факторах, которые могли бы повлиять на результаты исследования; гинекологическое обследование (осмотр, цитологические соскобы с поверхности шейки матки и цервикального канала); инструментальные исследования (УЗИ органов малого таза, маммография); лабораторные исследования (липидный профиль, индекс атерогенности (ИА: общий холестерин-ЛПВП/ЛПНП), коагулограмма).
При проведении анкетирования использовали шкалу Грина для оценки степени выраженности КС, которая рассчитывается по количеству баллов: 1-11 баллов - слабая степень выраженности, 12-19 баллов - средняя, 20 баллов и выше - тяжелая [2].
Применялась краткая шкала оценки психического статуса (MMSE), которая является самой распространенной методикой для скринингового обследования пациентов с когнитивными нарушениями [6]. Степень нарушений оценивалась в баллах: 28-30 баллов - отсутствие нарушений или легкие когнитивные расстройства, 24-27 баллов - умеренные когнитивные нарушения, 20-23 балла - деменция легкой степени выраженности, 11-19 баллов -деменция умеренной степени, 0-10 баллов - тяжелая деменция.
В данном исследовании использовали госпитальную шкалу тревоги и депрессии (Hospital Anxiety and Depression Scale, HADS), разработанную для первичного выявления депрессии и тревоги в условиях общемедицинской практики [9]. При анкетировании пациент отвечает на вопросы шкалы HADS, состоящей из подшкал тревоги и депрессии. Суммарный показатель по каждой из подшкал - 7 баллов и более - выявлялся у респондентов с легкой (субклинически выраженной) тревогой и депрессией; свыше 11 баллов характерен для тяжелой (клинически выраженной) тревоги и депрессии [9].
В работе также использовалась шкала женского сексуального дистресса (FSDS), состоящая из 13 пунктов. Психосексуальное здоровье оценивали исходя из полученных баллов при ответе на вопросы. Низкий балл отражает нормальное сексуальное здоровье, тогда как высокий балл указывает на неудовлетворенность сексуальным здоровьем. Оценка >15 баллов соответствует клинически значимой проблеме [20].
В связи с тем, что наступление каждого возрастного периода сопровождается физиологическими изменениями цикла «сон-бодрствование», в ходе проводимого исследования мы использовали анкету качества сна [15, 21, 22]. О наличии проблем со сном у обследуемых пациенток мы судили по количеству набранных баллов. Количество баллов от 22 и более указывало на отсутствие нарушений сна, 19-21 балл - пограничные значения, менее 19 баллов указывало на наличие нарушений.
Точки контроля результатов были обозначены в начале исследования (исходно), через 2 и 6 месяцев наблюдения.
Критериями исключения из исследования были наличие побочных эффектов в ходе проводимой работы, отказ пациентки от участия в исследовании.
Участницы исследования были разделены на 3 группы. 1-ю группу составили 21/62 (33,9%) женщин, принимавших препарат тиболон 2,5 мг ежедневно. 2-ю группу составили 17/62 (27,4%) пациенток, которые принимали в непрерывном режиме 1 мг эстрадиола в сочетании с 5 мг дидрогестерона (E2/ DYD). 3-ю группу составили 24/62 (38,7%) пациентки, не принимавшие препараты МГТ.
Результаты
По результатам анамнеза, гинекологического осмотра, проведения инструментального и лабораторного обследования, основные показатели женщин всех трех групп были сопоставимы (табл. 1).
При сопоставлении возраста, уровня D-димера не удалось установить значимых различий среди групп.
При анализе веса, ИМТ, длительности постменопаузы, толщины М-эхо, ИА, не удалось установить значимых различий среди групп.
Следует отметить, что в ходе исследования 7/17 (41,2%) пациенток 2-й группы через 2 месяца приема препарата предъявляли жалобы на боли и нагрубание молочных желез. Дообследование молочных желез не выявило патологических изменений. У 4/17 (23,5%) пациенток данной группы проявления мастодинии сохранились через 6 месяцев приема E2/DYD.
При проведении повторного анализа в ходе динамического наблюдения через 2 и 6 месяцев были получены результаты, представленные в таблице 2.
Анализ показал, что в 1-й группе, где пациентки принимали тиболон, отмечалось значимое снижение веса за 6 месяцев, такие же изменения отмечались во 2-й группе E2/DYD. В 3-й группе без МГТ было установлено значимое повышение веса.
При проведении анализа изменений толщины эндометрия в ходе проводимого исследования были получены данные, представленные в таблице 3.
На фоне приема гормональных препаратов у пациенток 1-й и 2-й групп значимых изменений толщины эндометрия не наблюдалось. Однако необходимо отметить, что у 3/17 (17,6%) пациенток 2-й группы в течение 6 месяцев наблюдений отмечались кровяные выделения из половых путей, которые самостоятельно купировались в течение нескольких дней. С учетом отсутствия патологии эндометрия при УЗИ органов малого таза от хирургического вмешательства решено было воздержаться.
В 3-й группе без МГТ было установлено значимое увеличение толщины эндометрия, что у 4/24 (16,7%) пациенток потребовало проведения с диагностической целью раздельного диагностического выскабливания под контролем гистероскопии.
Анкетирование
При оценке степени тяжести КС по шкале Грина были получены следующие результаты. В начале исследования степень тяжести в разных группах была сопоставима и составляла [Me (Q1; Q3)]: в 1-й группе - 46,0 (38,0; 52,0) балла, во 2-й группе - 42,0 (37,0; 48,0) балла, в 3-й группе - 46,0 (41,75; 52) балла. На фоне проводимого лечения у пациенток 1-й и 2-й групп и при динамическом наблюдении за пациентками 3-й группы были выявлены значимые изменения.
Через 2 месяца и, тем более, через 6 месяцев наблюдения было выявлено значимое уменьшение степени выраженности КС у пациенток, принимающих препараты МГТ (1-я и 2-я группы). А у пациенток 3-й группы наблюдалось значимое ухудшение течения КС.
Таблица 1. Характеристики обследуемых пациенток
|
Показатели |
Группы |
||
|
1-я: тиболон (n=21) |
2-я: E2/DYD (n =17) |
3-я: без МГТ (n=24) |
|
|
Возраст, лет, Me (Q1; Q3) |
50,0 (49,0; 52,0) |
51,0 (49,0; 52,0) |
50,0 (48,75; 52,0) |
|
Вес, кг, M±SD |
73,81±11,38 |
78,94±9,65 |
72,92±9,65 |
|
ИМТ, кг/м2, M±SD |
26,88±4,0 |
28,82±2,99 |
26,92±3,16 |
|
Постменопауза, мес., M±SD |
23,62±7,77 |
21,71±8,00 |
23,46±6,57 |
|
М-эхо, мм, M±SD |
3,17±0,62 |
3,11±0,68 |
3,42±0,59 |
|
ИА, M±SD |
2,41±0,53 |
2,71±0,54 |
2,54±0,47 |
|
АЧТВ, с, M±SD |
28,58±2,05 |
28,52±2,43 |
28,21±2,56 |
|
D-димер, нг/мл, Me (Q1; Q3) |
228,0 (147,0; 274,0) |
174,0 (165,0; 246,0) |
214,0 (157,75; 264,0) |
Примечание. Me - медиана, (Q1; Q3) - 1-й и 3-й квартили; M - среднее арифметическое, SD - стандартное отклонение. АЧТВ - активированное частичное тромбопластиновое время.
Таблица 2. Изменение веса у пациенток в ходе исследования
Группы | Динамика веса (кг) в разные периоды наблюдения | ||
исходно | через 2 мес. | через 6 мес. | |
M±SD | M±SD | M±SD | |
1-я: тиболон (n=21) | 73,81± 11,38 | 72,86±10,50 | 72,00±9,94 |
2-я: E2/DYD (n =17) | 78,94±9,65 | 78,53±10,49 | 77,47±10,47 |
3-я: без МГТ (n=24) | 72,92±9,65 | 73,83±9,98 | 75,21±9,88 |
При оценке психического статуса у пациенток 1-й группы средний показатель [Me (Q1; Q3)] был равен 29,0 (28,0; 30,0) балла, через 2 месяца - 29,0 (28,0; 30,0) балла, через 6 месяцев - 30,0 (29,0; 30,0) балла. У пациенток 2-й группы все показатели психического статуса в начале исследования, через 2 месяца и 6 месяцев были равны и составили 29,0 (28,0; 30,0) баллов. У пациенток 3-й группы без МГТ при оценке психического статуса были получены результаты: исходно - 29,5 (28,0; 30,0) балла, через 2 месяца и 6 месяцев - 30,0 (29,0; 30,0) балла. Мы не наблюдали значимых изменений у пациенток на фоне приема МГТ и при динамическом наблюдении. Однако надо отметить, что умеренные когнитивные нарушения были обнаружены у 5/62 (8,1%) пациенток, причем у 4 в группах, которые в дальнейшем принимали МГТ (1-я и 2 группы), и у 1 пациентки 3-й группы (без МГТ).
При анализе госпитальной шкалы тревоги и депрессии были получены результаты, представленные в таблице 4.
Таблица 4. Данные по шкале тревоги и депрессии в ходе исследования у пациенток разных групп
Группы | Шкала тревоги (баллы) | |||||
исходно | через 2 мес. | через 6 мес. | ||||
Me | Q1; Q3 | Me | Q1; Q3 | Me | Q1; Q3 | |
1-я: тиболон (n=21) | 8,0 | 7,0;10,0 | 6,0 | 5,0; 7,0 | 5,0 | 5,0; 6,0 |
2-я: E2/DYD (n =17) | 9,0 | 8,0; 11,0 | 8,0 | 7,0;10,0 | 6,0 | 5,0; 6,0 |
3-я: без МГТ (n=24) | 9,0 | 7,0; 11,0 | 12,0 | 10,75; 13,25 | 14,0 | 13,0; 14,0 |
При анализе обращает на себя внимание отсутствие значимых отличий по группам в начале исследования. Уже через 2 месяца у пациенток 1-й группы и через 6 месяцев у пациенток 1-й и 2-й групп было выявлено значимое уменьшение количества баллов по госпитальной шкале тревоги и депрессии, что указывает на положительное влияние МГТ на состояние пациенток. У пациенток 3-й группы (без МГТ) было выявлено значимое увеличение количества баллов, что может потребовать дополнительной консультации невролога, консультации психотерапевта.
Схожие результаты были получены при оценке по шкале женской сексуальной дисфункции (табл. 5).
В начале исследования все группы были сопоставимы, значимые отличия отсутствовали. Через 2 месяца применения тиболона уже отмечались значимые изменения по сравнению с пациентками 3-й группы. Что касается препарата E2/DYD, то значимые изменения отмечались только через 6 месяцев его применения, за счет некоторого уменьшения дискомфорта во влагалище. Значимое уменьшение количества баллов по представленной шкале указывает на уменьшение проявлений сексуальной дисфункции. У пациенток 3-й группы, которые не принимали препараты МГТ, было выявлено значимое увеличение количества баллов, что указывает на усугубление нарушений со стороны сексуальной функции.
 И, наконец, при проведении анализа, направленного на выявление нарушений сна, были получены результаты, представленные на рисунке.
И, наконец, при проведении анализа, направленного на выявление нарушений сна, были получены результаты, представленные на рисунке.
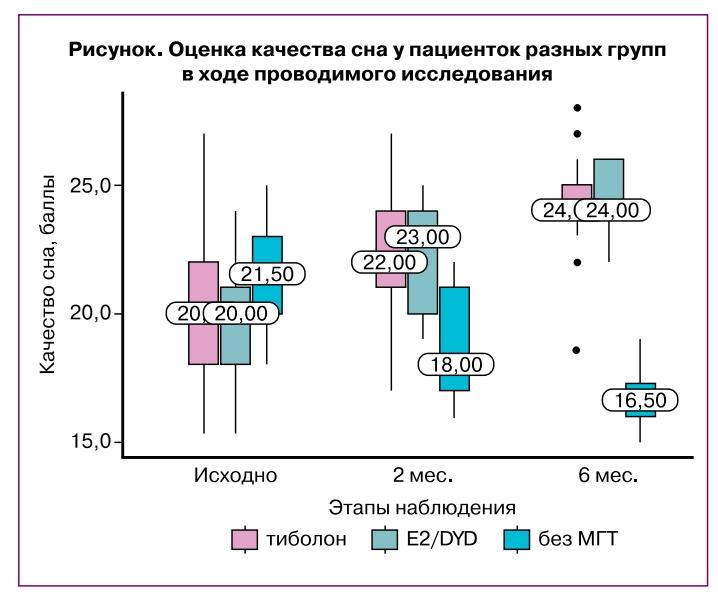
В начале исследования показатели качества сна у пациенток разных групп были сопоставимы. Через 2 месяца и 6 месяцев у пациенток 1-й и 2-й групп было выявлено значимое повышение показателей, что указывает на уменьшение нарушений. У пациенток 3-й группы (без МГТ) нами было выявлено значимое уменьшение количества баллов при проведении повторного анкетирования по качеству сна, что указывает на появление новых нарушений.
В данной работе мы также пытались оценить степень влияния выраженности КС на психический статус пациентки, на выраженность тревоги и депрессии, качество сна, сексуальную функцию. Надо отметить, что это влияние явно прослеживается между пациентками, которые принимают препараты МГТ, и теми, кто их не принимает. Были получены результаты, указывающие на то, что чем выраженнее степень тяжести КС, тем больше вероятность развития тревоги и депрессии, нарушений сна, а также нарушений сексуальной функции. В нашем исследовании мы не обнаружили выраженного влияния особенностей течения КС на психический статус, возможно, это связано с тем, что когнитивные нарушения могут развиваться в более отдаленные сроки постменопаузального периода.
Обсуждение
Период менопаузы характеризуется постепенным снижением, а затем и «выключением» функции яичников. Физиологические изменения в организме женщины сопровождаются развитием нейропсихических, вегетативно-сосудистых, нейроэндокринных симптомов, которые в последующем могут приводить к развитию других заболеваний, увеличивающих летальность [1, 2].
При выборе тактики ведения пациентки необходимо учитывать многие факторы. Так, при подборе препаратов МГТ должны учитываться безопасность их назначения, факторы риска развития заболеваний, а также эффективность в купировании симптомов КС.
В ходе проведенного исследования было выявлено, что действие тиболона сопоставимо с действием препарата E2/DYD, который рекомендован к применению пациентками через 12 месяцев после наступления менопаузы, в плане исчезновения симптомов КС, облегчения его тяжести [2]. Уже через 2 месяца приема тиболона отмечалось значимое уменьшение степени выраженности КС. Также в литературе имеются результаты исследования, посвященного терапии симптомов, возникающих в результате применения аналогов гонадолиберина у больных миомой матки, было показано значительное улучшение настроения, качества жизни и сохранение когнитивных функций при использовании тиболона без снижения эффекта основной терапии [1].
При проведении нашего исследования оказалось, что через 2 месяца приема E2/DYD у 41,2% пациенток появилась мастодиния, которая сохранилась к 6 месяцам приема данного препарата в 23,5% случаев. Пациентки, которые принимали тиболон, жалоб на боли и нагрубание молочных желез не предъявляли. Полученные результаты подтверждаются данными исследований, представленных в литературе, о том, что при применении тиболона значительно реже отмечаются болезненность молочных желез и масталгия в сравнении с эстроген-гестагенными препаратами. Соответственно, реже имеет место прекращение лечения тиболоном [23].
Следует подчеркнуть, что у пациенток, принимающих E2/DYD, в 17,6% случаев отмечались кровяные выделения, что может негативно сказываться на психоэмоциональном состоянии и играть определяющую роль в решении вопроса о дальнейшем приеме препарата. Согласно имеющимся данным, аномальные маточные кровотечения в постменопаузе на фоне применения МГТ являются одной из частых жалоб. При сравнительном анализе оказалось, что наименьшая частота прорывных кровотечений наблюдалась при применении тиболона [18].
Тиболон также может быть эффективным средством для терапии сексуальной дисфункции у женщин в постменопаузе за счет метаболита, обладающего андрогенным эффектом [2]. По данным литературы, использование тиболона оказалось эффективнее в отношении уменьшения психических расстройств и повышения либидо, чем прием дегидроэпиандростерона и 17в-эстрадиола, и было сопоставимо по действию с конъюгированными эстрогенами, но при меньшем числе побочных реакций [24]. В нашем исследовании на фоне проводимого лечения тиболоном уже через 2 месяца терапии отмечалось значимое уменьшение количества баллов по шкале женской сексуальной дисфункции, что указывает на уменьшение проявлений сексуальной дисфункции. Известно, что системная МГТ может быть недостаточно эффективна для купирования симптомов генитоуринарного менопаузального синдрома (ГУМС) и потребовать дополнительного назначения локальных форм терапии эстрогенами [2]. Тиболон же может быть эффективной альтернативой для профилактики развития ГУМС с учетом особенностей его действия.
Также наши результаты показывают высокую эффективность тиболона при коррекции эмоциональных расстройств. Уже через 2 месяца приема препарата было выявлено значимое уменьшение количества баллов по госпитальной шкале тревоги и депрессии, что указывает на положительное влияние МГТ на состояние пациенток. Результаты нашего исследования подтверждаются результатами работы, где проводилось сравнение безопасности и эффективности тиболона и антидепрессанта (эсциталопрама) у женщин в постменопаузе [25]. В исследовании первичный результат оценивался по изменению показателей климактерических симптомов по климактерической шкале Грина, тяжести депрессии и тревожности по Гамильтоновской шкале оценки депрессии (HAM-D) и Гамильтоновской шкале оценки тревожности (HAM-A), а также сексуального функционирования по Аризонской шкале сексуального опыта (ASEX). Вторичный результат — благополучие — оценивался по шкале качества жизни Всемирной организации здравоохранения (QOL)-BREF. Оказалось, что тиболон в большей степени, чем антидепрессант, улучшал состояние при депрессии, климактерических симптомах, а также повышал физическое и психологическое качество жизни с дополнительным преимуществом в виде восстановления сексуальной функции [25]. Hsiao S.M. и Liao S.C. продемонстрировали результаты сравнения влияния тиболона и комбинированного препарата МГТ на климактерические симптомы и психологический стресс. Оказалось, что тиболон более эффективен в отношении улучшения психологического состояния [26].
Заключение
Таким образом, применение тиболона значительно улучшает сексуальную функцию, снижает тревожность и депрессию, облегчает симптомы менопаузы, улучшает сон, способствует стабилизации веса, при этом отсутствует пролиферативное влияние на эндометрий.
По нашему мнению, тиболон в составе препарата «Леатриса» может рассматриваться в качестве эффективной терапии для многих женщин в постменопаузе. Необходимо учитывать ряд особенностей действия тиболона и, исходя из этого, определять возможность назначения данной терапии конкретной пациентке.
Литература / References
1. Кузнецова И.В. Выбор между гормональной и альтернативной терапией в периоде менопаузального перехода и постменопаузе. РМЖ. 2018; 2(1): 43-7. [Kuznetsova I.V. The choice of hormonal and alternative therapy in menopausal and post-menopausal period. RMJ. 2018; 2(1): 43-7 (in Russian)].
2. Министерство здравоохранения Российской Федерации. Российское общество акушеров-гинекологов. Клинические рекомендации. Менопауза и климактерическое состояние у женщины. М.; 2021. 55 с. [Ministry of Health of the Russian Federation. Clinical guidelines. Menopause and menopausal syndrome in women. Moscow; 2021. 55 p. (in Russian)].
3. Thurston R.C., El Khoudary S.R., Tepper P.G., Jackson E.A., Joffe H., Chen H.Y. et al. Trajectories of vasomotor symptoms and carotid intima media thickness in the study of women’s health across the nation. Stroke. 2016; 47(1): 12-7. dx.doi.org/10.1161/STROKEAHA.115.010600
4. Ярмолинская М.И., Колошкина А.В. Возможности тканеселективной эстрогенной регуляции у пациенток в постменопаузе. Акушерство и гинекология. 2024; 5: 32-43. [Yarmolinskaya M.I., Koloshkina A.V. Possibilities of tissue-selective estrogen regulation in postmenopausal patients. Obstetrics and Gynecology. 2024; (5): 32-43 (in Russian)]. https:// dx.doi.org/10.18565/aig.2024.117
5. Ткач В.В., Нуруддинова Э.С., Ткач А.В. Когнитивные расстройства у женщин в период менопаузы. Научное обозрение. Медицинские науки. 2022; 3: 91-6. [Tkach V.V., Nuriddinova E.S., Tkach A.V. Cognitive disorders in menopausal women. Scientific review. Medical sciences. 2022; 3: 91-6 (in Russian)].
6. Багинская Н.Н., Козловский В.И. Методы оценки когнитивных нарушений у пациентов с сердечно-сосудистыми заболеваниями в общей врачебной практике. Здравоохранение (Минск). 2022; 2(899): 49-58. [Baginskaya N.N., Kozlovsky V.I. Methods for assessing cognitive impairments in patients with cardiovascular diseases in general medical practice. Health Care (Minsk). 2022; 2(899): 49-58 (in Russian)].
7. Zhang C., Zhao M., Li Z., Song Y. Follicle-stimulating hormone positively as sociates with metabolic factors in perimenopausal women. Int. J. Endocrinol. 2020; 2020: 7024321. dx.doi.org/10.1155/2020/7024321
8. Maki P.M., Kornstein S.G., Joffe H., Bromberger J.T., Freeman E.W., Athappilly G. et al. Guidelines for the evaluation and treatment of perimenopausal depression: summary and recommendations. J. Womens Health (Larchmt). 2019; 28(2): 117-34. dx.doi.org/10.1089/jwh.2018.27099.mensocrec
9. Ахмедова А.А., Горобец Л.Н. Особенности клинической картины аффективных расстройств у женщин в период менопаузального перехода и ранней постменопаузы. Журнал неврологии и психиатрии им. С.С. Корсакова. 2024; 124(4): 75-9. [Akhmedova A.A., Gorobets L.N. Features of the clinical picture of affective disorders in women during the menopausal transition and early postmenopause. S.S. Korsakov Journal of neurology and psychiatry. 2024; 124(4): 75-9 (in Russian)]. dx.doi.org/10.17116 jnevro202412404175
10. Мазо Г.Э., Ганзенко М.А. Депрессии у женщин в период менопаузального перехода. Психиатрия и психофармакотерапия (Журнал им. П.Б. Ганнушкина. 2016; 18(6): 30-6. [Mazo G.E., Ganzenko M.A. Depression in women during the menopausal transition. Psychiatry and Psychopharmacotherapy (P.B. Gannushkin Journal). 2016; 18(6): 30-6 (in Russian)].
11. Петрова А.В. Психоэмоциональные расстройства у женщин с ожирением в постменопаузальном периоде. Уральский медицинский журнал. 2015; 125(2): 92-5. [Petrova A.V. Psycho-emotional disorders in woman with obesity in postmenopause. Ural Medical Journal. 2015; 125(2): 92-5 (in Russian)].
12. Nazarpour S., Simbar M., Tehrani F.R. Factors affecting sexual function in menopause: a review article. Taiwan. J. Obstet. Gynecol. 2016; 55(4): 480-7. dx.doi.org/10.1016/j.tjog.2016.06.001
13. Сандакова Е.А., Жуковская И.Г. Гинекологические аспекты сексуальной дисфункции в постменопаузальном периоде. РМЖ. Мать и дитя. 2023; 6(1): 26-30. [Sandakova E.A., Zhukovskaya I.G. Gynecological aspects of sexual dysfunction in the postmenopausal period. RMJ. Mother and child. 2023; 6(1): 26-30 (in Russian)]. dx.doi.org/10.32364 2618-8430-2023-6-1-26-30
14. Nazarpour S., Simbar M., Khorrami M., Jafari Torkamani Z., Saghafi R., Alavi-Majd H. The association between sexual function and body image among postmenopausal women: a crosssectional study. BMC Womens Health. 2021; 21(1): 403. dx.doi.org/10.1186/s12905-021-01549-1
15. Мадаева И.М., Семенова Н.В., Астафьев В.А., Дружинина Е.Б., Лабыгина А.В. Особенности сна у женщин в климактерическом периоде (обзор литературы). Acta biomedica scientifica. 2018; 3(3): 75-81. [Madaeva I.M., Semenova N.V., Astafyev V.A., Druzhinina E.B., Labygina A.B. Sleep features in menopausal women (literature review). Acta biomedica scientifica. 2018; 3(3): 75-81 (in Russian)]. dx.doi.org/10.29413 ABS.2018-3.3.11
16. Gao C.C., Kapoor E., Lipford M.C., Miller V.M., Schroeder D.R., Mara K.C. et al. Association of vasomotor symptoms and sleep apnea risk in midlife women. Menopause. 2017; 25(4): 391-8. dx.doi.org/10.1097 GME.0000000000001020
17. Baber R.J., Panay N., Fenton A. Recommendations on women's midlife health and menopause hormone therapy. Climacteric. 2016; 19(2): 109-50. https:// dx.doi.org/10.3109/13697137.2015.1129166
18. Доброхотова Ю.Э., Ильина И.Ю., Сафарли С.Э. Аномальные маточные кровотечения и кровотечения в постменопаузе на фоне приема менопаузальной гормональной терапии: современные данные. РМЖ. Мать и дитя. 2024; 7(3): 241-7. [Dobrokhotova Yu.E., Ilyina I.Yu., Safarli S.E. Abnormal uterine bleeding and postmenopausal bleeding in women taking menopausal hormone therapy: current data. RMJ. Mother and child. 2024; 7(3): 241-7 (in Russian)]. dx.doi.org/10.32364/2618-8430-2024-7-3-9
19. Tsiligiannis S., Wick-Urban B.C., van der Stam J., Stevenson J.C. Efficacy and safety of a low-dose continuous combined hormone replacement therapy with 0.5 mg 17e-estradiol and 2.5 mg dydrogesterone in subgroups of postmenopausal women with vasomotor symptoms. Maturitas. 2020; 139: 20-6. dx.doi.org/10.1016/j.maturitas.2020.05.002
20. Ампилогова Д.М., Солопова А.Г., Блинов Д.В., Быковщенко Г.К., Хлопкова С.В., Иванов А.Е. Влияние реабилитации на качество жизни пациенток с вульвовагинальной атрофией. Акушерство, гинекология и репродукция. 2024; 18(3): 338-51. [Ampilogova D.M., Solopova A.G., Blinov D.V., Bykovshchenko G.K., Khlopkova S.V., Ivanov A.E. The impact of rehabilitation on the quality of life in patients with vulvovaginal atrophy.
Obstetrics, Gynecology and Reproduction. 2024; 18(3): 338-51 (in Russian)]. dx.doi.org/10.17749/2313-7347/ob.gyn.rep.2024.537
21. Lampio L., Polo-Kantola P., Polo O., Kauko T., Aittokallio J., Saaresranta T. Sleep in midlife women: effects of menopause, vasomotor symptoms, and depressive symptoms. Menopause. 2014; 21(11): 1217-24. dx.doi.org/10.1097/GME.0000000000000239
22. Phillips B.A., Mannino D. Correlates of sleep complaints in adults: the ARIC Study. J. Clin. Sleep Med. 2005; 1(3): 277-83.
23. Тихомиров А.Л., Манухин И.Б., Манухина Е.И., Казенашев В.В. Для кого тиболон? Лечащий врач. 2016; 9: 78-80. [Tikhomirov A.L., Manukhin I.B., Manukhina E.I., Kazenashev V.V. For whom is tibolon? Lvrach.ru. 2016; 9: 78-80 (in Russian)].
24. Gupta B., Mittal P., Khuteta R., Bhargava A. A comparative study of CEE, tibolone, and DHEA as hormone replacement. J. Obstet. Gynecol. India. 2013; 63(3): 194-8. dx.doi.org/10.1007/s13224-012-0297-7
25. Raj R., Sharma N., Garg R., Goyal E. Comparative safety and efficacy of tibolone and escitalopram in postmenopausal women. Ind. Psychiatry J. 2021; 30(1): 140-8. dx.doi.org/10.4103/0972-6748.328805
26. Hsiao S.M., Liao S.C. Effect of tibolone vs hormone replacement therapy on climacteric symptoms and psychological distress. J. Chin. Med. Assoc. 2024; 87(2): 189-95. dx.doi.org/10.1097/JCMA.0000000000001012
Поступила 08.09.2025
Принята в печать 23.09.2025
Сведения об авторах:
Ильина Ирина Юрьевна, д.м.н., профессор кафедры акушерства и гинекологии лечебного факультета, РНИМУ им. Н.И. Пирогова Минздрава России, 117513, Россия, Москва, ул. Островитянова, д. 1, стр. 9, iliyina@mail.ru, orcid.org/0000-0001-8155-8775
Доброхотова Юлия Эдуардовна, д.м.н., профессор, заведующая кафедрой акушерства и гинекологии лечебного факультета, РНИМУ им. Н.И. Пирогова Минздрава России, 117513, Россия, Москва, ул. Островитянова, д. 1, стр. 9, pr.dobrohotova@mail.ru, orcid.org/0000-0002-7830-2290
Нариманова Метанат Рафиг кызы, к.м.н., доцент кафедры акушерства и гинекологии лечебного факультета, РНИМУ им. Н.И. Пирогова Минздрава России, 117513, Россия, Москва, ул. Островитянова, д. 1, стр. 9, orcid.org/0000-0003-0677-2952
THE ROLE OF TIBOLONE IN THE ELIMINATION OF CLIMACTERIC SYNDROME SYMPTOMS
I.Yu. Ilyina, Yu.E. Dobrokhotova, M.R. Narimanova
Pirogov Russian National Research Medical University of the Ministry of Health of Russia, Moscow, Russia
Background: Menopause is characterized by a gradual decline and eventual "turn-off " of ovarian function. Physiological changes in a woman's body are accompanied by the development of neuropsychiatric, vegetovascular, and neuroendocrine symptoms. Menopause is an important period associated with intense hormonal changes that can cause cognitive decline, anxiety and depression, sexual dysfunction, and sleep disturbances.
Objective: To conduct a comparative analysis of the use of various pharmacological drugs for the correction of menopausal symptoms.
Materials and methods: The study was conducted at the Pirogov City Hospital No. 1 during the period of September 2024—June 2025. The study included 62 postmenopausal women that were divided into 3 groups: Group 1 (n=21) — patients who received tibolone (Leatrisa) for 6 months; Group 2 (n=17) — patients who received a drug containing estradiol 1 mg and dydrogesterone 5 mg (E2/DYD); Group 3 (n=24) — postmenopausal women who did not receive menopausal hormontherapy (MHT). In addition to standard research methods, a questionnaire was administered (Greene Menopause Index, Mini-Mental State Examination (MMSE), Hospital Anxiety and Depression Scale (HADS), Female Sexual Distress Scale (FSDS), sleep quality questionnaire).
Results: Tibolone's effect was found to be comparable to that of E2/DYD, a drug recommendedfor use 12 months after menopause, in terms of relieving menopausal symptoms and alleviating their severity. Tibolone is effective in treating sexual dysfunction in postmenopausal women due to its androgenic metabolite. The results of the study showcase that tibolone has no proliferative effect on the endometrium.
Conclusion: Tibolone significantly improves sexual function, reduces anxiety and depression, alleviates menopausal symptoms, and promotes weight stabilization, without causing endometrial proliferative effects. We believe tibolone can be considered an effective therapy for many postmenopausal women.
Keywords: tibolone, menopausal hormone therapy, menopause, climacteric syndrome, sleep disorders, sexual dysfunction, anxiety and depression scale.
Authors’ contribution: Ilyina I.Yu., Dobrokhotova Yu.E., Narimanova M.R. - study concept and design, material collection and processing, manuscript conduction and editing.
Conflicts of interest: The authors declare no conflicts of interest.
Funding: The study had no sponsorship.
Patient Consent for Publication: All patients provided informed consent for the publication of their data.
Authors' Data Sharing Statement: The data supporting the findings of this study are available on request from the corresponding author after approval from the principal investigator.
For citation: Ilina I.Yu., Dobrokhotova Yu.E., Narimanova M.R. The role of tibolone in the elimination of climacteric syndrome symptoms. Akusherstvo i Ginekologiya/Акушерство и гинекология. 2025; (9): (in Russian) dx.doi.org/10.18565/aig.2025.248
Received 08.09.2025
Accepted 23.09.2025
Authors’ information:
Irina Yu. Ilyina, Dr. Med. Sci., Professor, Department of Obstetrics and Gynecology, Faculty of Medicine, Pirogov Russian National Research Medical University, Ministry of Health of Russia, 117513, Russia, Moscow, Ostrovitianov str., 1-9, iliyina@mail.ru, orcid.org/0000-0001-8155-8775
Yulia E. Dobrokhotova, Dr. Med. Sci., Professor, Head of the Department of Obstetrics and Gynecology, Faculty of Medicine, Pirogov Russian National Research Medical
University, Ministry of Health of Russia, 117997, Russia, Moscow, Ostrovityanov str., 1-9, pr.dobrohotova@mail.ru, orcid.org/0000-0002-7830-2290
Metanat R. Narimanova, PhD, Associate Professor at the Department of Obstetrics and Gynecology, Faculty of Medicine, Pirogov Russian National Research Medical University, 117513, Russia, Moscow, Ostrovityanov str., 1-9, orcid.org/0000-0003-0677-2952