Опыт применения тиболона в качестве препарата менопаузальной гормональной терапии
СтатьиИльина И.Ю.1, Доброхотова Ю.Э.2
1 ФГАОУ ВО «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Минздрава России, Москва, Россия;
2 ФГБОУ ВО «Ярославский государственный медицинский университет» Минздрава России, Ярославль, Россия
Актуальность: В настоящее время имеется тенденция к увеличению продолжительности жизни женщин, что формирует потребность в длительном приеме препаратов менопаузальной гормональной терапии (МГТ). Улучшение качества жизни является одним из основных критериев для назначения МГТ. Однако не всегда при назначении препаратов МГТ польза превышает риски при наличии некоторых заболеваний. Поэтому использование МГТ должно быть строго оправдано и индивидуально.
Цель: Изучить клинические, лабораторные и инструментальные показатели у женщин в ранней постменопаузе на фоне приема тиболона.
Материалы и методы: Проведено наблюдательное исследование на базе ГКБ №1 им. Н.И. Пирогова в период с сентября 2024 г. по сентябрь 2025 г., в котором приняла участие 41 женщина в постменопаузе. Участницы принимали препарат МГТ тиболон (Леатриса) в течение 6 месяцев. В ходе исследования анализировали жалобы, проводилось динамическое наблюдение за основными инструментальными и лабораторными показателями через 2 и 6 месяцев.
Результаты: По результатам проводимого исследования было выявлено, что на фоне приема тиболона не отмечается роста эндометрия (3,16 мм в начале исследования, 2,95 мм через 6 месяцев приема тиболона). Аномальное маточное кровотечение наблюдалось кратковременный период у 7,3% пациенток, что не потребовало проведения оперативного вмешательства. При проведении анализа основных показателей (липидный профиль, индекс атерогенности, коагулограмма, D-димер) статистически значимых изменений за время наблюдения получено не было, что указывает на отсутствие отрицательного влияния исследуемого гормонального препарата на липидный профиль, гемостаз. Кроме того, не было выявлено ухудшений со стороны экстрагенитальной патологии, так, у пациенток с гипертонической болезнью не отмечалось повышения цифр артериального давления, что не потребовало коррекции гипотензивной терапии.
Заключение: Данные нашего исследования показали, что тиболон не оказывает пролиферативной активности в отношении эндометрия и молочных желез, не оказывает влияния на рост миоматозных узлов в краткосрочной перспективе, а также при его применении отсутствует отрицательное влияние на липидный профиль, гемостаз. На фоне применения тиболона женщины отметили значительное уменьшение и выраженность климактерических симптомов.
Ключевые слова: тиболон, менопаузальная гормональная терапия, менопауза, климактерический син дром, аномальные маточные кровотечения, мастодиния
Вклад авторов: Ильина И.Ю., Доброхотова Ю.Э. – концепция и дизайн исследования, сбор и обработка материала, написание текста, редактирование.
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Работа выполнена без спонсорской поддержки.
Согласие пациентов на публикацию: Пациенты подписали информированное согласие на публикацию своих данных.
Обмен исследовательскими данными: Данные, подтверждающие выводы этого исследования, доступны по запросу у автора, ответственного за переписку, после одобрения ведущим исследователем.
Для цитирования: Ильина И.Ю., Доброхотова Ю.Э. Опыт применения тиболона в качестве препарата менопаузальной гормональной терапии. Акушерство и гинекология. 2025; 11: 156-162. dx.doi.org/10.18565/aig.2025.328
В современном мире наметилась тенденция к увеличению продолжительности жизни женщин, что привело к необходимости длительного приема препаратов менопаузальной гормональной терапии (МГТ) [1].
Основной задачей назначения МГТ у женщин является восполнение дефицита половых гормонов. Принципы назначения препаратов МГТ заключаются в использовании минимальных, но эффективных доз, направленных на улучшение самочувствия пациенток, уменьшение проявлений климактерического синдрома, профилактику обменных нарушений, проявляющихся в более позднем периоде [2]. Также препараты рассматриваются у пациенток группы высокого риска по остеопорозу и низкотравматичным переломам в качестве профилактики развития данных заболеваний.
Наиболее оптимальными периодами назначения препаратов МГТ являются возраст до 60 лет и длительность постменопаузального периода менее 10 лет. Дозы и продолжительность приема МГТ играют большую роль. Грамотный анализ соотношения пользы и рисков МГТ при назначении и в процессе динамического наблюдения в ходе проводимого лечения позволяет обеспечить максимальную безопасность назначения препаратов МГТ [3].
История назначения препаратов МГТ включает период, когда применение МГТ было поставлено под сомнение из-за опасений в отношении сердечно-сосудистых и цереброваскулярных рисков, а также рака молочной железы. Данные суждения возникли после опубликованных результатов крупного рандомизированного плацебо-контролируемого исследования. Однако более расширенные исследования с продолжительным периодом наблюдения, а также другие, более современные клинические испытания предоставили новые результаты, указывающие на эффективность препаратов МГТ. На сегодняшний день известно, что гормональная терапия облегчает имеющиеся симптомы, способствует снижению риска сердечно-сосудистых заболеваний, увеличению минеральной плотности костной ткани и снижению риска переломов костей [3–6].
По данным многочисленных исследований, своевременное начало приема препаратов МГТ приходится на период перименопаузы или первые 5 лет постменопаузы и в данном случае снижает риск развития субклинического атеросклероза, ишемической болезни сердца и когнитивных нарушений (при условии нормальной когнитивной функции на момент старта МГТ) [2, 7]. Кроме того, известно, что МГТ положительно влияет на липидный профиль у женщин в пери- и постменопаузе. Также известно, что своевременное начало приема МГТ может снизить риск развития сахарного диабета 2 типа на 30% [2, 7].
Одним из основных критериев для назначения препаратов МГТ является улучшение качества жизни. Однако не всегда при назначении данных препаратов польза превышает риски, особенно при наличии некоторых заболеваний. Поэтому использование МГТ должно быть строго оправдано и индивидуально [8, 9].
На сегодняшний день свою эффективность доказал препарат, относящийся к тканеселективному регулятору эстрогеновых рецепторов. Тиболон (7α-метилнорэтинодрел) является эффективным и безопасным препаратом для назначения пациенткам в постменопаузе. После приема внутрь препарат метаболизируется в печени и тонком кишечнике, в результате образуются биологически активные метаболиты с эстрогенными, прогестагенными и андрогенными свойствами (3α- и 3β-гидроксиметаболиты связываются с рецепторами эстрогенов, а 4-Δ-изомер – преимущественно с андрогенными и гестагенными рецепторами) [2, 10–12].
Известно, что на фоне применения тиболона в постменопаузе отмечаются эффективное устранение вазомоторных симптомов, проявлений генитоуринарного менопаузального синдрома (ГУМС), повышение минеральной плотности костной ткани, наблюдаются положительные эффекты в отношении сердечно-сосудистой и центральной нервной систем. Также известно, что применение тиболона значительно улучшает сексуальную функцию, снижает тревожность и депрессию, облегчает симптомы менопаузы, улучшает сон, способствует стабилизации веса, при этом отсутствует пролиферативное влияние на эндометрий [13]. Таким образом, тиболон обладает избирательной эстрогенной активностью и регулирует действие в различных тканях, что делает его уникальным представителем класса STEAR [11]. То есть тиболон рассматривается в качестве эффективной терапии для многих женщин в постменопаузе. При решении вопроса о назначении тиболона необходимо учитывать ряд особенностей его действия и, исходя из этого, определять возможность назначения данной терапии для пациентки в индивидуальном порядке [11, 14].
Учитывая все вышеизложенное, цель нашего исследования: изучить клинические, лабораторные и инструментальные показатели у женщин в ранней постменопаузе на фоне приема тиболона.
Материалы и методы
Было проведено наблюдательное исследование на базе ГКБ №1 им. Н.И. Пирогова в период с сентября 2024 г. по сентябрь 2025 г. [14]. Все пациентки, принимающие участие в исследовании, подписали информированное добровольное согласие.
В исследовании приняла участие 41 пациентка в постменопаузе от +1а до +1с стадии в соответствии с критериями классификации репродуктивного старения STRAW+10, то есть женщины, у которых отсутствовали менструации от 1 до 3 лет. Критериями включения также были: наличие менопаузальных симптомов, отсутствие абсолютных противопоказаний к назначению МГТ, отсутствие тяжелой экстрагенитальной патологии, готовность принять участие в исследовании.
В рамках исследования проводились анкетирование, детальный сбор анамнеза, физикальный осмотр (измерение веса, индекса массы тела (ИМТ)), гинекологическое обследование, инструментальные исследования (ультразвуковое исследование (УЗИ) органов малого таза, маммография), лабораторные исследования (липидный профиль, индекс атерогенности (общий холестерин-ЛПВП/ЛПНП), коагулограмма, D-димер).
При проведении анкетирования использовали шкалу Грина для оценки степени выраженности климактерического синдрома, которая рассчитывается по количеству баллов: 1–11 баллов – слабая степень выраженности, 12–19 – средняя, 20 и выше – тяжелая [2, 14].
Точки контроля за результатами были обозначены в начале исследования, через 2 месяца наблюдений и 6 месяцев.
Критериями исключения из исследования были наличие побочных эффектов в ходе проводимой работы, отказ пациентки от участия в исследовании [14].
Статистический анализ
Статистический анализ проводился с использованием программы StatTech v. 4.9.4 (ООО «Статтех», Россия). Количественные показатели оценивались на предмет соответствия нормальному распределению с помощью критерия Шапиро–Уилка. Количественные показатели, выборочное распределение которых соответствовало нормальному, описывались с помощью средних арифметических величин (M) и стандартных отклонений (SD). В качестве меры репрезентативности для средних значений указывались границы 95% доверительного интервала (95% ДИ). В случае отсутствия нормального распределения количественные данные описывались с помощью медианы (Me) и нижнего и верхнего квартилей (Q1–Q3). Для сравнения трех и более связанных групп по нормально распределенному количественному признаку применялся однофакторный дисперсионный анализ с повторными измерениями. При сравнении трех и более зависимых совокупностей, распределение которых отличалось от нормального, использовался непараметрический критерий Фридмана с апостериорными сравнениями с помощью критерия Коновера–Имана с поправкой Холма. Различия считались статистически значимыми при p<0,05.
Результаты
По результатам сбора анамнеза, гинекологического осмотра, проведения инструментального и лабораторного обследования были получены следующие результаты.
Средний возраст наблюдаемых женщин составил 50,0 года (Q1–Q3: 49–52 года), вес – 76 кг (Q1–Q3: 65–85 кг), ИМТ – 27,5 (3,7) кг/м². Средний период после менопаузы составил 25 месяцев (Q1; Q3; 16–30 месяцев).
При определении степени тяжести климактерического синдрома оказалось, что средний балл был равен 44,6 (7,21). Надо отметить, что у всех пациенток отмечалось тяжелое течение климактерического синдрома. Инструментальные и лабораторные данные представлены в таблице 1.

У 14/41 пациенток (34,1%) при проведении УЗИ органов малого таза была обнаружена миома матки 3–6 типов по FIGO размерами от 15 до 30 мм, что не явилось критерием исключения из исследования.
Из экстрагенитальной патологии у 8/41 пациенток (19,5%) отмечалось варикозное расширение вен нижних конечностей; у 12/41 женщин (29,3%) – гипертоническая болезнь, по поводу чего пациентки принимали гипотензивную терапию. На момент начала исследования цифры артериального давления были в пределах референсных значений. У 3/41 пациенток (7,3%) наблюдались субклинический гипотиреоз, медикаментозный эутиреоз. Все вышеперечисленные заболевания не являются противопоказанием для назначения препаратов МГТ.
Также пациенткам в начале исследования проводили УЗИ молочных желез и маммографию. По результатам обследования у 6/41 пациенток (14,6%) были выявлены признаки кистозно-фиброзной мастопатии, что также не является противопоказанием для назначения препаратов МГТ.
Пациенткам был назначен тиболон (препарат «Леатриса»). В ходе наблюдения мы проводили сравнительный анализ основных показателей через 2 и 6 месяцев. Надо отметить, что в ходе исследования ни одна пациентка не выбыла из исследования по причине отказа от приема препарата. Были получены следующие данные.
На фоне приема тиболона уже через 2 месяца отмечалось статистически значимое уменьшение количества баллов по шкале Грина, характеризующих выраженность климактерического синдрома. Через 6 месяцев также отмечалось статистически значимое уменьшение количества баллов, и у 15/41 (36,6%) пациенток проявления климактерического синдрома из разряда «тяжелая степень» перешли в среднюю степень (табл. 2, рис. 1).

При динамическом наблюдении за весом пациенток на фоне приема тиболона были получены результаты, представленные в таблице 3.
Отмечалось хоть и не столь значительное, но статистически значимое снижение веса через 6 месяцев от начала приема препарата.
При проведении УЗИ органов малого таза через 2 и 6 месяцев наблюдения за пациентками увеличения миоматозных узлов отмечено не было, также не отмечалось изменений в сторону усиления кровотока при проведении допплерометрии, что позволило данной категории пациенток продолжить прием препарата в дальнейшем.
При измерении М-эхо в динамике были получены результаты, указывающие на отсутствие его увеличения в ходе приема тиболона. До начала исследования величина М-эхо составляла 3,16 (0,62) мм (95% ДИ 2,96–3,36), через 2 месяца применения тиболона – 3,06 (0,6) мм (95% ДИ 2,87–3,25), через 6 месяцев М-эхо было равно 2,95 (0,46) мм (95% ДИ 2,81–3,1) (рис. 1).
Следует упомянуть, что 3/41 (7,3%) пациентки в первые 2 месяца отмечали скудные кровяные выделения из половых путей. С учетом отсутствия патологии по данным УЗИ органов малого таза прием тиболона был продолжен. Спустя 5–10 дней выделения прекратились и больше не возобновлялись.
При проведении сравнительного анализа изменения индекса атерогенности были получены результаты, представленные на рисунке 3, указывающие на его статистически значимое уменьшение через 6 месяцев приема тиболона.
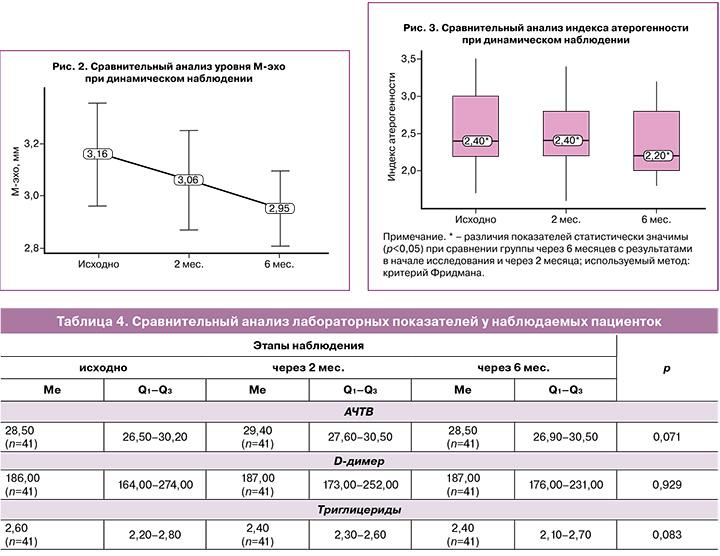
При проведении сравнительного анализа результатов АЧТВ, D-димера, триглицеридов статистически значимых изменений на фоне приема тиболона в течение 6 месяцев получено не было (табл. 4).
Надо отметить, что ухудшений со стороны экстрагенитальной патологии не наблюдалось. У пациенток с гипертонической болезнью не отмечалось повышения цифр артериального давления, что не потребовало коррекции гипотензивной терапии.
При повторном проведении УЗИ молочных желез через 6 месяцев приема тиболона дополнительной патологии выявлено не было. 2/41 (4,9%) пациенткам было проведено дополнительное УЗИ молочных желез через 1–2 месяца от начала приема препарата МГТ в связи с жалобами на нагрубание молочных желез. При обследовании патологии обнаружено не было. Жалобы спонтанно исчезли через 2–3 месяца приема препарата. Наличие данных жалоб не явилось поводом для отказа от приема данного препарата.
Обсуждение
Период менопаузы сопровождается комплексом физиологических изменений в организме женщины, связанных с прекращением овуляции, снижением выработки половых гормонов. Это естественный биологический процесс, который, однако, сопровождается развитием нейропсихических, вегетативно-сосудистых, нейроэндокринных симптомов, приводящих к возможному развитию других заболеваний, увеличивающих летальность, а также данные изменения могут значительно влиять на качество жизни пациентки [2, 10, 15, 16].
При выборе препарата МГТ с целью купирования симптомов климактерического синдрома должны учитываться не только его эффективность в устранении данных симптомов, но и безопасность.
Действие тиболона в отношении исчезновения симптомов климактерического синдрома, облегчения его степени тяжести сопоставимо с действием препарата, содержащего 1 мг эстрадиола в сочетании с 5 мг дидрогестерона (E2/DYD), который рекомендован к применению пациенткам через 12 месяцев после наступления менопаузы [2].
Аномальные маточные кровотечения в постменопаузе на фоне применения препаратов МГТ являются одной из частых жалоб. Эти эпизоды кровотечений являются одной из основных причин отказа пациенток от проводимого гормонального лечения и требуют дополнительного обследования для исключения гиперплазии эндометрия и других структурных нарушений [17–19].
Прорывные кровотечения на фоне применения тиболона возникают реже, чем при комбинированной гормональной терапии [20]. Hammar M.L. et al. [21] продемонстрировали меньшую частоту аномальных маточных кровотечений на фоне приема тиболона в течение 7–9 и 10–12 месяцев (11,4% и 10,0%) по сравнению с применением низких дозировок 17β-эстрадиола (E2)/норэтистерона ацетата (E2/NETA) (19,9% и 13,8% соответственно). Похожие результаты продемонстрировал систематический обзор Formoso G. et al. [19], указывающий на то, что тиболон ассоциирован с меньшим количеством прорывных кровотечений по сравнению с препаратами комбинированной гормональной терапии.
В нашем исследовании вышеописанные результаты нашли подтверждение. Так, лишь 7,3% пациенток в первые 2 месяца отмечали скудные кровяные выделения из половых путей, которые спустя короткое время прекратились и более не возобновлялись. Данная ситуация не потребовала проведения оперативного лечения и отказа от приема препарата.
Также в ходе исследования не было выявлено влияния приема тиболона на изменение размеров миоматозных узлов, что подтверждает данные, представленные в источниках литературы [2, 22, 23].
Известно, что в 41,2% случаев через 2 месяца приема E2/DYD появляются жалобы на мастодинию, которая сохраняется у 23,5% пациенток до 6 месяцев приема данного препарата [14]. В нашем исследовании только 2 пациентки (4,9%) предъявляли жалобы на нагрубание молочных желез, что потребовало дополнительного проведения УЗИ молочных желез через 1–2 месяца от начала приема препарата МГТ. При обследовании патологии обнаружено не было. Жалобы спонтанно исчезли через 2–3 месяца приема препарата [14].
Надо отметить, что при проведении анализа основных показателей (липидный профиль, индекс атерогенности, коагулограмма, D-димер) статистически значимых изменений за время наблюдения получено не было, что указывает на отсутствие отрицательного влияния исследуемого гормонального препарата на липидный профиль, гемостаз, что было подтверждено в результате других исследований [2, 14]. Кроме того, в нашем исследовании не отмечалось ухудшений со стороны экстрагенитальной патологии. У пациенток с гипертонической болезнью не отмечалось повышения цифр артериального давления, что не потребовало коррекции гипотензивной терапии.
Заключение
Данные нашего исследования показали, что тиболон не оказывает пролиферативной активности в отношении эндометрия и молочных желез, не оказывает влияния на рост миоматозных узлов, а также при его применении отсутствует отрицательное влияние на липидный профиль, гемостаз. На фоне применения тиболона женщины отметили значительное уменьшение и выраженность климактерических симптомов.
Список литературы
- Балан В.Е., Тихомирова Е.В., Зайдиева Я.З., Кручинина Е.В., Журавель А.С., Титченко Ю.П., Фомина-Нилова О.С., Царькова А.В. Меняющееся лицо менопаузальной гормональной терапии. Российский вестник акушера-гинеколога. 2020; 20(4): 95-9.
- Министерство здравоохранения Российской Федерации. Клинические рекомендации. Менопауза и климактерическое состояние у женщин. М.; 2025. 93 с.
- Якушевская О.В., Юренева С.В. Роль менопаузальной гормональной терапии в профилактике остеопороза. Остеопороз и остеопатии. 2022; 25(3): 139-40.
- Иловайская И.А. Менопаузальная гормональная терапия и риски сердечно-сосудистых заболеваний: современный взгляд. Гинекология. 2018; 20(4): 40-3.
- Шабалова О.В., Юренева С.В., Ермакова Е.И., Хохлова С.В., Гарданова Ж.Р., Якушевская О.В. Хирургическая менопауза как фактор риска раннего развития коморбидных состояний у женщин репродуктивного возраста. Акушерство и гинекология. 2021; 6: 54-9.
- Шляхто Е.В., Сухих Г.Т., Серов В.Н., Дедов И.И., Арутюнов Г.П., Сучков И.А. Российские критерии приемлемости назначения менопаузальной гормональной терапии пациенткам с сердечно-сосудистыми и метаболическими заболеваниями. Согласительный документ Российского кардиологического общества, Российского общества акушеров-гинекологов, Российской ассоциации эндокринологов, Евразийской ассоциации терапевтов, ассоциации флебологов России. Акушерство и гинекология. 2023; 11: 211-32.
- Miller V.M., Naftolin F., Asthana S., Black D.M., Brinton E.A., Budoff M.J. et al. The kronos early estrogen prevention study (KEEPS): what have we learned? Menopause. 2019; 26(9): 1071-84. dx.doi.org/10.1097 GME.0000000000001326
- Сушкевич А.С. Менопаузальная гормональная терапия – стоит ли? Молодой ученый. 2020; 4(294): 209-11.
- Genazzani A.R., Monteleone P., Giannini A., Simoncini T. Hormone therapy in the postmenopausal years: considering benefits and risks in clinical practice. Hum. Reprod. Update. 2021; 27(6): 1115-50. dx.doi.org/10.1093 /humupd/dmab026
- Кузнецова И.В. Выбор между гормональной и альтернативной терапией в периоде менопаузального перехода и постменопаузе. РМЖ. Мать и дитя. 2018; 26(1-2): 43-7.
- Ярмолинская М.И., Колошкина А.В. Возможности тканеселективной эстрогенной регуляции у пациенток в постменопаузе. Акушерство и гинекология. 2024; 5: 32-43.
- Балан В.Е., Юренева С.В., Сметник В.П., Ильина Л.М. Кардиометаболические расстройства у женщин в постменопаузе: негативная роль андрогенов с позиций доказательной медицины. Проблемы репродукции. 2013; 3: 77-85.
- Ампилогова Д.М., Солопова А.Г., Блинов Д.В., Быковщенко Г.К., Хлопкова С.В., Иванов А.Е. Влияние реабилитации на качество жизни пациенток с вульвовагинальной атрофией. Акушерство, гинекология и репродукция. 2024; 18(3): 338-51.
- Ильина И.Ю., Доброхотова Ю.Э., Нариманова М.Р. Роль тиболона в устранении симптомов климактерического синдрома. Акушерство и гинекология. 2025; 9: 160-7.
- Wend K., Wend P., Krum S.A. Tissue-specifc effects of loss of estrogen during menopause and aging. Front. Endocrinol. (Lausanne). 2012; 3: 1-14. dx.doi.org/10.3389/fendo.2012.00019
- Hsiao S.M., Liao S.C. Effect of tibolone vs hormone replacement therapy on climacteric symptoms and psychological distress. J. Chin. Med. Assoc. 2024; 87(2): 189-95. dx.doi.org/10.1097/JCMA.0000000000001012
- Доброхотова Ю.Э., Сафарли С.Э., Нариманова М.Р., Ильина И.Ю., Казиева М.Д. Цитокиновый профиль эндометрия при аномальных маточных кровотечениях у уженщин на менопаузальной гормональной терапии: данные по интерлейкинам-2, -6 и -15. Лечащий врач. 2025; 28(7-8): 64-71.
- Hamdaoui N., Boubli L. La gestion des effets secondaires sous traitement hormonal de la ménopause : saignements utérins anormaux. RPC Les femmes ménopausées du CNGOF et du GEMVi.
- Доброхотова Ю.Э., Ильина И.Ю., Сафарли С.Э. Аномальные маточные кровотечения и кровотечения в постменопаузе на фоне приема менопаузальной гормональной терапии: современные данные. РМЖ. Мать и дитя. 2024; 7(3): 241-7.
- Lee S.R., Cho M.K., Cho Y.J., Chun S., Hong S.H., Hwang K.R. et al. The 2020 menopausal hormone therapy guidelines. J. Menopausal Med. 2020; 26(2): 69-98. dx.doi.org/10.6118/jmm.20000
- Hammar M.L., van de Weijer P., Franke H.R., Pornel B., von Mauw E.M., Nijland E.A. Tibolone and low dose continuous combined hormone treatment: vaginal bleeding pattern, efficacy and tolerability. BJOG. 2007; 114(12): 1522-9. dx.doi.org/10.1111/j.1471 0528.2007.01537.x
- Formoso G., Perrone E., Maltoni S., Balduzzi S., Wilkinson J., Basevi V. et al. Short-term and long-term effects of tibolone in postmenopausal women. Cochrane database Syst. Rev. 2016; 10(10): CD008536. dx.doi.org/10.1002/14651858.CD008536.pub3
- Sarri G., Pedder H., Dias S., Guo Y., Lumsden M.A. Vasomotor symptoms resulting from natural menopause: a systematic review and network meta-analysis of treatment effects from the National institute for health and care excellence guideline on menopause. BJOG. 2017; 124(10): 1514-23. dx.doi.org/10.1111/1471-0528.14619
Поступила 12.11.2025
Принята в печать 27.11.2025
Об авторах / Для корреспонденции
Ильина Ирина Юрьевна, д.м.н., профессор кафедры акушерства и гинекологии института хирургии, РНИМУ им. Н.И. Пирогова Минздрава России,
117513, Россия, Москва, ул. Островитянова, д. 1, стр. 9; профессор кафедры акушерства, гинекологии и репродуктивной медицины, ЯГМУ Минздрава России,
150000, Россия, Ярославль, ул. Революционная, д. 5, iliyina@mail.ru, orcid.org/0000-0001-8155-8775
Доброхотова Юлия Эдуардовна, д.м.н., профессор, заведующая кафедрой акушерства и гинекологии института хирургии, РНИМУ им. Н.И. Пирогова Минздрава России, 117513, Россия, Москва, ул. Островитянова, д. 1, стр. 9, pr.dobrohotova@mail.ru, orcid.org/0000-0002-7830-2290