Оценка эффективности хемолитической терапии при лечении коралловидного уратного нефролитиаза.
СтатьиВ.А. Малхасян1,2, Х.У. Тунгузбаев1, С.А. Пульбере3, А.Р. Геворкян4, С.О. Сухих2, Н.К. Гаджиев5, Д.Ю. Пушкарь1,2
1ФГБОУ ВО «Российский университет медицины» Минздрава России, Москва, Россия; 2ГБУЗ «Московский многопрофильный научно-клинический центр им. С.П. Боткина» ДЗМ, Москва, Россия; 3ГБУЗ «Городская клиническая больница № 1 им. Н.И. Пирогова», ДЗМ, Москва, Россия; 4ГБУЗ «Городская поликлиника № 212» ДЗМ, Москва, Россия; 5ФГБОУ ВО «Санкт-Петербургский государственный университет», Клиника высоких медицинских технологий им. Н.И. Пирогова, Санкт-Петербург, Россия
Автор для связи: В.А. Малхасян — д.м.н., профессор кафедры урологии ФГБОУ ВО «РосУниМед», Москва, Российская Федерация; заведующий урологическим отделением № 67, ГБУЗ «ММНКЦ им. С.П. Боткина» ДЗМ, Москва, Россия; e-mail: vigenmalkhasyan@gmail.com
Введение. Уратный коралловидный нефролитиаз представляет собой одну из наиболее сложных форм мочекаменной болезни, а подходы к его лечению продолжают вызывать активные обсуждения и остаются открытым вопросом среди специалистов.
Цель исследования. Оценить эффективность и безопасность хемолитической терапии коралловидного уратного нефролитиаза цитратными смесями.
Материалы и методы. С января 2023 г. по октябрь 2024 г. было проведено проспективное когортное мультицентровое исследование с участием пациентов с диагностированными, по данным компьютерной томографии, коралловидными конкрементами (К2—К4) и предположительным уратным составом камня (средние значения pH мочи ≤5,8, средняя плотность конкремента ≤650 HU, рентгеннегативность камня на обзорной урограмме или топограмме), которые получали пероральную хемолитическую терапию цитратной смесью, состоящей из лимонной кислоты, калия бикарбоната, натрия цитрата («Блемарен»). Набор пациентов осуществлялся из поликлиник и стационаров Москвы.
Результаты исследования. Из 49 пациентов, включенных в исследование, в течение первых двух месяцев были исключены два пациента. В результате у 30 (63,8%) пациентов констатировали полное растворение камня, 17 (36,2%) пациентам выполнено хирургическое удаление камня. В четырех (8,5%) наблюдениях для полного растворения конкремента понадобился один месяц терапии, в 18 (38%) — три месяца, а в восьми (17%) — шесть месяцев. Среди удаленных камней 12 (70,6%) были кальций-оксалатными, пять (29,4%) — уратными. Соответственно, доля пациентов с некальций-оксалатными камнями, у которых не удалось добиться полного растворения камней, составила 14,3%. Единственным параметром, который статистически значимо влиял на вероятность растворения камня, а также на риск оперативного вмешательства, была плотность камня (р<0,05). Согласно данным регрессионного анализа, при увеличении плотности камня на одну единицу шанс растворения камня снижается в 1,012 раза, а риск операции увеличивается в 1,008раза.
Заключение. Хемолитическая терапия уратного коралловидного нефролитиаза цитратными смесями является эффективным и безопасным методом лечения, позволяющим избежать оперативного лечения большинству пациентов. Данный метод может использоваться в качестве альтернативы оперативному лечению, уменьшая сопряженные риски как анестезиологического пособия, так и вмешательства.
Ключевые слова: мочекаменная болезнь, уратный коралловидный нефролитиаз, литолитическая терапия, цитратные смеси
Авторы заявляют об отсутствии конфликта интересов.
Для цитирования: Малхасян В.А., Тунгузбаев Х.У., Пульбере С.А., Геворкян А.Р., Сухих С.О., Гаджиев Н.К., Пушкарь Д.Ю. Оценка эффективности хемолитической терапии при лечении коралловидного уратного нефролитиаза. Урология. 2024;6:17-23.
Doi: https://dx.doi.org/10.18565/urology.2024.6.17-23
Введение. Мочекаменная болезнь (МКБ, нефролитиаз) — одно из наиболее распространенных урологических заболеваний, частота которого варьируется от 7 до 13% в Северной Америке, от 5 до 9% в Европе и от 1 до 5% в Азии [1]. Несмотря на снижение количества случаев МКБ в 2020 г. по сравнению с предыдущими годами, данный показатель в Российской Федерации остается на высоком уровне и составляет 790 330 случаев [2]. Камни, состоящие из мочевой кислоты, выявляются в 10% всех случаев МКБ в США и в 5-40% случаев МКБ в мире [3-5]. Заболеваемость МКБ также несет значительное экономическое бремя. В США ежегодные затраты на лечение всех форм нефролитиаза увеличились с 1,3 млрд долл. в 1994 г. до 2 млрд долл. в 2000 г. [3, 6]. Мочекаменная болезнь оказывает значительное влияние на качество жизни даже у тех пациентов, кто не испытывает выраженных симптомов [7]. По данным различных авторов, уратный нефролитиаз составляет от 10 до 15% всех случаев
МКБ и чаще встречается у мужчин в возрасте от 60 до 65 лет [8]. Типичные факторы риска формирования уратных камней включают ожирение, гипергликемию, метаболический синдром и артериальную гипертензию [9]. Ранее считалось, что бессимптомные коралловидные конкременты относительно безопасны, однако более поздние исследования показали, что около 30% пациентов, получавших только консервативное лечение, в итоге умерли от сепсиса или почечной недостаточности. Общая 15-летняя выживаемость при отсутствии лечения коралловидных камней составляет примерно 41%. Хроническое воспаление, вызванное такими камнями, в редких случаях может привести к плоскоклеточному раку почечной лоханки [10, 11]. Хирургическое лечение коралловидных камней, хотя и эффективно, сопряжено с высоким риском осложнений и рецидивов [12, 13]. Несмотря на обнадеживающие данные последних исследований, свидетельствующие о высокой эффективности перорального хемолиза, которая достигает 61—88%, исследования, оценивающие результаты хемолиза коралловидных конкрементов, в современной литературе практически отсутствуют [14, 15]. Данное обстоятельство подчеркивает актуальность подобных исследований.
Цель исследования: оценить эффективность и безопасность хемолитической терапии коралловидного уратного нефролитиаза цитратными смесями.
Материалы и методы. В период с января 2023 г. по октябрь 2024 г. проведено проспективное когортное мультицентровое исследование, в которое включены пациенты с диагностированными коралловидным нефролитиазом. Набор пациентов осуществлялся из поликлиник и стационаров Москвы. Исследование одобрено межвузовским комитетом по этике (МКЭ) (протокол № 7 от 24 января 2023 г.). Исследование зарегистрировано в ClinicalTrials.gov 22.01.2023.
Критерии включения:
• коралловидный конкремент, занимающий одну или более чашечек и лоханку (К2—К4 по классификации коралловидных конкрементов) [16];
• предположительно уратный состав камня, подтвержденный следующими критериями:
- отсутствие тени конкремента на рентгенограмме/топо-грамме,
- среднее значения pH мочи <5,8 по результатам 72-часового мониторинга,
- средняя плотность конкремента <650 единиц Хаунсфилда (HU),
- отсутствие мочеточникового стента и/или нефростомического дренажа,
- отсутствие признаков обструкции мочеточника на МСКТ с контрастным усилением,
- информированное согласие пациента на участие в исследовании.
Критерии невключения:
• множественные камни;
• двухсторонний нефролитиаз;
• хроническая болезнь почек 4-5 стадии;
• эрозивно-язвенные заболевания ЖКТ в стадии обострения;
• наличие острой инфекции мочевыводящих путей;
• камни единственной почки или нефункционирующая контралатеральная почка;
• камни нефункционирующей почки;
• противопоказания к применению цитратных смесей;
• наличие мочеточникового стента и/или нефростомического дренажа;
• признаки обструкции мочеточника на МСКТ с контрастным усилением;
• камни мочеточника.
У всех пациентов фиксировали антропометрические показатели (рост и масса тела), рассчитывали индекс массы тела (ИМТ). Всем пациентам была выполнена мультиспиральная компьютерная томография (МСКТ) мочевыводящих путей с контрастным усилением для оценки объема и плотности конкрементов до начала терапии, а также оценки проходимости мочеточников и функции почек. Биохимический анализ крови включал в себя определение уровня креатинина крови с последующим расчетом скорости клубочковой фильтрации (СКФ). Мониторинг pH мочи проводили в течение 72 ч при помощи электронного pH-метра до начала терапии. На основании полученных данных, которые пациенты фиксировали в дневнике трижды в день, рассчитывали средний показатель pH. Пациентов, соответствующих критериям включения, после подписания информированного согласия включали в исследование. Пациентам назначали пероральную литолитическую терапию цитратной смесью, состоящей из лимонной кислоты, калия бикарбоната, натрия цитрата (препарат «Блемарен»). Дозировку подбирали индивидуально для каждого пациента, целевым показателем pH считали значение 7,2.
Спустя один месяц от начала терапии пациентам выполняли контрольную нативную МСКТ для оценки эффективности лечения. Главным критерием эффективности был показатель редукции объема конкремента. При фиксации положительной динамики в виде растворения камня регистрировали результат. При фиксации положительной динамики в виде редукции объема камня более чем на 10% от исходного терапию продлевали еще на два месяца. При отсутствии динамики терапию прекращали, а пациенту предлагали оперативное лечение. Спустя три месяца от начала терапии пациентам, продолжавшим получать лечение, выполняли контрольную нативную МСКТ для оценки динамики. При фиксации положительной динамики в виде растворения регистрировали результат. При фиксации положительной динамики в виде редукции объема камня более чем на 20% от исходного терапию продлевали еще на три месяца. При отсутствии динамики терапию прекращали, а пациенту предлагали оперативное лечение. У всех пациентов, подвергшихся оперативному лечению, фиксировали метод оперативного вмешательства и выполняли анализ химического состава камня. Спустя шесть месяцев от начала терапии пациентам, продолжавшим получать лечение, выполняли контрольную нативную МСКТ для оценки динамики, после чего фиксировали результаты: факт растворения камня, объем редукции камня, факт выполнения оперативного лечения, вид выполненного оперативного вмешательства и химический состав камня. После получения данных рассчитывали показатель достижения полного и/или частичного растворения камня, а также оценивали динамику редукции объема камня. Также проводили оценку связи растворения камня и риска оперативного лечения с такими показателями, как пол, возраст, ИМТ, СКФ, pH, плотность и объем камня.
Методы статистической обработки данных. При анализе количественных данных проведено предварительное тестирование переменных на нормальность распределения с помощью теста Шапиро-Уилка. В случае нормального распределения параметр представляли в виде среднего и стандартного отклонения (mean±std), при отклонении от нормального распределения - в виде медианы и нижнего и верхнего квартилей (Me [Q1; Q3]).
Для моделирования вероятности растворения камня за весь период терапии, а также анализа параметров, влияющих на эту вероятность, использована модель многофакторной логистической регрессии. Для оценки качества модели проведен ROC-анализ.
Временной анализ растворения камня проведен с помощью метода Каплана-Майера по визитам наблюдения один, три и шесть месяцев. Оценка построена с цензурированием по пациентам, которым была проведена операция. Анализ риска оперативного лечения проводили с помощью регрессии Кокса для модели пропорциональных рисков.
Результаты. В исследование включены 49 пациентов, среди которых было 23 (46,9 %) мужчины и 26 (53,1 %) женщин. Возраст пациентов составил 63 [55; 71] года.
Уровень креатинина - 98 (92; 103) мкмоль/л. Скорость клубочковой фильтрации - 64 [54; 69] мл/мин. Индекс массы тела - 31,6 [29,4; 34,9] кг/м2. Значение pH мочи - 5,6 [5,4; 5,6]. Плотность камня - 520,63±88,64 HU. Объем камня до начала терапии - 13 [7; 16,72] см3.
В течение первого месяца два пациента были исключены из исследования по причинам, связанным с развитием побочных и нежелательных эффектов терапии: один пациент - из-за эпизодов неконтролируемого повышения артериального давления, второй - по причине развития эпизодов почечных колик, потребовавших хирургического лечения. Исследование закончили 47 пациентов. На момент окончания исследования 30 (63,8%, 95% ДИ 48,577,3%) пациентам удалось полностью растворить камни, тогда как 17 (36,2%, 95% ДИ 22,7-51,5%) была выполнена операция. Спустя один месяц терапии полное растворение камня зафиксировано у четырех (8,5%) пациентов, спустя три месяца - у 18 (38%), спустя шесть месяцев - у восьми (17%) пациентов.
Плотность камней у пациентов, у которых камни растворились, составила 500,13±80,56 HU. Средняя плотность камней у пациентов, у которых камни не растворились, составила 565,71±89,82 HU.
Среди 17 пациентов, которым потребовалось хирургическое удаление камней, трем (17,5%) пациентам была выполнена перкутанная нефролитотомия, а 14 (82,5%) пациентам камень был удален посредством ретроградной интраренальной хирургии. Среди удаленных камней 12 (70,6%) были кальций-оксалатными, а пять (29,4%) уратными.
Субгрупповой анализ. После исключения пациентов с кальций-оксалатными камнями доля пациентов с камнями предположительно уратной природы, у которых не удалось добиться полного растворения камней, составила 14,3%.
Среди пациентов, потребовавших оперативного лечения, у трех (6,4%) наблюдалось снижение объема камня на протяжении всей терапии, однако на момент окончания исследования полного растворения камня достигнуто не было. У двоих из этих пациентов камни имели кальций-оксалатную природу.
Таблица 1. Модель логистической регрессии
|
Параметр |
Эффективность терапии |
р -значение |
ОШ |
2,5% граница 95% ДИ |
97,5% граница 95% ДИ |
|
Пол (М) |
-1,781 |
0,311 |
0,169 |
0,003 |
4,352 |
|
Возраст |
0,024 |
0,66 |
1,024 |
0,921 |
1,156 |
|
Индекс массы тела |
-0,033 |
0,617 |
0,968 |
0,837 |
1,095 |
|
Скорость клубочковой фильтрации |
0,027 |
0,756 |
1,028 |
0,87 |
1,266 |
|
Значение pH мочи |
-1,284 |
0,434 |
0,277 |
0,008 |
6,034 |
|
Плотность камня |
-0,012 |
0,039 |
0,988 |
0,976 |
0,998 |
|
Средний объем камня |
-0,109 |
0,126 |
0,897 |
0,77 |
1,027 |
Регрессионный анализ. Для модели логистической регрессии в качестве независимых переменных были выбраны такие характеристики, как пол, возраст, ИМТ, СКФ, значение pH мочи, а также плотность и объем камня (табл. 1). Единственным параметром, который статистически значимо влиял на вероятность растворения камня, была плотность камня (р=0,039). Согласно данным регрессионного анализа шанс растворения камня снижается в 1,012 [1,002; 1,025] раза при увеличении плотности камня на одну единицу. AUC для ROC-кривой данной модели логистической регрессии составила 0,81, что говорит о хорошем качестве модели (рис. 1).
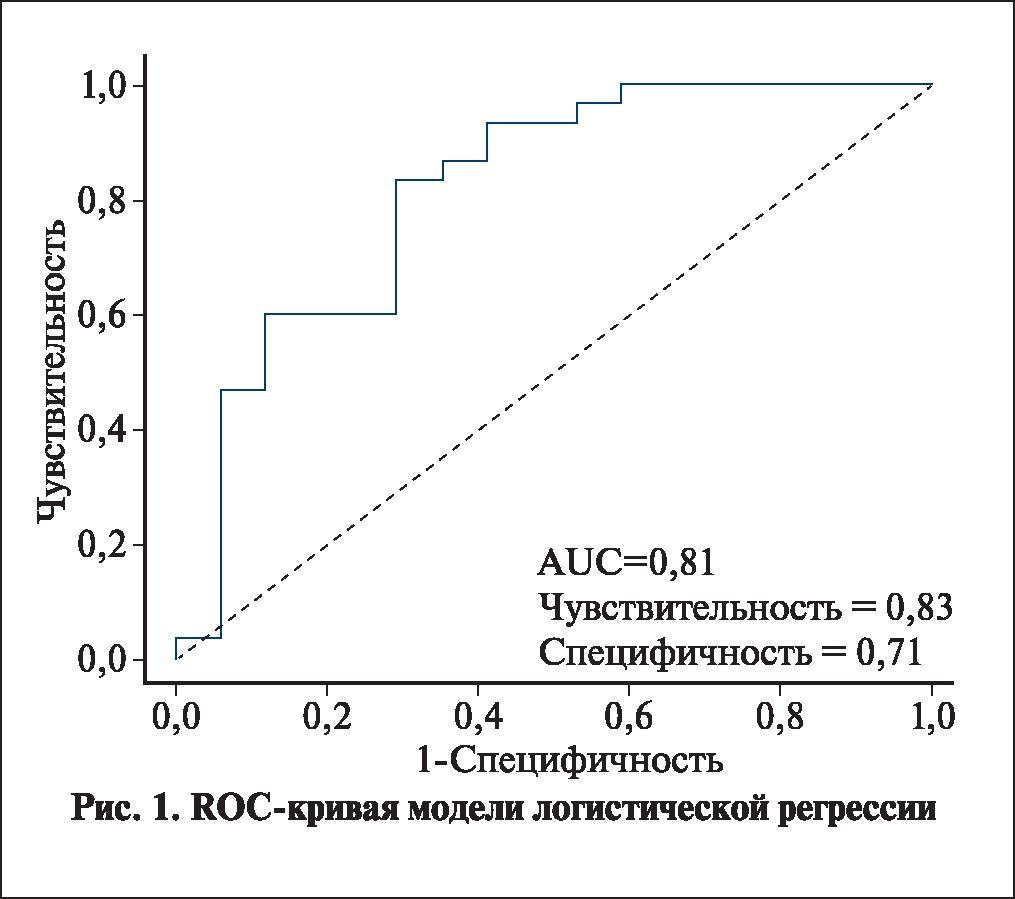
Для частот растворенных и нерастворенных камней построены 95% доверительные интервалы (ДИ) Клоппера-Пирсона.
Для регрессии Кокса использовали пол, возраст, плотность камня и средний объем камня (табл. 2). Единственным статистически значимым фактором, увеличивающим риск оперативного вмешательства, была плотность камня (р<0,001): увеличение риска в 1,008 [1,001; 1,015] раза с увеличением плотности камня на одну единицу.
Таблица 2. Регрессия Кокса для риска проведения операции
Параметр | Оценка коэффициента регрессии Кокса | р -значение | Отношение рисков | 2,5% граница 95% ДИ | 97,5% граница 95% ДИ |
Пол (М) | 0,723 | 0,162 | 2,061 | 0,748 | 5,677 |
Возраст | 0,001 | 0,956 | 1,001 | 0,961 | 1,043 |
Плотность камня | 0,008 | 0,025 | 1,008 | 1,001 | 1,015 |
Средний объем камня | 0,054 | 0,225 | 1,056 | 0,967 | 1,152 |
Согласно анализу Каплана-Майера редукция объема камня составила 51% [0; 69] в месяц (рис. 2).
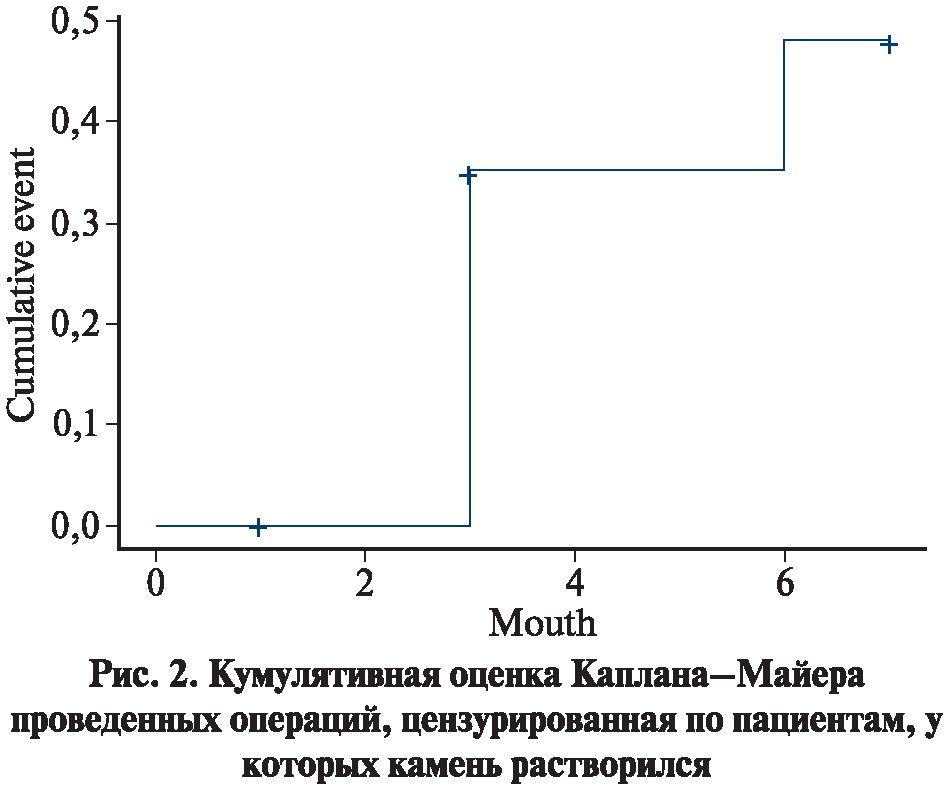
Обсуждение. В настоящем исследовании медиана возраста пациентов составила 63 [55; 71] года, что соответствует международным данным, согласно которым уратный нефролитиаз в два раза чаще регистрируется у пациентов старше 65 лет [17, 18]. Анализ первичных данных также показал легкое снижение СКФ в когорте пациентов (медиана значения СКФ 64 [54; 69] мл/мин), что может указывать на признаки нефропатии и наличие хронической болезни почек 2-q стадии, обусловленной коралловидным нефролитиазом.
Доказано, что пероральный хемолиз является основным методом лечения пациентов с уратными конкрементами, его эффективность, по данным зарубежных авторов, варьируется от 70 до 88% [14, 15, 19], однако результаты исследований, изучающих результаты растворения коралловидных уратных конкрементов, в международной литературе отсутствуют. В проведенном нами исследовании полное и частичное растворение камня было достигнуто у 63,8 и 6,4% пациентов соответственно, что соответствует данным международных работ. Так, в работе А. Tsaturyan и соавт. [15] частота полного и частичного растворения камней при применении перорального хемолиза через три месяца терапии составила 61 и 14% соответственно. Схожие результаты получены M. Normand и соавт. [14], которые добились полного или частичного растворения конкрементов при приеме калия цитрата в 88 и 12% случаев соответственно. Во всех перечисленных исследованиях с целью перорального хемолиза применялся калий цитрат, в качестве критерия уратного состава камня использовалась рентгенпрозрачность камня, а в качестве критерия оценки динамики редукции камня не использовался объем камня.
Диспепсические расстройства нередко появляются у пациентов в связи с приемом цитратных смесей, до 48% пациентов прекращают терапию из-за данного побочного явления [21]. Многие авторы в своих работах предлагают использование гастропротективной терапии и большого количества жидкости на фоне приема цитратных смесей. В нашем исследовании, учитывая правильную выборку пациентов с отсутствием эрозивно-язвенной болезни ЖКТ в стадии обострения, данных неблагоприятных явлений не наблюдалось. Лишь у двух (4,26%) пациентов на фоне литолитической терапии были отмечены явления (эпизоды неконтролируемого повышения артериального давления и развитие эпизодов почечных колик), ставшие причиной исключения пациентов из исследования.
В результате проведенного регрессионного анализа выявлено, что плотность камня является единственным важным критерием при отборе пациентов для консервативного лечения, шанс растворения камня снижается в 1,012 [1,002; 1,025] раза при увеличении плотности камня на одну единицу. Пациенты с плотностью камня менее 500 HU имели наибольший шанс на успешное лечение. Конкременты плотностью более 550 HU, вероятнее всего, имеют смешанный состав [21]. Полученные нами данные коррелируют с номограммой, разработанной L. Zieber и соавт. [22], согласно которой конкременты плотностью менее 450 HU, скорее всего, являются камнями из мочевой кислоты и будут хорошо поддаваться хемолизу. Смешанный химический состав камня можно было предположить и на основании того, что среди наших пациентов, потребовавших оперативного лечения, у трех (6,4%) инициально наблюдалась положительная динамика и ответ на терапию, что выражалось в снижении объема камня, однако на момент окончания исследования полного растворения камня достигнуто не было. У двоих из этих пациентов камни имели кальцийоксалатную природу. Данное наблюдение можно объяснить возможным наличием у этих пациентов в составе конкрементов так называемого оксалатного ядра. Примечательно и то, что после исключения пациентов с кальций-оксалатными камнями доля пациентов с камнями предположительно уратной природы, у которых не удалось добиться полного растворения камней, составила всего 14,3%.
Ограничением нашего исследования можно считать малый объем выборки, однако даже при таком количестве пациентов были получены репрезентативные данные.
Заключение. Хемолитическая терапия уратного коралловидного нефролитиаза цитратными смесями является эффективным и безопасным методом лечения, позволяющим избежать оперативного лечения большинству пациентов. Этот метод может использоваться в качестве альтернативы хирургическому лечению, уменьшая сопряженные риски хирургического лечения.
ЛИТЕРАТУРА / REFERENCES
1. Sorokin I., Mamoulakis C., Miyazawa K., et al. Epidemiology of stone disease across the world. World J Urol. 2017;35(9):1301-1320. doi: 10.1007/s00345-017-2008-6.
2. Kaprin A.D., Apolikhin O.I., Sivkov A.V., et al. Incidence of urolithiasis in the Russian Federation from 2005 to 2020. Experimental and Clinical Urology 2022;15(2)10-17; doi.org/10.29188/2222-8543-2022-15-2-10-17. Russian (Каприн А.Д., Аполихин О.И., Сивков А.В., и соавт. Заболеваемость мочекаменной болезнью в Российской Федерации с 2005 по 2020 гг. Экспериментальная и клиническая урология 2022;15(2)10-17; doi.org/10.29188/2222-8543-2022-15-2-10-17).
3. Ma Q., Fang L., Su R., et al. Uric acid stones, clinical manifestations and therapeutic considerations. Postgrad Med J. 2018 Aug;94(1114):458-462. doi: 10.1136/postgradmedj-2017-135332.
4. Moses R., Pais V.M. Jr, Ursiny M., et al. Changes in stone composition over two decades: evaluation of over 10,000 stone analyses. Urolithiasis. 2015 Apr;43(2):135-9. doi: 10.1007/s00240-015-0756-6.
5. Liu Y., Chen Y., Liao B., Luo D., Wang K., Li H., Zeng G. Epidemiology of urolithiasis in Asia. Asian J Urol. 2018 Oct;5(4):205-214. doi: 10.1016/j. ajur.2018.08.007.
6. Ngo Tin C., Assimos Dean G. Uric acid nephrolithiasis: recent progress and future directions. Rev Urol. 2007;9(1):17—27.
7. Penniston K.L., Sninsky B.C., Nakada S.Y. Preliminary Evidence of Decreased Disease-Specific Health-Related Quality of Life in Asymptomatic Stone Patients. J Endourol. 2016 May;30 Suppl 1:S42-5. doi: 10.1089/end.2016.0074.
8. Hall PM. Nephrolithiasis: treatment, causes, and prevention. Cleve Clin J Med. 2009 Oct;76(10):583-91. doi: 10.3949/ccjm.76a.09043.
9. Sakhaee K. Recent advances in the pathophysiology of nephrolithiasis. Kidney Int. 2009 Mar;75(6):585-95. doi: 10.1038/ki.2008.626. Epub 2008 Dec 10.
10. Jongyotha K., Sriphrapradang C. Squamous Cell Carcinoma of the Renal Pelvis as a Result of Long-Standing Staghorn Calculi. Case Rep Oncol. 2015 Oct 3;8(3):399-404. doi: 10.1159/000440764.
11. Karki N., Leslie S.W. Struvite and Triple Phosphate Renal Calculi. [Updated 2023 May 30]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024.
12. Akilov F.A. et al. Intraoperative complications of endoscopic removal of stones from the upper urinary tract. Urologiia. 2013;(2):79-82. Rassian (Акилов Ф.А. и др. Интраоперационные осложнения эндоскопического удаления камней из верхних мочевыводящих путей. Урология. 2013;(2):79-82).
13. Golovanov S.A. et al. Multipoint analysis of the mineral composition of coralloid stones in the study of the peculiarities of their formation. Experimental and clinical urology. 2017;(3):52-57. Russian (Голованов С.А. и др. Многоточечный анализ минерального состава коралловидных камней в изучении особенностей их формирования. Экспериментальная и клиническая урология. 2017; (3):52-57).
14. Normand M., Haymann J.P., Daudon M. Medical treatment of uric acid kidney stones. Can Urol Assoc J. 2024 Jun 17. doi: 10.5489/cuaj.8774.
15. Tsaturyan A., Bokova E., Bosshard P., Bonny O., Fuster D.G., Roth B. Oral chemolysis is an effective, non-invasive therapy for urinary stones suspected of uric acid content. Urolithiasis. 2020 Dec;48(6):501-507. doi: 10.1007/s00240-020-01204-8.
16. Yanenko E., Khurtsev K., Makarova T. Classification of coralloid nephrolithiasis and algorithm of therapeutic tactics, Proceedings of the IV All-Union Congress of Urologists 1990. С. 600-601. Russian (Яненко Э., Хурцев К., Макарова Т. Классификация коралловидного нефролитиаза и алгоритм лечебной тактики, Материалы IV Всесоюзного съезда урологов 1990. С. 600-601).
17. Mandel N.S., Mandel G.S. Urinary tract calculus disease in the United States veteran population. II. Geographical analysis of variations in composition. J Urol. 1989;142:1516-1521. doi: 10.1016/s0022-5347(17)39145-0.
18. Gault M.H., Chafe L. Relationship of frequency, age, sex, calculus weight, and composition in 15,624 calculi: comparison of results for 1980 to 1983 and 1995 to 1998. J Urol. 2000;164:302-307
19. Abou-Elela A. Epidemiology, pathophysiology, and management of uric acid urolithiasis: A narrative review. J Adv Res. 2017 Sep;8(5):513-527. doi: 10.1016/j.jare.2017.04.005. Epub 2017 Apr 28.
20. Mattle D., Hess B. Preventive treatment of nephrolithiasis with alkali citrate - a critical review. Urolithiasis 2005;33:73-9. doi.org/10.1007 s00240-005-0464-8
21. Chew B.H., Wong V.K.F., Halawani A., Lee S., Baek S., Kang H., Koo K.C. Development and external validation of a machine learning-based model to classify uric acid stones in patients with kidney stones of Hounsfield units < 800. Urolithiasis. 2023 Sep 30;51(1):117. doi: 10.1007/s00240-023-01490-y.
22. Zieber L., Creiderman G., Krenawi M., Rothenstein D., Enikeev D., Ehrlich Y., Lifshitz D. A nomogram to predict «pure» vs. «mixed» uric acid urinary stones. World J Urol. 2024 Oct 31;42(1):610. doi: 10.1007/s00345-024-05340-3.
Поступила 18.11.2024
Принята в печать 25.11.2024
Received 18.11.2024
Accepted 25.11.2024
Источник финансирования: Отсутствует
Financing source: Absents
Информация об авторах:
Малхасян В.А. - д.м.н, профессор кафедры урологии ФГБОУ ВО «РосУниМед», заведующий урологическим отделением № 67, ГБУЗ «ММНКЦ им. С.П. Боткина» ДЗМ, Москва, Российская Федерация; е-mail: vigenmalkhasyan@gmail.com, orcid. org/0000-0002-2993-884X
Тунгузбаев Х.У. - аспирант кафедры урологии ФГБОУ ВО «РосУниМед», Москва, Российская Федерация, e-mail: tunguzbiev. xamzat@bk.ru orcid.org/0009-0009-0575-2782
Пульбере С.А. - заведующий урологическим отделением ГБУЗ «Городская клиническая больница № 1 им. Н.И. Пирогова, ДЗМ, Москва, Российская Федерация, e-mail: pulpiv@mail.ru, https:// orcid.org/0000-0001-7727-4032
Геворкян А.Р. - врач-уролог ГБУЗ «Городская поликлиника № 212» ДЗМ, Москва, Российская Федерация, e-mail:Ashot_ Gevorkyan@mail.com
Сухих С.О. - к.м.н., врач-уролог ГБУЗ «ММНКЦ им. С.П. Боткина» ДЗМ, Москва, Российская Федерация, e-mail: docsukhikh@gmail.ru. orcid. org/0000-0002-3840-0259
Гаджиев Н.К. - д.м.н., заместитель директора по медицинской части (урология) клиники высоких медицинских технологий им. Н.И. Пирогова ФГБОУ ВО «Санкт-Петербургский государственный университет», Санкт-Петербург, Российская Федерация; e-mail: nariman.gadjiev@gmail.com, orcid. org/0000-0002-6255-0193
Пушкарь Д.Ю. - академик РАН, д.м.н., профессор, заведующий кафедрой урологии ФГБОУ ВО «Российский университет медицины», руководитель Московского урологического центра ММНКЦ им. С. П. Боткина ДЗМ, Москва, Российская Федерация; e-mail: pushkardm@ mail.ru. orcid.org/0000-0002-6096-572
EFFICACY OF ORAL CHEMOLYSIS IN THE MANAGEMENT OF STAGHORN URIC ACID NEPHROLITHIASIS
V.A. Malkhasyan1,2, H.U. Tunguzbaev1, S.A. Pulbere3, A.R. Gevorkyan4, S.O. Sukhikh2, N.K. Gadzhiev5, D.Yu. Pushkar1,2
1Russian University of Medicine, Moscow, Russian Federation; 2Botkin City Clinical Hospital, Moscow, Russian Federation; 3Pirogov City Clinical Hospital №1, Moscow, Russian Federation; 4Outpatient Clinic № 212, Moscow, Russian Federation; 5 Saint Petersburg State University, N.I. Pirogov High Medical Technologies Clinic, Saint Petersburg, Russian Federation
Corresponding author: V.A. Malkhasyan - Doctor of Medical Sciences, Professor of the Department of Urology, Russian University of Medicine, Moscow, Russian Federation; Head of Urology Department №67, Botkin City Clinical Hospital, Moscow, Russian Federation, e-mail: vigenmalkhasyan@gmail.com
Staghorn nephrolithiasis represents one of the most complex forms of urolithiasis, with treatment approaches remaining a subject of ongoing debate among specialists. This study aims to assess the effectiveness and safety of oral chemolysis using citrate mixtures in treating staghorn urate nephrolithiasis. A prospective, multicenter cohort study was conducted from January 2023 to October 2024 among patients with CT-diagnosed staghorn stones of presumed urate composition (average urine pH < 5.8, average stone density < 650 HU, radiolucent on urogram or topogram) who received oral chemolysis with a citrate mixture containing citric acid, potassium bicarbonate, and sodium citrate («Blemaren»). Patients were recruited from outpatient clinics and hospitals in Moscow.
Results: Of the 49 patients included in the study, 2 were excluded within the first 2 months. Complete stone dissolution was achieved in 30 patients (63.8%), while 17 patients (36.2%) eventually required surgical intervention. Among these, 4 patients (8.5%) achieved complete stone dissolution within 1 month of therapy, 18 patients (38%) within 3 months, and 8 patients (17%) within 6 months. Of the stones removed surgically, 12 (70.6%) were calcium oxalate, and 5 (29.4%) were uric acid stones. Consequently, the proportion of patients with noncalcium oxalate stones who did not achieve complete stone dissolution was 14.3%. Stone density was the only parameter that significantly influenced the likelihood of stone dissolution and the risk of surgical intervention (p<0.05). According to regression analysis, the likelihood of stone dissolution decreased by a factor of 1.012 with each unit increase in stone density, while the risk of surgery increased by a factor of 1.008 under the same conditions.
Conclusions: The results of this study demonstrate that oral chemolysis for staghorn uric acid nephrolithiasis is an effective method and may serve as a viable alternative to surgical treatment, potentially reducing the associated risks of anesthesia and surgery for this patient group.
Keywords: urolithiasis, staghorn uric acid stones, oral chemolysis, citrate mixtures
The authors declare no conflict of interest. For citation: Malkhasyan V.A., Tunguzbaev H.U., Pulbere S.A., Gevorkyan A.R., Sukhikh S.O., Gadzhiev N.K., Pushkar D.Yu. Efficacy of oral chemolysis in the management of staghorn uric acid nephrolithiasis. Urologiia. 2024;6:17-23.
Doi: https://dx.doi.org/10.18565/urology.2024.6.17-23
Information about the authors:
Malkhasyan V.A. - M.D.; Professor of the Department of Urology, Russian University of Medicine, Head of Urology Department No67, Botkin City Clinical Hospital, Moscow, Russian Federation; e-mail: vigenmalkhasyan@gmail.com. orcid.org/0000-0002-2993-884X
Tunguzbaev H.U. - resident of the Department of Urology, Russian University of Medicine, Moscow, Russian Federation, e-mail: tunguzbiev.xamzat@bk.ru orcid.org/0009-0009-0575-2782
Pulbere S.A. - Head of the Urological Department of Pirogov City Clinical Hospital №1, Moscow, Russian Federation, e-mail: pulpiv@ mail.ru orcid.org/0000-0001-7727-4032.
Gevorkyan A.R. - Urologist, Outpatient Clinic № 212, Moscow, Russian Federation, e-mail:Ashot_Gevorkyan@mail.com
Sukhikh S.O. - Ph.D., urologist of Botkin City Clinical Hospital, Moscow, Russian Federation; e-mail: docsukhikh@gmail.ru. https:// orcid.org/0000- 0002-3840-0259
Gadzhiev N.K. - MD, Deputy Director for the Medical part (Urology) of the High Medical Technologies Clinic named after N.I. Pirogov St. Petersburg State University, St. Petersburg, Russian Federation; e-mail: nariman.gadjiev@gmail.com, orcid.org/0000-0002-6255-0193
Pushkar D.Yu. - Academician of the Russian Academy of Sciences, M.D.; Professor, Head of the Department of Urology of the Russian University of Medicine, Moscow, Russia. Head, Moscow Urological Centre, Botkin City Clinical Hospital, Moscow, Russian Federation; e-mail: pushkardm@mail.ru. orcid.org/0000-0002-6096-5723