Уважаемый посетитель!
Эта информация для специалистов здравоохранения
Нажимая «ПРОДОЛЖИТЬ», Вы подтверждаете, что им являетесь
Противовоспалительные и хондропротективные свойства препаратов Эльбона и Элтуфлоп БИО - результаты экспериментального исследования
СтатьиКукес И.В.1 , П.Р. Камчатнов2,3, А. В. Чугунов2, Н.Д. Малашенко4, А.Ю. Казаков2
1 ФАНО «Научный центр клинической метаболомики, генетики и фармакологии», Москва, Российская Федерация
2 ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н. И. Пирогова» Минздрава России, Москва;
3 ГБУЗ «Городская клиническая больница им. В.М. Буянова Департамента здравоохранения города Москвы», Москва, Россия;
4 ГБУЗ «НИИ скорой медицинской помощи им. Н.В. Склифосовского Департамента здравоохранения города Москвы», Москва, Россия
Цель исследования: провести экспериментальную оценку сопоставимости действия симптоматических препаратов замедленного действия для лечения остеоартрита (Symptomatic Slow Acting Drugs for Osteoarthritis, SYSADOA): препаратов биоактивного концентрата из мелких морских рыб и препаратов глюкозамина.
Материал и методы: исследование выполнено на 70 крысах. Модель артрита создавали путем введения коллагена II типа и неполного адъюванта Фрейнда в соотношении 1:1. Препараты ЭЛТУФЛОП® БИО или два препарата биоактивного концентрата из мелких морских рыб (препарат 1 (Пр1) и препарат 2 (Пр2)), препарат Эльбона® или препарат глюкозамин (Пр3) вводились животным 14 сут с момента моделирования артрита. В сыворотке крови определяли концентрации цитокинов: фактора некроза опухоли α (ФНО-α) и интерлейкина (ИЛ) 6. В гомогенате сустава задней конечности определяли концентрации матриксных металлопротеиназ (matrix metalloproteinase, ММР) 9, ММР-2, малонового диальдегида (МДА), апоптоз-индуцирующего фактора (АИФ). Полученные результаты сравнивали с показателями группы ложнооперированных животных и группы негативного контроля, в которой препаратов не получали.
Результаты исследования: эффективность применения у животных с экспериментальным артритом препарата ЭЛТУФЛОП® БИО сопоставима с эффективностью препарата Пр1 и превосходит эффективность препарата Пр2 по выраженности угнетения процессов воспаления (снижение концентрации ИЛ-6 и ФНО-α), резорбции хрящевой ткани (снижение содержания ММР-2 и ММР-9), апоптоза (концентрация АИФ), окислительного стресса (содержание МДА). Нормализация содержания биохимических маркеров сопровождалось уменьшением выраженности отека. Глюкозамин-содержащие препараты Эльбона® и Пр3 продемонстрировали сопоставимый уровень активности.
Заключение: полученные результаты позволяют рассматривать препараты ЭЛТУФЛОП® БИО и Эльбона® в качестве долговременной терапии больных с хроническими суставно-мышечными болевыми синдромами, обусловленными остеоартритом различной локализации.
Ключевые слова: артрит, Элтуфлоп БИО, глюкозамин, Эльбона, хондроитина сульфат, лечение.
Камчатнов П.Р. - orcid.org/0000-0001-6747-3476
Чугунов А. В. - orcid.org/0000-0003-4506-8095
Кабанов А.А. - orcid.org/0000-0002-8684-8058
Казаков А.Ю. - orcid.org/0000-0003-2367-545X
Малашенков Н.Д. - orcid.org/0000-0001-7334-7820
Для цитирования: Кукес И.В., Камчатнов П.Р., Чугунов А.В., Малашенко Н.Д., Казаков А.Ю. Противовоспалительные и хондропротективные свойства препаратов Эльбона® и ЭЛТУФЛОП® БИО — результаты экспериментального исследования. РМЖ. Медицинское обозрение. 2024;8(10):568-575. DOI: 10.32364/2587-6821-2024-8-10-4.
Введение
На сегодняшний день в мире исключительно широко распространены заболевания суставно-мышечной системы, что в значительной степени обусловлено трудностями ранней диагностики данной группы заболеваний, отчего, ограниченной эффективностью имеющихся в распоряжении клиницистов методов лечения и профилактики данных состояний [1]. Среди разнообразных суставно-мышечных болевых синдромов одной из наиболее распространенных форм является поражение суставов и мягких тканей позвоночника - дорсалгия [2]. Исключительная распространенность данных патологических состояний, значительные материальные затрат на ведения пациентов требуют поиска новых решений для повышения эффективности лечебно-профилактических мероприятий и снижения бремени заболевания.
Результаты исследования последних лет позволили установить тесную связь таких болевых синдромом с остеоартритом. В частности, показана связь остеоартрита дугоотросчатых суставов, дегенеративного поражения межпозвонковых дисков с наличием болевого синдрома [3, 4]. Важным явилось установление акта воспаления, которое лежит в основе болевого синдрома у таких больных, и которое в значительно степени соответствует выраженности структурных изменений позвоночного двигательного сегмента [5, 6]. Понимание роли воспалительного процесса низкой интенсивности расширяет возможности для выбора патогенетической терапии таких пациентов.
В этой связи значительный интерес вызывает группа препаратов, обладающих способностью изменять течения заболевания, которые длительное время рассматривались как хондропротекторы, позволяющие замедлить дегенерацию хрящевой ткани суставов и, вероятно, способствовать ее регенерации.
Исследования последних лет позволили установить целый ряд ранее неизвестных эффектов данной группы препаратов, в частности, было установлены способность их воздействия на процессы воспаления и дегенерации тканей у пациентов с различными суставными заболеваниями, в частности, с остеоартритом. Вследствие этого хондропротекторы с полным основанием рассматриваются как симптоматические препараты замедленного действия для лечения остеоартрита (англ.: Symptomatic Slow Acting Drugs for Osteoarthritis, SYSADOA). SYSADOA - группа биологических препаратов различного происхождения, обладающих способностью оказывать воздействие на хрящевую ткань, которое, со значительно долей условности, можно разделить на симптом-модифицирующий эффект, обеспечивающий восстановление функций суставов и снижение интенсивности болевого синдрома, а также на структурно-модифицирующий, способный замедлить процессы прогрессирования воспаления и дегенеративно-дистрофического поражения хрящевой и костной тканей [7]. Препараты данной группы обладают способностью угнетать активность ферментов, участвующих в дегенерации суставного хряща за счет активации синтеза гликозаминогликанов. Благодаря этим эффектам восстанавливается метаболизм гиалина и замедляются процессы разрушения хрящевой ткани. Продемонстрирована эффективность препаратов SYSADOA на различных стадиях дегенеративного поражения суставов.
Широко распространено применение препаратов SYSADOA, содержащих хондроитина сульфат (ХС), глюкозамин, а также их комбинацию. В соответствии с решением Европейской противоревматической лигой (EULAR) [8] в 2003 г. эти препараты рассматриваются как средства замедленного действия для симптоматического лечения пациентов с остеоартритом различных суставов. В ряде стран, в том числе, в Российской Федерации, SYSADOA включены в клинические рекомендации по лечению пациентов с многочисленными дегенеративно-дистрофическими заболеваниями суставно-мышечного аппарата [9-11]. Действующим веществом многих препаратов данной группы является ХС. Формы выпуска лекарственных форм ХС весьма разнообразны, они предназначены для перорального, парентерального и наружного применения. Имеются данные о том, что более предпочтительным является применение препаратов ХС в форме для приема приема внутрь (системное действие) и наружно (местное действие) [12].
Также получены данные о том, что ХС способен восстанавливать обмен веществ в костной и хрящевой тканях, обладает противовоспалительным действие, способен ингибировать хемотаксис лейкоцитов и фагоцитов [13]. Также показана способность ХС предупреждать повреждение клеточных мембран вследствие воздействия свободных радикалов, угнетать образование циклооксигеназы 2-го типа и выработку хондроцитами простагландина-2. Таким образом, противовоспалительное действие ХС обусловлено опосредованным воздействием на клеточный компонент воспаления, а также стимуляцией синтеза протеогликанов и гиалуроновой кислоты, подавлением активости протеолитических ферментов [14]. Способностью обеспечивать нормализацию обмена веществ хрящевой и костной тканей также обладает глюкозамин, который синтезируется в хрящевой ткани. Глюкозамин активирует образование аминогликанов, вследствие чего способствует восстановлению хрящевой выстилки сустава и нормализации образования внутрисуставной жидкости.
Ключевыми механизмами, объясняющими клинические эффекты препаратов SYSADOA, являются угнетение образования медиаторов воспаления (гиалуронидаза, N-ацетилглюкозаминидаза, миелопероксидаза, эластаза, коллагеназа), замедление процессов дегенерации тканей суставов, стимуляция синтеза основных компонентов межклеточного матрикса (ХС, гиалурон, протеингликан) [15]. Целесообразность широкого применения SYSADOA в клинической практике обусловлена их способностью снижать интенсивность болевого синдрома, уменьшать выраженность клинических проявлений остеоартрита различных суставов, и, что принципиально важно, улучшать функций суставов (устранение или уменьшение скованности, расширение объема активных и пассивных движений без болевых ощущений и пр.).
SYSADOA не следует рассматривать как полную альтернативу нестероидным противовоспалительными препаратами (НПВП), оптимальный клинический эффект достигается при одновременном применении. Комбинированное лечение позволяет уменьшить дозы НПВП и сроки их назначения, что ассоциировано со снижением риска развития нежелательных эффектов [16]. Риск развития лекарственных взаимодействий при этом отсутствует. Принимая во внимание, что SYSADOA – препараты замедленного действия, развитие клинического эффекта на фоне их назначения наблюдается через несколько недель от начала терапии. Именно в этом периоде целесообразно их совместное применение с НПВП. Назначение SYSADOA подразумевает длительные сроки лечения, целесообразно проведение повторных курсов терапии на протяжении многих лет. Указанные особенности терапевтического процесса следует обсудить с пациентом при начале лечения. Несомненным достоинством SYSADOA является хороший профиль безопасности их применения. Хорошая переносимость данный препаратов обусловлена, в первую очередь, их биологическим сродством со структурами суставного хряща. Препараты SYSADOA легко проникают в ткани, не инактивируются при поступлении в желудочно-кишечный тракт.
Результаты метаанализа серии рандомизированных плацебо-контролируемых исследований продемонстрировали клиническую эффективность и хорошую переносимость ХС у пациентов с заболеваниями дегенеративно-дистрофического характера, в том числе было доказано наличие анальгезирующих и противовоспалительных эффектов [17]. По данным клинического исследования, посвященного изучению возможности применения комбинированной терапии, хондропротекторного магнитофореза с наличием «бегущего» импульсного магнитного поля и использованием хондроксида (трансдермальная гелевая форма) у пациентов, страдающих остеоартритом коленного сустава. В исследование были включены пациенты с остеоартритом коленного сустава II-III степени, которые были распределены в три группы: 1-ю группа (n=25) получала локальную терапию - магнитофорез хондроксида с использованием РПМФ (20 мТл, частота 6,25 Гц, время воздействия 20 мин, № 12); 2-я группа (n=25) и 3-й группе получала плацебо-магнитотерапию хондроксидом; а 3-я группа - РПМФ без использования местной терапии хондроксидом. По результатам этого исследования было установлено, что комбинированная терапия в виде местного использования магнитофореза трансдермальной формы хондроксида, благоприятно влияет на состояние пациентов с остеоартритом коленного сустава, представляет собой эффективный и безопасный способ лечения [18].
Клиническое исследования направленное на изучение эффективности и безопасности использования парентерального введения ХС и глюкозамина сульфата при рецидивах хронической боли в суставах и дорсалгии в условиях реальной клинической практики. Представляло собой открытое сравнительное исследование интермиттирующей схемы при котором пациентам с генерализованным остеоартритом в течении 6 нед проводилась инъекционная терапия с использованием ХС и глюкозамина сульфата. Для исследования было отобрано 70 пациентов, распределенных на две группы, сопоставимые между собой по ряду показателей: пол, возраст, коморбидным состояния, клинические и физиологические параметры. Пациентам 1-ой группы назначали комбинированную терапию с интермиттирующей схемой внутримышечного введения ХС (2,0 мл через день, № 20) и ГС (3,0 мл через день № 20; больные 2-ой группы получали стандартное лечение, включая НПВП в режиме «по потребности» для достижения удовлетворительного обезболивания и другие препарата для лечения имеющихся сопутствующих заболеваний. В результате проведенного исследования было установлено, что лечение позволило добиться эффективного обезболивания у 91,4% пациентов1-ой группы, тогда как при монотерапии НПВП эффективное обезболивание было достигнуто только у 62,9% больных. Таким образом, по мнению авторов исследования, представляется целесообразным использование интермиттирующей схемы комбинированного лечения у пациентов с хронической скелетно-мышечной болью, обусловленной генерализованным остеоартритом [19].
Таким образом, принимая во внимание высокую киническую эффективность препаратов SYSADOA у пациентов со скелетно-мышечными болевыми синдромами, разнообразие оказываемых ими эффектов, представляется важным изучение конкретных механизмов действия препаратов данной группы. Несомненный интерес представляет оценка воздействия различных представителей данной группы лекарственных средств на основные механизмы повреждения тканей суставов у таких пациентов. Цель исследования: провести экспериментальную оценку сопоставимости действия SYSADOA.
Задачи исследования:
− сравнение эффективности препарата Элтуфлоп БИО и двух препаратов биоактивного концентрата из мелких морских рыб (Пр1 и Пр2) по выраженности воздействия на содержания в крови ключевых медиаторов воспаления и маркеров повреждения тканей: фактор некроза опухоли-альфа (ТNF-α), матриксные интерлейкин (IL)-6, металлопротеиназы (ММР)-9, ММР-2, малоновый диальдегид (МДА), апоптоз-индуцирующий фактор (АИФ)
− Определение преимуществ препарата Эльбона в сравнении с глюкозамином (Пр3) по ключевым маркерам воспаления (IL-6, ТNF-a, ММР-9, ММР-2, МДА, АИФ).
Материал и методы
Экспериментальные животные
Исследование выполнено на 70 половозрелых самцах крыс линии Wistar (масса тела 200-220 г). Животные получены из питомника «Рапполово» (Россия, Ленинградская обл.). Перед началом эксперимента животные в течение 14 сут содержались на карантине. В период проведения эксперимента животные размещались в стандартных макролоновых клетках со свободным доступом к пище и воде; температура окружающего воздуха 22±20С0, относительная влажность - 60±5%, естественная смене суточного цикла (12 ч день/12 ч ночь). Содержание животных и проводимые с ними манипуляции соответствовали нормам экспериментальной этики (Directive 2010/63 / EU of the European Parliament and of the council on the protection of animals used for scientific purposes, September 22, 2010). В каждой экспериментальной группе было по 10 животных.
Характеристика исследуемых объектов
В качестве анализируемых объектов выступали лекарственные препараты SYSADOA, содержащие экстракт концентрированный из мелкой морской рыбы (Элтуфлоп БИО®, препарат 1 (Пр1) и препарат 2 (Пр2)) и глюкозамин (Эльбона® и препарат 3 (Пр3)). Изучавшиеся препараты вводились курсом 14 сут (однократно в сутки) с момента моделирования артрита в дозах, рассчитанных с учетом межвидового коэффициента пересчета доз, которые для экстракта, концентрированного из мелкой морской рыбы составили 0,1 мл; для глюкозамина - 93 мг/кг [20]. Полученные результаты сравнивали с показателями группы ложнооперированных животных (ЛО) и группы негативного контроля (НК, терапии по поводу артрита не получали).
Экспериментальная модель артрита.
Модель артрита создавали путем введения коллаген II типа и неполного адъюванта Фрейнда в соотношении 1:l. Индуктор артрита вводили внутрикожно в основание хвоста [21]. Выраженность отека конечностей оценивали на основании полуколичественной шкалы, в соответствии с которой 0 баллов – норма, 1 балл - воспаление и отек одного пальца стопы; 2 балла - воспаление и отек > 1 пальца с воспалением и отеком всей лапы или легким отеком всей лапы; 3 балла - воспаление и отек всей лапы; 4 балла - сильное воспаление и отек всей лапы или анкилоз суставов [22].
Подготовка биоматериала для анализа.
Крыс анестезировали хлоралгидратом (350 мг/кг, внутрибрюшинно), после чего производили забор крови в пробирки с цитратным наполнением. Кровь центрифугировали 20 мин при 1000 g, в полученной сыворотке оценивали концентрацию ФНО-α и ИЛ-6. Далее проводили диссипацию сустава задней конечности (art. tarsocruralis), полученный материал гомогенизировали в Трис-НСI буфере и центрифугировали при 10000g. В полученном супернатанте определяли концентрации ММР-9, ММР-2, МДА и АИФ.
Оценка концентрации МДА
Концентрацию МДА определяли спектрофотометрическим методом в реакции конденсации с 2-тиобарбитуровой кислотой. Образующийся в ходе реакции окрашенный комплекс имеет максимум поглощения при 532 нм, при этом окраска раствора пропорциональна концентрации МДА. Количество МДА рассчитывали по величине молярного коэффициента экстинкции (1,56*105 л/моль-1*см-1), результаты представлены в мкмоль/л [23].
Иммуноферментное (ИФА) исследование
Концентрацию ИЛ-6, ФНО-a, ММР-9, ММР-2 и АИФ определяли Методом ИФА с использованием реактивов производства Cloud clone (Хьюстон, США) в соответствии с инструкцией производителя. Считывание результатов осуществляли с применением полуавтоматического планшетного ИФА-ридера F50 (Tecan, Австрия). Обработку входящего сигнала производили в системе Magellan 50.
Статистический анализ.
Статистический анализ результатов проведен с использованием программного пакета «Statplus 7.0» (AnalystSoft). Данные представлены в виде среднего и стандартной ошибки среднего ( M±SEM). Анализ результатов проводили методом однофакторного дисперсионного анализа ANOVA с пост-тестом Ньюмена-Кейлса, отличия принимались статистически значимыми при уровне p<0,05.
Результаты
Результаты применения лекарственных препаратов, содержащих экстракт концентрированный из мелкой морской рыбы
В ходе изучения изменения концентрации цитокинов ИЛ-6 и ФНО-α в сыворотке крови экспериментальных животных было установлено, что у в группе НК показатели были выше, чем у группы ЛО в 4,0 (p<0,05) и 8,4 (p<0,05) раза соответственно, тогда как применение препаратов Элтуфлоп Био, Прп1 и Пр2 сопровождалось уменьшением содержания ИЛ-6 на 36,9% (p<0,05), 13,6% (p<0,05) и 35,9% (p<0,05) соответственно, а ФНО-α – на 47,9%, 26,1% и 37,3% (все отличия статистически значимы, p<0,05). При этом концентрация в крови ИЛ-6 и ФНО-α у крыс, получавших Элтуфлоп Био, была ниже таковой в группе животных, получавших Пр2 на 27,0% (p<0,05) и 29,5% (p<0,05) соответственно (рис.1).
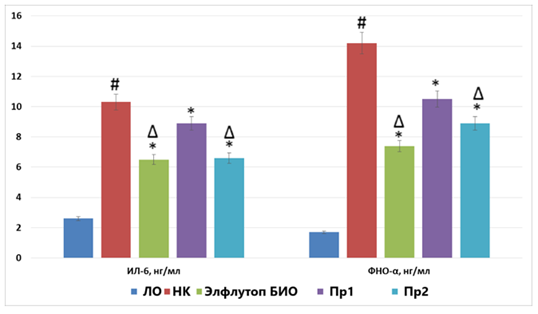
Рисунок 1. Влияние препаратов, содержащих экстракт концентрированный из мелкой морской рыбы, на изменение концентрации цитокинов в крови крыс с экспериментальным артритом
Примечание: тут и на рис.2-5- # - отличия статистически значимы по сравнению с группой ЛО; * - отличия статистически значимы по сравнению с группой НК; Δ – отличия статистически значимы по сравнению с группой, получавшей Пр2.
Также было установлено, что в группе НК имело место повышение по сравнению с группой ЛО группы концентрации ММР-2 и ММР-9 в 3,6 (p<0,05) и 3,64 (p<0,05) раза соответственно. Применение препаратов Элтуфлоп Био, Пр1 и Пр2 сопровождалось уменьшением концентрации ММР-2 по сравнению с группой НК на 42,6% (p<0,05), 24,5% (p<0,05) и 34,8% (p<0,05) соответственно, тогда как концентрация ММР-9 снизилась на 21,2% (p<0,05), 11,7% (p<0,05) и 15,5% (p<0,05) соответственно. Важно, что на фоне введения препарата Элтуфлоп Био концентрация ММР-2 и ММР-9 оказалась статистически значимо ниже, чем при применении препарата Пр2 – на 23,9% (p<0,05) и 10,7% (p<0,05) соответственно (рис.2).
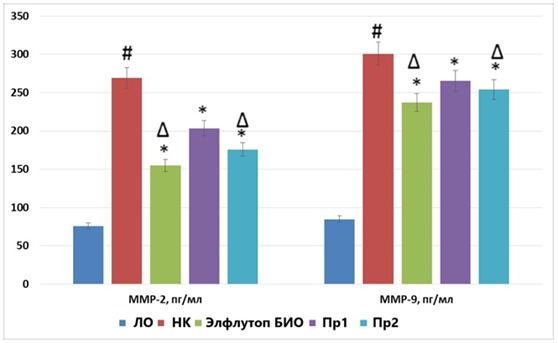
Рисунок 2. Влияние препаратов, содержащих экстракт концентрированный из мелкой морской рыбы, на концентрацию ММР в крови крыс с экспериментальным артритом
Результаты определения концентрации МДА (рис. 3) и АИФ (рис. 4) позволили установить, что в группе НК рассматриваемые показатели были выше, чем в группе ЛО в 4 (p<0,05) и 5,3 (p<0,05) раза соответственно. В группах применения препаратов Элтуфлоп Био, Пр1 и Пр2 концентрация МДА оказалась статистически значимо ниже - на 44,6% (p<0,05), 25,0% (p<0,05) и 41,1% (p<0,05) соответственно, чем в группе НК, при этом концентрация АИФ снизилась на 39,3% (p<0,05), 22,3% (p<0,05) и 31,3% (p<0,05). Необходимо отметить, что в группе крыс, получавших Элтуфлоп Био, концентрация МДА и АИФ была ниже, чем в группе животных, которым вводили Пр2 – на 26,2% (p<0,05) и 21,9% (p<0,05).
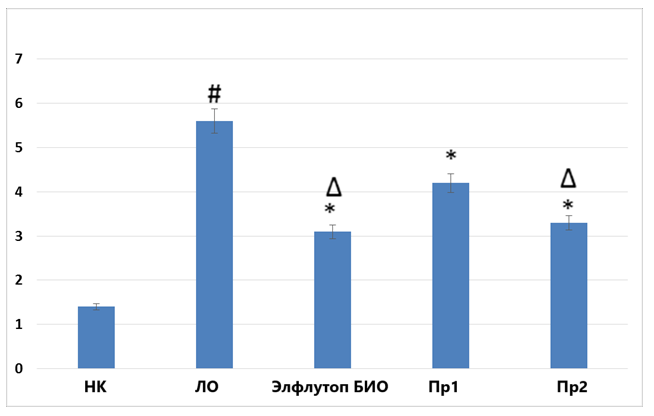
Рисунок 3. Влияние препаратов, содержащих экстракт концентрированный из мелкой морской рыбы, на концентрацию МДА в крови крыс с экспериментальным артритом
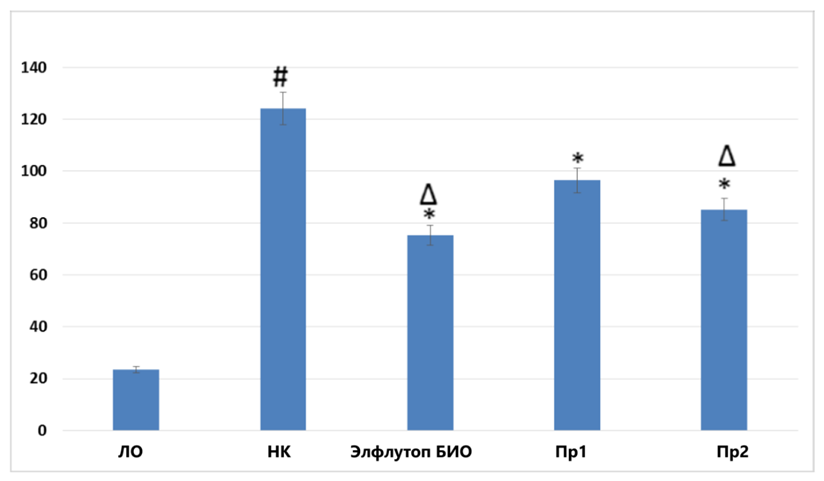
Рисунок 4. Влияние препаратов, содержащих экстракт концентрированный из мелкой морской рыбы, на концентрацию АИФ в крови крыс с экспериментальным артритом
В совокупности выявленные изменения в группе НК привели к формированию выраженного отека лап (3,75±0,67 балла). На фоне применения препаратов Элтуфлоп Био, Пр1 и Пр2 выраженность отека лап (рис.5) снизилась на 46,7% (p<0,05), 26,7% (p<0,05) и 33,3% (p<0,05) в сравнении с показателем в группе НК. При этом отек лап при использовании Элтуфлоп Био был достоверно ниже аналогичного в группах применения Пр2 на 27,3% (p<0,05).
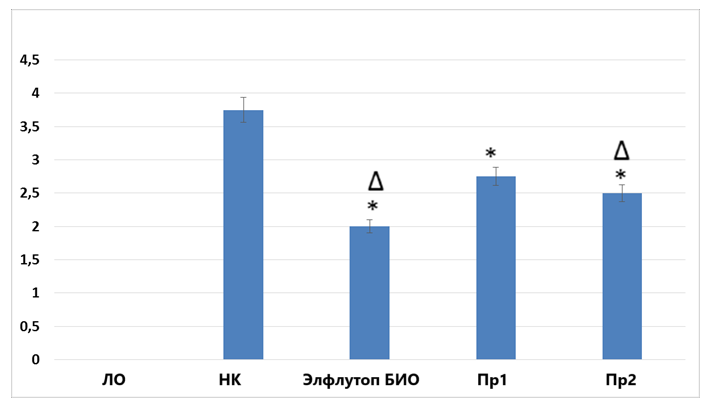
Рисунок 5. Влияние препаратов, содержащих экстракт концентрированный из мелкой морской рыбы, на выраженность отека лап у крыс с экспериментальным артритом
Результаты анализа эффектов лекарственных препаратов, содержащих глюкозамин
В результате исследования было установлено, что применение препаратов Эльбона и Пр3 (рис. 6) сопровождалось уменьшением концентрации ИЛ-6 на 48,5% (p<0,05) и 46,6% (p<0,05), при снижении концентрации ФНО-α на 56,3% (p<0,05) и 52,8% (p<0,05). Также выявлено уменьшение концентрации ферментов ММР-2 и ММР-9 в группах животных, которым вводили препарат Эльбона на 47,2% (p<0,05) и 29,2% (p<0,05), а животных, получавших Пр3 – на 42,2% (p<0,05) и 25,2% (p<0,05) соответственно (рис.7).
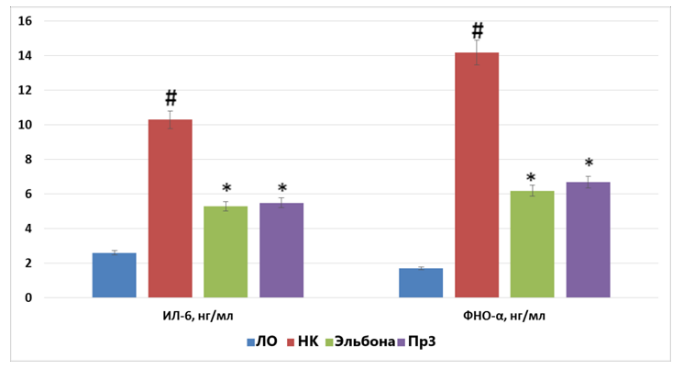
Рисунок 6. Влияние препаратов, содержащих глюкозамин, на изменение концентрации цитокинов у крыс с экспериментальным артритом
Примечание: тут и на рис 7-10 - отличия статистически значимы по сравнению с группой ЛО; * - отличия статистически значимы по сравнению с группой НК; Δ – отличия статистически значимы по сравнению с группой, получавшей Пр3.
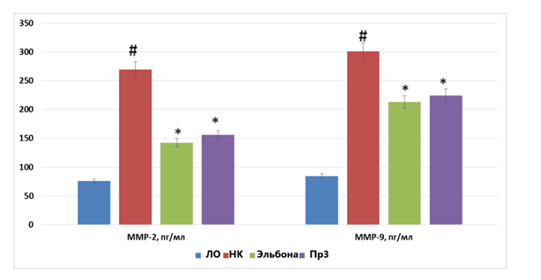
Рисунок 7. Влияние препаратов, содержащих глюкозамин, на концентрацию ММР у крыс с экспериментальным артритом
Концентрация МДА в группах животных, которым вводили препараты Эльбона и Пр3, была ниже соответствующих показателей в группе НК на 41,1% (p<0,05) и 39,3% (p<0,05) соответственно (рис. 8). Также было установлено уменьшение содержания в крови АИФ в данных группах животных на 31,0% (p<0,05) и 27,4% (p<0,05) соответственно (рис. 9).
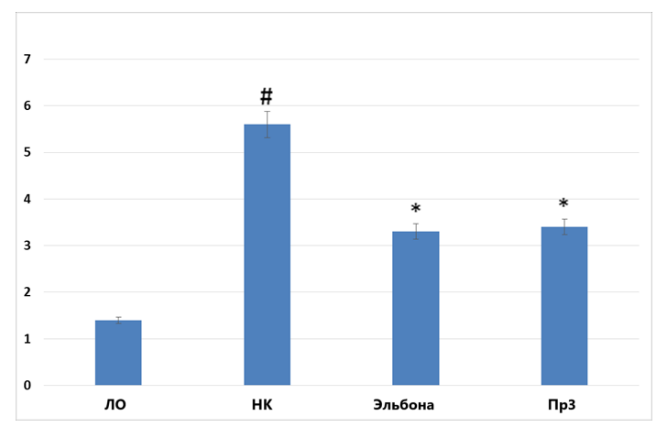
Рисунок 8. Влияние препаратов, содержащих глюкозамин, на концентрацию МДА у крыс с экспериментальным артритом
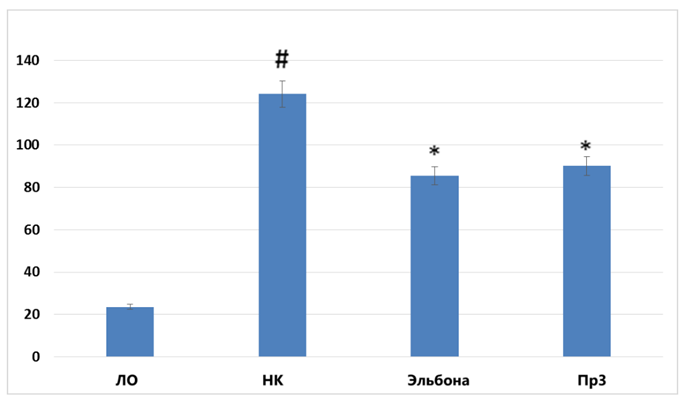
Рисунок 9. Влияние препаратов, содержащих глюкозамин, на концентрацию АИФ у крыс с экспериментальным артритом
Выраженность отечности конечностей при применении препаратов Эльбона и Пр3 была статистически значимо ниже, чем в группе НК - на 46,7% (p<0,05) и 46,7% (p<0,05) соответственно (рис. 10). Следует отметить, что статистически значимых отличий между группами животных, которым вводили препараты Эльбона и Пр3, при анализе всех исследуемых показателей, установлено не было.
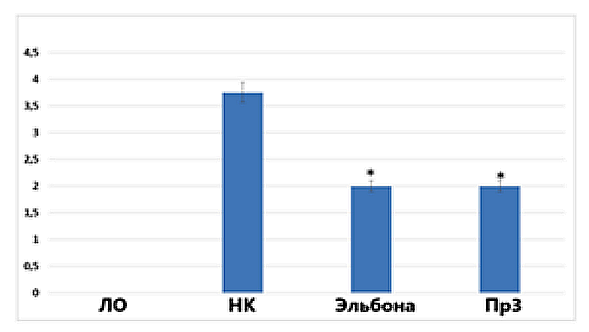
Рисунок 10. Влияние препаратов, содержащих глюкозамин, на выраженность отека лап у крыс с экспериментальным артритом
Полученные данные свидетельствуют о выраженной способности изменять течение острого экспериментального артрита препаратов группы SYSADOA.Результаты проведенного исследования продемонстрировали, что применение у животных с экспериментальным артритом препарата Элтуфлоп Био сопоставимо по своей эффективности с препаратами Пр1 и превосходит препарат Пр2 по выраженности угнетения процессов воспаления (снижение концентрации ИЛ-6 и ФНО-α), резорбции хрящевой ткани (снижение содержания ММР-2 и ММР-9), апоптоза (концентрация АИФ), окислительного стресса (содержание МДА). Улучшение со стороны биохимических маркеров сопровождалось клиническим улучшением в виде уменьшения выраженности отека, обусловленного экспериментальным артритом. Глюкозамин-содержащие препараты Эльбона и Пр3 у животных с экспериментальных артритом продемонстрировали сопоставимый уровень активности.
Заключение
Имеющиеся результаты позволяют рассматривать препараты Элтуфлоп и Эльбона в качестве долговременной терапии больных с хроническими суставно-мышечными болевыми синдромами, обусловленными остеоартритом различной локализации, в том числе, у пациентов с различными формами дорсалгии.
Литература
- Global, regional, and national burden of low back pain, 1990–2020, its attributable risk factors, and projections to 2050: a systematic analysis of the Global Burden of Disease Study 2021 GBD 2021 Low Back Pain Collaborator. Lancet Rheumatol 2023; 5: e316–29.
- de Luca K., Tavares P., Yang H. et al. Spinal Pain, Chronic Health Conditions and Health Behaviors: Data from the 2016-2018 National Health Interview Survey. Int J Environ Res Public Health. 2023 Apr 3;20(7):5369. DOI: 10.3390/ijerph20075369
- Ko S, Vaccaro AR, Lee S, Lee J, Chang H. The prevalence of lumbar spine facet joint osteoarthritis and its association with low back pain in selected Korean populations. Clin Orthop Surg. 2014;6(4):385–391. doi:10.4055/cios.2014.6.4.385
- Du R., Xu G., Bai X., Li Z.Facet Joint Syndrome: Pathophysiology, Diagnosis, and Treatment. Journal of Pain Research 2022:15 3689–3710.
- Максимова М.Ю., Котляр Я.А., Шабалина А.А. Показатели системы цитокинов и неоангиогенеза в крови при острой дискогенной пояснично-крестцовой радикулопатии у пациентов молодого возраста. Российский неврологический журнал. 2022;27(5):51–58. [Maksimova M.Yu., Kotlyar Ya.A., Shabalina A.A. Indicators of the cytokine system and neoangiogenesis in the blood in acute discogenic lumbosacral radiculopathy in young patients. Russian Neurological Journal. 2022;27(5):51-58. (In Russ.)]. DOI. 10.30629/2658-7947-2022-27-5-51-5.]
- Новикова А. В., Правдюк Н. Г., Саклакова В. С. и др. Дегенеративная болезнь диска у молодых: цитокиновый профиль и факторы ангиогенеза. Вестник РГМУ. 202; 16: 81-89. [Novikova A.V., Pravdyuk N. G., Saklakova V. S. and others. Degenerative disc disease in young people: cytokine profile and angiogenesis factors. Bulletin of the Russian State Medical University. 202; 16: 81-89. (In Russ.)].
- Имаметдинова Г.Р., Чичасова Н.В. Хондроитина сульфат при заболеваниях опорно-двигательного аппарата: эффективность и безопасность с позиций доказательной медицины. РМЖ. 2016;22:1481-1488. [Imametdinova G.R., Chichasova N.V. Chondroitin sulfate in diseases of the musculoskeletal system: efficacy and safety from the standpoint of evidence-based medicine. RMZh. 2016;22:1481-1488. (In Russ.)].
- Martel-Pelletier J, Farran A, Montell E, et al. Discrepancies in composition and biological effects of different formulations of chondroitin sulfate. Molecules. 2015;20(3):4277-4289. doi: 10.3390/molecules20034277
- Алексеева Л.И., Аникин С.Г., Зайцева Е.М. и др. Исследование эффективности, переносимости и безопасности препарата Хонрогард у пациентов с остеоартрозом. Фарматека. 2013;7(260):58-62. [Alekseeva L.I., Anikin S.G., Zaitseva E.M. et al. To study the efficacy, tolerability and safety of Honrogard in patients with osteoarthritis. Pharmateca. 2013;7(260):58-62. (In Russ.)].
- Барулин А.Е., Курушина О.В. Хондропротекторы в комплексной терапии болей в спине. РМЖ. 2013;21(30):1543-1549. [Barulin A.E., Kurushina O.V. Chondroprotectors in the complex therapy of back pain. RMJ. 2013;21(30):1543. (In Russ.)].
- Данилов Ал.Б., Лила А.М., Маджидова Ё.Н. и др. Фармаконутрицевтик Хондрогард®ТРИО для профилактики заболеваний опорно-двигательного аппарата и нутритивной поддержки пациентов с остеоартритом и неспецифической болью в спине: оценка клинических возможностей. Резолюция Первого мультидисциплинарного двустороннего экспертного совета Россия – Узбекистан. Неврология, нейропсихиатрия, психосоматика. 2023;15(2):134–146 [Danilov AlB, Lila AM, Majidova YoN, et al. Pharmaconutraceutical Chondrogard®TRIO for the prevention of musculoskeletal diseases and nutritional support for patients with osteoarthritis and nonspecific back pain: an assessment of clinical options. Resolution of the First Multidisciplinary Bilateral Russia – Uzbekistan Expert Council. Nevrologiya, neiropsikhiatriya, psikhosomatika = Neurology, Neuropsychiatry, Psychosomatics. 2023;15(2):134–146. (In Russ.)]. DOI: 10.14412/2074-2711-2023-2-134-146
- Новиков В. Е. Хондропротекторы. Обзоры по клинической фармакологии и лекарственной терапии. 2010; 8(2): 41-47. [Novikov V. E. Chondroprotectors. Reviews of clinical pharmacology and drug therapy. 2010; 8(2): 41-47. (In Russ.)].
- David-Raoudi M, Mendichi R, Pujol JP. For intra-articular delivery of chondroitin sulfate. Glycobiology. 2009;19(8):813-815. doi:10.1093/glycob/cwp069.
- Буйлова Т.В. Открытое рандомизированное исследование эффективности и безопасности препарата Хондроксид в комплексном лечении больных с хронической вертеброгенной люмбоишалгией. РМЖ. 2010;17:1678-1686. [Builova T.V. An open randomized study of the efficacy and safety of the drug Chondroxide in the complex treatment of patients with chronic vertebrogenic lumboishalgia. RMJ. 2010;17:1678-1686. (In Russ.)].
- Chen L, Ling PX, Jin Y, Zhang TM. Hyaluronic acid in combination with chondroitin sulfate and hyaluronic acid improved the degeneration of synovium and cartilage equally in rabbits with osteoarthritis. Drug Discov Ther. 2011;5(4):190-194. doi:10.5582/ddt.2011.v5.4.190
- Алексеева Л. И., Шарапова Е. П. Хондроитин сульфат в лечении остеоартроза. РМЖ. 2009; 17(21): 1448–1453. [Alekseeva L. I., Sharapova E. P. Chondroitin sulfate in the treatment of osteoarthritis. RMJ. 2009; 17(21): 1448-1453. (In Russ.)].
- McAlindon T.E., LaValley M.P., Gulin J.P., Felson D.T. Glucosamine and chondroitin for treatment of osteoarthritis: a systematic quality assessment and meta–analysis. JAMA. 2000. Mar 15; 283(11): 1469–1475.
- Основина И.П., Алексеева Н.В., Герасименко М.Ю. Трансдермальный магнитофорез хондропротектора при остеоартрите коленных суставов. Вопросы куротоолгии, физиотерапия и лечебной физкультуры. 2020; 97(1):42-50. [Osnovina I.P., Alekseeva N.V., Gerasimenko M.Yu. Transdermal magnetophoresis of the chondroprotector in osteoarthritis of the knee joints. Vopr. Kurortol Fizioter Lech Fiz Kult. 2020; 97(1):42-50. (In Russ.)]. doi: 10.17116/kurort20209701142.
- Наумов А.В., Шаров М.Н., Ховасова Н.О., Прокофьева Ю.С. Результаты применения интермиттирующей схемы парентерального введения хондроитина сульфата и глюкозамина сульфата в старт-терапии хронической боли в суставах и спине у коморбидных пациентов. РМЖ. 2018;4(II):47-54. [Naumov A.V., Sharov M.N., Khovasova N.O., Prokofieva Y.S. Results of the use of an intermittent parenteral regimen of chondroitin sulfate and glucosamine sulfate in the start-up therapy of chronic joint and back pain in comorbid patients. RMJ. 2018;4(II):47-54. (In Russ.)].
- FDA Estimating the Maximum Safe Starting Dose in Initial Clinical Trials for Therapeutics in Adult Healthy Volunteers. 2005. https://www.fda.gov/regulatory-information/search-fda-guidance-documents/estimating-maximum-safe-starting-dose-initial-clinical-trials-therapeutics-adult-healthy-volunteers
- Choudhary N, Bhatt LK, Prabhavalkar KS. Experimental animal models for rheumatoid arthritis. Immunopharmacol Immunotoxicol. 2018;40(3):193-200. doi:10.1080/08923973.2018.1434793
- Hajizadeh A, Abtahi Froushani SM, Tehrani AA, et al. Effects of Naringenin on Experimentally Induced Rheumatoid Arthritis in Wistar Rats. Arch Razi Inst. 2021 Oct 31;76(4):903-912. doi:10.22092/ari.2020.351612.1527.
- Стальная И.Д., Гаришвили Т.Г. Метод определения малонового диальдегида с помощью ТБК. Современные методы в биохимии /под. ред. Ореховича В.Н. М.: Медицина. 1977 – С. 44-46. [Stalnaya I.D., Garishvili T.G. Method of determination of malondialdehyde using TBK. Modern methods in biochemistry / ed. Orekhovich V.N. M.: Medicine. 1977: 44-46. (In Russ.)].
Anti-inflammatory and chondroprotective properties of Elbon and Eltuflop BIO preparations - results of an experimental study
P.R. Kamchatnov1,2, A.V. Chugunov1,3, A.A. Kabanov1, N.D. Malashenkov4, A.Yu. Kazakov1
1 Russian National Research Medical University named after. N.I. Pirogov, Russia, Moscow;
2 V.M. Buyanov City Clinical Hospital na, Moscow, Russia;
3 Research Institute of Healthcare Organization and Healthcare Management of the Moscow, Moscow, Russia
4 GBUZ "Research Institute of Emergency Medical Care named after N.V. Sklifosovsky of the Moscow City Health Department ", Moscow, Russia
Summary
The purpose of the study. To conduct an experimental assessment of the comparability of the action of SYSADOA.
Material and methods. The study was performed on 70 mature male Wistar rats (body weight 200-220 g). The arthritis model was created by introducing type II collagen and an incomplete Freund adjuvant in a ratio of 1:l. The drugs Eltuflop BIO and two medicines - bioactive concentrates from small marine fish (Pr1 and Pr2) and Elbona and glucosamine (Pr3) were administered to animals for 14 days from the moment of arthritis modeling. The concentration of TNF-α and IL-6 was determined in the blood serum. Concentrations of MMP-9, MMP-2, MDA and AIF were determined in the art. tarsocruralis homogenate.
Results. The use of Elflutop Bio in animals with experimental arthritis is comparable in its effectiveness with Pr1 preparations and surpasses Pr2 in terms of the severity of inhibition of inflammatory processes (decrease in IL-6 and TNF-α concentrations), cartilage resorption (decrease in MMP-2 and MMP-9), apoptosis (AIF concentration), oxidative stress (MDA content). Improvement on the part of biochemical markers was accompanied by clinical improvement in the form of a decrease in the severity of edema. Glucosamine-containing preparations of Elbona and Pr3 demonstrated a comparable level of activity.
Conclusion. The available results allow us to consider Elflutop and Elbona drugs as long-term therapy for patients with chronic musculoskeletal pain syndromes caused by osteoarthritis of various localization.
Keywords: arthritis, Eltuflop BIO, glucosamine, Elbona, chondroitin sulfate, treatment.
Kamchatnov P.R. - orcid.org/0000-0001-6747-3476
Chugunov A.V. - orcid.org/0000-0003-4506-8095
Kabanov A.A. - orcid.org/0000-0002-8684-8058
Kazakov A.Yu. - orcid.org 0000-0003-2367-545X
Malashenkov N.D. - https://orcid.org/0000-0001-7334-7820