Консенсус врачей-экспертов «О применении препаратов на основе полинуклеотидов для инъекционной терапии патологии верхней конечности, нижней конечности и позвоночника
СтатьиБогатов В.Б., Девальд И.В., Пастель В.Б., Колесников Я.Г., Чанцев А.В.
Резюме: Полинуклеотиды (ПН; препараты ДНК) используются в медицине уже более 20 лет. Популярность использования ПН в качестве лечебной опции обусловлена не только их безопасностью, но и плейотропными биологическими эффектами. Для определения общего подхода к терапии ПН, уточнения нюансов использования при различных ортопедических патологиях был созван Экспертный совет практикующих специалистов, результатом работы которого стало формирование Консенсуса. В нем обозначены основные принципы использования ПН для локальной инъекционные терапии, режимы введения, возможности использования с другими препаратами, ограничения и противопоказания к применению. Информация, представленная в Консенсусе, может быть полезна коллегам травматологов-ортопедов — ревматологам, неврологам.
Ключевые слова: полинуклеотиды, гиалуроновая кислота, нестероидные противовоспалительные препараты, остеоартрит, синовит, периоперационное ведение, импиджмент-синдром.
Для цитирования: Богатов В.Б., Девальд И.В., Пастель В.Б., Колесников Я.Г., Чанцев А.В. Консенсус врачей-экспертов «О применении препаратов на основе полинуклеотидов для инъекционной терапии патологии верхней конечности, нижней конечности и позвоночника». РМЖ. 2024;3:53-60.
Введение
Полинуклеотиды (ПН) являются проприетарным и зарегистрированным препаратом, производным ДНК. Это смесь дезоксирибонуклеотидов с молекулярной массой 50–1500 кДа. Их получают из ДНК молок Oncorhynchus mykiss (японский лосось) или Oncorhynchus keta (кета). Самая часто встречаемая фракция имеет молекулярную массу от 80 до 200 кДа (пик распределения по Гауссу составляет 132 кДа). ПН экстрагируют и очищают при высокой температуре с помощью процедуры, которая позволяет восстанавливать более 95% чистой активной субстанции при инактивации белков и пептидов. Это гарантирует безопасность продукта и отсутствие любых иммунологических нежелательных реакций [1].
Лечебные свойства фрагментов ДНК (полидезоксирибонуклеотиды и ПН) малой и средней молекулярной массы уже более 20 лет используются различными медицинскими специалистами во всем мире.
Хирурги применяют их локально для ускорения заживления ран и трофических язв (диабетических [2], артериальных [3], венозных [4], пролежней [5]); неврологи и нейрохирурги вводят их периневрально при мононевропатиях [6] и плексопатиях [7], а также эпидурально [8]; гинекологи и андрологи используют для улучшения качества кожи и слизистых половых органов при возрастных изменениях [9], воспалительной патологии [10] и после операций [11]; дерматокосметологи и пластические хирурги — для лечения патологии кожи [12], в качестве патогенетического и симптоматического лечения старения кожи [13–15], решения проблем волосяных луковиц [16], приживления кожных трансплантатов [17–19] и улучшения косметических рубцов [20, 21].
Популярность использования фрагментов ДНК в качестве лечебной опции обусловлена не только их безопасностью (молекулы ДНК универсальны для всех эукариотических организмов, а фрагменты ДНК, являясь сигнальными молекулами, определяются во всех тканях и жидкостях организма человека), но и их плейотропными биологическими эффектами.
Сами по себе фрагменты ДНК являются молекулами «клеточной тревоги», ведь их концентрация в тканях и жидкостях тела повышается при повреждении ядер клеток. Повышение концентрации ПН — естественный универсальный стимул репаративных процессов как ответа на повреждение. Фрагменты ДНК средней молекулярной массы благодаря большому количеству водородных связей обладают осмотической силой и, притягивая молекулы воды, могут способствовать восстановлению реологических свойств различных жидкостей тела [22]. Данные молекулы из-за небольшой молекулярной массы и гидрофильности обладают высокой биодоступностью.
Фрагменты ДНК, будучи донорами водорода, способны инактивировать реактивные формы кислорода и другие активные радикалы, т. е. обладают антиоксидантной активностью. После введения в организм экзогенные фрагменты ДНК подвергаются воздействию ферментов (эндо- и экзонуклеазы), расщепляясь до мононуклеотидов, нуклеозидов и азотистых оснований. Эти низкомолекулярные соединения легко проникают даже в плотные ткани, диффундируя на расстояния, измеряемые в сантиметрах от места введения. Продукты гидролиза ДНК активируют мембранные рецепторы (рецепторы аденозина наиболее изучены на сегодняшний день) и после каскадов внутриклеточного сигналинга [23] изменяют экспрессию генов [1]. Основными эффектами изменения экспрессии генов после активации мембранных рецепторов являются антикатаболический, анаболический, гуморальный и клеточный противовоспалительный, модулирующий ангиогенез.
Локальная инъекционная терапия ПН много лет используется ортопедами-травматологами. В тканях опорно-двигательного аппарата фрагменты ДНК демонстрируют безопасность и высокую эффективность. Имеются данные, подтверждающие положительные свойства ПН при патологии костной [24], хрящевой [22], синовиальной [25], плотной волокнистой соединительной [25] и жировой [26, 27] тканей.
Клиницист принимает решение об использовании инъекционных ПН на основе знаний об этиопатогенезе заболеваний опорно-двигательного аппарата, понимания эффектов, на которые он может рассчитывать после введения ПН, а также после многофакторного анализа субъективных и объективных данных о суставной патологии и сопутствующих заболеваниях конкретного пациента.
Эффекты ПН
- Улучшение реологии синовиальной жидкости (СЖ) за счет онкотической силы и формирования 3D-геля в полости сустава.
- Антикатаболический эффект в суставных тканях, проявляющийся в ограничении зоны некроза за счет антиоксидантного действия, предотвращении апоптоза, уменьшении экспрессии генов и снижении активности матриксных металлопротеиназ, что способствует лучшей выживаемости клеток, поддерживает клеточный пул и улучшает прогноз.
- Анаболический эффект, являющийся следствием усиления экспрессии генов факторов роста (фибробластических и эпидермального, инсулиноподобного фактора роста 1, фактора роста соединительной ткани), проявляется в тканях опорно-двигательного аппарата в активации синтеза компонентов внеклеточного матрикса, как фибриллярных, так и нефибриллярных. ПН также являются митогенами и в тканях с наличием клеток, способных к делению, могут увеличивать и поддерживать клеточный пул за счет пролиферативного эффекта, что также позволяет рассчитывать на улучшение прогноза.
- Противовоспалительный эффект, являющийся следствием активации продуктами ферментативного гидролиза ПН аденозиновых рецепторов на мембранах лейкоцитов (макрофагов, нейтрофилов, Т- и В-лимфоцитов), а также изменения экспрессии генов провоспалительных (↓ИЛ-1, ИЛ-6, ИЛ-8, ФНО-α, HMBG-1↓) и противовоспалительных (↑ИЛ-10, ИЛ-12↑) цитокинов.
- Эффект модуляции ангиогенеза, являющийся следствием усиления экспрессии генов сосудисто-эндотелиальных факторов роста и проявляющийся в виде вазодилатации и увеличения оксигенации тканей сустава, а также неоангиогенеза (и кровеносного, и лимфатического) в васкуляризированных тканях.
Мировое врачебное сообщество располагает данными о положительных результатах внутрисуставного введения ПН при лечении патологии плечевого [28], коленного [29–31], тазобедренного [32–34], голеностопного [35] суставов, а также околосуставных мягких тканей: ротаторной манжеты [36–38], эпикондилитов [39–41], тендинита «гусиной лапки» [42], плантарного фасциита [43], других энтезопатий верхних и нижних конечностей [44], поражений мягких тканей у пациентов с ревматоидным артритом [45], при лечении аваскулярного остеонекроза [46].
Несмотря на то, что результаты применения ПН при целом ряде патологий ограничены описанием отдельных клинических наблюдений, по мере накопления опыта использования ПН в ортопедо-травматологической практике появляется возможность систематизации данных в рамках систематических обзоров и метаанализов [47–49].
Для оценки эффективности лечения неоднократно проводились прямые сравнения терапии ПН с консервативным лечением [36, 41], плацебо-инъекциями [43], введением местных анестетиков [50], озонотерапией [51], пролотерапией [40], инъекциями глюкокортикостероидов (ГКС) [28], обогащенной тромбоцитами плазмы (Platelet Rich Plasma, PRP) [52, 53], линейной [54, 55] и поперечносшитой [56, 57] гиалуроновой кислотой (ГК) при различных суставных патологиях.
По данным литературы, комбинация внутрисуставного введения ПН и препаратов ГК в некоторых случаях остеоартрита (ОА) коленного сустава может быть более эффективна, чем введение только ГК или только ПН [58–61], вероятно, из-за взаимного усиления и продления терапевтических эффектов.
В последние годы ведутся изыскания относительно комбинации внутрисуставного и околосуставного введения ПН со стволовыми клетками [62] и физиотерапевтическим лечением [63, 64], в том числе после операций, но пока положительные эффекты этих комбинированных методик лечения показаны в исследованиях на животных.
Полинуклеотиды в мире разрешены для внутримышечного, внутрисуставного, околосуставного, периневрального, эндолюмбального введения. Зарегистрированные в Российской Федерации медицинские изделия на основе ПН разрешены для внутрисуставного применения в ортопедии, а также для внутрикожного и подкожного применения в эстетической медицине с 18 лет. Однако стоит отметить, что у некоторых отечественных специалистов имеется положительный личный опыт применения ПН off-label (как околосуставного введения, так и применения у пациентов младше 18 лет).
Для создания общего подхода к терапии ПН, уточнения нюансов использования при различных ортопедических патологиях в феврале 2023 г. в Москве был созван экспертный совет врачей, который сформировал Консенсус.
Редакторами Консенсуса выступили:
Богатов Виктор Борисович — д.м.н., профессор кафедры травматологии, ортопедии и хирургии катастроф ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), практикующий ортопед-травматолог (Москва);
Девальд Инесса Валерьевна — к.м.н., доцент кафедры ИДПО ФГБОУ ВО ЮУГМУ
Минздрава России, ревматолог, врач ультразвуковой диагностики, терапевт высшей категории, ООО «Клиника профессора Кинзерского» (Челябинск);
Пастель Владимир Борисович — к.м.н., врач-ортопед, артролог, врач высшей категории, главный врач Клиники Музалевского (Саратов);
Колесников Ян Геннадьевич — врач-хирург, ортопед, врач ультразвуковой диагностики, Институт хирургической коррекции и восстановления, преподаватель-исследователь, член РОХ, АТОР, ICRS, ESVS (Москва);
Чанцев Александр Вениаминович — к.м.н., доцент кафедры травматологии и ортопедии ФГБОУ ВО АГМУ Минздрава России (Барнаул).
Общие подходы к применению ПН
- Локальная инъекционная терапия (ЛИТ) с применением ПН может быть как единственным методом лечения, так и компонентом комплексного лечения с использованием оптимального спектра немедикаментозных и медикаментозных коррекций.
- Перед проведением ЛИТ целесообразна комплексная диагностика: сбор жалоб, анамнеза, физикальный осмотр, лабораторная диагностика, а также инструментальные методы обследования (рентгенография, УЗИ, компьютерная томография и др.) с целью определения фенотипа заболевания, а также уточнения анатомической локализации и объема повреждения тканей сустава.
- Возраст 18+. Исключение (оff-label) — дети-спортсмены (с 12 лет)1.
- Суставы, не несущие вес тела: мелкие суставы кистей, лучезапястный, локтевой, плечевой, акромиально-ключичный и грудино-ключичный суставы, височно-нижнечелюстной, реберно-позвоночные и дугоотростчатые суставы, мелкие суставы переднего отдела стопы, пателлофеморальный сустав, проксимальный межберцовый и суставы, несущие вес тела: крестцово-подвздошное сочленение, тазобедренный, бедренно-большеберцовый, надтаранный и подтаранный суставы, суставы Шопара, Лисфранка и межклиновидные суставы стопы в зависимости от степени повреждения — являются перспективными для лечения ПН.
- Клиническую выгоду от введения ПН получат пациенты с патологией не только костной и хрящевой тканей, но и других внутрисуставных тканей, не требующих оперативного лечения, как, например, при частичном повреждении:
- фиброзно-волокнистого хряща: мениска, суставной губы, диска, треугольного фиброзно-хрящевого комплекса, менискоида;
- капсульно-связочного аппарата: медиальной коллатеральной и передней крестообразной связок в коленном суставе, верхней плечелопаточной и клювовидно-плечевой связок в плечевом суставе, дельтовидной связки и латерального связочного комплекса голеностопного сустава (ГСС); мышечно-сухожильных структур: удерживателей надколенника, подколенного сухожилия, сухожилий ротаторной манжеты, сухожилия длинной головки бицепса плеча;
- жировых тел: жировой ткани в центре вертлужной впадины тазобедренного сустава, наднадколенниковых жировых подушек, тела Гоффа в коленном суставе, клетчатки Кагера в ГСС, жировых тел в венечной и локтевой ямках в локтевом суставе.
- Предпочтительны инъекции в «сухой» сустав. Даже если выпот небольшой, до 10 мл, необходимо выяснить, с чем связано увеличение количества СЖ, перед проведением ЛИТ. После введения ПН рекомендовано избегать тепловых процедур на протяжении трех дней и местного применения различных мазей.
- Целесообразность использования ПН выше при небольшой степени анатомических изменений (ранний ОА I–II стадии по Kellgren — Lawrence, «перегрузочные» болевые синдромы без выраженных анатомических изменений, дегенеративные изменения, частичные повреждения мягких тканей, не требующие оперативного лечения).
- Использование ЛИТ вообще и внутрисуставное введение ПН в частности возможно в периоперационном периоде. В комплексе мер по подготовке пациента к плановой операции возможно использование ПН для улучшения функции сустава и переносимости реабилитационных мероприятий, но завершающее введение должно быть выполнено не позднее чем за 6 мес. до даты оперативного лечения. Введение ПН после операции с целью облегчения реабилитационных мероприятий, усиления регенеративных процессов, профилактики посттравматического ОА, а также с противовоспалительной целью возможно после разрешения гемартроза (как правило, через 14 дней после операции).
- При наличии показаний к ЛИТ нескольких анатомических локализаций у одного пациента возможно в асептических условиях разделить препарат ПН из одного преднаполненного шприца для введения в разные зоны во время одной инъекционной процедуры. Остатки препарата подлежат утилизации. Хранить невведенный препарат запрещается.
- Внутрисуставное введение — основной путь введения ПН согласно инструкции. Количество введений ПН в лечебном курсе в большинстве случаев — не менее двух.
- В случае выраженного воспаления перед введением ПН целесообразна противовоспалительная терапия (системное прекондиционирование) не менее 7 дней.
- Перед введением ПН следует оценить интенсивность болевого синдрома и амплитуду движений в суставе, подлежащем лечению. В случае отсутствия положительной динамики болевого синдрома и прироста амплитуды движений после двух введений третье и последующие введения нецелесообразны.
- В случае отчетливого положительного эффекта в отношении боли и функции курсы инъекционного лечения целесообразно повторять 1 раз в 6–12 мес., даже при отсутствии симптоматики, в том числе с целью воздействия на прогноз заболевания.
- При ревматологическом заболевании введение ПН возможно только в период ремиссии. Ремиссия должна быть стойкой, не менее 6 мес.
Использование ПН при различных патологиях
Полный консенсус
Подакромиальный импиджмент-синдром, частичное повреждение, тендиноз сухожилий вращательной манжеты плеча, поддельтовидно-подакромиальный бурсит(при отсутствии показаний к операции или при противопоказаниях/невозможности/отказе от оперативного лечения)
- Применение ПН показано.
- Введение ПН по 2,0 мл в полость плечевого сустава 2–4 раза на курс.
- Интервал между введениями — 5–10 дней.
- Суммарная доза действующего вещества — от 80 мг на курс.
- При значительных объемах повреждения мягких тканей применение ПН также оправданно в качестве адъювантной терапии после реконструктивного оперативного вмешательства на структурах ротаторной манжеты. Целесообразна интеграция ЛИТ в реабилитационный протокол в режиме, аналогичном вышеуказанному.
Омартроз (остеоартроз плечевого сустава, остеоартроз плечелопаточного сустава)
- Применение ПН показано.
- Введение ПН по 2,0 мл 2–4 раза на курс.
- Интервал между введениями — 5–10 дней.
- Суммарная доза действующего вещества — от 80 мг на курс.
Остеоартрит локтевого сустава, ОА лучезапястного сустава (ОА луче-/локтезапястного сустава, ОА среднезапястного сустава, ОА запястно-пястного сустава)
- Применение ПН показано.
- Введение ПН по 1,0–2,0 мл 2–4 раза на курс.
- Интервал между введениями — 5–10 дней.
- Суммарная доза действующего вещества — от 40 мг на курс.
Гонартроз (ОА коленного сустава)
- Применение ПН показано.
- Наилучший инъекционный доступ в коленный сустав — латеральный средне-/верхненадколенниковый.
- Введение ПН по 2,0–4,0 мл 3–5 раз на курс.
- Возможно использование комбинации 2,0 мл ПН и любого из препаратов линейной ГК или поперечносшитой ГК 2–4 раза на курс (одновременное либо последовательное введение ПН, затем ГК).
- Интервал между введениями — 5–14 дней.
- Суммарная доза действующего вещества — от 80 мг на курс.
Тактика ведения пациентов с воспалением коленного сустава
Каждый пациент с признаками воспаления тканей коленного сустава должен быть обследован для исключения аутоиммунного, инфекционного и других процессов, ограничивающих введение ПН.
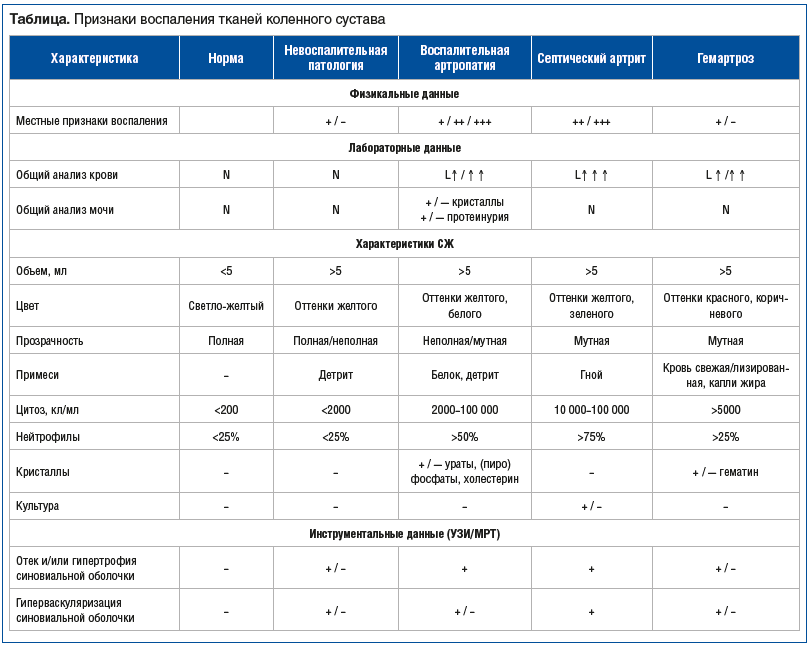
- Базовые методики обследования для дифференциальной диагностики синовита:
- физикальное обследование (местные признаки воспаления: болезненный отек области сустава, локальная гиперемия и гипертермия кожных покровов);
- лабораторная диагностика: общий анализ крови, общий анализ мочи, СОЭ, концентрация мочевой кислоты, С-реактивного белка, ревматоидного фактора и антител к цитруллинированным пептидам в плазме крови, а также характеристики СЖ: объем, цвет, прозрачность, примеси, микроскопия с оценкой цитоза, наличия микрокристаллов, результаты посева;
- инструментальные данные (утолщение вследствие отека и/или гипертрофии синовиальной оболочки, гиперваскуляризация по результатам УЗИ и/или МРТ с контрастным усилением или без него) (см. таблицу).
- В случаях гнойного артрита ЛИТ не показана.
- В случаях гемартроза ЛИТ с использованием ПН не показана.
- В случаях воспалительной артропатии ЛИТ с использованием ПН возможна.
- В случаях невоспалительной патологии ЛИТ с использованием ПН показана.
- Всем пациентам с признаками синовита, наличием непрозрачной синовиальной жидкости в случаях, когда объем СЖ превышает 20 мл, перед проведением ЛИТ с использованием ПН показана комплексная противовоспалительная терапия на основе местного и системного применения нестероидных противовоспалительных препаратов (НПВП) длительностью не менее 7–14 дней после аспирации содержимого полости сустава и лабораторного исследования СЖ.
- Пациентам с сохраняющимися признаками синовита, наличием непрозрачной СЖ и/или ее объема, превышающего 20 мл, после завершения противовоспалительной терапии на основе НПВП показана консультация ревматолога и после аспирации содержимого полости сустава возможно однократное внутрисуставное введение ГКС.
- Пациентам с очевидной положительной динамикой со стороны синовиальной оболочки, прозрачной СЖ объемом до 20 мл после проведенной противовоспалительной терапии показано введение ПН по вышеуказанной схеме (как пациентам без признаков синовита). Во время следующего визита пациента для очередной процедуры ЛИТ целесообразно повторно оценить состояние синовиальной оболочки, прозрачность и объем СЖ. В случае отсутствия отрицательной динамики курс ПН и ЛИТ стоит продолжить. В случае отрицательной динамики по любому из показателей курс ПН и ЛИТ следует прервать для дообследования и пересмотра лечебной тактики.
«Изолированный» пателлофеморальный артроз
(ОА бедренно-надколенникового сустава)
- Введение ПН показано.
- По 2,0–4,0 мл на каждое введение.
- 3–5 введений на курс с интервалом в 5–10 дней.
- Суммарная доза действующего вещества — от 120 мг на курс.
Частичный консенсус
- Адгезивный капсулит плечевого сустава
- Применение ПН возможно на всех стадиях капсулита.
- Возможно введение ПН per se по 2,0–4,0 мл с интервалом 5–10 дней 2–3 раза на курс.
- Суммарная доза действующего вещества — от 80 мг на курс.
- Также курс ПН возможно предварить однократным введением ГКС длительного действия (например, 1,0 мл бетаметазона) в большом объеме слабоконцентрированного раствора местного анестетика (например, 0,25% прокаина или 1% лидокаина) внутрисуставно и околосуставно. В этом случае введение ПН начинается через 10–21 день от введения ГКС.
- Наибольшее значение в лечении адгезивного капсулита имеет мультимодальная физическая реабилитация, а ЛИТ должна быть интегрирована в реабилитационный протокол.
Спондилоартроз (ОА дугоотростчатого сустава)
- Применение ПН возможно.
- Для увеличения эффективности терапии введение целесообразно осуществлять под ультразвуковым, рентгеновским или компьютерно-томографическим контролем.
- Введение ПН по 0,5–1,0 мл 3–5 раз на курс с интервалом в 5–10 дней.
- Суммарная доза действующего вещества — от 30 мг для каждого отдельного сустава на курс.
Остеоартрит крестцово-подвздошного сочленения (КПС)
- Применение ПН возможно.
- Для увеличения эффективности терапии введение необходимо осуществлять под ультразвуковым, рентгеновским или компьютерно-томографическим контролем.
- Введение ПН по 1,0–2,0 мл 3–5 раз на курс с интервалом в 5–10 дней.
- Суммарная доза действующего вещества на курс — от 60 мг для одного КПС с одной стороны.
Коксартроз (ОА тазобедренного сустава)
Применение ПН возможно.
- Необходим ультразвуковой, рентгеновский или компьютерно-томографический контроль внутрисуставного введения.
- Предпочтительным следует признать передний инъекционный доступ.
- Введение ПН по 2,0–4,0 мл 3–5 раз на курс.
- Возможно использование комбинации 2,0 мл ПН и 2,0–3,0 мл линейной ГК с молекулярной массой 1,0–2,5 МДа 2–4 раза на курс (либо последовательное введение ПН, затем ГК).
- Интервал между введениями — 5–14 дней.
- Суммарная доза действующего вещества — от 80 мг на курс.
После пластики передней крестообразной связки, шва мениска
- Применение ПН возможно. Введение целесообразно не ранее 2 нед. после операции.
- Введение ПН по 2,0–4,0 мл 2–3 раза на курс с интервалом 5–10 дней.
- Суммарная доза действующего вещества — от 80 мг на курс.
Крузартроз (ОА таранно-берцового сустава, ОА надтаранного сустава)
- Применение ПН возможно.
- Введение ПН по 1,0–2,0 мл 3–5 раз на курс.
- Интервал между введениями — 5–10 дней.
- Суммарная доза действующего вещества — от 60 мг на курс.
- Остеоартрит первого плюснефалангового сустава, на фоне hallux valgus или без такового, а также в подостром периоде после оперативного лечения hallux valgus
Применение ПН возможно.
- Введение ПН по 0,5–1,0–1,5 мл 3–5 раз на курс.
- Интервал между введениями — 5–10 дней.
- Суммарная доза действующего вещества — от 30 мг на курс.
Асептический некроз (аваскулярный остеонекроз) и его частные виды
- Основные методы лечения: при возможности устранение этиологического фактора + разгрузка, препараты кальция, витамина D, по показаниям и off-label — бисфосфонаты, обезболивание, сосудистая терапия. ЛИТ — дополнительный метод лечения.
- Локальная инъекционная терапия с использованием ПН возможна на I–II стадии асептического некроза.
- Для самых частых локализаций: коленного и тазобедренного суставов в режиме 3–5 введений по 2,0–4,0 мл с интервалом 5–10 дней. Суммарная доза действующего вещества — от 120 мг на курс.
- Локальная инъекционная терапия с использованием ПН также возможна на III–IV стадии с симптоматической целью в случае невозможности выполнения более инвазивных/радикальных вариантов лечения.
- По прошествии острого периода (при уменьшении выраженности клинических, лабораторных и инструментальных изменений остеохондрального «блока» и синовиальной оболочки) в случае позитивного исхода асептического некроза во вторичный ОА с сохранением естественной геометрии суставных поверхностей возможно использовать комбинированное внутрисуставное введение ПН и ГК в одном курсе (одновременное или последовательное введение).
- Для самых частых локализаций: коленного и тазобедренного суставов в режиме 2–4 введения по 2,0 мл ПН и 2,0–3,0 мл линейной ГК с молекулярной массой 1,0–2,5 МДа с интервалом 5–10 дней. Суммарная доза действующего вещества — от 80 мг на курс.
Энтезопатии: плантарный фасциит и пяточная шпора, деформация Хаглунда; тендиниты: эпикондилит; после операции шва сухожилий; для стимуляции сращения замедленно консолидирующихся переломов трубчатых костей
- Применение ПН возможно.
- Эксперты высказались о положительном личном опыте введения ПН в мягкие ткани при лечении пациентов с вышеуказанными патологическими состояниями.
Варианты комбинаций с ПН в одну процедуру или в одном терапевтическом курсе
Полный консенсус
- Комбинация ПН внутрисуставно с линейной ГК внутрисуставно/околосуставно; ПН и кросс-линк ГК внутрисуставно — для взаимного усиления биологических эффектов ПН и ГК.
- В случае клинических подозрений на наличие низкоинтенсивного воспаления тканей сустава, подлежащего лечению, возможно начать лечебный курс с 1–2 введений ПН (локальное прекондиционирование) и завершить его
- 1–2 введениями ГК.
- Комбинация ПН внутрисуставно и тропоколлагена внутрисуставно/околосуставно; ПН и хондроитина сульфата внутрисуставно — потенцирование регенераторного и противовоспалительного эффектов.
- Комбинация ПН с пептидами, факторами роста, витаминами, антиоксидантами, аминокислотами — для получения дополнительных эффектов, обусловленных действием последних.
Частичный консенсус
- Комбинация ПН внутрисуставно с PRP внутрисуставно/околосуставно — для скорого начала лечебного эффекта и уменьшения вероятности обострения суставной патологии от введения PRP, для пролонгации эффекта обоих средств.
- Комбинация ПН с клеточными технологиями SVF, Lipo-Stem DUO, LipoCell — улучшает выживаемость мезенхимальных стволовых клеток из жировой ткани, стимулирует пролиферацию преадипоцитов.
Консенсус не достигнут
- Комбинация ПН с местными анестетиками. В этом случае не соблюдается «Протокол проведения местного обезболивания» и возможно развитие побочных нежелательных явлений. Также есть мнение, что местные анестетики повреждают ДНК.
- Сочетание ПН и ГКС (например, бетаметазона). Есть мнение, что нет смысла в такой комбинации из-за разнонаправленного действия веществ. Большинство экспертов высказались против одновременного введения ПН и ГКС. Избежать необходимости такого сочетания помогает тщательное обследование пациента. При наличии выраженного воспалительного процесса целесообразно сначала купировать воспаление путем использования ГКС и после этого через 7–21 сут вводить ПН.
Общие противопоказания к использованию ПН (консолидированное мнение врачей)
Полный консенсус
- Аллергия, индивидуальная гиперчувствительность, непереносимость, аутоиммунные реакции на ПН и/или любой из компонентов, входящих в состав конкретного медицинского изделия.
- Системные заболевания соединительной ткани.
- Обострение любого хронического заболевания или инфекционного процесса.
- Кожные заболевания в зоне введения.
- Повышенная кровоточивость, геморрагический синдром при патологии сосудисто-эндотелиального и/или плазменного (свертывающая, противосвертывающая системы, система тромболизиса) звеньев гемостаза.
- Микрокристаллический артрит сустава, подлежащего лечению, в стадии обострения.
- Септический артрит сустава.
- Эндопротез сустава.
- Беременность и период лактации.
Частичный консенсус
- Известная онкопатология до момента снятия пациента с диспансерного наблюдения (письменное подтверждение излечения от онколога).
- Одновременный прием препаратов, блокирующих аденозиновые рецепторы.
Действия при возникновении нежелательных явлений после введения ПН
- Разгрузка конечности. Иммобилизация или ортезирование.
- Холод местно по 15–20 мин 3–5 р/сут в течение
- 3 сут.
- Короткий курс НПВП.
- Блокатор Н1-рецепторов гистамина (препарат первого выбора — хлоропирамин) в средней терапевтической дозировке, в течение трех дней.
Заключение
Данный Консенсус является первым документом, в котором структурированы и объединены научные данные и клинический опыт лечения ПН заболеваний опорно-двигательного аппарата.
Документ составлен практикующими специалистами, чей опыт может быть полезен коллегам — травматологам, ревматологам, неврологам.
Препараты на основе ПН значительно расширяют диапазон возможностей лечения пациентов ортопедо-травматологического профиля и сохраняют концептуальные подходы регенеративной медицины и ортобиологии.
Участники Экспертного совета
Доктора медицинских наук: Беляева Елена Александровна (Тула), Богатов Виктор Борисович (Москва), Теплякова Ольга Вячеславовна (Екатеринбург), Царенок Светлана Юрьевна (Чита).
Кандидаты медицинских наук: Боженко Сергей Викторович (Мурманск), Бошмаков Борис Алексеевич (Москва), Егоров Денис Игоревич (Иркутск), Видасова Елена Витальевна (Москва), Виноградова Наталья Анатольевна (Москва), Гусев Денис Сергеевич (Москва), Девальд Инесса Валерьевна (Челябинск), Демкин Сергей Анатольевич (Волгоград), Епишин Виталий Валерьевич (Северск), Качесов Антон Владимирович (Нижний Новгород), Левашева Людмила Александровна (Владивосток), Михайлов Иван Николаевич (Иркутск), Пастель Владимир Борисович (Саратов), Петрачкова Татьяна Николаевна (Иркутск), Погонченкова Дарья Александровна (Томск), Сарапулова Анастасия Викторовна (Екатеринбург), Щербаков Григорий Ильич (Кемерово), Чанцев Александр Вениаминович (Барнаул).
Ведущие врачи-специалисты: Алферов Денис Евгеньевич (Санкт-Петербург), Андреев Александр Сергеевич (Самара), Ананьев Антон Николаевич (Ижевск), Булатов Константин Александрович (Новосибирск), Волошин Олег Владимирович (Севастополь), Ганиев Тимур Сагитович (Ижевск), Гончаренко Евгений Михайлович (Новокузнецк), Карапетян Сергей Васгенович (Санкт-Петербург), Лемешкин Степан Сергеевич (Сочи), Павлюченко Алексей Юрьевич (Красноярск), Павлов Алексей Сергеевич (Самара), Сиразитдинов Саяр Дамирович (Казань), Солодовникова Лариса Викторовна (Саранск), Тукаев Руслан Салихзянович (Тюмень), Шихзагиров Арсен Загидинович (Санкт-Петербург), Фомичев Артур Андреевич (Москва).
Организатором мероприятия выступило АО «СИСТЕМА ПЛЮС».
1В связи с большой нагрузкой на суставы при занятиях спортом применение внутрисуставной ЛИТ по показаниям представляется целесообразным, так как польза в данном случае превышает риск от ее применения.
Список литературы
1. Squadrito F., Bitto A., Irrera N. et al. Pharmacological Activity and Clinical Use of PDRN. Front Pharmacol. 2017;8:224. DOI: 10.3389/fphar.2017.00224.
2. Squadrito F., Bitto A., Altavilla D. et al. The effect of PDRN, an adenosine receptor A2A agonist, on the healing of chronic diabetic foot ulcers: results of a clinical trial. J Clin Endocrinol Metab. 2014;99(5):E746–753. DOI: 10.1210/ jc.2013-3569.
3. Altavilla D., Bitto A., Polito F. et al. Polydeoxyribonucleotide (PDRN): a safe approach to induce therapeutic angiogenesis in peripheral artery occlusive disease and in diabetic foot ulcers. Cardiovasc Hematol Agents Med Chem. 2009;7(4):313–321. DOI: 10.2174/187152509789541909.
4. De Caridi G., Massara M., Acri I. et al. Trophic effects of polynucleotides and hyaluronic acid in the healing of venous ulcers of the lower limbs: a clinical study. Int Wound J. 2016;13(5):754–758. DOI: 10.1111/iwj.12368.
5. Kim J.Y., Pak C.S., Park J.H. et al. Effects of polydeoxyribonucleotide in the treatment of pressure ulcers. J Korean Med Sci. 2014;29 Suppl 3(Suppl 3):S222–227. DOI: 10.3346/jkms.2014.29.S3.S222.
6. Huh J., Shim K.S., Cho H.J. et al. Polydeoxyribonucleotide injection in the treatment of patients with carpal tunnel syndrome: Retrospective preliminary study. Medicine (Baltimore). 2019;98(41):e17522. DOI: 10.1097/MD.0000000000017522.
7. Kim J.Y., Hwang J.M., Park J.S. et al. Ultrasound-guided peri-brachial plexus polydeoxyribonucleotide injection for a patient with postherpetic brachial plexopathy: A case report. Medicine (Baltimore). 2019;98(31):e16694. DOI: 10.1097/MD.0000000000016694.
8. Kang K.N., Kim T.W., Koh J.W. et al. Effect of transforaminal epidural polydeoxyribonucleotide injections on lumbosacral radiculopathy: A case report. Medicine (Baltimore). 2017;96(25):e7174. DOI: 10.1097/MD.0000000000007174.
9. Angelucci M., Frascani F., Franceschelli A. et al. Efficacy of intradermal hyaluronic acid plus polynucleotides in vulvovaginal atrophy: a pilot study. Climacteric. 2022;25(5):490–496. DOI: 10.1080/13697137.2022.2052840.
10. Laino L. Adjuvant clinical effects of polydeoxyribonucleotide in lichen sclerosus. Eur J Dermatol. 2012;22(4):575–576. DOI: 10.1684/ ejd.2012.1769.
11. Perino A., Genova G., Vita C. et al. The pharmacologic therapy of post-cauterization and post-laser vaporization with polydeoxyribonucleotide. Ann Ostet Ginecol Med Perinat. 1990;111(6):372–378. PMID: 2102064.
12. Noh T.K., Chung B.Y., Kim S.Y. et al. Novel Anti-Melanogenesis Properties of Polydeoxyribonucleotide, a Popular Wound Healing Booster. Int J Mol Sci. 2016;17(9):1448. DOI: 10.3390/ijms17091448.
13. Jeong G.J., Ahn G.R., Park S.J. et al. A randomized, patient/evaluator-blinded, split- face study to compare the efficacy and safety of polycaprolactone and polynucleotide fillers in the correction of crow’s feet: The latest biostimulatory dermal filler for crow’s feet. J Cosmet Dermatol. 2020;19(7):1593–1599. DOI: 10.1111/jocd.13199.
14. Lee Y.J., Kim H.T., Lee Y.J. et al. Comparison of the effects of polynucleotide and hyaluronic acid fillers on periocular rejuvenation: a randomized, double-blind, split-face trial. J Dermatolog Treat. 2022;33(1):254–260. DOI: 10.1080/09546634.2020.1748857.
15. Araco A., Araco F., Raichi M. Clinical efficacy and safety of polynucleotides highly purified technology (PN-HPT®) and cross-linked hyaluronic acid for moderate to severe nasolabial folds: A prospective, randomized, exploratory study. J Cosmet Dermatol. 2023;22(1):146–155. DOI: 10.1111/jocd.15064.
16. Lee S.H., Zheng Z., Kang J.S. et al. Therapeutic efficacy of autologous platelet-rich plasma and polydeoxyribonucleotide on female pattern hair loss. Wound Repair Regen. 2015;23(1):30–36. DOI: 10.1111/wrr.12250.
17. Rubegni P., De Aloe G., Mazzatenta C. et al. Clinical evaluation of the trophic effect of polydeoxyribonucleotide (PDRN) in patients undergoing skin explants. A Pilot Study. Curr Med Res Opin. 2001;17(2):128–131. PMID: 11759182.
18. Heo J.W., Kim Y.H., Kim E.S. et al. Effect of Polydeoxyribonucleotide on Chondrocutaneous Composite Grafts Survival. Aesthetic Plast Surg. 2019;43(4):1071–1077. DOI: 10.1007/s00266-019-01400-x.
19. Segreto F., Carotti S., Marangi G.F. et al. The use of acellular porcine dermis, hyaluronic acid and polynucleotides in the treatment of cutaneous ulcers: Single blind randomised clinical trial. Int Wound J. 2020;17(6):1702–1708. DOI: 10.1111/iwj.13454.
20. Araco A., Araco F. Preliminary Prospective and Randomized Study of Highly Purified Polynucleotide vs Placebo in Treatment of Moderate to Severe Acne Scars. Aesthet Surg J. 2021;41(7):NP866–NP874. DOI: 10.1093/asj/sjab125.
21. Kim B.R., Kwon S.H., Kim J.W. et al. Postoperative Injections of Polydeoxyribonucleotide Prevent Hypertrophic Scarring After Thyroidectomy: A Randomized Controlled Trial. Adv Wound Care (New Rochelle). 2023;12(7):361–370. DOI: 10.1089/ wound.2022.0025.
22. Gennero L., Denysenko T., Calisti G.F. et al. Protective effects of polydeoxyribonucleotides on cartilage degradation in experimental cultures. Cell Biochem Funct. 2013;31(3):214–227. DOI: 10.1002/cbf.2875.
23. Giuliani A.L., Sarti A.C., Di Virgilio F. Extracellular nucleotides and nucleosides as signalling molecules. Immunol Lett. 2019;205:16–24. DOI: 10.1016/j.imlet.2018.11.006.
24. Guizzardi S., Galli C., Govoni P. et al. Polydeoxyribonucleotide (PDRN) promotes human osteoblast proliferation: a new proposal for bone tissue repair. Life Sci. 2003;73(15):1973–1983. DOI: 10.1016/s0024-3205(03)00547-2.
25. Corciulo C., Cronstein B.N. Signaling of the Purinergic System in the Joint. Front Pharmacol. 2020;10:1591. DOI: 10.3389/fphar.2019.01591.
26. Raposio E., Guida C., Coradeghini R. et al. In vitro polydeoxyribonucleotide effects on human pre- adipocytes. Cell Prolif. 2008;41(5):739–754. DOI: 10.1111/j.1365-2184.2008.00547.x.
27. Mannino F., Pallio G., Bitto A. et al. Targeting Adenosine Receptor by Polydeoxyribonucleotide: An Effective Therapeutic Strategy to Induce White-to-Brown Adipose Differentiation and to Curb Obesity. Pharmaceuticals (Basel). 2021;14(8):728. DOI: 10.3390/ph14080728.
28. Park D., Yu K.J., Cho J.Y. et al. The effectiveness of 2 consecutive intra-articular polydeoxyribonucleotide injections compared with intra-articular triamcinolone for hemiplegic shoulder pain: A STROBE-complaint retrospective study. Medicine (Baltimore). 2017;96(46):e8741. DOI: 10.1097/MD.0000000000008741.
29. Vanelli R., Costa P., Rossi S.M., Benazzo F. Efficacy of intra-articular polynucleotides in the treatment of knee osteoarthritis: a randomized, double-blind clinical trial. Knee Surg Sports Traumatol Arthrosc. 2010;18(7):901–907. DOI: 10.1007/s00167-009-1039-y.
30. Saggini R., Di Stefano A., Cavezza T. et al. Intrarticular treatment of osteoartropaty knee with polynucleotides: a pilot study with medium-term follow-up. J Biol Regul Homeost Agents. 2013;27(2):543–549. PMID: 23830403.
31. Kim Y.N., Baek J., Kim Y.H. et al. Full recovery of near complete tear of anterior cruciate ligament without surgery: a case report. Medicine (Baltimore). 2020;99(18):e19899. DOI: 10.1097/MD.0000000000019899.
32. Migliore A., Graziano E., Martín L.S.M. et al. Three-year management of hip osteoarthritis with intra-articular polynucleotides: a real-life cohort retrospective study. J Biol Regul Homeost Agents. 2021;35(3):1189–1194. DOI: 10.23812/21-178-L.
33. Antonino S., Mauro L., Geraci G. et al. Polinucleotides versus ialuronic acid in ecoguided hip infiltration: preliminary results. J Orthopaed Traumatol. 2011;12(Suppl 1):S149.
34. Tormenta S., Arduini F., Migliore A. et al. Report of results in terms of efficacy and safety for the use of Condrotide in 23 patients suffering for a monolateral hip osteoarthritis undergoing to a cycle of ultrasound- guided intra-articular injections. Poster ECR 2013:C-2250. DOI: 10.1594/ecr2013/C-2250.
35. Guelfi M., Fabbrini R., Guelfi M.G. Intra-articular treatment of knee and ankle osteoarthritis with polynucleotides: prospective case record cohort vs historical controls. J Biol Regul Homeost Agents. 2020;34(5):1949–1953. DOI: 10.23812/20-238-L.
36. Yoon Y.C., Lee D.H., Lee M.Y., Yoon S.H. Polydeoxyribonucleotide Injection in the Treatment of Chronic Supraspinatus Tendinopathy: A Case-Controlled, Retrospective, Comparative Study With 6-Month Follow-Up. Arch Phys Med Rehabil. 2017;98(5):874–880. DOI: 10.1016/j.apmr.2016.10.020.
37. Ryu K., Ko D., Lim G. et al. Ultrasound-Guided Prolotherapy with Polydeoxyribonucleotide for Painful Rotator Cuff Tendinopathy. Pain Res Manag. 2018;2018:8286190. DOI: 10.1155/2018/8286190.
38. Do H.K., Lee J.H., Lim J.Y. Polydeoxyribonucleotide injection in the patients with partial-thickness tear of supraspinatus tendon: a prospective and pilot study using ultrasound. Phys Sportsmed. 2018;46(2):213–220. DOI: 10.1080/00913847.2018.1450059.
39. Lee G.J., Park D. Usefulness of polydeoxyribonucleotide as an alternative to corticosteroids in patients with lateral epicondyitis: A case series. Medicine (Baltimore). 2018;97(20):e10809. DOI: 10.1097/MD.0000000000010809.
40. Do H.K., Yi C.H., Lim J.Y. Safety and efficacy of polydeoxyribonucleotide injections versus prolotherapy for patients with elbow epicondylitis in a randomized double-blind active-controlled trial. Ann Phys Rehab Med. 2018;61S:e144. DOI: 10.1016/j.rehab.2018.05.322.
41. Shim B.J., Seo E.M., Hwang J.T. et al. Comparison of the effectiveness of extensor muscle strengthening exercise by itself, exercise with polydeoxyribonucleotide injection, and exercise with extracorporeal shockwave therapy in lateral epicondylitis: a randomized controlled trial. Clin Shoulder Elb. 2021;24(4):231–238. DOI: 10.5397/cise.2021.00290.
42. Mun J.U., Cho H.R., Bae S.M. et al. Effect of polydeoxyribonucleotide injection on pes anserine bursitis: A case report. Medicine (Baltimore). 2017;96(43):e8330. DOI: 10.1097/MD.0000000000008330.
43. Kim J.K., Chung J.Y. Effectiveness of polydeoxyribonucleotide injection versus normal saline injection for treatment of chronic plantar fasciitis: a prospective randomised clinical trial. Int Orthop. 2015;39(7):1329–1334. DOI: 10.1007/s00264-015-2772-0.
44. Gervaso P. Use of polydeoxyribonucleotide for peritendon injection treatment. Minerva Ortop Traumatol. 2014;65:51–56.
45. Lim T.H., Cho H.R., Kang K.N. et al. The effect of polydeoxyribonucleotide prolotherapy on posterior tibial tendon dysfunction after ankle syndesmotic surgery: A case report. Medicine (Baltimore). 2016;95(51):e5346. DOI: 10.1097/MD.0000000000005346.
46. Jung J., Lim H.S., Lee D.-W. Polydeoxyribonucleotide, as a novel approach for the management of medication-related osteonecrosis of the jaw: A preliminary observational study. J Korean Dent Sci. 2018;11:57–61. DOI: 10.5856/JKDS.2018.11.2.57.
47. Kim M.S., Cho R.K., In Y. The efficacy and safety of polydeoxyribonucleotide for the treatment of knee osteoarthritis: Systematic review and meta-analysis of randomized controlled trials. Medicine (Baltimore). 2019;98(39):e17386. DOI: 10.1097/MD.0000000000017386.
48. Gwak D.W., Hwang J.M., Kim A.R., Park D. Does polydeoxyribonucleotide has an effect on patients with tendon or ligament pain?: A PRISMA-compliant meta-analysis. Medicine (Baltimore). 2021;100(19):e25792. DOI: 10.1097/MD.0000000000025792.
49. Bizzoca D., Brunetti G., Moretti L. et al. Polydeoxyribonucleotide in the Treatment of Tendon Disorders, from Basic Science to Clinical Practice: A Systematic Review. Int J Mol Sci. 2023;24(5):4582. DOI: 10.3390/ijms24054582.
50. Saggini R., Di Stefano A., Capogrosso F. et al. al. Viscosupplementation with Hyaluronic Acid or Polynucleotides: Results and Hypothesis for Condro-synchronization. J Clin Trials. 2014;4:198. DOI: 10.4172/2167-0870.1000198.
51. Ata E., Kosem M. The Comparison of the Effects of Intra-Articular Ozone and Polynucleotide Gel Injections in Pain Management of Knee Osteoarthritis. Muğla Sıtkı Koçman Üniversitesi Tıp Dergisi. 2019;6(2):56–59.
52. Meccariello L. In the Aging Knee: Which Mitigation and Intervention Strategies do we apply in the Intra-articular Knee Joint Injection? The comparison of the effects of 5 drugs and review of the literature. Canadian Open Orthopaedics and Traumatology Journal. 2015;2(1):1–13.
53. Лычагин А.В., Богатов В.Б., Целищева Е.Ю., Музыченков А.В. Результаты лече- ния адгезивного капсулита плечевого сустава с применением обогащенной тром- боцитами плазмы и нуклеотидных препаратов: сравнительное исследование. Травматология и ортопедия России. 2022;28(4):126–135. [Lychagin A.V., Bogatov V.B., Tselishcheva E.Y., Muzychenkov A.V. Results of Shoulder Adhesive Capsulitis Treatment With the Use of Platelet Rich Plasma and Nucleotide Drugs: A Comparative Study. Traumatology and Orthopedics of Russia. 2022;28(4):126–135 (in Russ.)]. DOI: 10.17816/2311-2905-1782.
54. Meccariello L., Cioffi S., Franzese R. et al. Intraarticular knee joint injection: Hyaluronic acid vs polynucleotides. Euromediterranean Biomed J. 2013;8(7):35–41. DOI: 10.3269/1970-5492.2013.8.7.
55. Giarratana L.S., Marelli B.M., Crapanzano C. et al. A randomized double-blind clinical trial on the treatment of knee osteoarthritis: the efficacy of polynucleotides compared to standard hyaluronian viscosupplementation. Knee. 2014;21(3):661–668. DOI: 10.1016/j.knee.2014.02.010.
56. Kim J.Y., Kim Y.N., Lee Y.J. et al. Pilot Study to Evaluate the Efficacy of Polynucleotide Sodium Compared to Sodium Hyaluronate and Crosslinked Sodium Hyaluronate in Patients with Knee Osteoarthritis. J Clin Med. 2021;10(5):1138. DOI: 10.3390/ jcm10051138.
57. Moon J.Y., Kim J., Lee J.Y. et al. Comparison of polynucleotide, sodium hyaluronate, and crosslinked sodium hyaluronate for the management of painful knee osteoarthritis: a multi-center, randomized, double-blind, parallel-group study. Pain Med. 2023;24(5):496–506. DOI: 10.1093/pm/pnac155.202218:pnac155.
58. Yoon S., Kang J.J., Kim J. et al. Efficacy and Safety of Intra-articular Injections of Hyaluronic Acid Combined with Polydeoxyribonucleotide in the Treatment of Knee Osteoarthritis. Ann Rehabil Med. 2019;43(2):204–214. DOI: 10.5535/arm.2019.43.2.204.
59. Dallari D., Sabbioni G., Del Piccolo N. et al. Efficacy of Intra-Articular Polynucleotides Associated with Hyaluronic Acid Versus Hyaluronic Acid Alone in the Treatment of Knee Osteoarthritis: A Randomized, Double-Blind, Controlled Clinical Trial. Clin J Sport Med. 2020;30(1):1–7. DOI: 10.1097/ JSM.0000000000000569.
60. Zhang L., Lei N., Chang R. et al. Efficacy of intra-articular polynucleotides associated with hyaluronic acid vs hyaluronic acid alone in the treatment of knee osteoarthritis: A systematic review and meta-analysis of randomized clinical trial. Medicine (Baltimore). 2020;99(24):e20689. DOI: 10.1097/MD.0000000000020689.
61. Stagni C., Rocchi M., Mazzotta A. et al. Randomised, double-blind comparison of a fixed co-formulation of intra-articular polynucleotides and hyaluronic acid versus hyaluronic acid alone in the treatment of knee osteoarthritis: two-year follow-up. BMC Musculoskelet Disord. 2021;22(1):773. DOI: 10.1186/s12891-021-04648-0.
62. Kwon D.R., Park G.Y., Lee S.C. Treatment of Full- Thickness Rotator Cuff Tendon Tear Using Umbilical Cord Blood-Derived Mesenchymal Stem Cells and Polydeoxyribonucleotides in a Rabbit Model. Stem Cells Int. 2018;2018:7146384. DOI: 10.1155/2018/7146384.
63. Kim K.L., Park G.Y., Moon Y.S., Kwon D.R. The effects of treatment using polydeoxyribonucleotide through extracorporeal shock wave therapy: synergic regeneration effects on atrophied calf muscles in immobilized rabbits. Ann Transl Med. 2022;10(16):853. DOI: 10.21037/atm-22-854.
64. Kwon D.R., Moon Y.S., Kwon D.Y. Combination Therapy of Polydeoxyribonucleotide and Microcurrent in Muscle Regeneration on Cast-Induced Muscle Atrophy in Rabbit. Biomed Res Int. 2022;2022:7469452. DOI: 10.1155/2022/7469452.
Комментарии
ПРАКТИКА ПЕДИАТРА
