И стар и млад. Доброкачественная дисплазия молочных желёз в раннем и позднем репродуктивном периоде
СтатьиАвторы: Ирина Викторовна Высоцкая, докт. мед. наук, проф. кафедры онкологии Института клинической медицины им. Н.В. Склифосовского Первого МГМУ им. И.М. Сеченова; Сергей Александрович Дьяконов, канд. мед. наук, StatusPraesens (Москва).
Опубликовано в журнале "StatusPraesens" #3 [77] 07 / 2021: 67-76
Доброкачественная дисплазия молочных желёз (ДДМЖ) служит частым спутником гинекологических заболеваний — её частота при наличии таковых возрастает до 98% по сравнению с 50-60% в общей популяции женщин1. Именно поэтому терапия ДДМЖ часто зависит не только от результатов обследования молочных желёз, но и от наличия сопутствующих состояний (эндометриоз, бесплодие и т.д.)2. Как отметила проф. Тамара Викторовна Овсянникова, «при фиброзно-кистозной мастопатии и масталгии допускается назначение практически всех лекарственных препаратов, применяемых в гинекологической клинике»3.
Логичным итогом этой ситуации стало упразднение в 2015 году отдельной специальности «маммология» — теперь пациентку с установленным диагнозом ДДМЖ наблюдают и лечат акушеры-гинекологи. Именно они передний край обороны от самого распространённого «женского» злокачественного онкозаболевания — рака молочной железы (РМЖ).
Отсутствие в России единых алгоритмов онкогинекологического скрининга долго препятствовало эффективному раннему выявлению «женских» раков. Наконец принятые в 2020 году клинические рекомендации «Доброкачественная дисплазия молочной железы»4 и утверждённый приказом Минздрава РФ №1130н Порядок оказания медицинской помощи по профилю «акушерство и гинекология»5 систематизировали скрининг РМЖ. Маммография обеих молочных желёз в двух проекциях с двойным прочтением рентгенограмм предписана женщинам в возрасте от 40 до 75 лет включительно с периодичностью 1 раз в 2 года. Теперь главный вопрос — насколько успешно это будет реализовано на практике?
Скрининг в документах и в жизни
Весьма любопытны увидевшие свет в 2021 году результаты крупного популяционного исследования РМЖ и рака шейки матки (РШМ) в 10 постсоветских странах — скрининговые мероприятия наряду с назначением маммографии по показаниям, по всей вероятности, повысили частоту выявления РМЖ на I стадии у женщин 50—69 лет в некоторых российских регионах и Молдове6. Действительно, некоторые субъекты Федерации обеспечили почти полный охват целевой популяции маммографическим скринингом.
[ Нередкое отсутствие адекватной обратной связи между врачами-диагностами и ответственным за ведение и маршрутизацию пациентки акушером-гинекологом — не только российская, но и общемировая беда. ]
[ Положительные результаты весьма популярного у многих женщин метода самопальпации, к сожалению, — запоздалый сигнал тревоги, сообщающий пациентке и врачу, что беда уже наступила. ]
Тем не менее смертность от РМЖ в нашей стране отличается пугающей стабильностью: по данным Минздрава РФ, в 2018 году от этого онкозаболевания погибли 21 494 женщины, год спустя — 21 133. Причина «лежит на поверхности» — в 2019 году у более чем четверти (27,7%) из 66 990 российских пациенток с впервые поставленным диагнозом рака этой визуальной локализации имела место III—IV стадия болезни7.
Необходимо признать, что недостаточная эффективность маммографического скрининга, как и гинекологического онкоскрининга в целом, обусловлена не только частым игнорированием россиянками дат профилактических осмотров и обследований. SP уже писал о многочисленных «сбоях в системе», в том числе о нередком отсутствии адекватной обратной связи между врачами-диагностами и ответственным за ведение и маршрутизацию пациентки акушером-гинекологом. Это не только российская, но и общемировая беда*.
Корни проблемы смертности от злокачественных опухолей лежат глубоко — это низкая выявляемость ДДМЖ при профилактических осмотрах. Своевременное лечение доброкачественных состояний — единственный путь снизить заболеваемость РМЖ. К сожалению, большинство российских пациенток с ДДМЖ сообщают, что врач никогда не рекомендовал им маммографию.
Положительные результаты весьма популярного метода самопальпации, к сожалению, запоздалый сигнал тревоги, сообщающий пациентке и врачу, что беда уже наступила. Ещё в 2003 году российские эксперты опубликовали итоги проспективного рандомизированного контролируемого исследования самообследования молочных желёз женщин (n=123 748). Действительно, метод был ассоциирован с более частым выявлением как ДДМЖ (1,1% по сравнению с 0,5% в контроле; р<0,05), так и РМЖ (0,85% по сравнению с 0,69%; р<0,05)8.
Тем не менее даже регулярное и качественное выполнение самообследования молочных желёз (ежемесячно или каждые 2 мес) привело к пограничному по статистической значимости увеличению показателей 15-летней выживаемости (53,2% по сравнению с 45,8%; р=0,05105), но не повлияло на частоту летальных исходов8. К аналогичным выводам пришли и авторы Кокрейновского систематического обзора и метаанализа, включившие российское исследование9.
«Эффект Анджелины Джоли» уже признан международным медицинским сообществом — всё больше женщин заинтересованы в тестировании на опасные мутации генов BRCA1 и BRCA210. Оно в первую очередь ориентирован на пациенток с отягощённым наследственным анамнезом по РМЖ, и его не используют в общепопуляционном скрининге11. Отметим также, что при всех достоинствах УЗИ этот метод не может заменить маммографию в первичном онкоскрининге РМЖ12. УЗИ широко используют для уточнения диагноза — как дополнительный метод, нивелирующий ограничения рентгеновского исследования13.
Коронавирусная лавина
В 2020 году реализация всех скрининговых мероприятий, и в том числе маммографических исследований, получила двойной удар от пандемии COVID-19. С одной стороны, коронавирусная инфекция повысила нагрузку на практикующих врачей всех без исключения специальностей. С другой стороны, даже после возобновления временно прекращённых приёмов в рамках диспансеризации многие пациентки не желают «лишний раз» посещать медицинские учреждения из-за риска инфицирования.
Американские специалисты уже оценили «масштаб бедствия». Так, в апреле 2020 года количество плановых скрининговых обследований на РМЖ и РШМ в США упало на 87 и 84% соответственно по сравнению с усреднёнными за 5 лет показателями для этого месяца. В принявшем на себя тяжёлый удар первой волны COVID-19 Нью-Йорке гинекологический онкоскрининг практически перестал существовать — статистический регион здравоохранения, в состав которого входит крупнейший город США, сообщил о падении этих параметров на 96 и 95% соответственно. В мае-июне американки стали чаще проходить скрининговые обследования, но количество посещений не достигло и половины от «доковидных»28.
Наглядный пример того, как пандемия COVID-19 препятствует профилактической медицине, можно было наблюдать в российской столице в июне 2021 года. Всплеск заболеваемости коронавирусной инфекцией привёл к тому, что устроенные в парках павильоны «Здоровая Москва» были немедленно полностью перепрофилированы с диспансеризации на вакцинацию против SARS-CoV-229.
Собственно вакцинация против SARS-CoV-2 также может вызвать определённые трудности с диагностикой РМЖ — с начала 2021 года зарубежные специалисты описывают многочисленные клинические случаи одностороннего увеличения подмышечных лимфатических узлов после иммунизации30,31. Это затрудняет дифференциальную диагностику, а у вакцинированных пациенток онколога — позволяет заподозрить метастазирование32.
В любом случае при охвате целевой популяции маммографическим скринингом менее 80% нельзя ожидать от него успехов в борьбе с РМЖ. В этой связи особую важность приобретает квалифицированное ведение пациенток с ДДМЖ — основа профилактики онкозаболеваний этой локализации.
* Аминодова И.П. Скрининг на опухолевые заболевания шейки матки и молочных желёз. Анализ причин неэффективности // StatusPraesens. Гинекология, акушерство, бесплодный брак. 2019. №2 (55). С. 79-86.
«Все возрасты покорны»
Онкопрофилактику РМЖ следует начинать смолоду. Модификация образа жизни, включающая рациональное питание, потребление достаточного количества жидкости и достаточную физическую активность, позволит предотвратить ожирение — важнейший модифицируемый фактор риска РМЖ.
Более того, заболевания молочных желёз могут атаковать даже самых юных пациенток. Во время полового созревания маммарная ткань избыточно пролиферирует, в результате чего может развиться одно- или двусторонняя макромастия. Наиболее часто процесс начинается в возрасте 10—15 лет незадолго до наступления менархе или прогрессирует вскоре после него. В отдельных случаях наблюдают периоды ускоренного роста, как симметричного, так и асимметричного.
В зависимости от степени гипертрофии возникают косметические недостатки или ортопедические расстройства, в особенности со стороны позвоночника. При МРТ выявляют диффузно увеличенное поле железистой ткани (до гигантских размеров) без очаговых изменений, при этом жировая ткань по большей части полностью вытеснена. Гистологически обнаруживают, с одной стороны, пролиферацию протоков, с другой — застой крови и лимфы, а также регрессивные изменения железистой ткани. Наблюдается также пролиферация стромы протоков и долек — картина фиброаденоматозной гипертрофии без образования или с неполным образованием долек.
К счастью, РМЖ у детей диагностируют крайне редко — это 0,1% от общей распространённости этой опухоли и менее 1% от всех онкологических заболеваний этого возраста33. Тем не менее доброкачественные нарушения довольно распространены в этой когорте — доля больных с отклонениями или заболеваниями молочных желёз составляет 5—12% из числа обратившихся за консультацией к акушеру-гинекологу, оказывающему помощь детям и подросткам.
Отметим, что у девочек и девушек обычно не используют классификационную систему BI-RADS (Breast imaging reporting and data system), предназначенную для описания данных инструментальной диагностики молочной железы прежде всего в целях выявления злокачественного процесса.
Если «золотой стандарт» обследования взрослых пациенток — маммография, то в пубертатном периоде ткани очень чувствительны к ионизирующему излучению и имеют довольно высокую рентгенологическую плотность. Именно поэтому при наличии показаний к визуализирующим методам диагностики предпочтение следует отдавать УЗИ34, а в ряде случаев для уточнения диагноза использовать МРТ.
Отметим, что клинические рекомендации по ДДМЖ (2020) регламентируют ведение взрослых больных — для оказания помощи несовершеннолетним аналогичного протокола пока нет. Приказ Минздрава РФ №1130н предусматривает приёмы акушера-гинеколога в рамках профилактических осмотров несовершеннолетних для девочек в возрасте 3, 6, 13, 15, 16 и 17 лет. В случае если у юной пациентки диагностирована ДДМЖ девочку относят к III группе здоровья, и составляют индивидуальную программу лечения, а при необходимости — организуют диспансерное наблюдение по месту жительства5.
Изменения молочных желёз у девочек могут быть связаны с развитием органа, что требует дифференцированного подхода и максимально щадящего лечения. Не случайно самое частое доброкачественное новообразование у детей и подростков — чувствительная к эстрогенам фиброаденома, быстро растущая в период полового созревания.
Высокотехнологичные перспективы
Гипердиагностика РМЖ и сопряжённые с ней дискуссии о чувствительности метода14,15, повышенная тревожность пациенток16 и, конечно, споры о результативности его использования — при всех его преимуществах маммографический скрининг контраверсионен17. В этой ситуации на помощь врачам и женщинам в уточнении диагноза могут прийти высокие технологии.
С одной стороны, специалисты предлагают использовать искусственный интеллект при анализе рентгеновских снимков18. Не исчерпаны и возможности углублённого исследования уже известных маркёров — в июне 2021 года после анализа медицинской информации более 50 тыс. пациенток шведские врачи подтвердили прогностическую роль микрокальцинатов, особенно у женщин в пременопаузе. Кластеры Ca2+ были ассоциированы и с РМЖ in situ (ОШ 2,03; 95% ДИ 1,13-3,63)19. Биологические механизмы, ответственные за эти минеральные отложения и их ассоциацию со злокачественными новообразованиями, требуют дальнейшего изучения20.
С другой стороны, идёт поиск клеточных и молекулярных маркёров крови, позволяющих выявить РМЖ уже на ранних стадиях. На эти роли «пробуют» микроРНК — как «свободно плавающие», так и расположенные во внеклеточных везикулах21,22. Ещё один интересный подход — оценка разбалансированности адипо- и миокинов у пациенток с ожирением, известным фактором риска РМЖ. Греческие исследователи установили, что повышение сывороточной концентрации ирисина ассоциировано и с доброкачественными, и со злокачественными опухолями молочной железы, но в сочетании с параметрами оментина-1 оно указывало на наличие РМЖ23.
Циркулирующие в крови женщин с РМЖ кластеры опухолевых клеток считали в первую очередь признаком гематогенного метастазирования, и их предлагали изучать на предмет эволюции злокачественного новообразования и оценки ответа на лечение24. Тем не менее весной 2021 года исследователи показали, что этот инструмент прецизионной онкологии можно использовать намного раньше — «жидкая биопсия» выявила грозные кластеры уже на ранних стадиях РМЖ25,26. Диагностическое и клиническое значение этой находки ещё предстоит оценить.
Выявление наследственной предрасположенности к РМЖ не ограничилось мутациями в гене BRCA — в феврале 2021 года американские исследователи по результатам крупного популяционного исследования заключили, что помимо наиболее онкоопасных патологических вариантов генов BRCA1 и BRCA2 прогностическое значение имеют мутации гена PALB2 (ОШ 3,83; 95% ДИ 2,68-5,63). Изменения генов BARD1, RAD51C и RAD51D были ассоциированы с риском эстроген-рецептор-негативного РМЖ и РМЖ с тройным негативным фенотипом, а перестройки ATM, CDH1 и CHEK2, напротив, с риском эстроген-рецептор-позитивного РМЖ27.
Фиброаденомы — наиболее частые доброкачественные образования у детей и подростков (54—94%). Чаще всего они единичные — 85%, у 15% пациенток — множественные. Их часто наблюдают у кровных родственниц. 5—10% опухолей этого типа регрессирует в течение нескольких лет. Риск малигнизации при «типичных» фиброаденомах чрезвычайно низкий — 0,0125-0,3%.
При УЗИ фиброаденома выглядит как гипоэхогенная масса круглой или овальной формы с чёткой границей. Обычно размеры этого новообразования не превышают 2-3 см35. Тем не менее один из подтипов этого новообразования — ювенильная фиброаденома — склонен к быстрому росту за счёт активной пролиферации стромы. Именно поэтому особая проблема подросткового возраста — гигантские фиброаденомы, опухоли крупнее 5 см, массой свыше 500 г или замещающие по крайней мере 80% ткани молочной железы36.
Эти доброкачественные новообразования могут быть одно- или двусторонними, и их развитие возможно даже в период до менархе; они могут сопровождаться изъязвлением и разрушением соска и ареолы37. Наиболее крупную ювенильную фиброаденому описали в 2019 году врачи Тринидада и Тобаго — у 16-летней девочки опухоль достигла размера 28X25 см!38
Современные тактические подходы к ведению пациенток с фиброаденомой молочной железы хорошо известны.
- Все фиброаденомы должны быть верифицированы, лучше гистологически.
- Гистологически верифицированную фиброаденому размером менее 2 см можно динамически наблюдать каждые 6 мес.
- При росте на 15% между мониторингами рассматривают вариант хирургического лечения.
Гигантские новообразования фактически не оставляют выбора врачу и пациентке. В этой ситуации чаще всего прибегают к полному иссечению опухоли, стремясь сохранить паренхиму растущей молочной железы и сосково-ареолярный комплекс. В некоторых случаях необходима реконструкция органа39. Подростковая фиброаденома может рецидивировать после операции, что требует особой онконастороженности40.
Около 25% всех новообразований молочной железы представлены кистами. Большинство из них доброкачественные и не повышают риск РМЖ. Частота встречаемости кист в детском возрасте составляет 6—10%, при этом отсутствие клинической симптоматики — скорее правило, нежели исключение. Тем не менее у некоторых пациенток присутствуют признаки воспаления и болевой синдром.
Простые бессимптомные кисты не требуют дальнейшего обследования и специального лечения, однако если при УЗИ наблюдают так называемую атипичную или сложную кисту с неоднородным содержимым, пристеночными разрастаниями, нечёткостью контура и иными угрожающими признаками, необходима дифференциальная диагностика со злокачественными опухолями35. Такие образования всегда требуют морфологической верификации, поскольку риск озлокачествления в данном случае гораздо выше — до 0,3%. Классическая тактика при крупных единичных кистах — эвакуация содержимого с цитологическим исследованием с последующим склерозированием. Более широкое вмешательство может быть использовано при больших, неоднократно рецидивирующих образованиях35,44.
Два маршрута
При выявлении пальпируемого новообразования молочной железы у взрослых женщин обновлённые в 2020 году клинические рекомендации предусматривают два пути ведения в зависимости от возраста — до 30 лет и старше (см. инфографику).
Маршрут построен
Диагностика пальпируемых образований молочных желёз
Алгоритм обследования пациенток 30 лет и моложе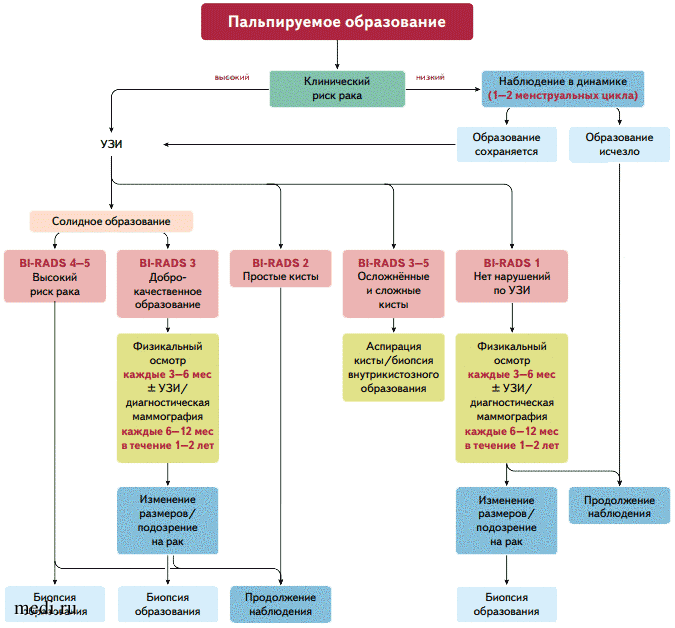 Алгоритм обследования пациенток 30 лет и старше
Алгоритм обследования пациенток 30 лет и старше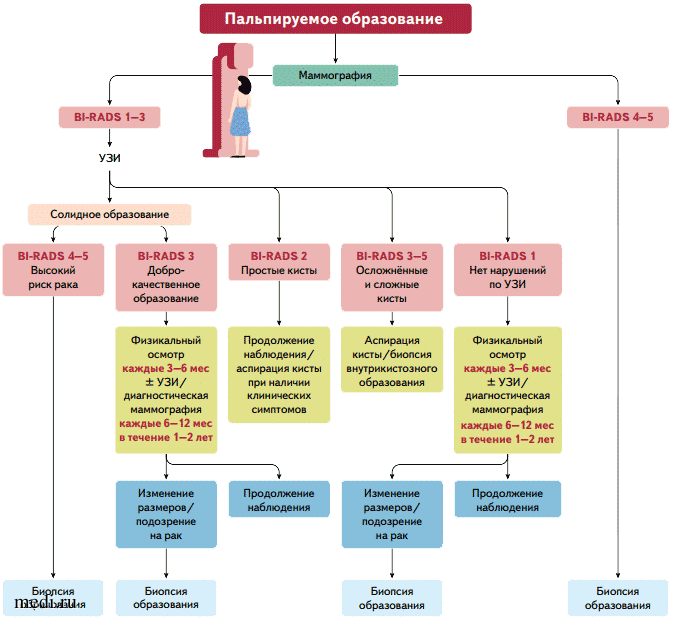 Вывод: Традиционное мнение, что молодым пациенткам достаточно выполнить УЗИ, а маммография показана только после 40 лет — ошибочно! При выявлении пальпируемого образования, независимо от возраста и давности скрининга, назначают все доступные уточняющие методы обследования, включая маммографию.
Вывод: Традиционное мнение, что молодым пациенткам достаточно выполнить УЗИ, а маммография показана только после 40 лет — ошибочно! При выявлении пальпируемого образования, независимо от возраста и давности скрининга, назначают все доступные уточняющие методы обследования, включая маммографию.
Железистая ткань молочной железы молодых девушек продолжает претерпевать изменения в ответ на циклическое повышение концентраций эстрадиола и прогестерона в плазме крови. Значительный рост уровня этих гормонов сопряжён с высокой вероятностью аденоза. Протоковые элементы редко вовлечены в патологический процесс, однако может возникнуть гиперплазия стромы, для которой характерна бугристость при пальпации или уплотнения, в дальнейшем требующие биопсии43.
У пациенток до 30 лет в первую очередь оценивают клинический риск злокачественного новообразования в соответствии с приведёнными в протоколе факторами риска РМЖ. В качестве метода визуализации новообразования в первую очередь используют УЗИ. Тем не менее при наличии узловых образований в молочных железах маммографию используют для верификации диагноза независимо от возраста.
Частота ДДМЖ достигает пика в возрасте от 30 до 50 лет — именно эти пациентки чаще всего обращаются к акушеру-гинекологу с жалобами на масталгию, выделения из сосков или пальпируемое новообразование. В 79—98% клинических ситуаций объяснение волнующих женщину симптомов будет «доброкачественным», но исключить уже не столь редкий в этой популяции РМЖ обязательно необходимо42.
Для позднего репродуктивного периода характерны гиперпластические процессы тканей молочной железы — склерозирующий аденоз или дольковая гиперплазия. При длительном течении возможно пальпаторное обнаружение этих элементов, а также их выявление с помощью визуализирующих методов диагностики. Протоковый компонент может претерпевать гиперпластические изменения, вплоть до развития карциномы in situ43.
У женщин старше 30 лет диагностический поиск при пальпируемом новообразовании молочной железы всегда начинают с маммографии — УЗИ используют для уточнения диагноза при результатах BI-RADS 1—3. Отметим, что разработанная с максимальным учётом требований онконастороженности классификация BI-RADS незаменима для характеристики пролиферативных процессов в маммарной ткани у взрослых. Её категории едины для всех методов визуализации (маммографии, УЗИ, МРТ), и акушеру-гинекологу необходимо хорошо их знать.
Таблица.
Классификация BI-RADS (2013)45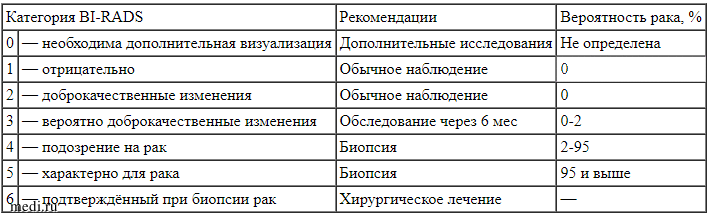 [ Простые бессимптомные кисты не требуют дальнейшего обследования и специального лечения, однако если при УЗИ есть так называемая атипичная или сложная киста с неоднородным содержимым и иными угрожающими признаками, нужна дифференциальная диагностика со злокачественными опухолями. ]
[ Простые бессимптомные кисты не требуют дальнейшего обследования и специального лечения, однако если при УЗИ есть так называемая атипичная или сложная киста с неоднородным содержимым и иными угрожающими признаками, нужна дифференциальная диагностика со злокачественными опухолями. ]
Согласно клиническим рекомендациям, при результатах BI-RADS 1 или 2 пациентку наблюдает врач акушер-гинеколог, при BI-RADS 4—6 — врач-онколог. При BI-RADS 0 или 3 необходима консультация последнего с определением дальнейшей тактики ведения4.
После исключения злокачественного процесса работа акушера-гинеколога по предотвращению онкопроцессов молочной железы продолжается. ДДМЖ, и прежде всего её пролиферативная форма с атипией, достоверно повышает вероятность РМЖ. Опубликованные в 2021 году результаты исследования частоты РМЖ в Испании, включившего почти 300 тыс. участниц, показали, что любая форма ДДМЖ в сочетании с высокой маммографической плотностью повышает риск РМЖ втрое на протяжении 15 лет наблюдения (СР 3,07; 95% ДИ 2,014,68)46. Отметим, что ДДМЖ и повышенная маммографическая плотность часто встречаются вместе. Так, по данным американских врачей, у женщин с ДДМЖ, диагностированной до первых родов, этот рентгенологический показатель был значимо выше47.
Выбор метода лечения
Согласно клиническим рекомендациям, акушер-гинеколог назначает терапию только пациенткам с диффузными формами ДДМЖ — «подведомственные» ему из пальпируемых образований простые кисты молочных желёз лишь наблюдают в динамике4.
Дисфункция яичников, гиперпластические процессы эндометрия, генитальный эндометриоз, миома матки — все эти состояния могут сопровождать ДДМЖ, и ведение последней будет зависеть от подхода, выбранного для лечения гинекологического заболевания. Отметим, что, по современным данным, чёткой ассоциации между ДДМЖ и самым распространённым в практике акушера-гинеколога эндокринным заболеванием — синдромом поликистоза яичников — не обнаружено48.
[ У пациенток до 30 лет для визуализации изменений в первую очередь используют УЗИ, тем не менее при наличии узловых образований в молочных железах прибегают к маммографии независимо от возраста. ]
Масталгия — самая частая жалоба у женщин с ДДМЖ. Выраженность болевых ощущений часто «подкреплена» онкобоязнью. Однако после исключения РМЖ и разъяснения, что болезненность молочных желёз не повышает риск рака, а также обсуждения причин и механизмов болевого синдрома у большинства пациенток сразу наступает облегчение симптоматики49. Эффективны также релаксирующие методики и психологическое корригирование50. Повысить эффективность лечения позволяет ношение мягкого комфортного бюстгальтера, подходящего по размеру и обеспечивающего хорошую поддержку молочных желёз51.
Влияющая на качество жизни пациентки масталгия, несомненно, основание для медикаментозного лечения. Как было отмечено выше, терапия ДДМЖ часто зависит от коморбидных состояний. В клинических рекомендациях отмечено, что трансдермальные препараты прогестерона эффективно облегчают болезненные ощущения. Тем не менее его назначение наиболее целесообразно при сочетанных гиперпластических процессах4. Ряд экспертов считают, что гормональная терапия при лечении мастопатии без сопутствующих заболеваний нецелесообразна, и рекомендуют прибегать к нестероидным противовоспалительным средствам, однако их длительное применение грозит осложнениями со стороны желудочно-кишечного тракта52.
Один из оптимальных вариантов, включённый в клинические рекомендации, — средства, содержащие витекс священный (Vitex agnus-castus, прутняк обыкновенный)4. Например, комбинированный лекарственный препарат «Мастодинон», в состав которого также входят стеблелист, цикламен, игнация, ирис, лилия. Этот фитопрепарат неоднократно подтвердил свою эффективность и разрешён для применения с возраста 12 лет61.
Его использование сопряжено со снижением частоты выявления признаков ДДМЖ у девочек подросткового возраста: через 3 мес — на 56,2%, через 6 мес — на 71,2%, а также с уменьшением циклической мастодинии. Через 3 мес лечения она уменьшилась с 90,5 до 52,1%, а через 6 мес — в 4,4 раза53. Препарат также продемонстрировал эффективность при лечении ДДМЖ у пациенток репродуктивного возраста (21-39 лет) с отягощённым акушерским анамнезом (самопроизвольный выкидыш, неразвивающаяся или внематочная беременность) и нарушениями менструального цикла. Улучшение состояния молочных желёз имело место у 86,7% участниц, а 58,3% из них отметили восстановление регулярных циклов и нормализацию объёма выделений после завершения курса лечения60.
В пери- и постменопаузальном периодах для лечения ДДМЖ с масталгией также можно эффективно использовать препараты витекса священного. В работе российских учёных описаны итоги лечения 475 пациенток, получавших симптоматические средства (настойку валерианы, пиона и седативные медикаменты) и витамины А, С, Е, группы В в течение 3 мес с последующей монотерапией «Мастодиноном» до 6 мес. По данным УЗ-мониторинга положительную динамику состояния молочных желёз зафиксировали у 36% женщин в группе 50-55 лет и у 58% — в группе 56-60 лет. При контрольных осмотрах через 12 мес сохранение ремиссии выявили у 83,7% участниц54.
Назначение фитопрепарата на основе витекса священного целесообразно и при наличии коморбидных состояний. Так, в отечественном клиническом исследовании (2017) при ДДМЖ в сочетании с миомой матки было продемонстрировано преимущество миомэктомии с последующей гормоно-или фитотерапией над изолированным хирургическим лечением. Из 93 пациенток (средний возраст 44,8±0,53 года) комплексное лечение получили 63 (67,7%), а в качестве группы сравнения выступили 30 женщин, отказавшихся от восстановительного консервативного лечения55.
Использование комплексной терапии обеспечило снижение интенсивности болевого синдрома и частоты рецидивов узловых форм ДДМЖ. Фитопрепарат (n=36) обеспечил облегчение боли по визуально-аналоговой шкале в среднем на 36,5 мм через 3 мес, тогда как терапия гормональными средствами (n=27) привела к снижению аналогично показателя в среднем на 23,6 мм. Контрольное УЗИ молочных желёз показало снижение гиперэхогенности железистого компонента, сокращение числа расширенных протоков, уменьшение неровности их контуров и карманообразных расширений в них, а также количества мелких кист у 81,6 и 76,1% пациенток соответственно55.
Основной эффект препаратов на основе витекса священного связан с подавлением избыточной секреции пролактина лактотрофными клетками, расположенными в передней доле гипофиза56. Однако в последние годы открываются всё новые положительные свойства этого растения. В российских и зарубежных исследованиях отмечено, что его компоненты способствуют нормализации эстроген-гестагенного баланса и обладают мягким опиоидным действием58.
В частности, в иранском рандомизированном контролируемом исследовании (2014) средство, содержащее витекс священный, обеспечило выраженное облегчение тревожности у пациенток с масталгией — после 3 мес терапии оценка по шкале Бека (Beck anxiety inventory) снизилась с 24,6±2,4 до 12,6±2,1 балла. При этом эффект был более выраженным по сравнению с контрольной группой и когортой получавших витамин E женщин40.
В отечественной научной работе (2019) было показано, что препарат «Мастодинон» способен корригировать баланс эстрогеновых метаболитов в сторону «антипролиферативных» — 2-ОНЕ1+2-OHE2*, тем самым существенно нивелируя влияние факторов риска ДДМЖ57.
Высокие концентрации пролактина крови и сопряжённый с ними дисбаланс половых стероидов могут привести к повышению маммографической плотности тканей. Российские исследователи описали снижение этого показателя после использования препарата на основе витекса священного в течение более 6 мес. Таким образом, фитосредства могут не только облегчить течение масталгии, но и уменьшить выраженность известного фактора риска маммарных опухолевых процессов41.
[ После исключения злокачественного заболевания работа по предотвращению онкопроцессов молочной железы продолжается: ДДМЖ, и прежде всего её пролиферативная форма с атипией, повышает риски РМЖ. ]
Квалифицированное ведение пациенток с ДДМЖ — наилучший ответ акушеров-гинекологов на вопрос, способна ли медицина остановить РМЖ. Специалист должен тщательно оценить у женщин с этим состоянием факторы риска РМЖ и разъяснить им значение маммографического скрининга. Отметим, что самостоятельное онкопротективное значение при ДДМЖ имеет отказ от алкоголя и табака59.
Онконастороженность в акушерстве и гинекологии обязательна, и статистически РМЖ — «главный противник» женщин. Именно поэтому важно тщательно осматривать и пальпировать молочные железы на приёме — независимо от возраста пациенток. Большое значение имеет сбор анамнеза и оценка факторов риска как РМЖ, так и ДДМЖ.
* Существует несколько гидроксиметаболитов эстрогенов. Для протективного по отношению к РМЖ эффекта важно преобладание 2-OHE1 и 2-OHE2 над «агрессивным» канцерогенным 16a-OHE1.
