Бризантин — Новый препарат для лечения никотиновой зависимости: результаты многоцентрового клинического исследования
СтатьиОпубликовано в журнале:
«ПОЛИКЛИНИКА»; № 4; 2013; стр. 1-6. А.Ф. Паращенко, к.м.н.
Государственное учреждение здравоохранения «Саратовская областная психиатрическая больница Святой Софии»
Е. В. Кулдыркаева, к.м.н.
Государственное учреждение здравоохранения «Республиканский психоневрологический диспансер»
Ю.Б. Барыльник, д.м.н.
Муниципальное учреждение здравоохранения «Городская клиническая больница №2 им. В. И. Разумовского» комитета здравоохранения администрации муниципального образования «Город Саратов»
И.И.Заярная
Государственное учреждение здравоохранения Ярославской области Ярославская областная клиническая психиатрическая больница
О.А. Козырев, профессор
Государственное образовательное учреждение высшего профессионального образования «Смоленская государственная медицинская академия» Министерства здравоохранения Российской Федерации, кафедра госпитальной терапии
Д.А. Чижов
Санкт-Петербургское государственное учреждение здравоохранения «Городская поликлиника №106»
А.С. Агафьина, к.м.н.
Санкт-Петербургское государственное учреждение здравоохранения «Городская больница №40 Курортного района»
Е.Н. Андрианова, д.м.н.,
НПФ «Материа Медика Холдинг»
Ежегодно в мире, охваченном глобальной табачной эпидемией, из-за курения погибают 6 миллионов человек [1 ]. Медицинские исследования указывают на явную связь табакокурения с раком легких, сердечнососудистыми и многими другими заболеваниями [2].
Частота самостоятельного отказа от курения у зависимых лиц не превышает 5% [1]. В подавляющем большинстве случаев они нуждаются в помощи врача и фармакологической терапии, направленной на уменьшение проявлений синдрома отмены [1, 2]. Сам факт назначения лекарств (плацебо-эффект) повышает частоту отказа от курения до 10% [2, 3]. К препаратам с доказанной эффективностью относят антидепрессанты (бупропион), никотинсодержащие средства и частичные агонисты никотиновых рецепторов (цитизин, варениклин) [3, 4, 5]. Однако их применение может сопровождаться развитием побочных эффектов, среди которых тошнота, повышение аппетита, головная боль, бессонница, необычные сновидения, сонливость, головокружение, дисгевзия, рвота, вздутие живота и другие.
Новый релиз-активный препарат для лечения никотиновой зависимости Бризантин создан компанией «Материа Медика Холдинг» на основе антител к мозгоспецифическому белку S100 (анти-S100) и каннабиноидному рецептору 1 типа (анти-СВ [11, 12, 13, 14]. Антидепрессивный и противотревожный эффекты первого компонента анти-S100, как показали клинические исследования, сопоставим по эффективности с амитриптилином, феназепамом, сертралином [1 0, 11, 12, 13]. Второй компонент (анти-СВ1) оказывает влияние на СВ1 -рецепторы, гиперактивация которых имеет место у хронических курильщиков, а также у лиц с ожирением. Нормализация функциональной активности центральных и периферических СВ1 -рецепторов снижает потребность в приеме никотина, а также препятствует повышению аппетита и набору веса людей, бросивших курить. Экспериментальные исследования доказали синергический антиаддиктивный эффект двух компонентов Бризантина при их совместном использовании [6, 14].
Ниже представлены результаты многоцентрового клинического исследования эффективности и безопасности Бризантина в лечении никотиновой зависимости, которое проводили в 7 медицинских центрах РФ в течение 2011-12 гг
Материалы и методы
В исследовании приняли участие 256 пациентов в возрасте от 18 до 65 лет (средний возраст 38,7±11,31 лет), имевшие средний «стаж» регулярного курения 1 6,2±1 0,5 лет (колебания от 1 до 51 года), выкуривавшие от 2 до 80 сигарет в сутки (среднее значение 1 9,3±9,8); 44% (n=113) участников исследования были женщины. Тяжесть никотиновой зависимости варьировала от легкой до тяжелой (показатель теста Фагерстрома от минимума в 2 балла до максимума в 1 0 баллов), причем у половины (53%; n=1 36) она была тяжелой [15].
После подписания информированного согласия на первом визите проводили начальное обследование, включавшее сбор анамнеза, демографических данных, сведений о сопутствующей терапии, объективный осмотр и лабораторные исследования. Фиксировали число выкуриваемых сигарет за сутки, предшествующие визиту. Степень тяжести никотиновой зависимости определяли с помощью теста Фагерстрома [15], выраженность тревоги и депрессии - по шкале HADS (Hospital Anxiety and Depression scale) [16], качество жизни - по опроснику SF-36 (The Short Form-36 Health Survey).
Участникам исследования выдавали Бризантин, который они принимали по 1 таблетке от 3 до 6 раз в день (в зависимости от выраженности тяги к курению) вне связи с приемом пищи, что весьма удобно, поскольку препарат выпускается в виде таблеток для рассасывания. Удобство терапии для пациента подтверждал почти 100%-й показатель комплаентности.
В ходе ежемесячных визитов пациентам проводили физикальное и лабораторное обследования, тестирование (тест Фагерстрома, HADS). У пациентов, отказавшихся от курения, регистрировали симптомы отмены с помощью опросника Mood and Physical Symptoms Scale (MPSS) [7], общая сумма баллов которого (от 10 до 60) позволяет выявить тяжесть абстинентного синдрома (от его отсутствия до максимальной степени выраженности).
В анализ по оценке эффективности вошли данные 248 пациентов (132 из них - с тяжелой никотиновой зависимостью). В качестве первичных критериев эффективности оценивали динамику выраженности никотиновой зависимости (по сумме баллов теста Фагерстрома), долю пациентов, отказавшихся от курения к концу 12-недельного курса лечения, и выраженность симптомов отмены никотина у них (по общей сумме баллов опросника MPSS). Вторичными критериями были динамика абстинентного синдрома и тяги к курению (по сумме баллов доменов М и С опросника MPSS), число сигарет, выкуриваемых за сутки лицами, продолжившими курение, а также изменение качества жизни участников исследования через 1 2 недель лечения (SF-36). Дополнительно анализировали динамику веса на фоне приема препарата.
О безопасности терапии судили на основании мониторинга лабораторных показателей и нежелательных явлений, в том числе со стороны центральной нервной системы, связанных с исследуемой терапией. По сумме баллов шкалы HADS регистрировали появление значимой/ухудшение текущей тревоги/депрессии.
Статистическую обработку проводил с помощью статистического пакета SAS-9.3. Использовали параметрические (для оценки непрерывных и интервальных случайных величин) и непараметрические (для получения оценок о равенстве/неравенстве долей пациентов при их сравнении для разных визитов, а также при анализе частот сравниваемых признаков) критерии.
Результаты
На фоне применения Бризантина прогрессивно и значимо уменьшалась степень тяжести никотиновой зависимости. Показатель теста Фагерстрома от исходного среднего значения 5,4±2,7 баллов в течение 1 2 недель терапии снизился более чем в 2 раза и составил 2,5±2,1 баллов (рис. 1). Однофакторный дисперсионный анализ для повторных измерений (One-way Repeated Measures ANOVA) показал значимое снижение выраженности никотиновой зависимости в ходе лечения (фактор Визит: F3/729 = 2 3 5,2; p<0,0001). Пост-хок анализ (Bonferroni) подтвердил значимые различия показателей между всеми визитами, в том числе, между 1 и 2 (z =1 0,9; p<0,0001), 2 и 3 (z =10,8; p<0,0001), 3 и 4 (z =8,4; p<0,0001) и 1 и 4 (z =1 9,8; p<0,0001). В подгруппе пациентов с тяжелой никотиновой зависимостью также получено более чем двукратное снижение суммарного балла по Фагерстрому, среднее значение которого (3,6±2,2) было ниже 4 баллов и свидетельствовало о переходе в легкую либо среднюю степень зависимости от никотина большинства участников исследования (F3/393 = 2 3 4 , 6; p<0,0001).
Рис. 1. Динамика выраженности никотиновой зависимости в процессе лечения (тест Фагерстрома, баллы) 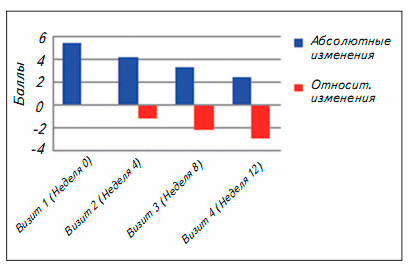
За 12 недель применения Бризантина 20% (n=49) участников исследования смогли отказаться от потребления табака, то есть не выкуривали ни одной сигареты к окончанию терапии в течение того или иного периода времени (рис. 2). Ответ на лечение проявлялся постепенно и нарастал в ходе всего 3-месячного курса. Через 4 недели от начала лечения (Визит 2) 9 (4%) участников исследования не курили; к 3 визиту - 23 (9%). Более существенный рост числа пациентов, бросивших курить, отмечался на третьем месяце приема Бризантина. Доля не куривших пациентов по результатам оценок в день Визита 4 возросла еще на 11% и составила 20% (n=49). Таким образом, 26 участников бросили курить в течение первых 2х месяцев, а 49 - через 2 месяца после начала терапии. Ответ на лечение был сопряжен с исходной тяжестью никотиновой зависимости и колебался от 1 3% до 28%. Частотный анализ показал значимое увеличение доли участников, отказавшихся от курения в течение 3 месяцев терапии (критерий Кохрана-Мантеля-Хенсзеля [CMH]: Х2=73,4; p<0,0001). Тяжесть абстинентного синдрома на фоне приема Бризантина была выражена умеренно и значимо снижалась в процессе лечения: с 17,1±3,5 баллов на втором визите до 1 5,3±3,2 - на визите 3 и 13,4±2,9 -к окончанию курса терапии (рис. 3). У пациентов, бросивших курить через 2 месяца от начала терапии, степень выраженности синдрома отмены никотина с 17,5±3,1 (на визите 2, когда они стали нерегулярными курильщиками) уменьшилась до 1 4,6±3,1 баллов (на визите 4). В подгруппе пациентов, прекративших курение в течение первых 2-х месяцев, суммарный балл за 8 недель лечения снизился от исходного 16,7±3,9 до 1 2,0±1,9 и демонстрировал практически полное отсутствие у них симптомов абстиненции (z =2,3; р=0,02) (рис. 3).
Рис. 2. Доля пациентов, отказавшихся от курения в процессе лечения (на 4, 8 и 12 неделях лечения)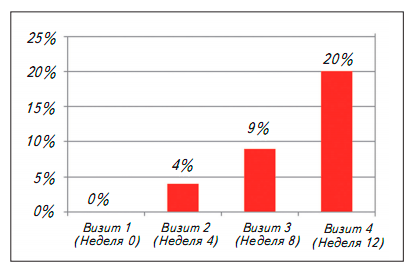
Рис. 3. Выраженность симптомов отмены никотина в процессе лечения у пациентов, (суммарный балл MPSS) ;* p<0,0001 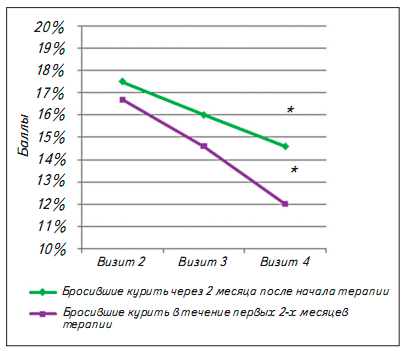
Средний балл домена М пациентов, бросивших курение на различные сроки, на втором визите составил 10,1 ±2,2, что свидетельствовало о наличии легких психо-эмоциональных расстройств, связанных с абстиненцией (рис. 4). Снижение показателя до 8,9±2,1 баллов по окончании курса терапии означало наличие минимальных проявлений ментального дискомфорта на фоне приема Бризантина, а у некоторых участников исследования - его полное отсутствие.
Рис. 4. Динамика симптомов абстиненции в группе А (показатели домена М опросника МРSS) в процессе лечения *р = 0,002 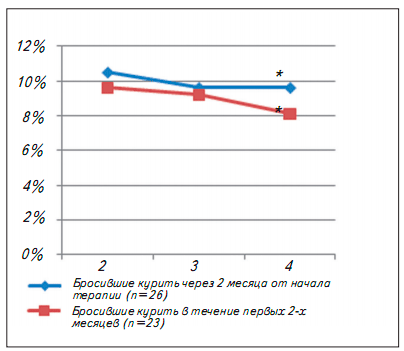
Тяга к курению по результатам среднего показателя домена С (3,6±1,3 баллов) в начале абстинентного периода была умеренно выраженной (рис. 5). К окончанию трехмесячного курса лечения отмечено более чем двукратное снижение показателя, в том числе у пациентов с тяжелой никотиновой зависимостью. Желание курить в подгруппе «бросивших курить через 2 месяца от начала терапии» от исходных 3,7±1,2 баллов уменьшилось до 1,9±1,2 к 4 визиту; в подгруппе «бросивших курить в течение первых 2 месяцев терапии» динамика была наилучшей (3,5±1,5 и 0,8±1,2 баллов соответственно) и свидетельствовала почти о полном отсутствии тяги к курению среди лиц, отказавшихся от сигарет на более продолжительный срок.
Рис. 5. Динамика выраженности тяги к курению (баллы домена С MPSS) у пациентов, отказавшихся от курения * р<0,0001 
Пациенты, которые продолжали курить (n=199), в том числе с тяжелой никотиновой зависимостью (n=1 1 5), существенно уменьшили дозу потребляемого никотина. Число выкуриваемых за сутки сигарет в результате 3-месячного курса терапии снизилось в 2 раза: от исходных 20,6±10,1 и 25,7±9,7 до 10,3±7,6 и 12,2±8,4 соответственно (рис. 6).
Рис. 6. Среднее число сигарет, выкуриваемых за сутки участниками исследования, продолжавшими курение к концу периода наблюдения *p<0,0001 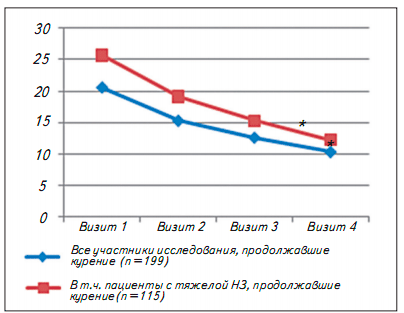
Отказ от курения на фоне приема Бризантина не сопровождался физическим либо психологическим дискомфортом, на что обычно жалуется человек, бросающий курить. Напротив, лечение Бризантином, по мнению участников исследования, улучшало их физическое и ментальное здоровье, что нашло отражение в показателях опросника качества жизни (рис. 7). Средний суммарный балл физической составляющей здоровья за 12 недель терапии увеличился с 51,3±8,3 до 53,9±6,9 баллов; психическая составляющая - с 43,2±6,4 до 46,0±5,4 баллов соответственно. Таким образом, применение Бризантина, наряду со снижением никотиновой зависимости, значимо повышало качество жизни участников исследования.
Рис. 7. Изменение качества жизни пациентов в процессе лечения р<0,0001 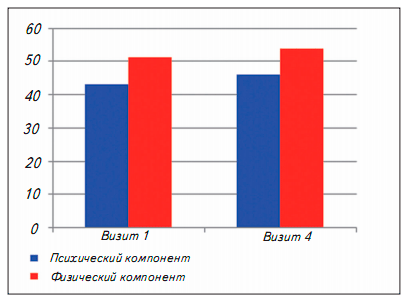
Анализ дополнительного критерия эффективности показал, что вес всех участников исследования не менялся в ходе 3 месяцев терапии. Среди пациентов, отказавшихся от курения, также не отмечено динамики веса: их средний показатель оставался стабильным в течение всех 12 недель приема препарата (табл. 1).
Таблица 1.
Динамика веса участников исследования в течение 12-недельного курса лечения
| Пациенты | Визиты | |||
| 1 | 2 | 3 | 4 | |
| Все участники исследования (n=248) | 76,9±14,5 | 77,0± 14,5 | 77,1±14,6 | 77,0±14,6 |
| Пациенты, отказавшиеся от курения (n=49) | 76,1±16,7 | 77,5±16,6 | 77,3±16,8 | 77,0±16,9 |
| В т.ч. пациенты с тяжелой НЗ (n=17) | 79,4±20,3 | 79,3±20,5 | 79,1±20,5 | 79,0±20,5 |
Одним из наиболее значимых эффектов лечения было анксиолитическое и антидепрессивное действие Бризантина, особенно у лиц, отказавшихся от курения. Несмотря на то, что исходно среднее значение подшкалы «Тревога» (НАDS) у всех участников исследования было низким (ниже 8 баллов), результаты тестирования свидетельствовали, что у 34% (n=88) пациентов при включении в исследование имела место субклинически (сумма баллов от 8 до 10; n=55; 21%) либо клинически (сумма баллов ≥11; n=33; 13%) значимая тревога.
Лечение Бризантином способствовало уменьшению доли пациентов с суб-/клиническими проявлениями тревоги: через 1 месяц - до 25% (n=65), через 2 месяца - до 1 3% (n= 33), к концу терапевтического курса их удельный вес сократился почти в 6 раз (n=16; 6%) Частотный анализ подтвердил значимое снижение удельного веса пациентов с отсутствием признаков тревоги (СМН: х2=72,9; р<0,0001) (рис. 8). Именно среди пациентов с исходной субклинически/ клинически значимой тревогой наиболее отчетливо проявился анксиолитический эффект Бризантина. За 1 2 недель применения препарата суммарный балл подшкалы HADS у них снизился вдвое - с 10,3±2,3 до 5,5±2,9 (Р3/243=1 1 3,8; р<0,0001).
Рис. 8. Доли пациентов с различной степенью выраженности тревоги в процессе лечения *р<0,0001 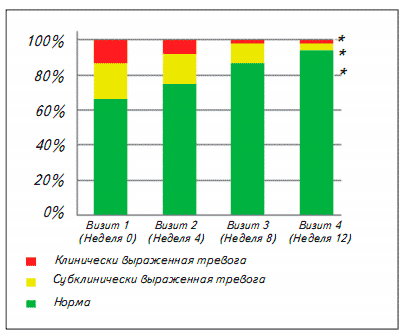
Показатель подшкалы «Депрессия» исходно превышал 7-балльное значение у 1 6% (n=40) участников, в том числе, у 1 3% (n=33) из них имела место субклинически и у 3% (n=7) - клинически выраженная депрессия. Лечение Бризантином в течение 1 2 недель привело к купированию депрессии у 11% (n=22) участников исследования; значимо сократилось число пациентов с субклинической (4%) и клинической (1 %) депрессией (СМН: х2=25,8; р<0,0001) (рис. 9). Значимое снижение среднего значения суммарного балла (с 9,3±1,6 до 5,7±2,7; р<0,0001) среди пациентов с исходной субклинически/клинически значимой депрессией подтверждало антидепрессивный эффект Бризантина.
Рис. 9. Доли пациентов с различной степенью выраженности депрессии в процессе лечения * p<0,0001 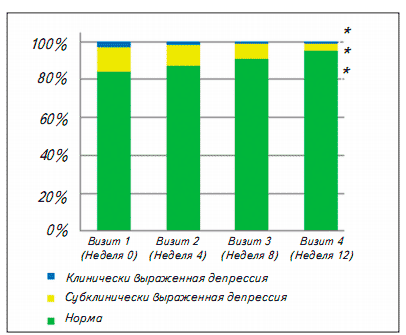
Мониторинг безопасности, который, помимо оценки влияния Бризантина на выраженность тревоги и депрессии, включал анализ витальных функций, регистрацию нежелательных явлений и повторные лабораторные исследования, не выявил каких-либо отклонений, достоверно связанных с терапией.
Выводы
Эффективность терапии, отмеченная в ходе клинического исследования, является, очевидно, результатом модифицирующего влияния компонентов Бризантина на функциональную активность молекул-мишеней - СВ1 -рецепторов и белка S100, вследствие чего снижается гиперактивация эндоканнабиноидной системы и устраняется нейромедиаторный дисбаланс [6, 7, 8, 10, 11]. В результате терапии нивелируются триггерные патогенетические механизмы, поддерживающие необходимость повторного приема никотина.
1. Результаты исследования свидетельствуют о том, что Бризантин - эффективное и безопасное средство для лечения никотиновой зависимости. Применение препарата в течение 1 2 недель привело к отказу от курения 20% участников исследования.
2. Действие препарата начинается с первых недель приема и прогрессивно нарастает по мере увеличения длительности лечения, что проявляется в увеличении числа пациентов, отказавшихся от курения в процессе терапии.
3. Отказ от курения на фоне лечения Бризантином не сопровождается развитием клинически значимого синдрома отмены, признаки абстиненции достаточно быстро угасают в процессе терапии. У пациентов, отказавшихся от курения после 4 недель приема Бризантина, симптомы отмены никотина выражены в наименьшей степени.
4. Прием Бризанитина значимо снижает никотиновую зависимость, что проявляется в прогрессивном уменьшении суммарного балла теста Фагерстрома. У лиц, отказавшихся от потребления никотина, желание курить на фоне приема Бризантина отсутствовало или было выражено в легкой степени;
5. 12-недельный курс лечения Бризантином приводит к уменьшению числа выкуриваемых сигарет и дозы потребления никотина, способствуя переводу лиц, продолжающих курить, в категорию нерегулярных курильщиков.
6. Лечение Бризантином улучшает физическое и ментальное здоровье пациентов, что наряду со снижением никотиновой зависимости, значимо повышает их качество жизни.
7. Отказ от курения на фоне приема Бризантина не приводит к прибавкам веса пациентов. Масса тела всех участников исследования, в том числе тех, кто отказался от курения, не увеличивается в течение всего курса терапии.
8. Прием Бризантина сопровождается значимым снижением симптомов тревоги и депрессии. Анксиолитический и антидепрессивный эффекты наиболее отчетливо выражены у лиц, отказавшихся от курения. Максимальное снижение суммарных баллов тревоги и депрессии отмечается среди пациентов, воздерживавших от курения более 4 недель.
9. Бризантин является безопасным лекарственным средством для лечения никотиновой зависимости. 12-недельный курс терапии в дозе 3-6 таблеток в сутки не приводит к развитию нежелательных явлений, в том числе, со стороны центральной нервной системы, не оказывает влияния на витальные функции, не вызывает патологических отклонений биохимических маркеров, показателей анализов крови и мочи, имеющих достоверную связь с приемом исследуемого препарата.
ЛИТЕРАТУРА:
1. Инициатива по освобождению от табачной зависимости
2. Guideline on the Development of Medicinal Products for the Treatment of Smoking. - European Medicines Agency, London, 18 December 2008. - Doc. Ref. CHMP/EWP/369963/05.
3. Cahill K., Stead L.F, Lancaster T. // Cochrane Database of Systematic Reviews. - 2008. - Issue 3. Art. No: P. CD006103. DOI -P 10.1002/14651858.CD006103.pub3. 4.
4. Hughes J. R., Stead L. F, Lancaster T. Antidepressants for smoking cessation. January 2010
5. Mills E.J., Wu P, Lockhart I., Wilson K., Ebbert J.O. Adverse events associated with nicotine replacement therapy (NRT) for smoking cessation. A systematic review and meta-analysis of one hundred and twenty studies involving 177,390 individuals. Tob Induc Dis. 2010;8:8.
6. Эпштейн О. И. Релиз-активность - от феномена до создания новых лекарственных средств // Бюллетень экспериментальной биологии и медицины. - 2012. - Том 157, №7. - С. 62-67.
7. Эпштейн О.И., Дыгай А.М., Шерстобоев Е.Ю., Сергеева С.А., Агафонов В.И., Боровская Т.Г, Ветошкина ТВ., Зуева Е.П., Жданов В.В., Суслов Н.И., Фомина Т.И., Гольдберг Е.Д. Экспериментальное исследование фармакологических эффектов сверхмалых доз антител к эндогенным регуляторам функций. // Бюл. экспер. биол. - 2008. - Приложение №2. - С.82-88.
8. Шабанов П.Д., Базиленко И.Б., Венков Д.А., Павлова Т. В. Нейроспецифический белок S-100 как основа создания противоалкогольных и анксиолитических препаратов: экспериментальный и клинический аспект//Материалы III съезда фармакологов России. - СПб. - 2007. - Т. 7; спец. выпуск. - С. 2009-10.
9. Tagirova RR, Timoshenko AKh, Gainutdinov KhL, Shtark MB, Epshtein OI. Serotonin precursor 5-hydroxytryptophan disturbs the protective effect of low doses of antibodies to S100B protein during the formation of long-term sensitization. Bull Exp Biol Med. 2009; Sep; 148(3): 560-2.
10. Духина И.А. Особенности антистрессорного действия тенотена (антитела к мозгоспецифическому белку S-100) в зависимости от типа эмоционально-стрессовой реакции (экспериментальное и клиническое исследование. //Автореф. дисс. ... канд. мед. наук. - Старая Купавна, 2006. - 23 с.
11. Шварков С.Б., Ширшова Е.В., Кузьмина В.Ю. Сверхмалые дозы антител кбелку S-100 в терапии вегетативных расстройств и тревоги у больных с органическими и функциональными заболеваниями ЦНС//Лечащий врач. - 2008. - №8. - С.83-85.
12. Voronina T.A., Sergeeva S.A., Martyushev-Poklad A.V., Dugina J.L., Epstein O.I. Antibodies to S-100 Protein in Anxiety-Depressive Disorders in Experimental and Clinical Conditions // “Animal Models in Biological Psychiatry", edit. Kalueff A.V. - New York, Nova Science Publishers, 2006. - Chapter 8. - P 137-152.
13. Voronina TA, Kheyfets IA, Molodavkin GM, Dugina YL, Borodavkina MV, Sergeeva SA, Epshtein OI. Antiaggressive activity of antibodies to S-100 protein in ultralow doses. Bull Exp Biol Med. 2009 Sep; 148 (3): 527-9.
14. Epstein OI, Pavlov IF, Shtark MB. Improvement of Memory by Means of Ultra-Low Doses of Antibodies to S-100B Antigen. Evid Based Complement Alternat Med. 2006 Dec; 3(4): 541-5.
15. Heatherton TF, Kozlowski LT, Frecker RC, Fagerstrom KO. The Fagerstrom test for nicotine dependence: a revision of the Fagerstrom Tolerance Questionnaire. Br J Addict 1991;86:1119-27.
16. Zigmond A. S., Snaith R.P The Hospital Anxiety and Depression scale // Acta Psychiatr. Scand. - 1983. - Vol. 67. - P 361-370.
Комментарии
ПРАКТИКА ПЕДИАТРА
