Лекарственные формы фторхинолонов с замедленным высвобождением
СтатьиОпубликовано в журнале:
«Антибиотики и химиотерапия» »» Том 49, 12, 2004.
С.В. Сидоренко
Государственный научный центр по антибиотикам, Москва.
Клиническая эффективность этиотропной терапии инфекционных болезней человека определяется уровнем природной активности антибактериального препарата в отношении патогена, наличием или отсутствием у последнего приобретенной резистентности, фармакокинетическими характеристиками препарата и точностью соблюдения пациентами режимов дозирования (выполняемостью).
К наиболее очевидным параметрам, оказывающим непосредственное влияние на исполнительность пациентов, а, следовательно, и на эффективность лечения, относится кратность приема препаратов в течении дня. Чем выше кратность приема, тем вероятнее нарушение режима дозирования и наоборот. Опубликованы данные о том, что при 3-кратном приеме препаратов режим дозирования соблюдают лишь 37.7% пациентов, при 2-кратном приеме – 68.9%, и при 1-кратном – до 79.6% [1]. Очевидно, что наилучшую выполняемость у пациентов удается обеспечить при приеме препаратов один раз в сутки.
С этой точки зрения вполне оправданным представляется стремление компаний-производителей антибактериальных препаратов к созданию средств, пригодных для однократного применения. К наиболее удачным примерам реализации такого подхода относится разработка макролидного антибиотика азитромицина, уникальные фармакокинетические свойства которого (формирование высоких концентраций внутри клеток человека и длительный период полувыведения) определяются его химической структурой. Однако в настоящее время появились подходы, позволяющие изменять режим дозирования и для хорошо известных препаратов. Речь, прежде всего, идет о создании специальных лекарственных форм, обеспечивающих замедленное высвобождение антибактериальных препаратов. Лекарственные формы с замедленным высвобождением должны обеспечивать возможность однократного приема при сохранении клинической и бактериологической эффективности на уровне традиционных лекарственных форм. Сохранение высоких показателей эффективности возможно в том случае если фармакокинетика лекарственных форм с замедленным высвобождением будет соответствовать особенностям фармакодинамики конкретных антибактериальных препаратов.
Фармакокинетика фторхинолонов при приеме лекарственных форм с замедленным высвобождением.
К наиболее интересным, из присутствующих на Российском рынке лекарственных форм с замедленным высвобождением относятся ципрофлоксацин (Цифран ОД) и офлоксацин (Заноцин ОД). При создании лекарственных форм фторхинолонов с замедленным высвобождением необходимо было обеспечить выполнение нескольких требований, определяемых особенностями фармакодинамики этой группы препаратов. Прежде всего показатель площади под фармакокинетической кривой (area under the curve - AUC) за период 24 ч при однократном в сутки приеме всей суточной дозы должен быть равен показателю, получаемому при дробном приеме. Пик концентрации препарата в сыворотке крови должен быть максимально высоким, но не превосходить безопасный уровень. Указанные требования определяются выраженной зависимостью бактерицидной активности фторхинолонов от их концентрации.
Лекарственные формы фторхинолонов c замедленным высвобождения представляют собой двухслойные таблетки, покрытые оболочкой. Из наружного слоя, происходит быстрое высвобождение фторхинолона, а из внутреннего – замедленное. В результате изменений в скорости высвобождения препаратов изменяется и скорость их всасывания. При приеме таблетки ципрофлоксацина 35% от общей дозы высвобождается и всасывается практически немедленно, а оставшиеся 65% - высвобождаются и всасывается в течение 3 ч. Важно отметить, что всасывание препарата происходит в верхних отделах желудочно-кишечного тракта (желудке и 12-ти перстной кишке) и отличается незначительной вариабельностью у отдельных лиц. По данным популяционной фармакокинетики коэффициент вариабельности процессов всасывания при приеме лекарственных форм немедленного высвобождения достигает 78.8%, а при приеме лекарственных форм замедленного высвобождения – 29.5% [2]. Прием пищи не влияет на абсолютные цифры всасывания ципрофлоксацина в лекарственной форме с замедленным высвобождением [3], но несколько увеличивает время нахождения препарата в верхних отделах желудочно- кишечного тракта. Это обстоятельство дополнительно удлиняет действие препарата.
Изменения в динамике всасывания фторхинолонов приводят к существенным изменениям в общей фармакокинетике этих препаратов. Фармакокинетические константы ципрофлоксацина при его приеме в различных дозах в лекарственных формах немедленного и замедленного высвобождения приведены в табл. 1.
Таблица 1.
Фармакокинетика ципрофлоксацина при приеме различных лекарственных форм
|
Лек.форма, доза, кратность приема |
Cmax (мкг/мл) |
AUC0-24 ч (мг•ч/л) |
T1/2 (ч) |
Tmax (ч) |
|
Ципрофлоксацин немедленного высвобождения, 500 мг, 2 р.д. |
2.06 ± 1.08 |
17.04 ± 4.79 |
5.66 ± 0.89 |
2.0 (0.5-3.5) |
|
Ципрофлоксацин замедленного высвобождения, 500 мг, 1 р.д. |
1.59 ± 0.43 |
7.97 ± 1.87 |
6.6 ± 1.4 |
1.5 (1.0-2.5) |
|
Ципрофлоксацин замедленного высвобождения, 1000 мг, 1 р.д. |
3.11 ± 1.08 |
16.83 ± 5.65 |
6.31 ± 0.72 |
2.0 (1-4) |
Стандартная суточная терапевтическая доза ципрофлоксацина для лечения осложненных инфекций мочевыводящих путей в настоящее время составляет 1000 мг, при неосложненных инфекциях суточная доза может составлять 500 мг. Предпринятые в свое время попытки сократить суточную дозу до 100 – 125 мг не дали положительных клинических результатов. Наибольший интерес представляет сопоставление фармакокинетических параметров ципрофлоксацина в лекарственной форме для замедленного высвобождения при однократном приеме 1000 мг и обычной лекарственной формы при двукратном приеме по 500 мг. Как следует из материалов таблицы, площадь под фармакокинетической кривой за 24 ч для обоих режимов практически одинакова. В то же время при однократном приеме 1000 удается получить существенно более высокий показатель максимальной концентрации в сыворотке крови.
Элиминации ципрофлоксацина из организма осуществляется в основном через почки, при этом до одной трети препарата выводится в неизмененном виде. При сопоставлении концентраций ципрофлоксацина в моче после приема 1000 и 500 мг в лекарственной форме замедленного высвобождения и двукратного приема по 250 мг обычного ципрофлоксацина выявляются закономерные различия (Рис.1) [4]. В течение первых 12 ч после приема 500 мг препарата в форме замедленного высвобождения концентрация ципрофлоксацина в моче существенно выше, чем после первого приема 250 мг немедленного высвобождения, но после второго приема 250 мг в этой же форме концентрация препарата в моче повышается. Однако для практики важно то, что даже через 24 ч после приема 1000 мг концентрация ципрофлоксацина в моче остается достаточно высокой ( 60 – 70 мкг/мл).
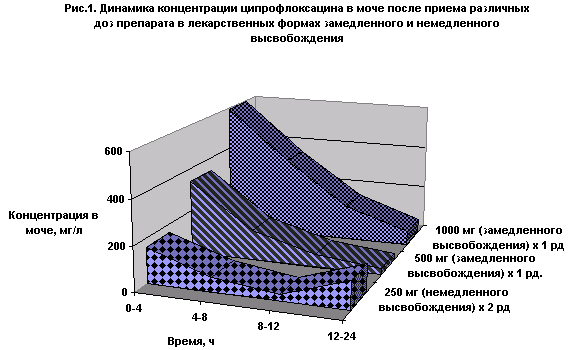
Фармакодинамика фторхинолонов при приеме в виде лекарственных форм для замедленного высвобождения.
Зависимость эффективности антибактериальной терапии от особенностей фармакокинетики препаратов, с точки зрения здравого смысла, очевидна, однако, конкретные закономерности этой зависимости имеют достаточно сложный характер. Выраженность антибактериального действия в очаге инфекции (фармакодинамика антибиотиков) определяется фармакокинетикой препаратов и особенностями их взаимодействия с патогенами при различных концентрациях. Однако оказалось, что сами по себе ни фармакокинетические (максимальная концентрация препарата в сыворотке крови, период полувыведения, площадь под фармакокинетической кривой), ни фармакодинамические параметры (ингибирующая, бактерицидная активность, постантибиотический эффект) не позволяют осуществить прогноз эффективности лечения.
Возможность прогнозирования эффективности антибиотиков появилась лишь в результате детального изучения закономерностей антибактериального действия различных препаратов in vitro, их эффективности при экспериментальных инфекциях и в клинике. Высокая прогностическая ценность была выявлена у ряда комплексных фармакокинетических/фармакодинамических (ФК/ФД) параметров. Такими параметрами оказались: отношение площади под фармакокинетической кривой к МПК возбудителя (AUC/MIC), отношение максимальной концентрации в крови к МПК (Сmax/MIC), а также время, в течение которого концентрация антибиотика в крови превосходит МПК . Причем для антибактериальных препаратов разных групп ценность отдельных параметров оказалась различной.
Установлено, что клиническая эффективность фторхинолонов наилучшим образом коррелирует с величиной параметров AUC/MIC [6]. Анализ результатов моделирования фармакокинетики in vitro, лечения экспериментальных инфекций и клинических наблюдений проведенный рядом исследователей [7, 8] позволяет сделать следующие заключения. При величине параметра AUC/MIC < 60 фторхинолоны проявляют умеренную бактериостатическую активность их эффект в клинике во многом определяется синергизмом с факторам резистентности макроорганизма (фагоцитами, комплементом и др.). При величине параметра AUC/MIC от 60 до 250 препараты проявляют умеренную бактерицидную активность, клинический эффект проявляется в течение 7 дней и более. Высокую бактерицидную активность и быструю эрадикацию патогена в клинике удается обеспечить при величине указанного соотношения более 250. В то же время в других работах приводят данные о высокой клинической эффективности фторхинолонов при режимах обеспечивающих значения параметра AUC/MIC 25 [9].
Для прогнозирования клинической эффективности ципрофлоксацина в лекарственной форме с замедленным высвобождением были проведены специальные эксперименты по моделированию его фармакокинетики in vitro [10]. В специальной камере с помощью перистальтических насосов воспроизводили динамику концентрации ципрофлоксацина полностью аналогичную динамике концентрации препарата в сыворотке крови человека при приеме различных доз ципрофлоксацина в обычной лекарственной форме и в форме с замедленным высвобождением. Питательный бульон, находящийся в камере, засевали штаммами Escherichia coli с различным уровнем устойчивости к ципрофлоксацину (МПК = 0.03, 0.5 или 2.0 мкг/мл) и наблюдали за динамикой размножения или отмирания бактерий.
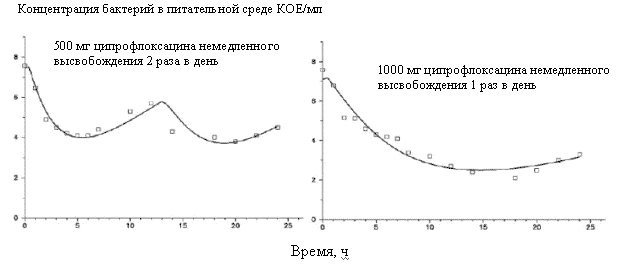
В результате экспериментов было установлено, что при моделировании двукратного приема обычной лекформы ципрофлоксацина по 500 мг или 1000 мг в форме с замедленным высвобождение в течение 6 - 7 ч происходит полное отмирание высокочувствительных бактерий (МПК = 0.03 мкг/мл). Если же МПК штамма составляла 0.5 мкг/мл, то динамика микробной обсемененности питательной среды была совершенно иной (Рис.2). После первоначального снижения обсемененности питательной среды наблюдали возобновление роста культуры E. coli. Однако при моделировании приема 1000 мг ципрофлоксацина в форме с замедленным высвобождением через 24 ч уровень обсемененности среды был значительно ниже чем при моделировании двукратного приема обычной лекарственной формы по 500 мг. Таким образом, несмотря на одинаковые значения параметров AUC и AUC/MIC лекарственная форма с замедленным высвобождением обеспечивает большее отмирание умеренно устойчивого штамма. Причину этого факта авторы видят в более высоких пиковых концентрациях ципрофлоксацина, создающихся при приеме лекарственной формы с замедленным высвобождением. При МПК бактерий 2.0 мкг/мл обе лекарственные формы вызывали лишь незначительное отмирание культуры и не предотвращали быстрое возобновление ее роста. Практически важным выводом из результатов приведенной работы является выявление преимуществ лекарственной формы с замедленным высвобождением в отношении штаммов со сниженной чувствительностью к ципрофлоксацину.
Рис. 2.
Динамика отмирания E. coli при фармакокинетическом моделировании приема различных доз ципрофлоксацина
Для прогнозирования клинической эффективности лечения инфекций мочевыводящих путей необходимо сравнение концентраций антибактериальных препаратов в моче и значения МПК основных уропатогенов, при этом необходимо принимать в учет локальный уровень антибиотикорезистентности. По нашим наблюдениям в Москве в настоящее время наблюдается тенденция к росту резистентности основных уропатогенов к фторхинолонам и, в частности, к ципрофлоксацину, различный уровень устойчивости проявляют до 10% штаммов грамотрицательных бактерий. Параметром, позволяющим в определенной степени охарактеризовать локальную ситуацию, может быть значение МПК, ингибирующей 90% штаммов (МПК90). Этот показатель для ведущих грамотрицательных возбудителей инфекций мочевыводящих путей (Escherichia coli, Klebsiella pneumoniae и Proteus spp.) равен 4.0 мкг/мл. Распределение МПК ципрофлоксацина в отношении указанных бактерий представлено на рис. 3.
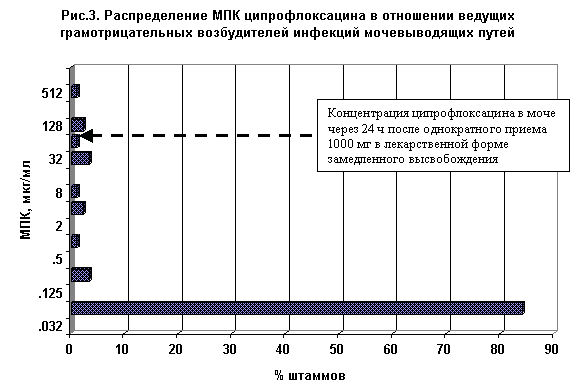
Клиническая эффективность фторхинолонов в лекарственных формах замедленного выведения.
Наибольшее количество исследований о клинической эффективности фторхинолонов с замедленным высвобождением касаются изучения ципрофлоксацина при инфекциях мочевыводящих путей.
При неосложненных инфекциях мочевыводящих путей у женщин в рандомизированных испытаниях с двойным слепым контролем сравнивали эффективность 3-х дневных курсов при однократном приеме 500 мг ципрофлоксацина с замедленным высвобождением и двукратном в сутки приеме 250 мг ципрофлоксацина в обычной лекарственной форме [11]. В исследование были включены 891 женщина, эффективность оценивали на 5-11 и 28-42 дни после окончания лечения. Клиническая эффективность ципрофлоксацина в лекарственной форме замедленного высвобождения в приведенные выше периоды оценки составила 97% и 83% соответственно. Клиническая эффективность препарата в обычной лекарственной форме была на несколько процентов ниже, но различия не достигали статистической значимости. Бактериологическая эффективность ципрофлоксацина в форме замедленного высвобождения в те же сроки оценки составила соответственно 88.8% и 69.3% и была выше чем у препарата в форме с немедленным высвобождением. В целом эти данные позволяют рекомендовать использование ципрофлоксацина с замедленным высвобождением при неосложненных инфекциях мочевыводящих путей у женщин и при этом рассчитывать на эффективность как минимум не меньшую чем у препарата в лекарственной форме с немедленным высвобождением.
В проспективном исследовании по оценке 3-дневного курса ципрофлоксацина в форме с замедленным высвобождением (500 мг однократно), включившем 7360 женщин с неосложненными инфекциями мочевыводящих путей, клинический эффект через 2-7 дней после окончания лечения был получен в 91.3% случаев, не было выявлено зависимости от возраста и других демографических характеристик [12]. Интересно отметить, что дизайн этого исследования в максимальной степени приближался к реальным условиям амбулаторной практики. Ципрофлоксацин назначали 1900 врачей общей практики в ходе их повседневной работы.
В многоцентровом плацебо контролируемом исследовании при остром неосложненном пиелонефрите и осложненных инфекциях мочевыводящих путей сравнивали эффективность лекарственной формы ципрофлоксацина замедленного высвобождения (1000 мг однократно) и обычной формы (500 мг 2 раза в день), длительность курсов составляла 7 – 14 дней [13]. Ципрофлоксацин в лекарственной форме замедленного высвобождения проявлял несколько большую клиническую и бактериологическую эффективность как на 5-11, так и на 28-42 дни после окончания лечения (различия статистически недостоверны). Интересно отметить тот факт, что применение ципрофлоксацина в лекарственной форме замедленного высвобождения сопровождалось меньшей частотой реинфекций и персистенции возбудителей.
Офлоксацин в лекарственной форме замедленного высвобождения изучен не столь подробно. В сравнительном исследовании показана равная эффективность офлоксацина в лекарственной форме замедленного высвобождения (800 мг однократно в сутки) и обычной лекарственной формы офлоксацина (400 мг 2 раза в сутки) при неосложненных инфекциях кожи и мягких тканей [14]. В несравнительных исследованиях показана эффективность офлоксацина в форме замедленного высвобождения при обострении хронического бронхита и внебольничной пневмонии, а также при осложненных инфекциях мочевыводящих путей [14].
В отечественной литературе опубликованы результаты исследований эффективности офлоксацина при воспалительных заболеваниях органов малого таза у женщин. Комбинация офлоксацина замедленного высвобождения (800 мг однократно в сутки) и метронидазола (тинидазола) по эффективности не уступала комбинации амоксициллина/клавуланата с макролидами или доксициклином [15]. Сопоставление офлоксацина замедленного высвобождения (800 мг однократно) при 10-ти дневном курсе и обычной лекарственной форм (400 мг 2 раза в день) при стандартном 14-ти дневном курсе также показало равную эффективность обоих режимов (во всех случаях офлоксацин комбинировали с тинидазолом) [16].
Заключение.
Таким образом, фармакокинетические параметры ципрофлоксацина в виде лекарственной формы с замедленным высвобождением обосновывают возможность однократного приема всей суточной дозы 1000 мг. Более того, учитывая фармакодинамические особенности действия препарата (зависимая от концентрации бактерицидная активность), однократный прием 1000 мг ципрофлоксацина замедленного высвобождения имеет преимущества перед двумя дозами по 500 мг обычного ципрофлоксацина за счет более выраженного бактерицидного действия.
Необходимо также подчеркнуть и то, что при назначении 1000 мг ципрофлоксацина в виде лек.формы с замедленным высвобождением максимальная концентрация препарата в сыворотке крови не превосходит безопасный уровень, в отличие от этого при приеме такой же дозы в виде обычной лек.формы концентрация препарата в крови превосходит 4.0 мкг/мл. С точки зрения безопасности существенным моментом является также отсутствие кумуляции при приеме повторных доз ципрофлоксацина с замедленным высвобождением.
Результаты экспериментального изучения фторхинолонов в лекарственных формах для замедленного выведения полностью подтверждаются данными о высокой клинической эффективности и безопасности, полученными в клинических испытаниях. Как ципрофлоксацин, так офлоксацин в указанных лекарственных формах проявили высокую клиническую и бактериологическую эффективность при неосложненных и осложненных инфекциях мочевыводящих путей, инфекциях кожи и мягких тканей, а также при внебольничных инфекциях дыхательных путей.
1 Cockburn J, Reid AL, Bowman JA, Sanson-Fisher RW: Effects of intervention on antibiotic compliance in patients in general practice. Med J Aust 1987;147:324-328.
2 Theil FP, Frede M, Stass H: Population pharmacokinetic characterization of the new ciprofloxacin MR formulation with ciprofloxacin IR. Clin Microbiol Infect 2003;9:292 [abstract p.1228].
3 Stass H, Nagelschmitz J, Brendel E, Schuekler F: The effect of food on the pharmakokinetics of a new ciprofloxacin onece daily formulation for treatment of uncomlicated urinary tract infections. J Investig Med 2002;50:154A [Abstract 23].
4 Stass H, Nagelschmitz J, Brendel E, Schuekler F: Pharmacokinetic characterisation of a new ciprofloxacin once daily formulation for treatment of uncomplicated urinary tract infections. J Investig Med 2002;50:155A [Abstract 24].
5 Forrest A, Nix DE, Ballow CH, Goss TF, Birmingham MC, Schentag JJ: Pharmacodynamics of intravenous ciprofloxacin in seriously ill patients. Antimicrob Agents Chemother 1993;37:1073-1081.
6 Preston SL, Drusano GL, Berman AL, Fowler CL, Chow AT, Dornseif B, Reichl V, Natarajan J, Corrado M: Pharmacodynamics of levofloxacin: a new paradigm for early clinical trials. JAMA 1998;279:125-129.
7 Schentag JJ, Meagher AK, Forrest A: Fluoroquinolone AUIC break points and the link to bacterial killing rates. Part 1: In vitro and animal models. Ann Pharmacother 2003;37:1287-1298.
8 Schentag JJ, Meagher AK, Forrest A: Fluoroquinolone AUIC break points and the link to bacterial killing rates. Part 2: human trials. Ann Pharmacother 2003;37:1478-1488.
9 Drusano GL, Preston SL, Fowler C, Corrado M, Weisinger B, Kahn J: Relationship between fluoroquinolone area under the curve: minimum inhibitory concentration ratio and the probability of eradication of the infecting pathogen, in patients with nosocomial pneumonia. J Infect Dis 2004;189:1590-1597.
10 Meagher AK, Forrest A, Dalhoff A, Stass H, Schentag JJ: Novel Pharmacokinetic-Pharmacodynamic Model for Prediction of Outcomes with an Extended-Release Formulation of Ciprofloxacin. Antimicrob Agents Chemother 2004;48:2061-2068.
11 Henry DC, Jr., Bettis RB, Riffer E, Haverstock DC, Kowalsky SF, Manning K, Hamed KA, Church DA: Comparison of once-daily extended-release ciprofloxacin and conventional twice-daily ciprofloxacin for the treatment of uncomplicated urinary tract infection in women. Clin Ther 2002;24:2088-2104.
12 Bayer Pharmaceutical. Data on file. 2005.
Ref Type: Data File
13 Talan DA, Klimberg IW, Nicolle LE, Song J, Kowalsky SF, Church DA: Once daily, extended release ciprofloxacin for complicated urinary tract infections and acute uncomplicated pyelonephritis. J Urol 2004;171:734-739.
14 Регистрационные документы по препарату Заноцин ОД для Российской Федерации; часть IV Клиническая документация; том 1, раздел Клиническое изучение; отчёты о мультицентровых клинических испытаниях; июль 2001 г.
15 А.Н. Стрижаков, А.И. Давыдов. КЛИНИЧЕСКАЯ ОЦЕНКА ЭФФЕКТИВНОСТИ ПРОЛОНГИРОВАННОЙ ФОРМЫ ОФЛОКСАЦИНА (ZANOCIN OD) В ЛЕЧЕНИИ БОЛЬНЫХ ОСТРЫМ САЛЬПИНГООФОРИТОМ «Вопросы гинекологии, акушерства и перинатологии» 2004, том 3, № 3
16 О.Г.Пекарев, Т.В.Киселева Новые подходы в терапии острых воспалительных заболеваний придатков матки. нОВОСИБИРСК., 2005.
Комментарии
ПРАКТИКА ПЕДИАТРА
