Первый опыт количественной оценки результатов терапевтического ангиогенеза
СтатьиОпубликовано в журнале:
Клеточная трансплантология и тканевая инженерия Том VII, № 4, 2012
И.И. Кательницкий, Иг.И. Кательницкий, Г.А. Алексеева
Ростовский Государственный медицинский Университет, Ростов-на-Дону
The First experience of quantitative evaluation of therapeutic angiogenesis results
I.I. Katelnitskiy, Ig.I. Katelnitskiy, G.A. Alexeeva Rostov State Medical University, Rostov-on-Don
Цель работы — объективная оценка эффективности терапевтического ангиогенеза у больных критической ишемией нижних конечностей атеросклеротической этиологии. Установлено, что индукция ангиогенеза препаратом Неоваскулген проявляется в ближайшем периоде хорошим клиническим эффектом, что сопровождается приростом тканевого кровотока, по данным лазерной допплерфлоуме-трии. Использование ангиосцинтиграфии c технецием-пер-технитатом-макроагрегатом при внутриартериальном введении препарата позволило объективно оценить прирост кровотока по увеличению объему сосудистого русла.
Ключевые слова: терапевтический ангиогенез, лечение больных облитерирующим атеросклерозом, качество жизни.
The goal of research is objective evaluation of effectiveness of therapeutic angiogenesis in patients with critical lower limb ischemia of the atherosclerotic etiology. It was shown that angiogenesis induction by drug Neovasculgen was manifested by good clinical effect in the nearest period and that was confirmed by growth of tissue blood flow according to laser Doppler flowmetry. Use of technetium-pertehnetate-macroaggregates angioscintigraphy with intra-arterial administration of the drug allowed to assess objectively the increase of blood flow to the increased volume of the vascularbed.
Key words: therapeutic angiogenesis, treatment of patients with atherosclerosis obliterans, the quality of life.
Диффузное поражение артерий голени, как правило, является противопоказанием к реконструктивной сосудистой операции [1—3]. С учетом того, что подобное сочетание поражений магистральных артерий характерно для значительного контингента больных с сосудистой патологией, а прогноз консервативного лечения у них крайне неблагоприятен, в подавляющем большинстве случаев в ближайшее время возникают показания к ампутации конечности [4—6]. Альтернативой ампутации у таких пациентов возможна реализация процедур терапевтического ангиогенеза, позволяющих увеличить плотность капилляров и уменьшить сосудистое сопротивление в области ишемии, обеспечив доставку крови в ми-кроциркуляторное русло [7—9].
Первый опыт применения геннотерапевтическо-го препарата «Неоваскулген», содержащего в качестве активного вещества плазмидную ДНК с геном vegf165 позволил говорить о клинической эффективности препарата: исчезали боли, увеличивалась дистанция безболевой ходьбы, увеличивалось тканевое напряжение кислорода. Вместе с тем, для объективной оценки применялся только лодыжечно-плечевой индекс (ЛПИ). Однако данный показатель не может быть измерен у пациентов с окклюзиями всех артерий голени. В этой связи вопрос объективной оценки состояния сосудистого русла у пациентов на фоне использования препарата «Неоваскулген» является актуальным. Известно, что с помощью ан-гиоартериографии возможно получить информацию о сохранности кровоснабжения тканей при окклюзиях артерий [10, 11]. При стандартной методике (внутривенном введении 99mTc пирфотеха) определяются зоны ишемии или некроза мышц, в которых он фиксировался.
Для количественной оценки проходимых капилляров в тканях конечностей применен комплекс радиофармпрепарата с белком, размер которого превышает диаметр капилляра. При внутриартери-альном введении макроагрегата он задерживается в капиллярах. При этом его количество будет больше в тех тканях, где имеется наибольшее количество проходимых капилляров. Такая методика позволяет оценить в динамике сосудистый бассейн, то есть выполнить количественную оценку неоангиогенеза.
Материал и методы
В работе оценены краткосрочные клинические результаты (30 сут.) лечения препаратом «Неова-скулген» и возможность количественного определения состояния сосудистого бассейна у четырех больных с атеросклеротическими окклюзиями бедренных артерий и окклюзиями или выраженными стенозами артерий голени с III степенью ишемии. Всем больным выполнено ангиографическое исследование, о тканевом кровотоке стоп судили с помощью лазерной допплерфлоуметрии. Ангиосцинтиграфия выполнялась путем введения препарата 99мТс-макротех — 130 МБк в пораженную конечность до начала и через месяц после окончания лечения на аппарате Гамма-камера SKYLight Az8 PHILIPS. Эффективная доза составила 4мЗв.
Все исследования выполнены в соответствии с «Всеобщей декларацией о биоэтике и правах человека» (2005).
Результаты и обсуждение
Клинический результат в виде уменьшения болей в покое или при ходьбе отмечен у всех больных уже через неделю после местного внутримышечного введения препарата. При этом у двоих из них отмечен достоверный прирост показателей тканевого кровотока на стопах. К моменту второго введения (14 сут.) тканевой кровоток увеличился у всех пациентов. Через две недели после второго введения он приростал на стопах в среднем на 15%, а в области нижней трети голени на 60—70%.
По данным ангиосцинтиграфии количество радиофармпрепарата, фиксированного в нижних конечностях увеличивалось у всех 4 пациентов на 35, 45, 47,3 и 55% соответственно (табл.). В основном это касается мышечного массива (рис. 1, 2).
Полученные результаты позволяют говорить о значительной стимуляции ангиогенеза и увеличении количества проходимых капилляров под воздействием «Неоваскулгена».
Таким образом, первый опыт применения методик количественной оценки показал его высокую достоверность: в ишемизированных конечностях количество радиофармпрепарата снижается пропорционально нарастанию степени ишемии.
У всех пациентов отмечен более активный прирост сосудов в дорзальных отделах голеней. Наблюдения за больными продолжаются и исследования будут повторены через 3 и 6 мес. после лечения. Планируется также усовершенствование методики сцинтиграфии с целью оценки прироста сосудов в единице объема тканей. Однако уже первые результаты использования ангиосцинтиграфии позволяют говорить о том, что метод является достоверным и подтверждает клинический эффект лечения Неоваскулгена.
Динамика ангиосцинтиграфической картины до и после лечения Неоваскулгеном
|
Количество радиофармпрепарата (%) |
Пациент № 1 |
Пацинт № 2 |
Пациент № 3 |
Пациент № 4 |
|
До лечения |
29 |
31,2 |
31,3 |
33,8 |
|
Через 30 сут. после введения препарата |
64 |
76,2 |
86,3 |
81,1 |
|
Разница |
35 |
45 |
55 |
47,3 |
Рис. 1. Кровоток в тканях нижней конечности на фоне лечения препаратом Неоваскулген, пациент № 3: А - до лечения;
Б - через месяц (2 нед. после второй инъекции) после лечения. Ant - сосуды передней поверхности конечности; Post - сосуды задней поверхности конечности. Ангиосцинтиграфия
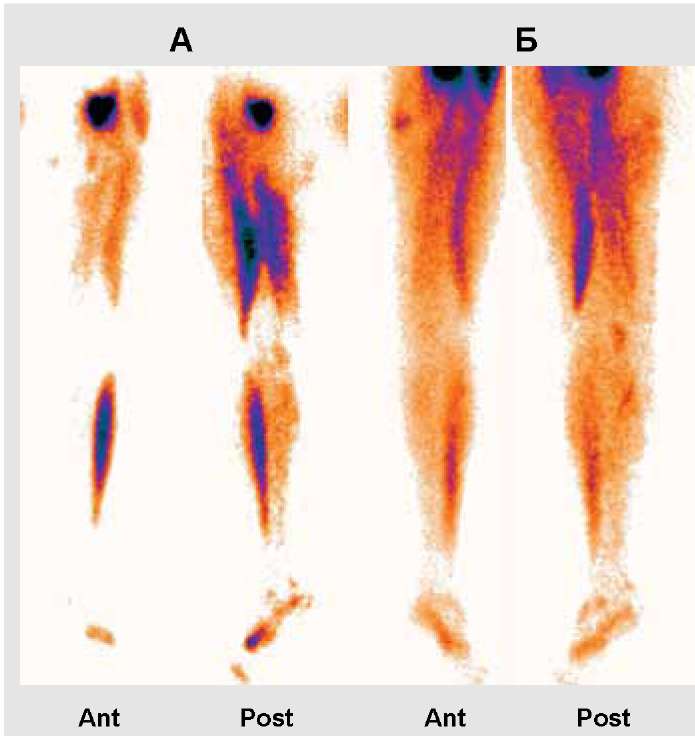
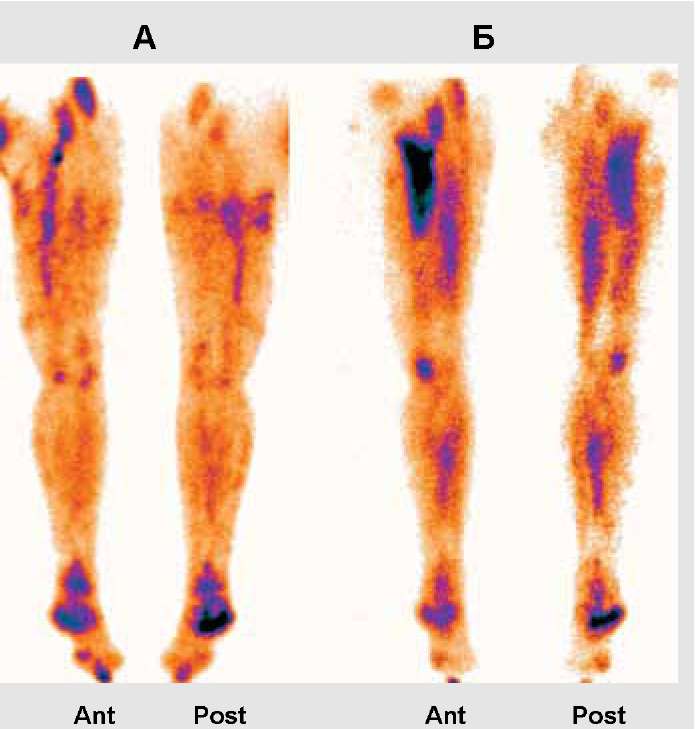
Рис. 2. Кровоток в тканях нижней конечности на фоне лечения препаратом Неоваскулген, пациент № 4:
А - до лечения; Б - через месяц (2 нед. после второй инъекции) после лечения.
Литература:
1. Покровский А.В., Москаленко Ю.Д., Кияшко В.А. Реконструктивные операции при тяжелой ишемии нижних конечностей. Хирургия 2007; 11: 20—7.
2. Покровский А.В. Клиническая ангиология: руководство для врачей. М.: Медицина; 2004.
3. Kosch M., Hausberg M., Westermann G. et al. Alteration in calcium and magnesium content of red cell membranes in patient with primary hypertension. Am. J. Hypertension 2000; 3: 254—8.
4. Dominguez L.J., Barbagallo M., Sowers J.R. et al. Magnesium responsiveness to insulin and insulin-like growth factor I in erythrocytes from normotensive and hypertensive subjects. J. Clin. Endocrinol. Metab. 1998; 12: 4402—7.
5. Handengue A.L., Del-Pino M., Simon A. et al. Erythrocyte disaggregation shear stress, sialic acid, and cell aging in humans. Hypertension 1998; 2: 324—30.
6. McDonald W., Blake M.P. Periostitis and localized myositis in polyarteriitis nodosa. Clin. Nucl. Med. 2004; 29(11): 547—9.
7. Аверьянов М.Ю., Измайлов С.Г. Тромбозы и эмболии магистральных артерий. Нижний Новгород; 2007.
8. Свирщевский Е.Б., Чазова Т.Е. Микроциркуляция в нижних конечностях при диабете. Вестник РАМН 2002; 5: 45—51.
9. Soyer H., Ulsu I. A patient with peripheral arterial stenosis diagnosed with low extremity perfusion scintigraphy. Clin. Nucl. Med. 2007; 32(6): 458—9.
10. Лишмакова Ю.Б., Чернова В.И. Радионуклидная диагностика для практических врачей. Томск; 2004.
11. Ishiyama K., Tomura N., Okada K. et al. Evaluating benign and malignant musculoskeletal lesions with radionuclide angiography and SPECT using Tc-99m-MIBb. Clin. Nucl. Med. 2005; 30(9): 598—603.
Поступила 24.12.2012
