СМОФлипид: Доклиническая и клиническая оценка эффективности, безопасности и переносимости
Статьи(Соевое масло, среднецепочечные триглицериды, оливковое масло, рыбий жир)
(Июнь 2010). Australian public assessment report for soya oil, medium chain triglycerides, olive oil, fish oil. proprietary product name: smoflipid
Детали продукта.
Новая комбинация жировых эмульсий, одобрена к применению в Австралии 15 марта 2010 года, содержит соевое масло, среднецепочечные триглицериды, оливковое масло, рыбий жир; эмульсия для внутривенного введения.
Содержание компонентов: Соевое масло - 6%, МСТ - 6%, Оливковое масло - 5%, Рыбий жир - 3%. Упаковка: пластиковый инфузионный мешок (контейнер). Дозировки: 100, 250 и 500 мл. Дозировки: взрослые - стандартная доза 1-2 г жиров/кг веса тела/день, что соответствует 5-10 мл эмульсии/кг веса тела/день. Рекомендуемая скорость инфузии -0,125 г жира/кг массы тела/час, что соответствует 0,63 мл СМОФлипида на кг массы тела/час, но не должна превышать 0,15 г жира/кг массы тела/час, что соответствует 0,75 мл СМОФлипида/кг массы тела/час. Дети: рекомендуется не превышать суточную дозу в 2 г жира/кг массы тела/день, что соответствует 10 мл СМОФлипида/кг веса тела/день. С увеличением потребностей у детей раннего возраста максимально возможное значение этого показателя должно составлять 3 г жира/кг массы тела/день. Новорожденные и младенцы: начальная доза должна составлять от 0,5-1 г жира/кг массы тела/день с последующим увеличением на 0,5-1 г жира/кг массы тела/день до 3 г жира/кг массы тела/день. Рекомендуется не превышать суточную дозу более 3 г жира/кг массы тела/день, что соответствует 15 мл СМОФлипида/кг массы тела/день. Скорость инфузии не должна превышать 0,125 г жира/кг массы тела/час. У недоношенных и детей, родившихся с низкой массой тела (LBW) СМОФлипид должен инфузироваться непрерывно в течение 24 часов.
Исходные данные для продукта.
Существует два принципиальных источника энергии для организма: углеводы и липиды. Глюкоза - углевод выбора. Этот физиологический субстрат требуется мозгу и метаболизируется всеми тканями организма. Концентрированный раствор глюкозы должен быть дан для удовлетворения потребностей в калориях. Липиды дают больше энергии на единицу объема, чем углеводы, и позволяют избежать осложнений, связанных с введением глюкозы (1). Возникновение концепции СМОФлипида связано с наличием определенных осложнений, характерных для существующих жировых эмульсий. В оригинальной технике полного парентерального питания (ППП, TPN) глюкоза±этиловый алкоголь использовались как источник энергии. В то же время проблемы гипергликемии (2) и дефицит незаменимых жирных кислот диктовали необходимость использования и липидов в качестве источника энергии с целью минимизации этих проблем.
Внутривенные жировые эмульсии содержат триглицериды, диспергированные в воде, вместе с эмульгаторами для поддержания стабильности этой системы. Ряд растительных масел, многие из которых служат причиной побочных эффектов, был изучен еще при создании первой жировой эмульсии до 1961 года. В 1961 году была создана первая жировая эмульсия для внутривенного введения на основе соевого масла, а роль эмульгатора выполняли фосфолипиды яичного желтка. Была показана ее хорошая переносимость в клинических условиях (Schuberth and Wretlind 1961) (3). В течение 45 лет эта эмульсия была доступна для применения под коммерческим названием Интралипид. Интралипид содержит длинноцепочечные триглицериды (LCTs) из соевого масла с двумя незаменимыми жирными кислотами: альфа-линоленовую и линолевую кислоты (alpha (α)-linolenic acid, linoleic acid). Одним из возможным недостатков этой LCTs-эмульсии связано с относительно высоким содержанием полиненасыщенных жирных кислот (PUFA), особенно в линолевой кислоте.
Следующим этапом развития жировых эмульсий для внутривенного введения стало добавление к LCTs среднецепочечных триглицеридов (MCTs). Преимуществами такой композиции стало не только снижение за счет разведения этих нежелательных эффектов, но и появление дополнительных нутритивных положительных свойств - ускорение утилизации и большая периферическая утилизация мышцами, нежели отложение в жировой ткани + поступление в митохондрии независимо от карнитина, уровень которого часто снижается у пациентов. MCTs имеет однако недостаток: если используется отдельно в количестве более 50%, вызывает риск гиперлактатацидемии, гиперкетонемии и токсического поражения центральной нервной системы. Добавление оливкового масла, богатого мононенасыщенными жирными кислотами ( ω-9), снижает это соотношение с PUFA. Влияние на воспалительный ответ зависит от соотношения α -линоленовой кислоты к α-линолевой (ratio of α-linolenic acid (ω-3) to linoleic acid (ω-6), при этом увеличение последней (как в случае с соевым маслом) оказывает провоспалительное действие. Таким образом, добавление рыбьего жира, обогащенного очень длинноцепочечными ω-3 жирными кислотами, особенно эйкоэапентаноевой кислотой (eicosapentaenoic acid (ЕРА) и докозагексаноевой кислотой (docosahexaenoic acid (DHA), должно еще больше уменьшить наблюдаемые негативные эффекты.
СМОФлипид 20% содержит жировые компоненты соевого масла, среднецепочечные триглицериды, оливковое масло и рыбий жир.
Эта композиция была создана для:
Доклинические данные
СМОФлипид - комбинация четырех жировых эмульсий для парентерального питания, каждая из которых зарегистрирована отдельно как: Интралипид (Intralipid (эмульсия на основе соевого масла) Fresenius Kabi Pty Ltd, Липовеноз (Lipovenos МСТ (включающий среднецепочечные триглицериды (МСТ)), Омегавен (Omegaven (эмульсия на основе рыбьего жира) - обе - Fresenius Kabi, и эмульсия на основе оливкового масла -КлинОлеик (Clinoleic, Baxter Healthcare Pty Ltd product).
Доклинические исследования включали: острую токсичность у крыс, 2 дозоповторяющихся исследования у собак (продолжительностью до 3-х месяцев), полный набор генотоксических исследований и локальной переносимости. Параллельно такие исследования проведены для Омегавена. Эти исследования сделаны в полном соответствии с международными рекомендациями для комбинированных продуктов (EMEA/CHMP/SWP/258498/2005: Guideline on the nonclinical development of fixed combinations of medicinal products).
Фармакология.
Первичная фармакодинамика. Фармакодинамика СМОФлипида складывается из таковой, характерной для Интралипида, с дополнением характеристик, свойственных MCTs и рыбьему жиру. MCTs преимущественно катаболизируются, нежели откладываются в жировой ткани, и поэтому выступают в составе СМОФлипида как быстрый источник энергии. Полиненасыщенные жирные кислоты рыбьего жира являются прекурсорами синтеза эйкозаноидов (простагландины, тромбоксаны, лейкотриены и другие медиаторы липидов).
Вторичная фармакодинамика и фармакология безопасности. Данные о безопасности СМОФлипида основываются на данных о безопасности отдельных компонентов, входящих в его состав. MCTs гидролизуются быстрее других триглециридов, входящих в состав СМОФлипида. MCTs слабо связываются с альбуминами крови, в связи с чем они легко проникают через гематоэнцефалический барьер. Влияние MCTs на центральную нервную систему (ЦНС) проявляется многообразными изменениями при концентрации в плазме 3-8 μmol/мл (432-1152 μg/мл) (обзор Johnson и Cotter, 1986 (4). При высокой скорости введения (превышающей в 10 раз рекомендованную для СМОФлипида) наблюдались летальные исходы у мышей, крыс, кроликов и собак, которые клинически проявлялись расстройством координации, аномалиями поведения и походки, тремором и апатией. Имела существенное значение концентрация среднецепочечных жирных кислот в плазме, зависящая от дозы и скорости введения. Риски появления этих эффектов, не характерных для Интралипида, но появляющихся в СМОФлипиде из-за добавления MCTs, легко регулировались и устранялись при соблюдении правильной скорости введения жировой эмульсии.
Фармакокинетика.
Фармакокинетика соевого масла и оливкового масла подробно освещена в литературе и не является предметом обсуждения в данной работе. Как MCTs, так и LCTs гидролизуются в капиллярах липопротеин-липазами до глицерола и свободных жирных кислот - среднецепочечных жирных кислот (MCFAs) и длинноцепочечных жирных кислот (LCFAs), соответственно. MCTs гидролизуются быстрее, чем LCTs, и поэтому быстрее выводятся. Свободные MCFAs затем легко проникают в печень, почки, сердце и другие периферические органы, где подвергаются окислению (бета-оксидация) и метаболизму в цикле лимонной кислоты с образованием диоксида углерода и воды. В качестве альтернативного варианта они ведут к образованию кетоновых тел, ацетоацетата и бета-гидроксибутирата. В противоположность этому, связанные с альбуминами LCFAs не быстро проникают в периферические органы и преимущественно метаболизируются в печени с преобладанием реэстерификации до фосфолипидов или триглицеридов и, поэтому, потенциально откладываются в жировой ткани. Таким образом, LCFAs имеют более низкую скорость реэстерификации, чем MCFAs, со сниженной тенденцией к отложению в жировом депо.
Включение MCTs в состав парентерального питания (ПП) ведет к возрастанию плазменного уровня среднецепочечных дикарбоксильных кислот, тригидроксижирных кислот и кетоновых тел. В токсикологических исследованиях с введением повторных доз СМОФлипида наблюдалась гиперкетонемия. При введении очень высоких доз MCTs способность внепеченочных тканей утилизировать кетоновые тела достигала предела (насыщение) и это могло потенциально создавать проблемы у некоторых пациентов с диабетом. Увеличение уровня кетоновых тел усиливает метаболический ацидоз и ускоряет нарушение гомеостатических механизмов (Bach и Babayan, 1982) (5). Полиненасыщенные жирные кислоты из рыбьего жира (С22:6 и С22:5) преимущественно дистрибьютируются до фосфолипидов, особенно в печени. Они менее склонны к накоплению в жировой ткани.
Токсикология.
Общая токсичность. Предоставляемые к рассмотрению токсикологические исследования включали работы с использованием соевого масла и MCFA-содержащих липидов. Они опубликованы ранее и не являются предметом рассмотрения в данной работе. В данном исследовании оценивалось внутривенное введение Омегавена 10%: две отдельные однократные дозы у мышей и крыс, и две повторные дозы (с соевым маслом). У ряда крыс, получивших максимальную однократную дозу 10% Омегавена, наблюдалось только уменьшение количества испражнений, но никаких других изменений. При введении повторных максимально возможных доз не наблюдалось каких-либо изменений, которые могли бы трактоваться как токсичные.
В исследованиях, использующих клинические формы выпуска СМОФлипида, изучалось токсическое влияние однократных доз у крыс и повторных доз в течение 13 недель - у собак. Суммарные данные этих исследования приведены в таблице 1. Используемые дозы были типичными для неклинических исследований ПП. Скорости инфузии были примерно в 5 раз выше рекомендованных для клиническошо применения. В дозе 36 г/кг веса наблюдалась гибель животных в течение 24 часов после инфузии. Клинические признаки токсического воздействия были аналогичны тем, что наблюдались при инфузии такой же дозы Интралипида или Липовеноза, и такой же скорости введения: снижение активности, атаксия, каталепсия редукция мышечного тонуса и диспноэ. У собак токсикологический профиль СМОФлипида исследовался в течение 13 недель и включал компоненты, характерные для токсического действия высоких доз каждой из жировых эмульсий, входящих в состав СМОФлипида: снижение или прекращение испражнений (рыбий жир), гиперкетонемия (MCTs), умеренная тромбоцитопения (оливковое и соевое масла), грануломатозная пневмония, обусловленная накоплением жиров в легких (соевое масло) и липофильные депозиты в печени (соевое масло, оливковое масло и MCTs). Жировые изменения в печени не полностью реверсировались после 4-х недель после прекращения введения эмульсии. Наблюдаемый Уровень Побочных Эффектов (The No Observable Adverse Effect Level (NOAEL) для токсического действия СМОФлипида составил 6 г/кг веса/день. В целом, по всем показателям уровень токсичности СМОФлипида не превышал уровней аналогичных показателей каждого из жировых компонентов, входящих в состав СМОФлипида.
Таблица 1
Соответствующие дозы СМОФлипида, используемые в токсикологических исследованиях
| Species (Strain) | Study; duration | Dose (g/kg/day) | Relative dose (based on g/kg) | Dose (g/m2/day)a | Relative dose (based on g/m2) | Infusion rate (g/kg/h) | Relative infusion rate (based on g/m2) |
| Rat (SD) | 9356/95 single dose | 0, 9, 18, 36 | 0, 3, 6, 12 | 0, 18, 108, 216 | 0, 0.2, 1, 2 | 6 | 7 |
| Dog (Beagle) | 9358/1/95 4 weeks | 0, 9 | 0, 3 | 0, 180 | 0, 2 | 1.5 | 6 |
| Dog (Beagle) | 10825/97 13 weeks | 0, 3, 6 | 0, 1, 2 | 0, 60, 120 | 0, 0.7, 1.2 | 1 | 4 |
| Human | - | 3 | - | 99 | - | 0.15 | - |
Генотоксичность.
Был применен стандартный набор генотоксических исследований в соответствии с клиническими формами препарата. Хотя по самой своей сути СМОФлипид не может быть генотоксичным препаратом, тем не менее, нами представлены данные по генной токсикологии. Не выявлено генной токсичности в доклинических исследованиях.
Репродуктивная токсичность.
Нет данных по репродуктивной токсичности СМОФлипида. В то же время, предыдущие исследования репродуктивной токсичности липидных компонентов ПП показали, что соевое масло не эмбриотоксично или тератогенно (исследования проведены на крысах и кроликах в дозе до 9 г/кг). Интралипид (соевое масло), комбинация соевого и оливкового масел, комбинация MCFAs и LCFAs специально не тестировались на репродуктивную токсичность. Не отмечено побочных эффектов у крыс, которые получали (орально) докозагексаноевую кислоту (C22:6ω3)(DHA) и эйкозапентаноевую кислоту (С20:5ωЗ) (ЕРА), жирные кислоты рыбьего жира. У самок крыс, которые получали 1,2 г/кг/день 20% MCT/LCT в течение 14 дней до спаривания (ниже клинической дозы), отмечалось усиление резорбции, удлинение сроков беременности и увеличение веса приплода. Эмбриофетальная токсичность (резорбция) и аномалии скелета наблюдались у кроликов вследствие инфузии 20% MCT/LCT (3:1) в течение периода органогенеза в дозе 4,28 г/кг/день, но не в дозе 1 г/кг/день; в опытах на крысах не было отмечено побочных эффектов (Henwood и соавт., 1997) (7). Сходные результаты (эмбриотоксичность и увеличение инцидентов скелетных аномалий) были получены в исследованиях эмбриофетального развития у кроликов, которые получали комбинацию MCFAs и LCFAs. Эти изменения были проявлениеми высокого уровня MCFAs в материнской плазме, гиперкетонемии и, возможно, гипогликемии.
Локальная переносимость.
Не выявлено в исследованиях на кроликах каких-либо локальных изменений, связанных с введением СМОФлипида интраартериально, паравенозно или подкожно.
Заключение.
Доклинические исследования СМОФлипида на мышах, крысах, кроликах и собаках не выявили каких-либо новых эффектов в плане токсичности по сравнению с уже известными и зарегистрированными компонентами парентерального питания. СМОФлипид хорошо переносится при интраартериальном, паравенозном, подкожном и внутривенном путях введения.
Клинические данные
Введение.
Клинические данные относительно применения жировых эмульсий в парентеральном питании наиболее полно даны в «Guidelines on Paediatric Nutrition of the European Society for Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN), European Society for Clinical Nutrition and Metabolism (ESPEN) and the European Society for Paediatric Research (ESPR).
Приведенные в данном Досье сведения включают:
Базисные исследования безопасности
Небазисные исследования эффективности ± безопасности у младенцев и детей
Исследование только поддающейся оценке безопасности
Исследования фармакокинетики
Фармакокинетика.
Исследование FE-SM-01-BE. Это исследование было открытым рандомизированным с целью сравнения внутрисосудистого метаболизма СМОФлипида 20% по сравнению с Липовенозом 20% у 10 здоровых мужчин-добровольцев (табл. 2). Оценивались показатели при скорости инфузии, необходимой для поддержания концентрации триглицеридов плазмы на уровне 3 ммоль/л (12) и скорости элиминации после окончания инфузии (табл.З). Неэстерифицированные жирные кислоты на 1, 2 и 4 часе возрастали значительно больше при введении СМОФлипида, чем Липовеноза. В наибольшей степени это относилось к липопротеинам низкой плотности (VLDL) - для СМОФлипида - 10%. Различия в больших аполипопротеинах (А-I, A-II и В) были минимальными. Рассматривая профиль жирных кислот, можно отметить, что сумма каприновой и каприловой кислот (продукты MCTs) значительна в случае со СМОФлипидом, в то время как при введении Липовеноза существенных изменений нет. Уровни Ω- 9 при введении СМОФлипида поддерживались, в то время как при введении Липовеноза они падали. Уровни Ω-6 в случае СМОФ были много выше, чем с Липовенозом. Показатели ω-3 кислот, альфа-линоленовой кислоты больше в случае Липовеноза, в то время как DHA и ЕРА - больше со СМОФ.
Таблица 2
Детали исследования FE-SM-01-BE
| Design; Study population; РК methods |
Subjects; Treatment; Dose, Duration | PK Results | Safety |
| Open-label, randomized 2-treatment, 2-period crossover study, to compare the intravascular metabolism of SMOFlipid 20% vs. Lipovenos 20% (soya based) in healthy volunteers. Primary efficacy variables were infusion rate to maintain plasma triglycerides at 3mmol/L and elimination rate after stopping infusion. Secondary variables were concentrations of lipids. apolipoproteins and fatty acid pattern. | 10 volunteer Males Age: mean 28y (range 21-36y). Weight: mean 72.4kg (range 61-84kg). All fasted ≥ 10h, then 2.5h prior they received concomitantly by peripheral IV infusion glucose 0.25 g/kg for first hour, then 0.16g/kg/h and amino acids 0.05g/kg/h to achieve low levels of gluconeogenesis and ketogenesis and fatty acid mobilisation from endogenous stores. These continued throughout for a total of S-8.3h. One of the two lipid products was given by peripheral IV infusion of lg of triglycerides/kg/h for 6 min, then approx 0.15g triglycerides/kg/h (to maintain plasma triglycerides at 3mmol/L ) for a total of 4h. Approx. 4-week washout between treatment periods. | During last 2h of infusion: SMOF 0.151 ±0.039 g/kg/h maintained plasma triglyceride at 3.2mmol L. Lipovenos 0.138 ±0.039 g/kg/h maintained plasma triglyceride at 3.0 mmol/L. There was no statistical difference. Triglyceride mean T1/2 (decay to 50% of the difference before/after infusion) was: SMOF 21.92 minutes Lipovenos. 26.96 minutes (There was no statistical difference). | Lipovenos:3 hadAE mild headache. SMOF: 4 had AE mild headache, 1 had stinging and ltchiness hands (latter felt possibly related to study drug). No clinically relevant abnormal changes in laboratory results. α-tocopherol increased with SMOF but not Lipovenos, γ-tocopherol increased with both preparations. |
Таблица 3
SM-01. Суммарные данные скорости инфузии липидной эмульсии и разрушения триглицеридов плазмы
| SMOF (N = 10) | Lipovenos (N = 10) | Difference SMOF-Lipovenos (N=10) | |
|
Rate of lipid infusion (g TG/kg/h), mean over last 2h | |||
| Mean | 0.151 | 0.138 | 0.013 |
| Median | 0.160 | 0.142 | 0.008 |
| SD | 0.039 | 0.039 | 0.033 |
| Range | 0.0.95 -0.203 | 0.083 -0.200 | -0.044-0.063 |
| 95% CIa | [-0.006, 0.032] | ||
| p. valuea | 0.163 | ||
|
Enzymatic triglyceride conc. (mmol/L), mean over last 2hours(3h, 4h) | |||
| Mean | 3.213 | 2.992 | 0.221 |
| Median | 3.236 | 3.067 | 0.112 |
| SD | 0.260 | 0.451 | 0.496 |
| Range | 2.644- 3.621 | 1.866-3.578 | -0.358 - 1.262 |
|
Half-life (Decay of Plasma trigycerides to 50% of the difference Before/After Infusion) (Minutes) | |||
| Mean | 21.92 | 26.96 | -5.04 |
| Median | 19.11 | 24.04 | -1.39 |
| SD | 8.15 | 12.69 | 9.20 |
| Range | 13.20-37.81 | 13.52 -52.41 | -18.91-5.20 |
| 95% CIa | [-11.57; 1.49] | ||
| p.valuea | 0.113 | ||
Первичными конечными точками оценки были триглицериды сыворотки и переносимость (лабораторные результаты, электрокардиограмма (ЭКГ, ECG), пульс, кровяное давление (ВР), температура и побочные эффекты (AEs). Вторичными конечными точками оценки были фосфолипиды сыворотки, холестерол, свободные жирные кислоты, свободный глицерол и локальная переносимость. Инфузия жировой эмульсии продолжалась более 6 часов со скоростью 0,125 г/кг/час с отмыванием (выведением) в течение 6 дней и более. Увеличение триглицеридов было больше в случае Липовеноза (статистически значимо) через 6 часов введения (табл. 5). Клиренс был больше для СМОФлипида, а время полувыведения его (Т1/2) было короче.
Таблица 4
| Design; Study population; РК methods | Subjects; |
PK Results | Safety | |||
|
Double-blind, randomized, active - 2-treatment. 2-period crossover study to compare, the safety, tolerability and elimination of triglycerides, and PKs of lipid parameters of SMOFlipid 20% vs. Lipovenos 20%. Primary endpoints: serum triglycerides Tolerability (lab results, ECG. pulse. BP. temperature & AEs). Secondary endpoints: serum phospholipids, cholesterol, free fatty acids, and free glycerol, local tolerability. |
12 volunteer males Age: mean 25.67 (range 18-30)years Weight: mean 72.74 (range 57.8-105.1)kg All fasted ≥ 10h prior and until after the 9h bloods were taken. | Parameter (mean ± SD) | SMOF | Lipovenos | Statistic |
Lipovenos: 1 AE (herpes). SMOF: 2 had AEs of headache (1 thought possibly related), 3 had abnormal sensation hands (thought possibly related), 1 had dizziness. All AEs were mild. 2 subjects showed mild to moderate increases in bilirubin |
| AUC0-ta [mg*h/dL] | 3002 ± 1331 | 3341 ± 1352 | ||||
| Cmaxb [mg/dL] | 291 ± 144 | 349±158 | ||||
| tmaxc [h] | 3.50 ± 0.80 | 5.44 ± 0.82 | ||||
| λzd[L/h] | 2.30 ± 0.88 | 1.42 ± 0.71 | P = 0.003 | |||
| t1/2e [h] | 0.34 ± 0.11 | 0.59 ± 0.25 | p = 0.0007 | |||
Таблица 5
SM-02.1. Параметры концентраций триглицеридов после 6-часовой инфузии СМОФлипида и Липовеноза
| Parameter | SMOF 20% mean ± SD median (range) | Lipovenos 20% mean ± SD median (range) | Statistic |
| AUC0-t [mg*h/Dl] | 3002 ±1331 2598 (1288 - 6164) | 3341 ± 1352 3177(1844-6099) | |
| Cmax [mg/dL] | 291±144 260 (100 - 657) | 349 ± 158 348 (137 - 678) | |
| tmax [h] | 3.50 ±0.80 3.00 (3.00- 5.00) | 5.44±0.82 6.00(4.00 - 6.17) | |
| λz [L/h] | 2.30 ±0.88 1.95 (1.27-4.28) | 1.42± 0.71 1.17 (0.71 -2.65) | P = 0.003 |
| t1/2 [h] | 0.34 ± 0.11 0.35 (0.16- 0.54) | 0.59±0.25 0.60 (0.26 - 0.89) | P = 0.0007 |
| C4h [mg/dL] | 264±127 225 (100 - 598) | 315 ± 141 276 (129 - 583) | P = 0.136a |
| C5h [mg/dL] | 263 ±144 216(90-657) | 333 ± 150 315 (137 - 647) | P = 0.058a |
| C6h [mg/dL] | 244±126 198 (88- 550) | 331 ± 150 348(114-576) | P = 0.0325 |
Рис. 1. Средние кривые концентрации триглицеридов вследствие 6-часовой инфузии СМОФлипида и Липовеноза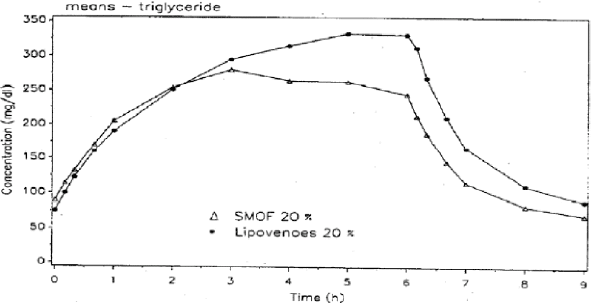
Кривая СМОФлипида слегка ниже, чем Липовеноза, но в целом картина сходная (табл.6, рис.2).
Рис.2. SM-02.4. Средние кривые концентраций свободных жирных кислот вследствие 6-часовой инфузии СМОФлипида и Липовеноза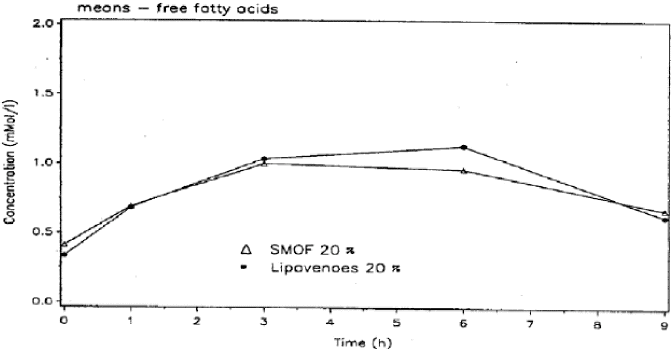
Хотя кривые изменений сходны у СМОФлипида и Липовеноза, все же данные отражают более быстрый гидролиз СМОФлипида.
Кривая изменения свободного триглицерола была сходной у СМОФлипида и Липовеноза (табл.7, рис.З). Общий холестерол варьировал незначительно.
Таблица 6
Параметры концентраций свободных жирных кислот вследствие введения СМОФлипида и Липовеноза
| Parameter | SMOF 20% mean ± SD median (range) | Lipovenos 20% mean ± SD median (range) |
| AUC0-t [mg*h/dL) |
15.4±2.81 15.5 (11.2 - 20.9) |
15.4±1.88 15.1 (12.3 - 19.2) |
| Cmax [mg/dL] |
1.04±0.23 0.98 (0.79 - 1.68) |
1.16±0.29 1.12 (0.82- 1.69) |
| tmax [h] |
4.25±2.01 3 (3 - 9) |
5.75±1.55 6 (3 - 9) |
Таблица 7.
Параметры концентраций свободного глицерола вследствие введения СМОФлипида и Липовеноза
| Parameter | SMOF 20% mean ± SD median (range) | Lipovenos 20% mean ± SD median (range) |
| AUC0-t [mg*h/dL) |
33.5 ±20.9 31.1 (5.30 - 83.8) | 26.9 ±11.0 24.3 (10-45.6) |
| Cmax [mg/dL] |
2.52 ± 1.13 2.1 (1.4 -4.9) | 2.08 ± 0.77 1.9 (1.3 -3.9) |
| tmax [h] |
2.83 ± 2.62 3.0 (0-9) | 7.01 ± 6.56 7.5 (0 - 24) |
Рис.З. SM-02.6. Средние кривые концентрации глицерола вследствие 6-часовой инфузии СМОФлипида и Липовеноза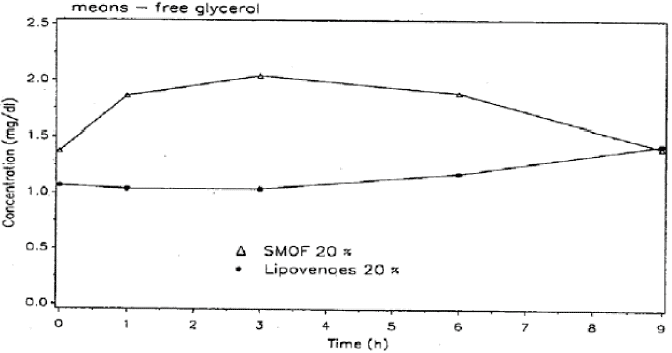
Фармакодинамика.
В доступной литературе нет данных относительно фармакодинамики комбинации липидов в СМОФлипиде. Индивидуальные же компоненты состава были исследовании на протяжении ряда лет в деталях. Липиды имеют частицы, сходные с хиломикронами, и они стабилизируются поверхностным слоем эмульгатора (например, фосфолипидами яичного желтка). Они связываются липопротеин-липазами эндотелия (например, в мышечной, жировой ткани) с гидролизом триглицеридов мягких жирных кислот (2, 13, 14, 15). Жирные кислоты имеют четыре пути метаболизма в организме: формировать клеточные мембраны; откладываться в жировой ткани; участвовать в синтезе эйкозаноидов и окисляться для обеспечения энергией (17). Соевое масло содержит полиненасыщенные длинноцепочечные триглицериды (LCTs), включающие незаменимые жирные кислоты с превышением (7:1) линолевой кислоты (ω-6) над альфа-линоленовой кислотой (ω-3). Эти жирные кислоты инкорпорируются в фосфолипиды мембран иммунных клеток. При возникновении воспалительного иммунного ответа они сохраняются как субстрат для синтеза эйкозаноидов: линолевая кислота (ω-6) формирует арахидоновую кислоту, альфа-линоленовая кислота (ω-3) формирует эйкозапентаеновую кислоту.
МСТ компонент больше водорастворим и среднецепочечные жирные кислоты имеют низкую аффинность к альбумину. Они более быстро подвергаются гидролизу и окислению (транспорт MCTs в митохондрии в высокой степени независим от карнитина). Они в значительной степени используются для получения энергии, чем депонируются в тканях по сравнению с LCTs.
Компоненты оливкового масла содержат значительные количества мононенасыщенной олеиновой кислоты (ω-9), которая конкурирует с ω-3 и ω-6 за инкорпорирование в фосфолипиды мембран. Рассматривается возможность снижения синтеза провоспалительных эйкозаноидов (19,20). Полиненасыщенные жирные кислоты снижают плазменный LDL-холестерол, но также снижают благоприятный HDL-холестерол, тогда как мононенасыщенные кислоты снижают LDL-холестерол, имея слабый эффект в отношении HDL-холестерола.
Рыбий жир, содержащий преимущественно ω-3 LCTs (главным образом эйкозапентаеновую кислоту), также повышает соотношение ω-3 к ω-6 в фосфолипидах мембран, вызывая дальнейшее снижение провоспалительных эйкозаноидов. Дополнительно - это улучшение функции печени (уровни билирубина и сывороточные энзимы печени) (21).
В процессе производства, хранения и внутривенного введения может происходить пероксидация (когда полное парентеральное питание - TPN - не защищено от света и ультрафиолетового излучения). Это может иметь место у младенцев in vivo и у взрослых на домашнем парентеральном питании - HPN, показателем чего является присутствие малонового диальдегида (MDA) в моче (13). Полиненасыщенные жирные кислоты могут действовать как субстраты для образования липидных гипероксидов (которые сами по себе могут быть провоспалительными агентами - 22). Оливковое масло с низким содержанием полиненасыщенных жирных кислот подвергается меньшей пероксидации как in vivo, так и in vitro (23).
Альфа-токоферол действует как свободный «сборщик» свободных радикалов in vivo и in vitro, снижая риск окислительных повреждений. Его содержание варьирует в различных маслах. Альфа-токоферол погружен в клеточных мембранах между фосфолипидами и поверхностями липопротеинов.
Эффективность.
В режиме проведения парентерального питания (PN), когда оральное или энтеральное питание невозможно, недостаточно или противопоказано, от липидных компонентов требуется следующее: обеспечение энергией; обеспечение незаменимыми жирными кислотами; обеспечение омега-3-жирными кислотами.
Основное исследование FM-SM-03-DE. Это проспективное рандомизированное двойное-слепое контролируемое исследование в параллельных группах у пациентов, нуждающихся в полном парентеральном питании (TPN) после хирургии (табл. 8). Исследование было мультицентровым и проводилось в Бельгии, Франции и Германии.
Таблица 8.
Детали исследования FM-SM-03-DE
|
Design; |
Treatments; |
Efficacy mеаsures/ |
Efficacy results |
Safety |
Double-blind randomized , active-controlled, parallel-group study of efficacy, safety. and tolerance of SMOFlipid (SMOF) 20% vs. Lipovenos 20% following major abdominal. thoracic. oar urological surgery. 249 randomised SMOF: 126 Lipovenos: 1123 |
Continuous infusion over 24h per day for 5days post-op. SMOFlipid 20% or Lipovenos 20% 1.5 g fat/kg/d by central IV infusion together with, amino acids 1.5 g/kg/d) and glucose (З.0-4.0 g/kg/d). The doses of lipids and glucose could each be optionally reduced by up to 50% on the first post-operative day. SMOF: (ITT =126, PP = 99) M/F 58(58.6%)/ 41(41.4%); Age mean 60.5 ± 14.15y (range 23 - 89y); Weight: mean 70.5 ± 11.70kg (ranee 45-92kg); M/F 65(65%)/35(35%). Age: mean 60.2 ± 13.75y (range 19 -84y). Weight: mean 71.6 ± 12.81kg (range 39-104.5kg). |
Primary: AUC of the difference between baseline serum triglyceride and concentrations at each measurement point up to day 6. Secondary: |
Рrimary: SMOF lipid infusion as assessed by Serum concentration of triglycerides mean daily AUC (difference from baseline) was non-inferior to Lipovenos infusion. Secondary: Eicosanoids. There was a statistical difference shown for LBT, between SMOFIipid and Lipovenos. but not for LTB4, TBX2 or TBX3. |
7 deaths none related to study drug. 12 SMOF and 11 Lipovenos patients had 37 possibly or probably treatment-related AEs, including: SMOF; nausea (5). vomiting (4). dysgeusia (2), cholestatic hepatitis (2), hyperglycaemia (2), hypertriglyceridaemia (2) (1 had severe nausea and vomiting). Lipovenos: nausea (5) vomiting (4). hepatocellular damage (2), cholestasis. hyperglycaemia. hypertriglyceridaemia. and headache (1 each) (1 had severe hyperglycaemia). Most treatment-related AEs were mild or moderate. There was one accidental overdose of Lipovenos that produced nausea and vomiting (the only treatment-related SAE). Patient discontinuations (treatment-related): SMOF; nausea and vomiting (2). vomiting (1). Lipovenos; |
СМОФлипид 20% и Липовеноз 20% давались в виде непрерывной инфузии в течение 24 часов в дозе 1,5 г жиров/кг веса тела/день (рекомендованная доза 1-2 г/день). Аминокислоты (примерно 1,5 г/кг/день) и глюкоза (3-4 г/кг/день) давались конкурентно. В зависимости от метаболического состояния пациента дозы липидов и глюкозы оптимально редуцировались до 50% в первый послеопрерационный день. Электролиты, микроэлементы и витамины вводились по потребности. Лечение начиналось утром первого дня после операции и продолжалось в течение 5 дней. Энтеральное питание в первые пять дней не проводилось. Исключение делалось для воды и чая, однако это не считалось основанием для исключения из исследования. Разрешались медикаменты для лечения сопутствующих заболеваний, исключая кортикостероиды в тех центрах, где анализировался синтез эйкозаноидов. Низкомолекулярный гепарин давался для профилактики тромбообразования. Определялись объективные показатели эффективности, безопасности и переносимости 20% СМОФлипида в процессе парентерального питания пациентов после больших абдоминальных, больших торакальных и больших урологических операций по сравнению со стандартной жировой 20% эмульсией Липовеноз. Первичная гипотеза основывалась на том, что элиминация СМОФлипида 20% будет, по крайней мере, такой же быстрой, что и элиминация 20% Липовеноза. Вторичными гипотезами были:
Критерии включения: Пациенты сразу же в послеоперационном периоде после больших абдоминальных, больших торакальных или больших урологических операций, таких как гастректомия, колектомия, резекция толстого кишечника, панкреаэктомия, эзофагэктомия или цистэктомия, и имели показания для парентерального питания не менее 5 дней.
Критерии исключения: Гиперлипидемия (уровень триглицеридов сыворотки на голодный желудок >250 мг/дл, общий холестерол>300 мг/дл); почечная или печеночная недостаточность.
Ключевые точки оценки. Первичная эффективность оценивалась как AUC различия между исходными концентрациями (базовой линией) триглицеридов сыворотки (25) и концентрациями в каждый момент измерений до 6 дня (соответственно 5 полных дней инфузии). Вторичными критериями эффективности были:
Критерии безопасности включали лабораторные параметры, общее состояние пациентов, а в отдельных исследовательских центрах - витамин Е в плазме (α-, γ-токоферолы).
Результаты оценки первичной эффективности.
Средняя дневная концентрация триглицеридов в сыворотке (отличие от базовой линии) для СМОФлипида составила 0.7340 ммол/л, для Липовеноза - 0.7197 ммол/л со средней разницей 0.0142. С этой точки зрения, эффективность СМОФлипида была не ниже эффективности Липовеноза. Вариантный анализ также не показал разницы в этих группах.
Средние концентрации перед хирургией (день 0) были 1.436 и 1.410 ммол/л для СМОФлипида и Липовеноза, соответственно. В первый день прединфузионные концентрации снижались до 0.920 и 0.894 ммол/л, соответственно. От 2 до 5 дня средние концентрации возрастали от 1.651 до 1.994 ммол/л для СМОФлипида и от 1.638 до 2.004 ммол/л для Липовеноза. На 6 день средние концентрации были ниже, но находились в районе базовой линии - 1.874 и 1.926 ммол/л для СМОФлипида и Липовеноза, соответственно. Различия в лечении составили 0.0499 ммол/л (табл.9).
Таблица 9
Концентрация триглицеридов в сыворотке (ммоль/л): среднее ежедневное AUC (отличие от базовой линии) ITT популяции
| Serum concentration of triglycerides | SMOF N = 123 | Lipovenos N =121 |
| Mean daily AUC (difference from baseline) | 0 7806 | 0.7307 |
| Difference of treatment means |
-0.0499 | |
| Lower limit of the one sided 95% CI for the difference of the treatment means |
-0.0474 | |
Данные по вторичной эффективности.
Средние концентрации общего холестерола в сыворотке, как и средние концентрации фосфолипидов были сопоставимы в обеих группах. Длительность пребывания в госпитале в целом (LOS в госпитале) была короче в группе со СМОФлипидом (15,688 дня), чем в группе с Липовенозом (17,827 дня) -12% в пользу СМОФлипида, разница же в длительности пребывания в ОРИТ (LOS в ICU) была не столь значительной - 4,66 дня против 5,19 дня -10,2% в пользу СМОФлипида.
Анализ подгрупп жирных кислот (19 пациентов - для СМОФлипида и 14 пациентов - для Липовеноза) показал:
Синтез (27) эйкозаноидов (19 - для пациентов со СМОФлипидом, 14 - для Липовеноза):
Другие результаты оценки эффективности - дети.
Было проведено одно исследование на детях и младенцах и два исследования на недоношенных младенцах.
Исследование 00-SMOF-002 у младенцев и детей.
Это двойное слепое рандимизированное, активно контролируемое исследование в параллельных группах безопасности и эффективности СМОФлипида 20% по сравнению с 20% Интралипидом у младенцев и детей, нуждающихся в долгосрочном парентеральном питании (табл. 10). В этом исследовании участвовали младенцы мужского и женского пола со стабильными заболеваниями, требующими парентерального питания по крайней мере в течение 4-х недель (13 пациентов в возрасте от 1 месяца до 2-х лет и 15 пациентов в возрасте 2-11 лет). В течение одной недели до исследования все получали 20% Интралипид, затем был один день перерыва (парентеральное питание, но без липидов). Затем вводились: 20% СМОФлипид или 20% Интралипид в дозе 2 г жиров/кг/день 12-14 часов в день через центральный инфузионный катетер в течение 4-5 дней в неделю. Рекомендованная скорость введения составляла 0,125 г жиров/кг/час с максимумом 0,15 г жиров/кг/час. Оральное/энтеральное поступление энергии составило менее или равное 50% от необходимых калорий. Дополнительное парентеральное питание (аминокислоты и глюкоза) варьировало в зависимости от веса пациента в целом. Примечание: по техническим причинам оценка липопротеина X не производилась. Отдельные дозы токоферола были исключены из листа назначений в смеси - мультивитаминные комплексы назначались в обеих группах.
Таблица 10
Детали исследования 00-SMOF-002
|
Design; |
Treatments; |
Efficacy measures/ |
Efficacy results |
Safety | |||||||
|
Randomized, double-blind, active-control, parallel-group study of safety and efficacy of SMOF 20% vs. Intralipid 20% in infants and children requiring long-term parenteral nutrition (4-5 days/week for 4 weeks). |
1 week prior to study Lntralipid 20%. 1 day washout (TPN no lipid). SMOFlipid 20% or lntralipid 20% as 2g fat/kg/d over 12-14h per day by central IV infusion for 4-5 days per week over 4 weeks. Oral/enteral intake ≤ 50% of calories. SMOF: 1-24 months: 7 patients |
Primary: Safety of long-term treatment with SMOFlipi d 20% vs. lntralipid 20% in children Secondary : Efficacy of longterm treatment with SMOFlipi d 20% vs. lntralipid 20% in children | Baseline mean ± SD | Change day 29, mean ± SD |
SMOF mean 27.3 ± 0.6 days of 1.43 ± 0.50g fat/kg/d28 (1.54 ± 0.45 g fat/kg/d for 1 -24 months age and 1.3S ± 0.52 g fat/kg/d for 2-11y). Intralipid mean 27.5 ±0.5 days of 1.41 ± 0.50 g fat/kg/d. 2 SAEs (1 on each treatment), no treatment-related SAEs or AEs. Most AEs were mild or moderate, 1 severe on lntralipid. | ||||||
| weight (kg) | SMOF | 12.34 ± 4.72 | 0.31 ± 0.19 | ||||||||
| lntralipid | 16.05 ± 8.06 | 0.30 ± 0.33 | |||||||||
|
height (cm) | SMOF | 86 40 ± 17.17 | 1.56 ± 1.52 | ||||||||
| lntralipid | 91.85 ± 18. 67 | 1.08 ± 0.95 | |||||||||
|
Secondary variables similar except for SMOF increase in ω-3fatty acids in plasma & RBC membrane and increase in plasma α-tocopherol | |||||||||||
Набор пациентов, их характеристики и распределение представлены в табл. 10.
Критерии оценки. Первичной оценкой была безопасность долгосрочного введения СМОФлипида 20% по сравнению с 20% Интралипидом у детей. Вторичными критериями была безопасность долгосрочного введения СМОФлипида 20% по сравнению с 20% Интралипидом у детей, определяемая профилем жирных кислот в плазме и фосфолипидах эритроцитов (RBC). Вариабельность первичной эффективности оценивалась с учетом веса тела, роста и индекса массы тела. Оценка вторичной эффективности включала учет ретинол-связывающего протеина, транстиретина (пре-альбумин) и альбумина. Оценка механизма действия (лабораторные показатели) включала: лецитин плазмы, паттерн жирных кислот в плазме и эритроцитах: С16:0, С18:1 n-9, С18:2 n-6, С20:3 n-9 / С20:4 n-6, С20:4 n-6, С18:3 n-3, С20:5 n-3 + С22:6 n-3, n-З/n-6, фосфолипиды, антиоксидантную способность плазмы, плазменный альфа-токоферол, LDL-TBARS (реактивную субстанцию тиобарбитуровой кислоты - показатель сывороточной пероксидации липидов); Аро (аполипопротеин) А-1, Аро 8-100.
Результаты первичной эффективности.
Данные пациентов, которым проводилась инфузия СМОФлипида:
Базовый вес, среднее значение 12.34 ± 4.72 кг (10.40 кг). Увеличение к 29 дню: в среднем 0.31 ± 0.19 кг (0,20 кг).
Базовый рост, среднее значение 86.40 ± 17.17 см (79.00 см). Увеличение к 29 дню в среднем 1.56 ± 1.52 см (1.00) см.
Intralipid infusion patients:
Базовый вес, среднее значение 16.05 ± 8.06 кг (12.80 кг). Увеличение к 29 дню в среднем 0.30 ± 0.33 кг (0.30 кг).
Базовый рост, среднее значение 91.85 ± 18.67 см (89.00 см). Увеличение к 29 дню в среднем 1.08 ± 0.95 см (1.00 см).
В обеих группах получены сходные результаты с небольшим увеличением показателей.
Другие результаты эффективности (табл. 11).
Таблица 11.
Результаты исследования вторичной эффективности
|
SMOF |
Intralipid | ||||
| Mean ± SD | Median | Mean ± SD | Median | ||
| Plasma Phospholipids (mmol/L) | Baseline | 1.437 ± 0.333 | 1.500 | 1.880 ± 0.324 | 1.950 |
| Change | 0.283 ± 0.441 | 0.165 | -0.100 ± 0.366 | -0 100 | |
| Plasma α-tocopherol (mcmol/'L) | Baseline | 12.618 ± 5.074 | 13.175 | 16.642 ±8.068 | 17.50 |
| Change | 15.675 ± 15.900 | 10.025 | 5.438 ± 15.151 | 1.700 | |
| LDL-TBARS (mcmol/L) | Baseline | 43.292 ± 18.344 | 43.050 | 37.504 ±20.054 | 40.250 |
| Change | 7.835 ± 19.017 | 1.40 | 8.750 ±37.389 | 0.00 | |
| Apo Al (g/L) | Baseline | 0.754± 0.123 | 0.775 | 0.765 ±0.216 | 0.700 |
| Change | 0.075 ±0.122 | 0.050 | -0.023 ± 0.224 | -0.050 | |
| Apo В100 (g/L) | Baseline | 0.479 ± 0.140 | 0.475 | 0.608 ±0.263 | 0.450 |
| Change | 0.039 ±0.175 | 0.050 | 0.012 ±0.227 | -0.050 | |
В целом получены сходные результаты, исключая профили жирных кислот, что отражает различия в составах жировых эмульсий, и более выраженные изменения альфа-токоферола в случае СМОФлипида. Только 2 из 15 детей не получали дополнительно оральное/энтеральное питание. В целом данные детской популяции сходны с таковыми у взрослых пациентов.
Другие результаты эффективности - младенцы.
Младенцы имеют отличные от взрослых пациентов указания, предназначенные для ручного приготовления липидов. В течение последнего триместра беременности ω-3 и ω-6 LCTs депонируются в быстрорастущих фетальных тканях, особенно в мозгу и сетчатке. Новорожденные младенцы и, особенно, недоношенные, часто имеют пониженную способность синтеза незаменимых жирных кислот (например, арахидоновой кислоты и докозагексаеновой кислоты) из линолевой и α-линоленовой кислот. Поэтому новорожденные в случае необходимости получают дополнительные адекватные и сбалансированные количества ω-3 и ω-6 жирных кислот.
Исследование 00-SMOF-004
Это двойное-слепое, рандомизированное, активно-контролируемое исследование в параллельных группах безопасности и переносимости в течение 7-14 дней лечения СМОФлипидом по сравнению с 20% Интралипидом у недоношенных младенцев (табл. 12). В этом исследовании производилась ежедневная 20-24 часовая в/в инфузия (через пупочную артерию) в течение 7-14 дней СМОФлипида 20% или Интралипида 20%. В таблю 12 показаны суммарные данные, характеризующие данные пациентов и вводимые дозы. Включено было 60 пациентов.
Таблица 12.
Детали исследования 00-SMOF-004
| Design; Population | Treatments; |
Efficacy measures/ outcomes |
Efficacy results | Safety | ||||
|
Double blind, randomized, active-controlled, parallel-group study of safety & tolerability of 7-14d of SMOFlipid 20% vs. Intralipid 20% in premature infants birth weight 1,000 to 2,500 g and requiring PN including fat for ≥ 7days Age gestation < 34 weeks: 0 to 7 days old. |
Infusion over 20-24 h/d for 7 - 14 days of SMOFlipid 20% or Intralipid 20% via umbilical artery or peripherally. Dose (in g fat/kg/d) Day 1: 0.5; Additional oral/enteral intake ≤ 30% of energy intake on days 1-3 and ≤ 50% on days 4-14. |
Primary: Safety and tolerability of 7 - 14 days of treatment with SMOFlipid 20% vs. Intralipid 20% in premature infants. Secondary: Efficacy of 7 - 14 days of treatment with SMOFlipid 20% vs. Intralipid 20% in premature infants assessed by relative increase шn body weight on Day 8. |
Birth weight |
Body weight on Day 8 (% increase) Mean ± SD |
Changes in Serum triglycerides were similar with similar numbers changing to high levels. 29 AEs in 13 patients on SMOF and 28 AEs in 14 patients on Intralipid, all mild or moderate, none treatment-related. No deaths, discontinuations due to AEs nor any SAEs. Only clinically relevant changes in laboratory values were for CRP due to infections. | |||
| N | SMOF | N | Intralipid | |||||
| Overall | 30 | 5.0 ± 6.5 | 30 | 5 1 ± 6.6 | ||||
|
The number of patients without oral nutrition fell from 14 to 2 on SMOF and fiom 10 to 0 on Intralipid. | ||||||||
Критерии оценки. Первичной оценкой был уровень триглицеридов сыворотки. Вторичная оценка включала:
Результаты оценки эффективности.
Среднее увеличение веса тела показано в табл. 12. В целом, увеличение веса тела было сходным. Также сходными были профили жирных кислот эритроцитов. Отмечались некоторые различия среди возрастных групп по базовым (исходным) показателям. На 8-ой день выявились различия в профилях жирных кислот в эритроцитах: большее увеличение содержания ω-3 в группе СМОФлипида (особенно, эйкозапентаноевой кислоты, хотя содержание докозагексаноевой кислоты снижалось в обеих группах); наблюдалось превышение ω-6 жирных кислот в группе Интралипида; в обеих группах повышалось содержание ω-9, немного больше - в группе СМОФлипида. Это отражает состав жировых эмульсий. Другие вторичные показатели представлены в табл. 13.
Таблица 13.
Вторичная вариабельность
|
SMOF |
Intralipid | ||||
| Mean ± SD | Median | Mean ± SD | Median | ||
|
Plasma α-tocopherol (mmol/L) | Day 0 | 14.197 ± 5.894 | 13.76 | 13.535 ±4.542 | 13.22 |
| Day 8 | 26.974±18.318 | 22.17 | 8.733 ± 11.409 | 7.34 | |
|
Plasma malondialdehyde,a (mmol/L) | Day 0 | 2.949 ± 0.828 | 3.02 | 2.931 ± 0.962 | 3.02 |
| Day 8 | -0.686 ±1.108 | -0.55 | -0.770 ±0.920 | -0.90 | |
Исследование 03-SMOF-005.
Это исследование было озаглавлено как изучение безопасности, переносимости и эффективности СМОФлипида 20% по сравнению с Интралипидом 20% (в течение 7-14 дней) у недоношенных младенцев. Оно представляет из себя множественные протокольные поправки в процессе исследования, где пациенты получали лечение в одном центре в некорректно калькулированных дозах. Впоследствии пациенты лечились очень различно в двух исследовательских центрах. Центр 2 включал большинство пациентов, лечившихся по протоколу, в то время как Центр 1 осуществлял рутинную лечебную практику, значительно отличавшуюся от протокольной, особенно в части назначения дозы липидов. При этом не выявлено различий между двумя группами по уровню триглицеридов (первичная оценка)
Заключение относительно эффективности
Как отмечено в начале этого раздела, существуют три возможности показать эффективность для части полного парентерального питания или частичного парентерального питания.
Обеспечение пациента энергией как части потребности в парентеральном питании.
Возможность обеспечить концентрированной энергией путем использования жировой эмульсии базируется на соевом масле (Интралипид), которое также содержит незаменимые жирные кислоты, способные уменьшить дневную потребность в глюкозе и уменьшить проблемы, связанные с ее применением: гипергликемию и необходимость использования инсулина.
Уровень триглицеридов плазмы при введении липидов будет зависеть от выбранной скорости введения и от конверсии липидов в жирные кислоты под влиянием липазы. Жирные кислоты имеют четыре возможных пути метаболизма в организме: в клеточныве мембраны; отложение в жировых тканях; синтез эйкозаноидов; окисление для обеспечения энергией.
Обеспечение незаменимыми жирными кислотами как части потребности в парентеральном питании.
Исследование ставило задачей доказать, что СМОФлипид обеспечивает организм незаменимыми жирными кислотами (по концентрации в плазме) также адекватно, как Интралипид или Липовеноз. Без соответствующих жировых добавок дефицит незаменимых жирных кислот развивается в организме пациента на полном парентеральном питании (TPN) через 2-4 недели; у 6-месячного младенца изменения наблюдаются уже через 4-5 дней (31). В исследовании SM-03-DE, средняя сумма ω-3 жирных кислот в фосфолипидах плазме возрастала в случае СМОФлипида (от 6.76 ± 1.63 мол 1% на 4.33 ± 1.66 мол%), в то время как при введении Липовеноза - снижалась (с 6.53 ± 1.37 мол% на -1.60 ± 1.42 мол%). Однако, средняя сумма ω-6 жирных кислот снижалась при введении СМОФлипида (от 29.46 ± 3.34 мол% на -5.71 ± 3.21 мол%), в то время как при введении Липовеноза - увеличивалась (от 30.51 ± 1.97 мол% на 1.26 ± 2.96 мол%). Эти изменения интерпретировались таким образом, что исследование проводилось только 5 дней - слишком короткий период, чтобы наступил дефицит незаменимых жирных кислот, однако результаты наводят на мысль, что СМОФлипид по сравнению с Липовенозом повышает соотношение ω-З/ ω-6, но не поддерживает уровень незаменимых ω-6 жирных кислот у взрослых В исследовании SMOF-002 средняя сумма ω-3 жирных кислот (ALA, ЕРА и DHA) в липопротеинах плазмы у СМОФлипида возрастала (с 2.38 мол% на 1.54 мол%), в то время как при введении Интралипида - снижалась (с 2.28 мол% на -0.14 мол%). В исследовании новорожденных 00-SMOF-004 средняя сумма ω-3 жирных кислот (ALA, ЕРА и DHA) в фосфолипидах эритроцитов при введении СМОФлипида возрастала (с 95.09 мкмол/л на 4.85 мкмол/л), в то время как при введении Интралипида -снижалась (с 103.31 мкмол/л на -7.45 мкмол/л).
Обеспечение омега-3-жирными кислотами как части потребности в парентеральном питании.
Как было показано выше, анализ исследования SM-03-DE на 19 СМОФлипид пациентах и 14 пациентах с Липовенозом показал значительные различия в изменении ω-3- жирных кислот. Из ω-3- жирных кислот DHA - важный структурный компонент клеточных мембран, в то время как ЕРА - прекурсор эйкозаноидов (простагландины, тромбоксаны, лейкотриены). В исследовании первичной эффективности (FM-SM-03-DE) были обнаружены статистически значимые различия между СМОФлипидом и Липовенозом в отношении LBT5, но не в отношении каких-либо других параметров
Дополнительное количество ω-3- жирных кислот способствует снижению провоспалительного эффекта избыточного содержания ω-6 линолевой кислоты (как в соевой эмульсии). Субгрупповой анализ в исследовании FM-SM-03-DE показал, что продолжительность пребывания в госпитале была значительно короче в группе со СМОФлипидом по сравнению с контрольной группой (13.4±2.0 против 20.4± 10.0 дней, р<0.05). В исследовании FM-SM-03-DE время пребывания в госпитале в случае СМОФлипида была короче (15.688 дня), чем при введении Липовеноза (17.827 дня).
Безопасность.
Суммарные данные по популяции, в которой исследовалась безопасность, приведены в табл. 14. Из 195 взрослых пациентов 11 пациентов (5,6%) имели хронический панкреатит, 9 пациентов (4,6%) имели рак поджелудочной железы, а 15 (7,7%) подверглись операции холецистэктомии. Продолжительность наблюдения составила для взрослых 5.3 ± 2.51 (1 - 15) дней; для детей - 28.3 ± 0.62 (27 - 29) дней; для недоношенных младенцев - 9.8 ± 3.60 (3 - 15) дней
Таблица 14.
Исследование безопасности и популяции
| Study | Population | Treatment | N | Planned duration |
| FE-SM-01-BE | Volunteers | SMOFlipid 20% | 10 | 4 hours |
| FE-SM-02-DE | Volunteers | SMOFlipid 20% | 12 | 6 hours |
| FE-SM-03-DE | Adults | SMOFlipid 20% | 126 | 5 days |
| FE-SM-04-CH | Adults | SMOFlipid 20% | 16 | 10-14 days |
| 03-ЗСВ7-001 | Adults | SmofKabiven | 26 | 5-7 days |
| 03-ЗСВ8-001 | Adults | SmofKabiven Peripheral | 27 | 5-7 days |
| 00-SMOF-002 | Children, infants and toddlers | SMOFlipid 20% | 15 | 4 weeks |
| 00-SMOF-004 | Preterm infants | SMOFlipid 20% | 30 | 7-14 days |
| 03-SMOF-005 | Pretenn infants | SMOFlipid 20% | 42 | 7-14 days |
Побочные эффекты.
Побочные эффекты отличались в каждом индивидуальном исследовании.
Основное исследование FM-SM-03-DE.
Для СМОФлипида средняя дневная доза составила 1.431 ± 0.1581 г/кг/день, а средняя продолжительность введения 4.714 дня, в то время как для Липовеноза эти показатели составили 1.447 ± 0.1068 г/кг/день и 4.765 дня. Показатели для других компонентов TPN были сходными в обеих группах. Анализ в группах показал, что в группах в целом средние концентрации в плазме α- и γ- токоферола возрастали в течение 1-6 дней наблюдения. В то же время в группе со СМОФлипидом отмечались значительно большие изменения для α-токоферола, а в группе с Липовенозом - для γ-токоферола. Общие результаты представлены в табл. 15. Побочные эффекты за время наблюдения в группе со СМОФлипидом не были связаны с применением препарата и включали: извращение вкуса (2 пациента), холестатический гепатит (2), гипергликемию (2), гипертриглицеридемию (2), в группе с Липовенозом отмечались: гепатоцеллюлярные нарушения (2), холестаз, гипергликемия, гипертриглицеридемия и головная боль.
Таблица 15.
Индивидуальные характеристики побочных эффектов (AEs) при введении жировых эмульсий - характеристика безопасности популяции
|
Numbers of patients reporting |
SMOF Group |
Lipovenos Group |
Total | |||
| N | % | N | % | N | % | |
| Nausea | 10 | 7.9 | 14 | 11.4 | 24 | 9.6 |
| Hyperglycaemia | 9 | 7.1 | 5 | 4.1 | 14 | 5.6 |
| Vomiting | 6 | 4.8 | 7 | 5.7 | 13 | 5.2 |
| Fever | 4 | 3.2 | 5 | 4.1 | 9 | 3.6 |
| Pneumonia | 4 | 3.2 | 3 | 2.4 | 7 | 2.8 |
| Hypertension | 4 | 3.2 | 2 | 1.6 | 6 | 2.4 |
| Sepsis | 4 | 32 | 2 | 1.6 | 6 | 2.4 |
| Tachycardia | 4 | 3.2 | 1 | 0.8 | 5 | 2.0 |
| Respiratory insufficiency | 0 | 0.0 | 4 | 3.3 | 4 | 1.6 |
Исследование FE-SM-04-CH.
Это было двойное-слепое, рандимизированное активноконтролируемое исследование в параллельных группах безопасности и переносимости СМОФлипида 20% по сравнению с 20% Липовенозом у пациентов, нуждающихся в долгосрочном полном парентеральном питании. Пациенты получали непрерывную внутривенную центральную инфузию СМОФлипида 20% или 20% Липовеноза в дозе ≤ 2 г жиров/кг/день свыше 18-24 часов/день в течение 10 - 14 дней вместе с аминокислотами в дозе 1-1.5 г/кг/день и глюкозой и соотношением энергии 50/50. Максимальная скорость инфузии составляла 0.125 г жира/кг/час и 2 г жира/кг/день. Оценочными точками были: клинические химические параметры, гематология, параметры коагуляции, общее состояние, и побочные эффекты (AEs). Критерием включения в исследование были пациенты, нуждающиеся в TPN в течение 10-14 дней. Критерии исключения были те же, что и в исследовании FM-SM-03-DE с дополнительным исключением случаев неконтролируемого сепсиса. Популяция исследования состояла из:
Результаты оценки безопасности. Среднее время введения составило 1.04 ± 0.3 г/кг/день в течение 10.94 ± 3.66 дня для СМОФлипида и 1.04 ± 0.32 г/кг/день в течение 8.56 ± 3.93 дня для Липовеноза. 12 пациентов со СМОФлипидом имели 27 побочных эффектов, с Липовенозом - 18. Наиболее частыми побочными эффектами были: увеличение триглицеридов (6 пациентов) и печеночных ферментов (3) в группе со СМОФлипидом и такие же для Липовеноза (3 и 3 пациента, соответственно). Побочные эффекты систематизированы в табл. 16. Не выявлено различий в группах по уровню триглицеридов сыворотки. В обеих группах гемоглобин, гематокрит и количество эритроцитов было ниже нормы. Средний объем тромбоцитов в группе со СМОФлипидом был нормальным, в группе с Липовенозом - ниже нормы, уровень лейкоцитов был нормальным в обеих группах. Не обнаружено различий в биохимических показателях.
Таблица 16.
Выраженность возможных или вероятных побочных эффектов, связанных с исследуемыми веществами - безопасность популяции
|
Body system/Preferred term |
SMOF 20% N=16 |
Lipovenos 20% N=16 | ||||||||
|
mild |
moderate |
No statement by principal investigator |
mild |
moderate | ||||||
| N | % | N | % | N | % | N | % | N | % | |
|
Liver and biliary system disorders | ||||||||||
| Gamma-glutamyl transferase increased | 0 | 0% | 1 | 6.3% | 0 | 0% | 2 | 12.5% | 0 | 0% |
| Hepatic enzymes increased | 2 | 12.5% | 0 | .0% | 0 | 0% | 1 | 6.3% | 1 | 6.3% |
|
Metabolic and nutritional disorders | ||||||||||
| Alkaline phosphatase serum increased | 0 | 0% | 1 | 6.3% | 0 | 0% | 2 | 12.5% | 0 | 0% |
| Serum lipid abnormal nos. | 7 | 43.8% | 0 | 0% | 0 | 0% | 3 | 18. 8% | 0 | 0% |
|
Body as a whole - general disorders | ||||||||||
| Pain | 0 | 0% | 0 | 0% | 1 | 6.3% | 0 | 0% | 0 | 0% |
Исследование 03-3CB7-001
Это открытое, рандомизированное активно-контролируемое исследование в параллельных группах безопасности и переносимости СМОФ Кабивена по сравнению с Кабивеном в течение 5-7 дней у послеоперационных пациентов, нуждающихся в парентеральном питании в едином клиническом центре. Пациенты получали непрерывную центральную внутривенную инфузию СМОФ Кабивена или Кабивена следующим образом: День 1 = 15.0 мл/кг/день (0.57 г СМОФ Кабивен липид/кг/день); Дни 2-4 = 22.5-30.0 мл/кг/день (0.86-1.14 г СМОФ Кабивен липид/кг/день); Дни 5-7 = 15.0-30.0 мл/кг/день (0.57-1.14 г СМОФ Кабивен липид/кг/день). СМОФ Кабивен имел более высокое содержание глюкозы и аминокислот, чем Кабивен периферический. В этом исследовании инфузионный насос не использовался и инфузия контролировалась вручную. Побочные эффекты отмечены у 25 пациентов со СМОФ Кабивеном (5) и у 23 - с Кабивеном (5). Суммарные данные представлены в табл. 17. Средний уровень глюкозы к концу исследования возрастал в группе со СМОФ Кабивеном до 27.13 (± 71.10), а в группе с Кабивеном - до 27.46 (± 45.26) мг/дл. Из-за включения в исследование диабетиков и недиабетиков вариабельность уровня глюкозы была достаточно высока. Не отмечено различий в группах по уровням гранулоцитов, С-реактивного белка, билирубина и других лабораторных показателей.
Таблица 17.
Побочные эффекты (AEs), у которых возможна потенциальная связь с исследуемыми веществами
|
All subjects N = 53 |
SMOF K N = 26 |
Kabiven N = 27 | |||||
| n | % | N | % | n | % | ||
|
Subjects with AEs | 48 | 90.6 | 25 | 96.2 | 23 | 85.2 | |
| Probable | Subjects with remarks | 1 | 1.9 | 1 | 3.8 | ||
| Nausea | 1 | 1.9 | 1 | 3.8 | |||
| Possible | Subjects with remarks | 27 | 50.9 | 16 | 61.5 | 11 | 40.7 |
| Nausea | 11 | 20.8 | 4 | 15.4 | 7 | 25.9 | |
| Vomiting | 9 | 17.0 | 7 | 26.9 | 2 | 7.4 | |
| Flatulence | 5 | 9.4 | 4 | 15.4 | 1 | 3.7 | |
| Abdominal Pain | 1 | 1.9 | 1 | 3.7 | |||
| Hyperglycaemia | 1 | 1.9 | 1 | 3.8 | |||
| Hypertension | 1 | 1.9 | 1 | 3.8 | |||
| Oedema | 1 | 1.9 | 1 | 3.8 | |||
Исследование 03-3CB8-001
Это открытое, рандомизированное активно-контролируемое исследование в параллельных группах безопасности и переносимости СМОФ Кабивена периферического (SMOF Kabiven Р) по сравнению с Кабивеном периферическим (Kabiven Р) в течение 5-7 дней. Пациенты получали ≤ 40 мл/кг/день (1.13 г СМОФ Кабивен липид/кг/день) путем внутривенной инфузии через периферическую вену в течение 14-24 часов в день, либо СМОФ Кабивен периферический или Кабивен периферический плюс ≤ 700 ккал орального/энтерального питания. СМОФ Кабивен периферический содержал немного большее количество глюкозы и аминокислот, чем Кабивен периферический. 24 из 27 пациентов в группе со СМОФ получили ≥ 5 инфузий, двое имели 6 инфузий, а один имел 7 инфузий; на Кабивене периферическим 16 из 25 имели ≥ 5 инфузий, трое имели 6 инфузий и 6 имели 7 инфузий. Основываясь на среднем объеме инфузий по отношению к среднему количеству инфузий и среднему весу, группа СМОФ Кабивен периферический получила 32.17 мл/кг/день, группа с Кабивеном периферическим - 29.7 мл/кг/день. Из 52 исследованных пациентов было 27 пациентов со СМОФ Кабеном периферическим и 25 пациентов - с Кабивеном периферическим. Всего был один серьезный побочный эффект в каждой группе, не связанный с введением препаратов. Не зафиксировано ни одного случая тромбофлебита. Большинство побочных эффектов носили мягкий или средний характер.
Исследование 00-SMOF-002
Обозначено как исследование эффективности. Средняя продолжительность введения СМОФ составила 27.3 ± 0.6 дня в дозе 1.43 ± 0.50 г жиров/кг/день (1.54 ± 0.45 г жиров/кг/день для возраста 1-24 месяца и 1.38 ± 0.52 г жиров/кг/день для 2-11 летних детей), для Интралипида эти показатели составили: 27.5 ± 0.5 дней и дозе 1.41 ± 0.50 г жиров/кг/день. Средняя скорость инфузии была 0.11 ± 0.04 г жиров/кг/час в обеих группах. Побочные эффекты представлены в табл. 18.
Таблица 18.
Суммарные данные по побочным эффектам (анализ безопасности)
|
SOC/ Preferred Tern |
All patients n = 28 |
SMOF N = 15 |
Intralipid N = 13 | |||
| n | % | n | % | n | % | |
| Patients with at least one AE | 13 | 46.4 | 7 | 46.7 | 6 | 46.2 |
| General disorders and administration site conditions | 6 | 26.6 | 4 | 26.7 | 4 | 30.8 |
| Pyrexia | 7 | 25.0 | 3 | 20.0 | 4 | 30.8 |
| Catheter site inflammation | 1 | 3.6 | 1 | 6.7 | ||
| Infections and infestations | 6 | 21 4 | 3 | 20.0 | 3 | 23.1 |
| Ear infection | t | 3.6 | 1 | 6.7 | ||
| Nasopharyngitis | 1 | 3.6 | 1 | 6.7 | ||
| Staphylococcal infection | 1 | 3.6 | 1 | 6.7 | ||
| Acute tonsillitis | 1 | 3.6 | 1 | 7.7 | ||
| Campylobacter gastroenteritis | t | 3.6 | 1 | 7.7 | ||
| Urinary tract infection | I | 3.6 | 1 | 7.7 | ||
| Gastrointestinal disorders | 2 | 7.1 | 1 | 6.7 | 1 | 7.7 |
| Vomiting | 2 | 7.1 | 1 | 6.7 | 1 | 7.7 |
| Injury, poisoning and procedural complications | 1 | 3.6 | 1 | 6.7 | ||
| Femur fracture | 1 | 3.6 | 1 | 6.7 | ||
| Metabolism and nutrition disorders | 1 | 3.6 | 1 | 6.7 | ||
| Acidosis | 1 | 3.6 | 1 | 6.7 | ||
Отмечено 2 выраженных побочных эффекта (по одному в каждой группе), не связанных с лечением. Большинство побочных эффектов носили мягкий или средний характер. Не отмечено клинически значимых изменений гематологических показателей или биохимии.
На СМОФлипиде систолическое и диастолическое давление снижались на 7 мм рт ст, снижение было более выраженным в возрастной группе 1-24 месяца (в среднем 14/11 мм рт ст. В группе с Интралипидом давление снижалось на 1/5 мм рт ст. Частота сердечных сокращений в группе со СМОФлипидом снижалась в среднем на 10 ударов в минуту, в группе с Интралипидом - на 4 удара в минуту. При введении СМОФлипида снижение ЧСС было более выраженным в возрастной группе 1-24 месяца (на 20 ударов в минуту). Средняя температура тела оставалась в пределах нормы.
Исследование OO-SMOF-004
Обозначено как исследование эффективности. Первичными показателями были изменения триглицеридов сыворотки. Изменения были сходными в группах СМОФлипида и Интралипида. Зафиксировано 29 побочных эффектов у 13 пациентов на СМОФлипиде и 28 - у пациентов на Интралипиде (табл. 19). Все они носили мягкий или средний характер и не были связаны с лечением.
Таблица 19.
Суммарные данные по побочных эффектам по органам и системам, потенциально связанные с исследуемыми жировыми эмульсиями
|
SOC/ Preferred term |
SMOF n = 30 |
lntralipid n = 30 | ||||||
|
Events |
Patients |
Events |
Patients | |||||
| n | % | n | % | n | % | n | % | |
| Patients with remark | 29 | 100.0 | 13 | 43.3 | 28 | 100.0 | 14 | 46.7 |
| Infections and infestations | 11 | 37.9 | 11 | 36.7 | 8 | 28.6 | 8 | 26.7 |
| Nosocomial infection | 7 | 24.1 | 7 | 23.3 | 5 | 17.9 | 5 | 16.7 |
| Staphylococcal infection | 1 | 3 4 | 1 | 3.3 | 1 | 3.6 | 1 | 3.3 |
| Eye infection | 1 | 3.4 | 1 | 3.3 | ||||
| Infection | 1 | 3.4 | 1 | 3.3 | ||||
| Neonatal infection | 1 | 3.4 | 1 | 3.3 | ||||
| Bacterial infection | 1 | 3.6 | 1 | 3.3 | ||||
| Escherichia sepsis | 1 | 3.6 | 1 | 3.3 | ||||
| Respiratory; thoracic and mediastinal disorders | 6 | 20.7 | 6 | 20.0 | 4 | 14.3 | 3 | 10.0 |
| Apnoea | 4 | 13.8 | 4 | 13.3 | 4 | 14.3 | 3 | 10.0 |
| Atelectasis | 1 | 3.4 | 1 | 3.3 | ||||
| Hypoventilation | 1 | 3 4 | 1 | 3.3 | ||||
| Blood and lymphatic system disorders | 3 | 10.3 | 3 | 10.0 | 5 | 17.9 | 3 | 10.0 |
| Anaemia. | 3 | 10.3 | 3 | 10.0 | 4 | 14.3 | 3 | 10.0 |
| Thrombocytopenia | 1 | 3.6 | 1 | 3 3 | ||||
| Nervous system disorders | 4 | 13.8 | 3 | 10.0 | 3 | 10.7 | 1 | 3.3 |
| Convulsion | 2 | 6.9 | 1 | 3.3 | 3 | 10.7 | 1 | 3.3 |
| Epilepsy | 1 | 3.4 | 1 | 3.3 | ||||
| Hydrocephalus | 1 | 3.4 | 1 | 3.3 | ||||
| General disorders and administration site conditions | 2 | 6.9 | 2 | 6.7 | 2 | 7.1 | 2 | 6,7 |
| Pyrexia | 2 | 6.9 | 2 | 6.7 | 2 | 7.1 | 2 | 6,7 |
| Investigations | 2 | 6.9 | 2 | 6.7 | 2 | 7.1 | 2 | 6,7 |
| Oxygen saturation decreased | 2 | 6.9 | 2 | 6.7 | 1 | 3 6 | 1 | 3 3 |
| Blood pressure increased | 1 | 3.6 | 1 | 3.3 | ||||
| Cardiac disorders | 1 | 3.4 | 1 | 3.3 | 2 | 7.1 | 1 | 3.3 |
| Bradycardia | 1 | 3.4 | 1 | 3.3 | 2 | 7.1 | 1 | 3.3 |
| Eye disorders | 1 | 3.6 | 1 | 3.3 | ||||
| Conjunctivitis | 1 | 3.6 | 1 | 3.3 | ||||
| Gastrointestinal disorders | 1 | 3.6 | 1 | 3.3 | ||||
| Abdominal distension | 1 | 3.6 | 1 | 3.3 | ||||
Исследование 03-SMOF-005
Обозначено как исследование эффективности. Это мнодественные поправки в процессе исследования. Включены очень различные по исходным параметрам пациенты в двух исследовательстких центрах с различными схемами лечения. Результаты сообщались отдельно каждым центром. В центре 2 большинство пациентов лечилось в соответствии с протоколом, в то время как в центре 1 проводилось рутинное лечение пациентов, отличающееся от протокола исследования, особенно в том, что касается дозы липидов. Это было двойное-слепое рандимизированное активно-контролируемое исследование в параллельных группах безопасности, переносимости и эффективности СМОФлипида 20№ по сравнению с 20% Интралипидом (в течение 7-14 дней) у недоношенных младенцев с весом тела при рождении от 500 до 2000 g и нуждающихся в парентеральном питании, включая жиры, по крайней мере в течение 7 дней, гестационный возраст <34 недель, от 0 до 7-дневного возраста. Инфузия продолжалась свыше 20-24 часов в день в течение 7-14 дней для СМОФлипида 20% или Интралипида 20% через периферическую или центральную вену. Дозы (в г жиров/кг/день) были следующими: Дни 1-3: 1.0; День 4: 2.0; День 5: 3.0; Дни 6-14: 3.5. Максимальная скорость введения составила 0.17 г жира/кг/час. Если уровень триглицеридов превышал > 300 мг/дл дозу липидов снижали. Поступление дополнительного орального/энтерального питания составляло ≤ 30% от общего поступления энергии в День 1-3, ≤ 50% в Дни 4-17 и ≤ 70% в Дни 8-14. Первичными критериями безопасности был уровень триглицеридов сыворотки (как оценка, что скорость элиминации СМОФлипида будет не менее быстрой, чем у Интралипида). Вторичными критериями эффективности были: вес тела и рост, паттерн жирных кислот в эритроцитах и плазме. Вторичные критерии безопасности включали: общее состояние, побочные эффекты, гематологию, биохимию (включая ALT, GGT, глюкозу, креатинин, электролиты, билирубин, холестерол - общий, HDL, LDL), триглицериды сыворотки >300 мг/дл. Исследование проводилось в двух местах и включало 84 пациента. Не выявлено различий между двумя группами по показателям эффективности и безопасности. Побочные эффекты представлены в табл. 20.
Таблица 20.
Количественная характеристика пациентов с побочными эффектами всех системных органных классов и наибольшей частотой побочных эффектов (сообщенных хотя бы однажды) - безопасность популяции
| System Organ Class/Preferred Term | SMOF N = 42 | Intralipid N = 42 | Total N = 84 |
| Blood and lymphatic system disorders | 6 (14.3%) | 4 (9.5%) | 10(11.9%) |
| Anaemia | 3(7.1%) | 1 (2.4%) | 4 (4.8%) |
| Thrombocythaemia | 0 (0.0%) | 2 (4.8%) | 2 (2.4%) |
| Thrombocytopenia | 2 (4.8%) | 0 (0.0%) | 2 (2.4%) |
| Cardiac disorders | 0 (0.0%) | 1 (2.4%) | 1(1.2%) |
| Gastrointestinal disorders | 2 (4.8%) | 4 (9.5%) | 6(7.1%) |
| Ileus paralytic | 0 (0.0%) | 2 (4.8%) | 2 (2.4%) |
| General disorders and administration site conditions | 1 (2.4%) | 2 (4.8%) | 3 (3.6%) |
| Hepatobiliary disorders | 4 (9.5%) | 7 (16.7%) | 11(13.1%) |
| Hyperbilirubinaemia | 3 (7.1%) | 5(11.9%) | 8(9.5%) |
| Infections and infestations | 5 (11.9%) | 11 (26.2%) | 16 (19.0%) |
| Amniotic infection syndrome of Blane | 1 (2.4%) | 1 (2.4%) | 2 (2.4%) |
| Eye infection | 0 (0.0%) | 2 (4.8%) | 2(2.4%) |
| Infection | 1 (2.4%) | 1 (2.4%) | 2 (2.4%) |
| Respiratory tract infection | 1 (2.4%) | 1 (2.4%) | 2 (2.4%) |
| Rhinitis | 0(0.0%) | 2 (4.8%) | 2 (2.4%) |
| Sepsis | 1 (2.4%) | 1 (2.4%) | 2 (2.4%) |
| Staphylococcal sepsis | 1 (2.4%) | 3 (7.1%) | 4 (4.8%) |
| Investigations | 0 (0.0%) | 1 (2.4%) | 1 (1.2%) |
| Metabolism and nutrition disorders | 5 (11.9%) | 8 (19.0%) | 13 (15.5%) |
| Hyperglycaemia | 2 (4.8%) | 2 (4.8%) | 4(4.8%) |
| Metabolic acidosis | 3 (7.1%) | 5(11.9%) | 8 (9.5%) |
| Nervous system disorders | 3 (7.1%) | 1 (2.4%) | 4 (4.8%) |
| Intraventricular haemorrhage | 2 (4.8%) | 0(0.0%) | 2 (2.4%) |
| Respiratory, thoracic and mediastinal disorders | 2 (4.8%) | 2 (4.8%) | 4 (4.8%) |
| Surgical and medical procedures | 2 (4.8%) | 3 (7.1%) | 5 (6.0%) |
| Catheter removal | 1 (2.4%) | 2 (4.8%) | 3 (3.6%) |
| Vascular disorders | 1 (2.4%) | 1 (2.4%) | 2 (2.4%) |
| Hypotension | 1 (2.4%) | 1 (2.4%) | 2 (2.4%) |
Постмаркетинговый опыт исследования безопасности.
Постмаркетинговые наблюдения за применением препарата представлены в European Summary of Product Characteristics (SPC). He выявлено проблем, требующих какого-либо решения в плане дозирования препарата. В период с сентября 2004 года по декабрь 2007 года имелось только одно спонтанное сообщение о побочных реакциях (случай слабовыраженной эритемы).
ССЫЛКИ:
1. Intensive Care Manual, Fourth Edition, ТЕ Oh (ed), Oxford Butterworth-Heinemann 1997. Chapter 84, Parenteral Nutrition, page 725.
2. Waitzberg DL, Torrinhas RS, Jacintho TM. New parenteral lipid emulsions for clinical use. J Parenter Enteral Nutr. 2006; 30:351-67.
3. Acta Chirurgica Scandinavica Supplemenium 278. Stockholm 1961, page 3
4. Johnson RC, Cotter R. Metabolism of medium-chain triglyceride lipid emulsion. Nutr Internat 1986; 2: 150-158.
5. Bach AC, Babayan VK. Medium-chain triglycerides: an update. Am J Clin Nutr 1982; 36: 950-962.
6. NTP. Comparative toxicology studies of corn oil, safflower oil and tricaprylin (CAS Nos8001-30-7, 8001-23-8 and 538-23-8) in male F344/N rats as vehicles for gavage. Natl Toxicol Program Tech Rep Ser 1994; 426: 1-314.
7. Henwood S, Wilson D, White R, Trimbo S. Developmental toxicity study in rats and rabbits administered an emulsion containing medium chain triglycerides as an alternative caloric source. Fund Appl Toxicol 1997; 40: 185-190
8. The leukotriene findings have been published by Grimm H, Mertes N, Goeters C, Schlotzer E, Mayer K, Grimminger F, Furst P. Improved fatty acid and leukotriene pattern with a novel lipid emulsion in surgical patients. Eur J Nutr 2006; 45: 55-60.
9. Based on patient numbers, authors etc. this appears to have been published as Mertes N, Grimm H, Furst P, Stehle P. Safety and efficacy of a new parenteral lipid emulsion (SMOFlipid) in surgical patients: A randomized, double-blind, multicentre study. Ann Nutr Metab 2006; 50: 253-9.
10. The literature search is described as non systemic. The actual notes of the pre submission meeting and teleconference use the term non-systematic.
11. pp. 99 - 106 of Rules 1998 (3C) - ЗССЗа Pharmacokinetic Studies in Man
12. The reference for this level was given as Carpentier Y A, Kinney JM. Siderova VS, Richelle M, Nishiwaki H, Olivecrona T. Deckelbaum R. Hypertriglyceride clamp: a new model for studying lipid metabolism. Clin Nutr 1990; 9: Spec Suppl; however, this described the technique but used higher plasma triglyceride targets (~6 mmol/L) to show differences between 2 lipids. The reason for choosing 3 mmol/L was not given.
13 Carpentier YA, Dupont IE. Advances in intravenous lipid emulsions. World J Surg 2000; 24: 1493-7.
14. Driscoll DF. Lipid injectable emulsions. Nutr Clin Pract 2006; 21:381-6.
15. Ulrich H, Pastores SM, Katz DP, Kvetan V. Parenteral use of medium-chain triglycerides: a reappraisal. Nutrition 1996; 12: 231-8.
16. Lai H-S, Lin W-H, Wu H-C, Chang K-J, Chen W-J. Effects of a medium-chain triacylglycerol/long-chain triacylglycerol fat emulsion containing a reduced ratio of phospholipid to triacylglycerol in paediatric surgical patients. Nutrition 2005; 21:825-30.
17. Gentili A, Pigna A, lannella E, Mondardini MC, Ceccarelli PL, Baccarini E, Baroncini S. Prolonged neonatal parenteral nutrition with a fat emulsion containing medium-chain triglycerides. Rivista Italiana di Nutrizione Parenterale ed Enterale 2000; 18:134—42.
18. Lee S, Gura KM, Kim S, Arsenault DA, Bistrian BR, Puder M. Current clinical applications of omega-6 and omega-3 fatty acids. Nutr Clin Pract 2006; 21:323-41.
19. G Wanten. An Update on Parenteral Lipids and Immune Function: only smoke or is there fire. Current Opinion in Clin Nutr Metabol Care 2006; 9: 79-83.
20. Vahedi K, Atlan P, Joly F, Le Brun A, Evard D, Perennec V, Roux-Haguenau D, Bereziat G, Messing B. A 3-month double-blind randomised study comparing an olive oil- with a soyabean oil-based intravenous lipid emulsion in home parenteral nutrition patients. Br J Nutr 2005; 94: 909-16.
21. G Wanten, P Calder Immune Modulation by Parenteral Lipid Emulsions Am J Clin Nutr 2007; 85: 1171-84.
22. Trebble T, Arden NK, Stroud MA, Wootton SA, Burdge GC, Miles EA Ballinger AB, Thompson RL, Calder PC. Inhibition of tumour necrosis factor-alpha and interleukin 6 production by mononuclear cells following dietary fish-oil supplementation in healthy men and response to antioxidant co-supplementation. Br JNutr 2003; 90: 405-12.
23. Pironi L, Guidetti M, Zolezzi C, Fasano MC, Paganelli F, Merli C, Bersani G, Pizzoferrato A, Miglioli M. Peroxidation potential of lipid emulsions after compounding in all-in-one solutions. Nutrition. 2003; 19:784-8.
24. The initial stage in utilisation of the lipid infusions involves binding to endothelial lipoprotein lipase (e.g. in muscle, adipose tissue) with hydrolysis of triglycerides yielding fatty acids.
25. Amended to pre-infusion 16 November 1998. This was in order to take into account the greater variability in post-operative (but pre-infusion) serum triglyceride concentrations compared to baseline values.
26. Protocol amendment 16 November 1998. Originally 88/group gave 85% power for noninferiority and 77% for superiority. The source of the assumptions on which these calculations were based is not given but the original is said to be inconsistent with Chapter 3.1.in protocol amendment 4.
27. Leukotrienes (LT) and thromboxanes (TX) are formed from fatty acids LTB5 and TXB3 are derived from EPA (ω3 fatty acid), while LTB4 and TXB2 are derived from AA (ω6 fatty acid).
28. The text uses the unit g fat/kg/PN -PN = parenteral nutrition
29. Scott IA. Non-inferiority trials: determining whether alternative treatments are good enough. MJA 2009; 190: 326-330.
30. Schauder P, Rohn U, Schafer G, Korff G, Schenk HD. Impact of fish oil enriched total parenteral nutrition on DNA synthesis, cytokine release and receptor expression by lymphocytes in the postoperative period. Br J Nutr 2002; 87: S 103-110.
31. Hamilton C, Austin T, Seidner DL. Essential fatty acid deficiency in human adults during parenteral nutrition. Nutr Clin Pract. 2006; 21:387-94.
32. Schauder P, Rohn U, Schafer G, Korff G, Schenk HD. Impact of fish oil enriched total parenteral nutrition on DNA synthesis, cytokine release and receptor expression by lymphocytes in the postoperative period. Br J Nutr. 2002 Jan;87 Suppl l:S 103-110.
33. pp. 175 - 180 of Rules 1998 (3C) - ЗСС10а Fixed-Combination Medicinal Products.
34. CHMP/EWP/83561/2005 Guideline on Clinical Trials in Small Populations
Приложение III.
суммарные данные основных исследований СМОФлипида
|
Уровень триглицеридов сходен или лучше, чем в контроле | |||
| Schlotzer Е. | Ann. Nutr.Metab. 2004, 48: 263-268 | Добровольцы | Значительно ниже содержание ТГ и быстрее элиминация, чем в случае соевого масла (СМ) |
| Antebi Н. | JPEN 2004, 28: 142-148 | Хирургические пациенты | Незначительное увеличение ТГ в плазме со СМОФ по сравнению со значительным увеличением в группе с СМ |
| Genton L. | Clin. Nutr. 2004, 24: 793 (abstr.) | Смешанная популяция в ОРИТ | Сходный уровень ТГ по сравнению с СМ |
| Mertes N. | Ann. Nutr.Metab., 2006, 50: 253-259 | Хирургические пациенты | Сходный уровень ТГ по сравнению с СМ |
| Piper S. | Eur.J.Anaesthesiol., 2009, 26: 1087-1092 | Хирургические пациенты | ТГ на низком уровне во 2 и 5 дни в группе СМОФ, со значительным увеличением в группе с оливковым маслом (ОО). |
| Tomsits E. | JPGN, 2010, 51: 514-521 | Недоношенные младенцы | Сходный уровень ТГ по сравнению с СМ |
| Pichler J. | JPGN, 2010, 50 (S'): E185 (abstr.) | Ретроспективный обзор у детей с кишечной недостаточностью | ТГ были сходны у СМОФ и МСТ LCT и находились в нормальных пределах |
| Rayyan M. | JPEN, 2011, submitted Ped.Crit. Care Med., 2007, 8(S3): A318 (abstr.) | Недоношенные младенцы | Сходный уровень ТГ по сравнению с СМ |
|
Снижение продолжительности пребывания в госпитале | |||
| Grimm Н. | Eur.J.Nutr., 2006, 45: 55-60 Schulzki и соавт. Clin. Nutr. 1999, 18 (Sl): 7 (abstr.) | Хирургические пациенты | Время пребывания в госпитале (LOS) значительно короче, чем при применении СМ |
| Mertes N. | Ann. Nutr.Metab., 2006, 50: 253-259 | Хирургические пациенты | Тенденция к укорочению LOS по сравнению с СМ |
|
Ниже печеночные ферменты | |||
| Antebi Н. | JPEN 2004, 28: 142-148 | Хирургические пациенты | Меньшее увеличение печеночных ферментов со СМОФ, указывающее на лучшую функцию печени |
| Mertes N. | Ann. Nutr.Metab., 2006, 50: 253-259 | Хирургические пациенты | Меньше инцидентов с печеночными ферментами по сравнению с СМ |
| Piper S. | Eur.J.Anaesthesiol., 2009, 26: 1087-1092 | Хирургические пациенты | ALAT, ASAT и гамма-GST значительно ниже по сравнению с оливковым маслом (ОМ) на 2-5 день. СМОФ способен поддерживать гепатоцеллюлярную целостность |
| Singer P. | Clin. Nutr., 2009, 4 (S2): 63-64 (abstr.) | Кишечная недостаточность | Тренд к снижению печеночных ферментов по сравнению с СМ |
| Tomsits E. | JPGN, 2010, 51: 514-521 | Недоношенные младенцы | Значительно ниже уровень гамма-GT по сравнению с СМ в конце исследования |
| Pichler J. | JPGN, 2010, 50 (S'): E185 (abstr.) | Ретроспективный обзор у детей с кишечной недостаточностью | Тесты функции печени значительно улучшаются при СМОФ и MCT/LCT |
| Anish A. | BSPGHAN winter meeting 27-28th January 2010 | 8 детей с кишечной недостаточностью (case reports) | Обозначен и провозглашен поворот к применению СМОФлипида. Среднее время нормализации уровней билирубина, АТ и АР -до 13 недель |
|
Ниже уровня билирубина | |||
| Ferreira N. | BSPGHAN winter meeting 28-30th January 2009; 734 (abstr.) | 9 детей с PNALD (case reports) | У 3-х из 9 детей билирубин вернулся к нормальному уровню при замене СМ на СМОФ. |
| Rafeeq М. | BSPGHAN winter meeting 28-30th January 2009; 53. Pediatr.Gastroenterol.Nutr.2009, 48 (S3): E140 (abstr.) | 8 детей с PNALD (case reports) | В течение 1-3 месяцев после перехода с СМ на СМОФ наблюдалось выраженное падение билирубина у 6 из 8 пациентов |
| Goulet О. | JPEN, 2010, 34: 485-495 | Педиатрические пациенты на ДПП | Значительное улучшение общего билирубина плазмы по сравнению с СМ |
| Anish А. | BSPGHAN winter meeting 27-28th January 2010 | 8 детей с кишечной недостаточностью (case reports) | Намечено улучшение в результате замены СМ на СМОФ. Среднее время нормализации уровней билирубина, АТ и АР - до 13 недель |
| Hailey J. | Hepatol.-Gastroenterol., 2010, 57: 1069-1073 | Хирургические пациенты | Общий и конъюгированный билирубин значительно снижается со СМОФ по сравнению с MCT/LCT |
| Rayyan М. | JPEN, 2011, submitted Acta Ped. 2009, 98: S460 (abstr.) | Недоношенные младенцы | Значительно большее снижение от базовой линии общего билирубина со СМОФ по сравнению с СМ |
| Skouroliakou М. | Eur.J.Clin.Nutr., 2010, 64: 940-947 | Недоношенные младенцы | Значительное снижение общего билирубина со СМОФ по сравнению с СМ |
| Pichler J. | JPGN, 2010, 50 (S'): E185 (abstr.) | Ретроспективный обзор у детей с кишечной недостаточностью | Гипербилирубинемия исчезала у 30% и наблюдалось значительное улучшение уровней билирубина у 72% как в группе СМОФ, так и MCT/LCT |
| Проблемы заболеваний печени, связанные с ПП - Parenteral Nutrition Associated Liver Disease (PNALD): | |||
| Ferreira N. | BSPGHAN winter meeting 28-30th January 2009; 734 (abstr.) | 9 детей с PNALD (case reports) | У 3 из 9 детей билирубин вернулся к норме вследствие перехода на СМОФ от СМ |
| Rafeeq M. | BSPGHAN winter meeting 28-30th January 2009; 53. Pediatr.Gastroenterol.Nutr.2009, 48 (S3): E140 (abstr.) | 8 детей с PNALD (case reports) | В течение 1-3 месяцев после перехода с СМ на СМОФ наблюдалось выраженное падение билирубина у 6 из 8 пациентов |
| Pichler J. | JPGN, 2010, 50 (S'): E185 (abstr.) | Ретроспективный обзор у детей с кишечной недостаточностью | Тесты функции печени значительно улучшаются при СМОФ и MCT/LCT |
| Anish A. | BSPGHAN winter meeting 27-28th January 2010 | 8 детей с кишечной недостаточностью (case reports) | Обозначен и провозглашен поворот к применению СМОФлипида. Среднее время нормализации уровней билирубина, АТ и АР -до 13 недель |
| Ниже параметры воспаления | |||
| Antebi Н. | JPEN 2004, 28: 142-148 | Хирургические пациенты | Нет значительного возрастания С-реактивного белка по сравнению с СМ |
| Grimm Н. | Eur.J.Nutr., 2006, 45: 55-60 Schulzki и соавт. Clin. Nutr. 1999, 18 (Sl): 7 (abstr.) | Хирургические пациенты | Выход LTB5 значительно усиливается на 6 день, а выход LTB4 снижается по сравнению с СМ |
| Piper S. | Int. Care Med. 2008, 34 (Sl): S259 Philip-0stermann и соавт., Int.Care Med. 2009, 35 (Sl): S150 (abstr.) | Хирургические пациенты | На 5 день значительно ниже концентрации IL-6, TNF-альфа и sE-селектина по сравнению с оливковым маслом (ОО), что указывает на значительное снижение воспалительного ответа. Соотношение IL-6/IL-10 значительно выше с ОО на 5 день. Противовоспалительный ответ (LTB5) значительно повышался со СМОФ. Уровни параметров адгезии существенно ниже на 5 день со СМОФ. |
| Schareyka S. | DAC Congress 2008, Poster 3.7.9. (abstr.) | Хирургические пациенты | Тенденция к более хорошему соотношению респираторное напряжение/способность к фагоцитозу со СМОФ по сравнению с MCT/LCT, указывающее на улучшение иммунного ответа гранулоцитов |
| Mangiante GL. | Clin.Nutr., 2010, 5 (S2): 128 (abstr.) | 1 пациент с резекцией печени, 3 -с панкреатитом | С-реактивный белок снижается в течение первых 2-х недель со СМОФ |
Выше уровни ЕРА и DHA в плазме и/или эритроцитах | |||
| Goulet О. | JPEN, 2010, 34: 485-495 | Педиатрические пациенты на ДПП | ЕРА и DHA в плазме и эритроцитах возрастают на 29 день при применении СМОФ по сравнению с СМ |
| Grimm Н. | Eur.J.Nutr., 2006, 45: 55-60 Schulzki и соавт. Clin. Nutr. 1999, 18 (Sl): 7 (abstr.) | Хирургические пациенты | Выше соотношение ЕРА/АА в плазме на 6 день по сравнению с СМ (значительно) |
| Piper S. | Philip-0stermann и соавт., Int.Care Med. 2009, 35 (SI): S150 (abstr.) | Хирургические пациенты | Значительно выше ЕРА, DHA и соотношение ЕРА/АА на 2 и 5 день по сравнению с ОО |
| Tomsits Е. | JPGN, 2010, 51: 514-521 | Недоношенные младенцы | Возрастание ЕРА в эритроцитах по сравнению с СМ |
| Rayyan М. | JPEN 2011. submitted Ped.Crit.Care Med. 2007, 8(S3): A318 J.Pediatr.Gastroenterol.Nutr.2007, 44: e314 (abstr.) | Недоношенные младенцы | Существенное увеличение в плазме ЕРА и DHA со СМОФ, но не с СМ |
|
Увеличение соотношения омега-З/омега-6 жирных кислот, снижение соотношения n-6/n-З | |||
| Grimm Н. | Eur.J.Nutr., 2006, 45: 55-60 | Хирургические пациенты | Выше соотношение n-З/n-6 жирных кислот в фосфолипидах плазмы по сравнению с СМ |
| Goulet О. | JPEN, 2010, 34: 485-495 | Педиатрические пациенты на ДПП | Соотношение n-З/n-6 жирных кислот возрастает значительно по сравнению с СМ |
| Rayyan М. | JPEN 2011. submitted Ped.Crit.Care Med. 2007, 8(S3): A318 J.Pediatr.Gastroenterol.Nutr.2007, 44: e314 (abstr.) | Недоношенные младенцы | Большее снижение соотношения n-6/n-З со СМОФ по сравнению с СМ |
| Повышение антиоксидантного статуса | |||
| Antebi Н. | JPEN 2004, 28: 142-148 | Хирургические пациенты | Уровни альфа-токоферола, ретинола и LDL-альфа-токоферола повышались при применении СМОФ |
| Grimm Н. | Eur.J.Nutr., 2006, 45: 55-60 | Хирургические пациенты | Выше содержание альфа-токоферола в плазме по сравнению с СМ |
| Singer Р. | Clin. Nutr., 2009, 4 (S2): 63-64 (abstr.) | Кишечная недостаточность | Значительное увеличение концентрации витамина Е в плазме со СМОФ по сравнению с СМ |
| Goulet О. | JPEN, 2010, 34: 485-495 | Педиатрические пациенты на ДПП | Альфа-токоферол увеличивается в плазме больше со СМОФ, чем с СМ |
| Tomsits Е. | JPGN, 2010, 51: 514-521 | Недоношенные младенцы | Выше содержание альфа-токоферола в плазме по сравнению с СМ |
| Skouroliakou М. | Eur.J.Clin.Nutr., 2010, 64: 940-947 | Недоношенные младенцы | Сывороточный витамин Е и ТАР значительно выше со СМОФ по сравнению с СМ |
|
Нет увеличения пероксидации липидов | |||
| Goulet О. | JPEN, 2010, 34: 485-495 | Педиатрические пациенты на ДПП | Концентрация в сыворотке LDL-TBARS была сопоставима в обеих группах |
| Tomsits Е. | JPGN, 2010, 51: 514-521 | Недоношенные младенцы | MDA плазмы показало умеренное снижение по сравнению с базовой линией в обеих исследованных группах |
| Сходный рост (только педиатрия) | |||
| Tomsits Е. | JPGN, 2010, 51: 514-521 | Недоношенные младенцы | Вес тела увеличивается такими же темпами, что и при введении СМ |
| Rayyan М. | JPEN 2011. submitted Ped.Crit.Care Med. 2007, 8(S3): A318 J.Pediatr.Gastroenterol.Nutr.2007, 44: e314 (abstr.) | Недоношенные младенцы | Сходное и значительное увеличение веса тела со СМОФ и СМ |
| Skouroliakou М. | Eur.J.Clin.Nutr., 2010, 64: 940-947 | Недоношенные младенцы | Сходное и значительное увеличение веса тела со СМОФ и СМ |
Приложение IV. Использование жировых эмульсий ω-3 жирных кислот в интенсивной терапии: взгляд клинициста
(F. Grimminger , W. Seeger , К. Mayer)
Justus Liebig University Giessen, Germany (Correspondence to: K. Mayer, Department O' Internal Medicine, Justus. Liebig University Giessen, KlinikstraSe 36, D-35392 Giessen, Germany)
Резюме
ω-3 липиды использовались в медицине давно, благодаря своей способности снижать активность воспалительных заболеваний. В отделениях интенсивной терапии (ОИТ) у пациентов с острыми воспалительными болезнями, такими как сепсис и острый респираторный дистресс-синдром (ОРДС), часто возникает необходимость в искусственном питании. Патогенетическая основа этих заболеваний гипервоспалительный ответ с чрезмерной активностью лейкоцитов, последующими нарушениями микроциркуляции и вторичным повреждением органов. Лечение этих пациентов затруднено тем, что гипервоспалительная (синдром системного воспалительного ответа [SIRS]) и гиповоспалительная (компенсаторный противовоспалительный синдром [CARS]) фазы могут чередоваться в течение заболевания. По этой причине широкий ряд противовоспалительных агентов не продемонстрировал эффективности при лечении септических пациентов: являясь эффективными средствами подавления гипервоспаления во время SIRS, они ослабляли антимикробную защиту при CARS. Противовоспалительные цитокины, эффективные в раннюю фазу сепсиса, могут быть вредными, когда назначаются в позднюю фазу. Недавно, в качестве нового подхода, стали доступными ω-3 жировые эмульсии. Назначение ω-3 жирных кислот (ЖК) энтеральным путем для влияния на воспаление при сепсисе не эффективно, т. к. на это потребуются месяцы. Парентеральное введение чистых омега-3 липидов значительно превосходит энтеральное по кинетике и эффективности. При внутривенном использовании ω-3 жировых эмульсий может быть смягчено гипервоспаление и предотвращено последующее развитие противовоспалительной фазы. Так как ω-3 ЖК взаимодействуют с трансмембранными сигнальными молекулами, они, вероятно, способны снижать гиперреактивность в обеих составляющих сепсиса (SIRS и CARS). Благодаря этому свойству ω-3 ЖК способны ингибировать неконтролируемый выброс активных лейкоцитов и перенаправить защитные функции макроорганизма на борьбу с микробами.
Ключевые слова: лейкоциты; сепсис; ОРДС; ω-3 жировые эмульсии; парентеральное питание.
Введение
Концепция фармакологической интервенции с помощью ω-3 липидов
Возможность ω-3 липидов при пероральном / энтеральном назначении изменять активность лейкоцитов, продукцию медиаторов липидной природы и высвобождение цитокинов давно вызывала дискуссии (1, 2). Недавно стали доступны жировые эмульсии на основе рыбьего жира, богатого ω-3 липидами для внутривенного введения, которые имеют еще больший потенциал в фармакологическом воздействии. В этом обзоре описываются биохимические основы введения разных жировых эмульсий на воспалительный ответ и обсуждаются потенциальные возможности использования жировых эмульсий при заболеваниях с гиперактивацией иммунной системы.
Влияние ω-3 липидов на межклеточную передачу информации - медиаторы и цитокины
Медиаторы липидной природы синтезируются по липооксигеназному, циклооксигеназному путям и с помощью цитохрома Р-450 из жирных кислот, таких как арахидоновая (АА), в качестве субстрата. К ним относятся эйкозаноиды (простагландины, тромбоксаны, лейкотриены (LT), липоксины, гидроксидные и эпоксидные производные жирных кислот) и фактор активирующий тромбоциты (PAF). Они действуют как внутриклеточные сигнальные молекулы и могут влиять на секрецию иммунорегуляторных цитокинов. Эйкозаноиды вовлечены как в про- так и в противовоспалительные процессы при сепсисе.
Арахидоновая кислота (АА) относится к семейству ω-6 ЖК и представляет наиболее распространенную полиненасыщенную жирную кислоту в рационе европейского человека. Омега-3 ЖК, в которых последняя двойная связь от метильного конца находится межу третьим и четвертым атомами углерода, представлены эйкозапентаеновой (ЕРА) и докозагексаеновои (DHA) кислотами, входящими в состав мяса тюленей и холодноводных рыб. Они служат альтернативными субстратами для липооксигеназного, циклооксигеназного путей и, возможно, для цитохрома Р-450, что приводит к образованию триеновых простаноидов (вместо диеновых из АА) и 5-го ряда LT (вместо 4-го из АА) (2). Несмотря на тот факт, что большинство воспалительных липидных медиаторов являются производными АА, ЕРА представляет собой более предпочтительный субстрат для липоокигеназного пути, чем АА. При одинаковой доступности обеих жирных кислот в результате их метаболизма образуется больше производных ЕРА за счет уменьшения количества производных АА. Большинство производных ЕРА, включая 5-й ряд цистеинил-лейкотриенов, LTB5 и тромбоксан АЗ обладают гораздо меньшим воспалительным и вазомоторным потенциалом, чем производные АА и даже могут иметь антагонистические с ними свойства (5).
Более того, ЕРА и DHA способны модулировать воспаление путем уменьшения синтеза провоспалительных цитокинов: несколько недель приема ω-3 ЖК приводит к уменьшению продукции фактора некроза опухоли α (TNF-α) и интерлейкина 1 (IL-1) мононуклеарными клетками (6, 7). Вдобавок, лейкоциты сами по себе крайне чувствительны к свободным ПНЖК. Обогащение диеты ПНЖК или экспозиция лейкоцитов с ПНЖК in vitro приводила к подавлению продукции IL-2, презентации антигена, пролиферации лимфоцитов и активности натуральных киллеров (2). Таким образом, основной целью назначения ω-3 ЖК больным в критических состояниях является уменьшение метаболизма АА до провоспалительных медиаторов.
Влияние ω-3 липидов на внутриклеточную передачу информации - метаболизм второго мессенджера
Присоединение к рецептору приводит к активации фосфатидил-инозитол-специфичной фосфолипазы С (PI-PLC). Этот фермент расщепляет фосфатидил-инозитол-дифосфат (РIР2) на диацилглицерол (DAG) и инозитол-трифосфат (IРз). От того, какие ЖК входят в состав PIP2, зависит генерация инозитол-фосфатов (IPX), т. к. накопление ω-3 ПНЖК в фосфатидил-инозитоле (PI) при потреблении рыбьего жира ведет к снижению образования IPX и DAG с последующим уменьшением лейкоцитарного ответа на воспалительный стимул (8). Далее, жирнокислотный состав DAG влияет на DAG-зависимую активацию протеинкиназы С (РКС). DAG с ω-3 ПНЖК в позиции sn-2 слабее индуцирует РКС, чем если в этой позиции находится АА. После DAG-активации, РКС перемещается на клеточную мембрану и присоединяется к фосфатидилсерину. На реакцию влияет жирнокислотный состав фосфолипидов: фосфатидилсерин с высоким содержанием ω-3 ПНЖК ослабляет связывание и последующую активность РКС (9, 10). В результате этого, принимая во внимание сумму эффектов на систему второго мессенджера, можно ожидать ослабление сопряжения между стимулом и ответом, что влияет на активацию клетки. Следовательно, состояние иммунореактивных лейкоцитов может быть смещено от гиперреактивного в сторону нормальной функции. Таким образом, ω-3 липиды могут применяться при гипервоспалительном состоянии или в качестве профилактики этого состояния у пациентов высокого риска.
Влияние ω-3 липидов на поведение лейкоцитов
Истинное предназначение лейкоцита - это контролируемое высвобождение его деструктивного потенциала во время схватки с инфекционным агентом. На своем пути к очагу инфекции лейкоциты должны покинуть просвет сосуда и мигрировать в направлении бактериальной клетки в воспаленной ткани. Эта основная схема работает при остром и хроническом воспалении. Однако, если лейкоцит гиперреактивен, его оружие может быть неверно направлено против организма хозяина (гипервоспаление) - механизм, который работает при аутоиммунных болезнях и у больных в критическом состоянии. Чрезмерный воспалительный ответ может также сделать острую или хроническую болезнь очень продолжительной. Лейкоциты покидают просвет сосуда через эндотелий. В настоящее время этот процесс представляется многоэтапным. Трансэндотелиальная миграция лейкоцитов начинается с прилипания к стенке сосуда, затем происходит передвижение по эндотелиальным клеткам, плотная адгезия и миграция в субэндотелиальное пространство через межклеточные щели. В этом процессе участвуют молекулы адгезии, к которым относятся селектины и их антагонисты, р, и р2 интегрины и несколько представителей семейства иммуноглобулинов. Провоспалительные цитокины способны усиливать экспрессию молекул адгезии на эндотелиальных клетках. TNF-α и IL-1, образованные в воспаленной ткани, облегчают миграцию и направляют лейкоциты из внутрисосудистого пространства в очаг воспаления. Уменьшая TNF-зависимую активацию молекул адгезии, ω-3 ПНЖК снижают экстравазацию лейкоцитов.
Кроме того, ω-3 ПНЖК, доставленные внутривенной инфузией или освобожденные из липидов эндотелиальной мембраны влияют на поведение лейкоцитов при воспалении, воздействуя на синтез лейкотриенов. В условиях воспаления эндотелиальные клетки освобождают АА для того, чтобы присоединенные к ним нейтрофилы продуцировали LTA4. В свою очередь LTA4 используется самим нейтрофилом для синтеза LTB4 -мощного хемоаттрактанта, или смежной эндотелиальной клеткой для синтеза LTC4 -сильного поскапиллярного вазоконстриктора. Оба эти медиатора липидной природы способствуют экстравазации лейкоцитов. ЕРА, как описано выше, является более выгодным, по сравнению с АА субстратом для продукции лейкотриенов, и уменьшает АА-зависимый синтез лейкотриенов. Более того, лейкотриены - производные ЕРА, -ингибируют хемоаттрактантную активность и стимулирующий потенциал лейкотриенов -производных АА. Описанные эффекты объединяются в системный противовоспалительный эффект со снижением миграции и смягчением активации лейкоцитов.
Различный противовоспалительный потенциал энтерального и парентерального путей введения ω-3 липидов
Несмотря на то что основной опыт по применению ω-3 ПНЖК был получен при их энтеральном назначении, этот путь имеет отрицательные стороны. Терапевтический эффект наступает медленно и, следовательно, такой путь приема неприменим при острых заболеваниях. При использовании капсул с рыбьим жиром биодоступность молекул ω-3 ПНЖК ограничена, т. к. они попадают в системный кровоток после прохождения кишечного барьера, организации в везикулы в виде триглицеридов и попадания в печень, в результате чего теряются свободные ω-3 ПНЖК из-за процесса ремоделирования липидов. При этом доступность свободных жирных кислот для участия в процессе воспаления как в лейкоцитах, так и в эндотелиальных клетках ограничена. В отличие от этого, при внутривенной инфузии жировой эмульсии путь ремоделирования липидов в печени и кишечнике шунтируется, большое количество синтетических липидов активирует эндотелиальные липопротеинлипазы и вызывает перемещение этих ферментов из связанного с клеткой состояния в сосудистое русло. В результате резкого повышения концентрации свободных ЖК в плазме становится возможным их свободное потребление клетками, рост концентрации ЖК в клетках и свободные ЖК - предшественники медиаторов липидной природы (например, ЕРА или АА) становятся доступными в избытке (11). Внутривенная инфузия жировых эмульсий (Омегавен) обладает более выгодной фармакокинетикой и возможностью ввести большее количество ЖК, чем при энтеральном их потреблении (12, 13).
Терапия внутривенными ω-3 ЖК в отделении интенсивной терапии
Несмотря на тот факт, что в отделении интенсивной терапии ОИТ преимущество отдается энтеральному питанию как более физиологичному, некоторые пациенты нуждаются в парентеральном питании, т. к. их состояние не позволяет вводить питательные вещества в кишечник. Это также относится к пациентам после больших операций на желудочно-кишечном тракте и больным с обострениями воспалительных заболеваний толстой кишки, таких как болезнь Крона и неспецифический язвенный колит. Кроме того, в парентеральном питании могут нуждаться пациенты с тяжелым сепсисом или острым респираторным дистресс-синдромом (ОРДС), если у них не может быть обеспечен пассаж по кишечнику по причинам ишемии или применения медикаментов, приводящих к параличу гладкой мускулатуры. Ишемическое повреждение может быть вызвано шоком и сопутствовать синдрому недостаточности спланхнических органов. В этих случаях парентеральное питание является обязательным, а жировые эмульсии - это фундаментальная составляющая современных схем внутривенного питания благодаря своей калорической ценности и предотвращения жировых изменений в печени, которые имеют место при использовании углеводородов, как единственного источника энергии. Внутривенное введение эмульсий рыбьего жира предназначено не для парентерального питания, а для фармакологических эффектов чистых омега-3 ЖК. Поэтому эмульсии очищенного рыбьего жира могут применяться независимо от вида питания (парентеральное, энтеральное, естественное).
Гипервоспаление как терапевтическая мишень в отделении интенсивной терапии
Сепсис, тяжелый сепсис и септический шок продолжают оставаться причинами высокой летальности (от 30 до 60%). Современные достижения в интенсивной терапии не смогли повлиять на эти цифры (14-17). Таким образом, сепсис продолжает оставаться главной причиной смерти больных в ОИТ во всем мире.
Здоровый организм защищен от вторжения микробов сложной, хорошо регулируемой и мощной иммунной системой. Однако в определенных условиях, может происходить неконтролируемый выброс большого количества высокоактивных и потенциально аутотоксичных медиаторов, что ведет к неселективной гиперреактивности иммунной защиты (3, 8, 19). Кроме микробной инвазии, синдром системного воспалительного ответа (SIRS) может быть вызван разными видами повреждения тканей организма. Более того, не только микробы сами по себе, но и такие субстанции, как эндотоксин (липополисахарид [LPS]), экзотоксины, суперантигены, тейхоевая кислота, выделяемые бактерией, могут запустить избыточное высвобождение воспалительных медиаторов и вести к гипервоспалительному повреждению организма.
Традиционные средства для иммуносупрессии
Смягчение избыточного воспалительного ответа считается одной из целей в терапии сепсиса. Такая терапия исследовалась на животных и, несмотря на положительные результаты в эксперименте, III фаза клинических испытаний не показала положительного влияния на выживаемость (15). Главным недостатком обычно используемых иммуносупрессивных средств является то, что врач должен определить, находится ли пациент в состоянии гипервоспаления в данный момент. К сожалению, в настоящее время нет рутинного лабораторного теста, позволяющего дифференцировать гипер- и гиповоспалительный статусы. Задолго до появления современных взглядов на противовоспалительную терапию (например, антитела к TNF-α или IL-1) при сепсисе были опробованы высокие дозы стероидов и нестероидные противовоспалительные средства (HПBC) (например, ибупрофен). В больших мультицентровых исследованиях было доказано отсутствие влияния на выживаемость высоких доз стероидов при септическом шоке (20, 21). Более того, использование кортикостероидов в высоких дозах или в течение длительного времени было связано с повышенным риском желудочно-кишечного кровотечения и присоединения оппортунистических инфекций. В отношении НПВС недавнее мультицентровое исследование не продемонстрировало влияния на выживаемость (22). Кроме того, использование НПВС несет риск возникновения желудочно-кишечного кровотечения, почечной недостаточности и бронхоконстрикции. Оба этих терапевтических принципа в настоящее время считаются неприемлемыми в качестве препаратов первой линии при лечении септических пациентов. В заключении необходимо отметить, что теоретическое преимущество традиционных иммуносупрессивных препаратов в гипервоспалительную фазу оборачивается большим недостатком в фазу иммунопаралича.
Модуляция иммунитета с помощью ω-3 ЖК: влияние на поведение воспалительного лейкоцита при монофазных гипервоспалительных болезнях
В отличие от значительной иммунной супрессии, вызываемой кортикостероидами, метотрексатом или циклоспорином, обогащение диеты рыбьим жиром индуцирует умеренную модуляцию иммунной системы при некоторых заболеваниях. При болезни Крона медиаторы липидной природы и цитокины приводят к развитию хронического поражения кишечника (23). Рыбий жир в энтеросолюбильной оболочке применяли в течение 1 года у пациентов высокого риска с болезнью Крона в стадии ремиссии. Это привело к значительному уменьшению количества рецидивов и снижению лабораторных признаков воспаления (24).
В трансплантологии важнейшей проблемой для клинициста остается острое и хроническое отторжение трансплантата. Рутинно используемые иммуносупрессивные препараты обладают серьезными побочными эффектами и заставляют искать альтернативные способы терапии этих осложнений, ω-3 ЖК в экспериментах на животных показали обнадеживающие результаты в отношении реперфузионного повреждения и отторжения. Клиническое доказательство эффективности назначения рыбьего жира получено на реципиентах почки (25), которые начинали принимать его одновременно с трансплантацией. У этих пациентов отмечался поразительно высокий уровень гломерулярной фильтрации, по сравнению с пациентами контрольной группы.
Также сообщается о благоприятных эффектах назначения рыбьего жира у больных псориазом, неспецифическим язвенным колитом и ревматоидным артритом.
Использование ω-3 липидов при ОРДС и сепсисе: влияние на гиперреактивность лейкоцитов
Острый респираторный дистресс-синдром (ОРДС) описан как острое воспалительное нарушение, сопровождающееся повышенной проницаемостью альвеоло-капиллярной мембраны, ведущее к физиологическим и рентгенологическим отклонениям не вследствие гипертензии в левом предсердии. Недавние сообщения акцентируют внимание на локальном дисбалансе про- и противовоспалительных медиаторов, а также дисбалансе оксидантного стресса и антиоксидантов, как на причинах повышенной склонности к развитию ОРДС (26, 27). Основными характеристиками этого синдрома являются: острая легочная гипертензия, вызванная тромбоксаном А2, последующий отек легких, вызванный лейкотриенами, цитокинами и другими медиаторами, и угрожающие нарушения вентиляционно-перфузионного соотношения (28).
Протективный эффект ω-3 ЖК хорошо изучен на моделях острого легочного повреждения. Инфузия свободной арахидоновой кислоты (АА) усиливает развитие отека легких и легочной гипертензии на модели легких при сепсисе. В отличие от этого, инфузия свободной эйкозапентаеновой кислоты (ЕРА) уменьшает отек легких и снижает гипертензию в малом круге кровообращения (29-33), что связано с образованием медиаторов липидной природы из ω-3 ЖК. К тому же обогащение диеты ω-3 ЖК уменьшало острое легочное повреждение при сепсисе путем снижения легочной гипертензии, уменьшения формирования отека и миграции нейтрофилов в легкие, снижения продукции липидных медиаторов - производных арахидоновой кислоты (1,34-38).
Как описано при септическом шоке, гипервоспалительная реакция наблюдается в начальной стадии заболевания. Параллельно с воспалительным ответом на повреждение инициируется противовоспалительная реакция, названная «компенсаторным противовоспалительным синдромом» (CARS) (17). Он состоит из активации противовоспалительных цитокинов, нарушения функции нейтрофилов и инактивации моноцитов, что ведет к ослаблению иммунной защиты и повышению восприимчивости к вторичной инфекции (40-43).
ω-З липиды могут перенаправить иммунную защиту против микроорганизмов
Обе фазы сепсиса - гипервоспалительная (SIRS) и гиповоспалительная (CARS) - ведут к неэффективности защиты организма (Рис. 1 и 2). При SIRS лейкоциты с повышенной реактивностью высвобождают свой разрушающий потенциал еще до того, как достигнут очага инфекции, и повреждают организм с последующим развитием вторичной недостаточности органов. При CARS лейкоциты неспособны бороться с микроорганизмами, т. к. их потенциал уже использован в SIRS или они парализованы действием противовоспалительных медиаторов. Принимая во внимание описанные выше свойства ω-3 липидов, можно предположить, что назначение септическим пациентам жировых эмульсий на основе рыбьего жира может быть эффективно.
Рис. 1. (а) Двухфазное течение иммунных нарушений при сепсисе. После начала заболевания наблюдается взрывной выброс провоспалительных медиаторов, таких как TNF-α и IL-1, что приводит к возникновению гипервоспалительного ответа (SIRS). Далее, с компенсаторным ростом концентрации противовоспалительных медиаторов, развивается иммунопаралич (CARS).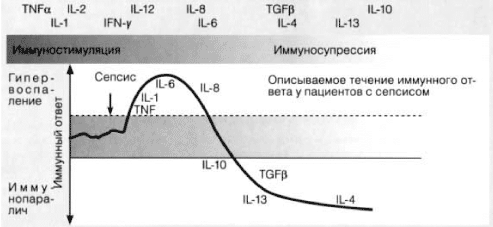
Рис. 1. (b) Из-за недостаточного клиренса микроорганизмов может развиться порочный круг и обострение септического процесса.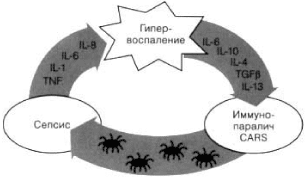
Рис. 2. (а) В двухфазном течении септического процесса гиперактивация лейкоцитов при SIRS приводит к вторичному повреждению органов. Последующий CARS характеризуется нарушением способности лейкоцитов поражать микробы и развитием вторичных инфекций.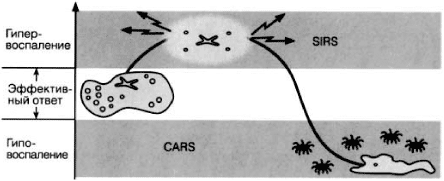
Рис. 2. (b) Инфузия ω-3 липидов смягчает как гипервоспаление, так и выраженный гиповоспалительный ответ путем влияния на меж- и внутриклеточную передачу информации.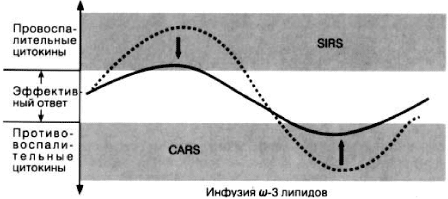
ω-3 жиры способны уменьшать избыточный иммунный ответ при SIRS и перенаправить «заблудившиеся» лейкоциты к очагу инфекции. Ограничивая саморазрушающие процессы в лейкоцитах, ω-3 липиды перенаправляют защиту организма против микроорганизмов и контролируют иммунный ответ. Важное исследование по энтеральному введению, подчеркивающее эту концепцию, было проведено Galban et al. (44), т. к. им удалось продемонстрировать снижение летальности у пациентов с сепсисом. Однако, ввиду того что их энтеральная смесь была обогащена не только ω-3 ЖК, нельзя сделать окончательный вывод об эффективности каждого из компонентов. Кроме того, эффекты перорального / энтерального и парентерального введения ω-3 ЖК могут отличаться, т. к. внутривенная инфузия (но не пероральное / энтеральное введение) эмульсии на основе рыбьего жира приводит к массивному повышению концентраций свободных ЕРА и DHA в плазме с выраженным эффектом на высвобождение провоспалительных медиаторов при SIRS.
ω-З липиды ослабляют повышенную реактивность лейкоцитов и предотвращают CARS /SIRS
Использование внутривенной инфузии чистых ω-3 липидов в ОИТ может влиять на иммунную реактивность организма. Снижение степени гипервоспаления в первой фазе сепсиса приводит к тому, что леикоциты не истощаются и не растрачивают свои деструктивный потенциал. Благодаря этому во второй фазе повышение концентрации противовоспалительных цитокинов не вызовет столь выраженного паралича лейкоцитов. Более сбалансированная иммунная защита организма будет обеспечена предотвращением «крайностей» в течении сепсиса (периодов гипер- и гиповоспаления).
Заключение
Недавние достижения в медицине показали, что добавление с схемы лечения омега-3 ЖК может влиять на воспалительные и иммунологические процессы при некоторых заболеваниях, ω-3 липиды способны модулировать синтез медиаторов липидной природы, высвобождение цитокинов, регулировать активацию лейкоцитов и эндотелиальных клеток. Энтеральный прием ω-3 липидов воздействует на активность хронических воспалительных болезней, таких как ревматоидный артрит, болезнь Крона, а также эффективен при трансплантации почки. Внутривенное введение ω-3 жировых эмульсий значительно превосходит оральное их потребление по фармакокинетике и конечной концентрации свободных ЖК в плазме и, следовательно, может применяться для терапии острых гипервоспалительных заболеваний в интенсивной терапии. У пациентов с сепсисом, благодаря снижению активности гипервоспалительной фазы, ω-3 ЖК сдерживают развитие последующего иммунопаралича. Они также ограничивают неконтролируемый выброс лейкоцитарных факторов повреждения, вследствие чего их цитотоксическая активность перенаправляется на истинную мишень иммунологической защиты - микроорганизм.
ССЫЛКИ:
1. Murray MJ, Kumar М, Gregory TJ, Banks PL, Tazelaar HD, DeMichele SI. Select dietary fatty acids attenuate cardiopulmonary dysfunction during acute lung injury in pigs. Am J Physiol 1995; 269 (6 Pt 2): H2090-2099
2. Calder PC. Immunoregulatory and anti-inflammatory effects of n-3 polyunsaturated fatty acids. Braz J Med Biol Res 1998;31:467-490
3. Heller A, Koch T, Schmeck J, van Ackern K. Lipid mediators in inflammatory disorders. Drugs 1998; 55:487-496
4. Mayer K, Seeger W, Grimminger F. Clinical use of lipids to control inflammatory disease. Curr Opin Clin Nutr Metab Care 1998; 1: 179-184
5. Kragballe K, Voorhees JJ, Goetzl EJ.Inhibition by leukotriene B5 of leukotriene B4-induced activation of human keratinocytes and neutrophils. J Invest Dermatol 1987; 88: 555-558
6. Endres S, Ghorbani R, Kelley VE, Georgilis K, Lonnemann Ci, van der Meer JWM et al. The effect of dietary supplementation with n-3 polyunsaturated fatty acids on the synthesis of interleukin-1 and tumor necrosis factor by mononuclear cells. N Engl J Med 1989; 320: 265-271
7. Caughey GE, Mantzioris E, Gibson RA, Cleland LG; James MJ. The effect on human tumor necrosis factor alpha and interleukin 1 beta production of diets enriched in n-3 fatty acids from vegetable oil or fish oil. Am J Clin Nutr 1996; 63: 116-122
8. Sperling Rl, Benincaso Al, Knoell CT, Larkin JK, Austen KF, Robinson DR. Dietary omega-3 polyunsaturated fatty acids inhibit phosphoinositide formation and chemotaxis in neutrophils. J Clin Invest 1993; 91: 651-660
9. May CL, Southworth AJ, Calder PC. Inhibition of lymphocyte protein kinase С by unsaturated fatty acids. Biochem Biophys Res Commun 1993; 195: 823-828
10. Terano T, Shiina T, Tamura Y. Eicosapentaenoic acid suppressed the proliferation of vascular smooth muscle cells thrOUgh modulation of various steps of growth signals. Lipids 1996; 31: S301-S304
11. Peterson J, Bihain BE, Bengtsson-Olivecrona Ci, Deckelbaum Rl, Carpentier YA, Olivecrona T. Fatty acid control of lipoprotein lipase: A link between energy metabolism and lipid transport. Proc Natl Acad Sci USA 1990; 87: 909-913
12. Rustan AC, Hustvedt BE, Drevon CA. Postprandial decrease in plasma unesterified fatty acids during n-3 fatty acid feeding is not caused by accumulation of fatty acids in adipose tissue. Biochem Biophys Acta 1998; 1390, 245-257
13. Lovegrove JA, Brooks CN, Murphy MC, Gould BJ, Williams CM. Use of manufactured foods enriched with fish oil as a means of increasing long-chain n-3 polyunsaturated fatty acid intake. Br JNutr 1997; 78: 223-236
14. Friedman Ci, Silva E, Vmcent JL. Has the mortality of septic shock changed with time? CritCare Med 1998; 26: 2078-2086
15. Wheeler AP, Bernard GR. Treating patients with severe sepsis. N Eng! J Med 1999; 340: 207-214
16. Bone RC, Grodzin CI, Balk RA. Sepsis: a new hypothesis tor pathogenesis of the disease process. Chest 1997; 112: 235-243
17. Bone RC. Sepsis SIRS and CARS. Crit Care Med 1996; 24: 1125-1128
18. Dinarello CA. Proinflammatory and anti-inflammatory cytokines as mediators in the pathogenesis of septic shock. Chest 1997; 112: 321S-329S
19. Chabot F, Mitchell JA, Guueridge JM, Evans TW. Reactive oxygen species in acute lung injury. Eur Resp J 1998; 11: 745-757
20. Annane D. Replacement therapy with hydrocortisone in catecholamine-dependenset ptic shock. J Endotoxin Res 2001;7:305-309
21. Anel RL, Kumar A. Experimental and emerging therapies fur sepsis and septic shock. Expert Opin Investig Drugs 2001; 10: 1471-1485
22. Bernard GR, Wheeler AP, Russell JA, Schein R, Summer WR, Steinberg KP et al. The effects of ibuprofen on the physiology and survival of patients with sepsis. The Ibuprofen in Sepsis Study Group. N Engl J Med 1997; 336: 912-918
23. Vilaseca J, Salas A, Guamer F, Rodriguez R, Malagelada JR. Participation of thromboxane and other eicosanoid synthesis in the courseo f experimentailn flarumatoryc olitis. Gastroenterology! 990; 98: 269-277
24. Belluzzi A, Brignola C, Campieri M, Pera A, Boschi S, Miglioli M et al. Effect of an enteric-coated fish oil preparation on relapses in Crohn's disease. N Engl J Med 1996; 334: 1557-1560
25. Vand er Heide JJH, B ilo HJG.D onkerj M, Wilmink JM, TegzesAs M. Effect of dietary fish oil on renal function and rejection in cyclosporine-treatedre cipients of renal transplants.N Engl J Med 1993; 329: 769-773
26. Suter PM, Ricou B. Cytokines and lung injury. Update in Intensive Care and Emergency Medicine 1998; 30: 41-53
27. Quinlan GJ, Lamb N, TiHey R, Evans TM, Gutteridge JMC. Plasma hypoxantine levels in ARDS: implications fur morbidity and mortality. Am J Respir Crit Care Med 1997; 155:479-484
28. Connelly KG, RepineJ E. Markers fur predictingt he developmenot f acuter espiratoryd istresss yndrome A. nnu RevM ed 1997; 48: 429-445
29. Grimrninger F, Wahn H, Mayer K, Kiss L, Walmrath D, Bahkdi S, SeegerW . Arachidonic acid increases, h ut eicosapentaenoica cid decreasese xotoxin induced lung vascular leakage-relation to 4-series versus 5-series leukotriene generation. Am J Respir Crit Care Med 1997; 155: 513-519
30. Grimrninger F, Mayer K, Kramer H-J, Stevens J , Walmrath D , Seeger W. Differential vasoconstrictor potencies of free fatty acids in the lung vasculature: 2- versus 3-series prostanoid generation. J Pharmacol Exp Ther 1993; 267: 259-265
31. Grimrninger F, Wahn H, Kramer HJ, Stevens J, Mayer K, Walmrath D, Seeger W. Differential influence of arachidonic vs. eicosapentaenoiacc id on experimentapl ulmonaryh ypertension. A m J Physioll995; 268 (6 Pt 2): H2252-H2259
32. Grimrninge'r F, Mayer K, Kiss L Wahn H, Walmrath D, Bakhdi S et al. Synthesis of 4- and 5-series leukotrienes in the lung rnicrovasculature challenged with Escherichia coli hemolysin: Critical dependenceo n exogenousfr ее fatty acids upply. A m J Respir Biol Cell Mol 1997; 16: 317-324
Опубликовано в журнале:
«CLINICAL NUTRITION»; 2009, 28: 359-479.
Приложение V. Рекомендации европейского общества клинического питания и метаболизма (ESPEN) 2009
Хирургия
Методические рекомендации Европейского Общества Парентерального и Энтерального Питания по применению парентерального питания в хирургии.
М. Брага,О. Люнгквист, П. Сотерс, К. Фирон, А. Вейманн, Ф. Бочетти
В оптимальный состав парентерального питания, по-видимому, должны входить n-3-жирные кислоты (Класс С). В течение многих лет стандартные жировые эмульсии имели своей основой соевое масло, в котором в большом количестве находятся n-6-ПНЖК. Однако n-6-ПНЖК обладают провоспалительным действием, и в исследованиях была отмечена тенденция к снижению частоты осложнений у пациентов, получающих парентеральное питание, в котором содержание этих жирных кислот снижено. При включении в парентеральное питание n-З -жирных кислот происходило снижение выраженности физиологической реакции на эндотоксин у здоровых индивидуумов. В открытых когортных исследованиях при применении n-3-ПНЖК в возрастающих количествах отмечалось уменьшение длительности пребывания в стационаре после проведения обширных оперативных вмешательств на органах брюшной полости, а в рандомизированном исследовании при включении в парентеральное питание n-3-ПНЖК наблюдалось уменьшение общей длительности пребывания в стационаре.140 Таким образом, в настоящее время имеются данные, указывающие на то, что включение в парентеральное питание n-З -жирных кислот может положительно влиять на функцию органов и способствовать снижению длительности госпитализации пациентов, перенесших обширные операции или пациентов, поступающих в ОРИТ хирургического профиля.
Интенсивная терапия (ОРИТ)
Методические рекомендации Европейского Общества Парентерального и Энтерального Питания по применению парентерального питания в интенсивной терапии.
Пьер Сингер, Мэттэ М. Бергер, Грит Ван дер Берг, Джанни Биоло, Филипп Кальдер, Алистер Форбс, Ричард Гриффитс, Георг Крейман, Ксавье Левёрв, Клод Пишар
Жировые эмульсии должны быть неотъемлемой частью ПП, являясь источником энергии, а для пациентов, находящихся в ОРИТ в течение длительного времени, -источником незаменимых жирных кислот. (Класс В). Классификация жирных кислот основывается на характеристиках их структуры, включающих длину углеродной цепи, наличие и положение двойных связей в цепи и их конфигурацию (то есть цис- или транс-). В общем виде их можно разделить на насыщенные (нет двойных связей) и ненасыщенные (одна или более двойная связь); последние подразделяют на мононенасыщенные (одна двойная связь) и полиненасыщенные (две или более двойных связи). В зависимости от длины цепи жирные кислоты разделяют на короткоцепочечные (<8 атомов углерода), среднецепочечные (8-14 атомов углерода) и длинноцепочечные (16 или более атомов углерода). Жирные кислоты, цепь которых состоит из 20 или более атомов углерода, иногда называют жирными кислотами с очень длинной цепью. По положению двойной связи в углеродной цепи, как правило, выделяют три семейства: омега-3, омега-6 и омега-9 (которые также обозначают n-З, n-6 и n-9). Цифра обозначает положение двойной связи по отношению к метальной группе, расположенной на конце цепи. Жирные кислоты выполняют множество различных функций, включающих обеспечение энергией, участие в формировании структуры и физических свойств клеточной мембраны, регуляцию клеточных реакций, в том числе и экспрессию генов, также они являются предшественниками биоактивных липидных метаболитов, таких как простагландины. В человеческом организме может синтезироваться большинство жирных кислот, за исключением двух (линолевая кислота - омега-6-жирная кислота, состоящая из 18 атомов углерода, и альфа-линоленовая кислота - омега-3-жирная кислота, также состоящая из 18 атомов углерода). Эти жирные кислоты должны поступать в организм человека извне; их называют незаменимыми жирными кислотами. Типичный пациент ОРИТ должен получать линолевую кислоту в количестве 9-12 г/сут и альфа-линоленовую кислоту в количестве 1-3 г/сут. Незаменимые жирные кислоты синтезируются в растениях и содержатся в большом количестве в растительных маслах (например, в подсолнечном, кукурузном и соевом масле). В процессе их метаболизма образуются менее насыщенные длинноцепочечные жирные кислоты, имеющие очень большое значение, такие как арахидоновая кислота (омега-6), эйкозопентаеновая кислота (ЭПК) и докозогексаеновая кислота (ДГК) (обе они - омега-3). Рыбий жир содержит ЭПК и ДГК. Оливковое масло содержит олеиновую кислоту, являющуюся омега-9-мононенасыщенной кислотой.
Внутривенно вводимые липиды являются неотъемлемой частью растворов для ПП типа «три в одном», в которых они выполняют роль источника энергии и незаменимых жирных кислот, необходимых для пациента, находящегося в ОРИТ в течение длительного времени. Применение липидов позволяет снизить количество вводимых углеводов, что облегчает контроль уровня глюкозы. При введении в количестве 1-2 г/кг/сут жировые эмульсии безопасны, хорошо переносятся и обеспечивают дополнительную энергию (например, 10 ккал/кг/сут). Aberg с сотр. провели оценку изменений метаболизма (методом гипертриглицеридемического клэмпа) и термогенеза (с помощью непрямой калориметрии) при введении экзогенных жиров в зависимости от возраста (пациенты молодого возраста и пожилые пациенты). Введение жиров обусловливало увеличение расхода энергии на 6-9%. Во время введения окисление жиров возрастало на 15-24% по сравнению с исходным состоянием. При этом отмечалось увеличение активности липопротеинлипазы (в 4-5 раз). Тарру с сотр. показали, что введение липидов приводило к снижению фракционного липогенеза de novo при сравнении с ПП на основе глюкозы, вызывало сравнительно менее выраженное увеличение (7% по сравнению с 26%) уровня глюкозы, уровня инсулина (40% по сравнению с 284%) и не обусловливало увеличения продукции С02, в то время как парентеральное питание на основе глюкозы приводило к ее увеличению на 15%. Липиды не подавляли эндогенное образование глюкозы и общее окисление белка. Эта же группа исследователей также обнаружила, что использование омега-3-жирных кислот было сопряжено со снижением расхода энергии. Уровни окисления глюкозы и липидов были одинаковыми, независимо от того вводились ли n-6-липиды или n-З-липиды. В другой работе сравнивалось применение питания на основе оливкового масла с применением ПП на основе глюкозы у пациентов с множественной травмой. В ней было обнаружено, что ПП на основе оливкового масла было таким же безопасным и эффективным, как и ПП на основе глюкозы. При использовании жировых эмульсий на основе оливкового масла уровень глюкозы крови был ниже.
Жирные кислоты могут оказывать влияние на воспалительные и иммунные процессы путем воздействия на структуру клеточных мембран и их функционирование, модификации профиля воспалительных медиаторов и изменения экспрессии генов. Таким образом, вид и качественные характеристики липидов, применяемых у пациентов в критическом состоянии, могут иметь большое значение для клинического исхода. В целом считается, что омега-3 жирные кислоты обладают менее выраженным провоспалительным действием, и, возможно, оказывают противовоспалительное действие. Омега-3-жирные кислоты могут противодействовать эффектам омега-6-жирных кислот, стимулирующим воспалительные процессы (арахидоновая кислота является субстратом для синтеза провоспалительных эйкозаноидов).
Добавление эйкозопентаеновой и докозогексаеновой кислоты к жировым эмульсиям оказывает заметное влияние на состояние клеточных мембран и воспалительные процессы (Класс В). Применение жировых эмульсий на основе рыбьего жира, по-видимому, способствует снижению длительности госпитализации пациентов, находящихся в критических состояниях (Класс В). Внутривенное введение эмульсии рыбьего жира, содержащей ЭПК и ДГК, приводит к возрастанию содержания этих кислот и уменьшению содержания арахидоновой кислоты в составе клеточных мембран, обусловливая снижение синтеза провоспалительных эйкозаноидов и цитокинов, включая ФНО-альфа, интерлейкин-6 и интерлейкин-8. Рыбий жир способствует снижению выраженности стрессовой реакции на внутривенное введение эндотоксина. Внутривенное введение эмульсии на основе рыбьего жира после абдоминальных хирургических вмешательств обусловливало снижение уровня ФНО-альфа и интерлейкина-6 в отличие от жировых эмульсий на основе LCT/MCT. Механизмы действия эмульсии на основе рыбьего жира были описаны недавно. В многоцентровом неслепом исследовании, посвященном изучению эффектов эмульсии на основе рыбьего жира, вводимой в различных дозах, в котором приняли участие 661 пациент (количество баллов по шкале SAPS II 32), было показано, что дополнительное внутривенное введение эмульсии рыбьего жира в количестве от 0,1 до 0,2 г/кг/сут оказывало положительное влияние на выживаемость, частоту инфекционных осложнений, потребность в антибиотиках и длительность госпитализации. Наиболее выраженный эффект наблюдался при абдоминальном сепсисе, при котором также отмечалось снижение расхода энергии в покое. Каких-либо других доступных определению изменений отмечено не было. Wichmann с сотр. провели рандомизированное исследование, в котором пациенты были распределены в группу, 5 дней получавшую ПП с эмульсией соевого масла, и в группу, получавшую жировую эмульсию на основе смеси LCT/MCT/рыбьего жира. Во второй группе наблюдалось значительное увеличение продукции ЭПК, LTB5 и антиоксидантов, а длительность госпитализации была достоверно ниже (17,2 сут по сравнению с 21,9 сут, р=0,006). Применение жировой эмульсии на основе рыбьего жира в парентеральном питании при тяжелом панкреатите также приводило к снижению выраженности воспалительной реакции и улучшению функции дыхания. В то же время, Friesecke с сотр.105 опубликовали данные о том, что применение жировой эмульсии на основе смеси LCT/MCT/рыбьего жира у пациентов ОРИТ, находящихся в критических состояниях, не оказывало влияния на уровень маркеров воспаления и на клинические исходы, включающие частоту инфекционных осложнений, потребность в ИВЛ и продолжительность пребывания в ОРИТ и в стационаре при сравнении с применением жировой эмульсии на основе LCT/MCT, не содержащей рыбьего жира. Авторы недавно опубликованного обзора эффектов включения рыбьего жира в парентеральное питание у пациентов ОРИТ пришли к заключению, что если рассматривать объединенные результаты исследований Heller, Wichmann, Тарру Wang и Friesecke, то можно сделать вывод, что длительность госпитализации достоверно снижается. В отношении смертности достоверных изменений отмечено не было. В дополнение к вышеприведенным данным, свидетельствующим в пользу включения рыбьего жира в жировые эмульсии, имеется ряд данных, подтверждающих его благоприятное действие на фармакологические свойства таких смесей. В двух исследованиях были использованы смешанные жировые эмульсии: в одном у здоровых добровольцев, в другом - у пациентов ОРИТ. В обеих работах в качестве контроля использовалась эмульсия соевого масла (LCT). Как было показано, смешанные жировые эмульсии превосходили эмульсию на основе LCT по скорости элиминации и переносимости у здоровых добровольцев и обеспечивали лучший антиоксидантный статус у пациентов ОРИТ, находящихся в стрессовом состоянии.
Заболевания поджелудочной железы
Методические рекомендации Европейского Общества Парентерального и Энтерального Питания по применению парентерального питания при заболеваниях поджелудочной железы.
Л. Джанотти, Р. Майер, Д. Н. Лобо, С. Басси, С. X. С. Дейонг, Дж. Окенга, О. Иртен, Дж. МакФай
В одном рандомизированном двойном слепом исследовании, проведенном Wang с сотр. (N=40), было отмечено, что у индивидуумов, получавших эмульсию рыбьего жира, были ниже выраженность воспалительной реакции, потребность в почечной заместительной терапии и отмечалось улучшение дыхательной функции, при сравнении с пациентами, получавшими жировую эмульсию на основе соевого масла (Wang, 2008). Необходимо проведение более крупных исследований, чтобы подтвердить эти предварительные результаты.
Гепатология
Методические рекомендации Европейского Общества Парентерального и Энтерального Питания по применению парентерального питания в гепатологии.
Матиас Плаот, Эдуард Кабре, Бернар Кампилло, Йенс Кондруп, Джулио Марчесини, Татьяна Шутц, Алан Шенкин, Джулия Уендон
При алкогольном стеатогепатите следует использовать жировые эмульсии, в которых n-6 ненасыщенные жирные кислоты содержатся в меньшем количестве, чем в традиционных жировых эмульсиях на основе соевого масла. Они должны покрывать 40-50% потребности в небелковой энергии (С). При сравнении с традиционными эмульсиями длинноцепочечных триглицеридов на основе соевого масла (n-6:n-3=8:1) новые жировые эмульсии имеют сниженное содержание n-6-ненасыщенных жирных кислот в связи с добавлением среднецепочечных триглицеридов (МСТ) и/или оливкового масла и/или рыбьего жира, что способствует снижению их угнетающего действия на лейкоциты и иммунную функцию и стимулирующего действия на продукцию провоспалительных иммуномодуляторов.
При циррозе печени следует использовать жировые эмульсии, в которых содержание n-6-ненасыщенных кислот ниже, чем в традиционных жировых эмульсиях на основе соевого масла. Жировые эмульсии должны удовлетворять 40-50% потребности в небелковой энергии (С). По сравнению с традиционными эмульсиями длинноцепочечных триглицеридов на основе соевого масла (n-6:n-3=8:1) новые жировые эмульсии содержат меньшее количество n-6-ненасыщенных жирных кислот из-за добавления среднецепочечных триглицеридов и/или оливкового масла и/или рыбьего жира, что способствует снижению их угнетающего действия на лейкоциты и иммунную функцию, и стимулирующего провоспалительного действия.
Онкология
Методические рекомендации Европейского Общества Парентерального и Энтерального Питания по применению парентерального питания у пациентов с нехирургическими онкологическими заболеваниями.
Ф. Бочетти, Дж. Арендc, К. Лундхольм, А. Майклрайт, Г. Цурхер, М. Мускаритоли
Анализ патофизиологических и клинических данных свидетельствует о том, что увеличение доли липидов в парентеральном питании (онкологических больных) (например, обеспечение 50% небелковой энергии липидами) оказывает положительное действие (Класс С). Simoens с сотр.78 провели исследование, посвященное сравнению клиренса триглицеридов жировой эмульсии (5:4:1), в которой массовая доля МСТ составляла 50%, доля LCT - 40% и доля триглицеридов рыбьего жира - 10%, и клиренса контрольной жировой эмульсии (5:5), в которой доля МСТ и LCT составляли по 50% каждая. Добавление 10% рыбьего жира в смешанную эмульсию способствовало увеличению клиренса плазмы от введенных триглицеридов (18%,p=0,0001).
Опыт парентерального применения эйкозопентаеновой кислоты (ЭПК) ограничен использованием ее у пациентов в периоперационном периоде. Ее краткосрочное применение было безопасным в отношении гемостаза, приводило к прогнозируемым изменениям состава эйкозаноидов, способствовало улучшению функции печени и поджелудочной железы, снижению выраженности иммунносупрессии, вызванной проведением в послеоперационном периоде химио- и лучевой терапии. Также в недавно проведенном рандимизированном клиническом исследовании, посвященном сравнению использования жировой эмульсии, содержащей рыбий жир, и стандартной жировой эмульсии на основе соевого масла, была отмечена достоверно меньшая длительность пребывания в стационаре при проведении ПП, включающего рыбий жир.
Комментарии
ПРАКТИКА ПЕДИАТРА
