Влияние показателей диастолической функции левого и правого желудочка на годовой прогноз больных после первичного ЧКВ при ИМпST
СтатьиСумин А. Н., Галимзянов Д. М., Сергеева Т. Ю., Барбараш О. Л.
ФГБУ «НИИ КПССЗ» СО РАМН, 650002, Кемерово, Сосновый бульвар, д. 6 Ключевые слова: диастолическая дисфункция левого желудочка, диастолическая дисфункция правого желудочка, инфаркт миокарда, прогноз, чрескожное коронарное вмешательство
Keywords: diastolic dysfunction of the left ventricle, diastolic dysfunction of the right ventricle, myocardial infarction, prognosis, transcutaneous coronary intervention
Ссылка на эту статью: Сумин А. Н., Галимзянов Д. М., Сергеева Т. Ю. и др. Влияние показателей диастолической функции левого и правого желудочка на годовой прогноз больных после первичного ЧКВ при ИМпST. Журнал Сердечная Недостаточность. 2014;82 (1):14–22.
Резюме
Актуальность. Долгосрочный прогноз у больных после ИМ с подъемом сегмента ST (ИМпST) определяется как клиническими факторами, так и показателями систолической и диастолической функции ЛЖ. Первичное чрескожное коронарное вмешательство (ЧКВ) у больных ИМпST существенно улучшает как результаты госпитального этапа лечения, так и отдаленные результаты, что может изменить относительный вклад различных прогностических факторов. Цель. Оценить прогностическое значение как показателей диастолической функции ПЖ и ЛЖ, так и других клинических и ЭхоКГ параметров после проведения первичного ЧКВ у больных ИМпST. Материалы и методы. В исследование было включены 79 больных ИМпST после первичного ЧКВ со стентированием инфаркт-связанной артерии. ЭхоКГ выполнялась в 1-е и 12-е сутки заболевания с оценкой показателей систолической и диастолической функции желудочков. В течение года летальный исход зафиксирован у 1 больного, повторный ИМ – у 15, инсульт – у 3, повторные реваскуляризации – у 11. Отсутствовали сердечно-сосудистые события у 46 больных, имелись – у 23. Эти группы больных были сопоставлены по клинико-анамнестическим, лабораторным показателям и параметрам внутрисердечной гемодинамики на 1-й и 12-й дни заболевания. Результаты. Группы различались по длительности АГ (р=0,042) и наличию многососудистого поражения коронарных артерий (р=0,034). На 12-й день заболевания в группе неблагоприятного прогноза отмечено повышение отношения ЕМ / еМ (р=0,051), снижение еМ (р=0,084), а также увеличение ВИРПЖ (р=0,0039). Корреляцию с неблагоприятным прогнозом имели следующие факторы: курение (р=0,040), длительность АГ (р=0,024), многососудистое поражение коронарных артерий (р=0,035), динамика показателя ВЗЕМ в ходе стационарного лечения (р=0,009). При многофакторном анализе только ВЗЕМ коррелировал с неблагоприятным прогнозом (р=0,038). Заключение. Неблагоприятный прогноз в течение года после ЧКВ у больных ИМпST был связан с числом пораженных коронарных артерий, длительностью АГ и динамикой показателя ВЗЕМ в ходе стационарного лечения. Первичное ЧКВ у больных ИМпST не только улучшает годичный прогноз, но и модерирует прогностическое значение ЭхоКГ показателей у данной категории пациентов.
Summary
Background. Log-term prognosis for patients who have had ST elevation myocardial infarction (STEMI) is determined by both clinical factors and parameters of LV systolic and diastolic function. In patients with STEMI, primary transcutaneous intervention (TCI) significantly improves both the response to hospital treatment and the remote outcome, which may change relative contributions of various predictive factors. Aim. To evaluate the predictive value of RV and LV diastolic function and other clinical and EchoCG parameters following a primary TCI in patients with STEMI. Materials and methods. The study included 79 patients with STEMI after a primary TCI with stenting of the infarct-related artery. EchoCG was recorded at 1 and 12 days of disease with evaluation of ventricular systolic and diastolic function. Over one year, one patient had a fatal outcome, 15 patients had recurrent MI, 3 patients had stroke, and 11 patients had repeated revascularization. 46 patients did not and 23 patients had cardiovascular events. These groups of patients were compared by clinical and historical data, laboratory data, and parameters of intracardiac hemodynamics at 1 and 12 days of disease. Results. The groups differed in duration of arterial hypertension (AH) (р=0.042) and presence of multi-vessel coronary disease (р=0.034). At 12 days, the group of unfavorable prognosis had increased Еm / еm ratio (р=0.051), reduced еm (р=0.084), and increased RV isovolumetric relaxation time (IRT) (р=0.0039). The following factors correlated with the unfavorable prognosis: smoking (р=0.040), AH duration (р=0.024), multi-vessel coronary artery disease (р=0.035), and changes in the Em deceleration time (DT) during the hospital treatment (р=0.009). Multifactorial analysis showed that only Em DT correlated with the unfavorable prognosis (р=0.038). Conclusion. The one-year unfavorable prognosis in patients with STEMI correlated with the number of affected coronary arteries, AH duration, and changes in Em DT during the hospital treatment. Primary TCI not only improved the one-year prognosis in patients with STEMI but also moderated the predictive value of EchoCG parameters in these patients.
Долгосрочный прогноз у больных после ИМ определяется как клиническими факторами, так и показателями систолической [1, 2] и диастолической функции ЛЖ [3] по данным ЭхоКГ. В работах последнего времени было показано, что показатели наполнения левых отделов сердца могут быть более чувствительными в этом плане, чем параметры насосной функции сердца [4], в частности, при нормальной ФВ ЛЖ. Кроме того, функция ПЖ может иметь прогностическое значение при наличии левожелудочковой дисфункции [5–7], в том числе и у больных ИМ [8, 9]. Следует отметить, что прогностические критерии после ИМ с подъемом сегмента ST (ИМпST) преимущественно основываются на больных, получавших тромболитичскую терапию. Первичное чрескожное коронарное вмешательство (ЧКВ) у больных ИМпST существенно улучшает как результаты госпитального этапа лечения, так и отдаленные результаты, что может изменить относительный вклад различных прогностических факторов [10]. Поскольку после первичной ЧКВ при ИМпST ухудшение состояния ЛЖ может быть минимальным, каково будет в этом случае прогностическое значение функционального состояния ПЖ остается неясным, там более, что эти параметры имеют неодинаковую динамику в ходе стационарного этапа лечения [11]. Данные соображения и послужили предпосылкой для проведения настоящего исследования, целью которого было оценить прогностическое значение как показателей диастолической функции ПЖ и ЛЖ, так и других клинических и ЭхоКГ параметров у больных с ИМпST после проведения первичного ЧКВ.
Материалы и методы
Работа выполнена в соответствии с Хельсинкской деклаpацией, протокол исследования утвержден локальным этическим комитетом, все пациенты подписали добровольное информированное согласие на участие в исследовании. В исследование (его дизайн представлен на рисунке 1) были включены 73 больных с острым ИМ с элевацией сегмента ST на ЭКГ после первичного ЧКВ со стентированием инфаркт-связанной артерии. Диагноз ИМ был выставлен в соответствии с рекомендациями ВНОК по диагностике и лечению больных острым ИМ с подъемом сегмента ST на ЭКГ. Критериями включения являлись: длительность заболевания от начала болевого синдрома до поступления в стационар до 24 часов, наличие адекватного ультразвукового акустического окна, синусового ритма, восстановление кровотока до уровня TIMI III в инфаркт-связанной артерии после ЧКВ. В исследование не включались пациенты с ранее перенесенным ИМ, с нарушением атрио-вентрикулярной проводимости, с клапанными пороками, при наличии митральной регургитации более 2 степени, с блокадой левой ножки пучка Гиса.
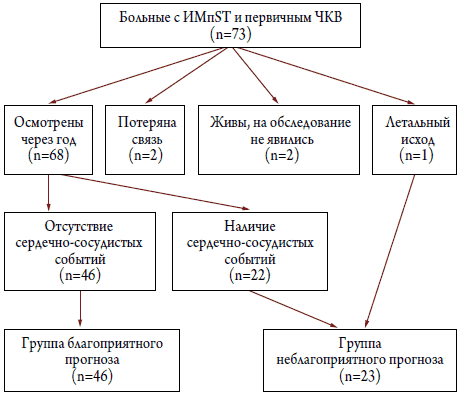
Рисунок 1. Дизайн исследования
Через год больные обследованы повторно, оценили встречаемость конечных точек (летального исхода, повторного ИМ, инсульта, повторной реваскуляризации миокарда). Через год контрольное обследование прошли 69 человек. Умер 1 больной. С двумя пациентами не удалось связаться. Один пациент не явился на обследование (причина неизвестна). Больных, перенесших ИМ, было 15, инсульт развился у 3 пациентов. Повторные реваскуляризации выполнены у 11 больных (в 10 случаях – ЧКВ, в 1– АКШ). Отсутствовали сердечно-сосудистые события в течение года у 46 больных – они составили группу с благоприятным прогнозом. Хотя бы одно сердечнососудистое событие в течение года отмечалось у 23 больных, они составили группу с неблагоприятным прогнозом после перенесенного ЧКВ при ИМпST. Группы с неблагоприятным и благоприятным прогнозом были сопоставлены по клинико-анамнестическим, лабораторным показателям и параметрам внутрисердечной гемодинамики на 1-й и 12-й дни заболевания.
Эхокардиография выполнялась в 1-е сутки (через 20–24 ч от начала заболевания) и 12-е сутки заболевания на ультразвуковой системе «ALOKA ALPHA 10 ProSound» (Япония) с использованием датчика 2–4 МГц. Исследования выполнялись в положении пациента на левом боку, изучаемые показатели регистрировались в конце нефорсированного выдоха. Оценивались средние значения, полученные при регистрации не менее 3-х кардиоциклов для каждого измерения. В М-режиме измерялись конечно-диастолический (КДР) и конечно-систолический (КСР) размеры ЛЖ и ПЖ, переднезадний размер левого предсердия (ЛП), расчитывали фракцию передне-заднего укорочения ПЖ (ФУ ПЖ).
В режиме двухмерной ЭхоКГ определяли продольный размер полости ЛЖ в диастолу (LЛЖ–Д) и систолу (LЛЖ–С), поперечный (ПП1) и продольный (ПП2) размеры правого предсердия. Конечно-диастолический объем (КДОЛЖ), конечно-систолический объем (КСОЛЖ), ФВ ЛЖ были вычислены с применением алгоритма Simpson. Диастолический индекс сферичности (ИСФД) ЛЖ вычислялся как отношение поперечного размера к его продольному размеру в диастолу, интегральный систолический индекс ремоделирования (ИСИР) рассчитывали по формуле: ИСИР=ФВ ЛЖ / ИСФД
В импульсном допплеровском режиме оценивали параметры трансмитрального и транстрикуспидального кровотоков: максимальную скорость раннего трансмитрального (ЕМ) и транстрикуспидального (ЕТ) потоков; максимальную скорость потока систолы левого (АМ) и правого (АТ) предсердий; отношений ЕМ / АМ, ЕТ / АТ; время изоволюмической релаксации ЛЖ (ВИРЛЖ); время замедления скорости раннего трансмитрального (ВЗЕМ) и транстрикуспидального (ВЗЕТ). Дополнительно оценивалась скорость распространения раннедиастолического потока в полости ЛЖ (СРМП) и ПЖ (СРТП) с расчетом отношения ЕМ / СРМП и ЕТ / СРТП. СРМП и СРТП определяли в комбинированном цветном допплеровском М-режиме, располагая курсор М-режима по центру цветового паттерна потока наполнения, максимально параллельно его направлению. Скорость распространения измерялась по углу наклона фронта цветовой волны на участке от атрио-вентрикулярного клапана до точки, расположенной на удалении 4 см по направлению к верхушке желудочка. В режиме тканевой допплерографии измеряли максимальную скорость движения фиброзных колец митрального (еМ) и трикуспидального (еТ) клапанов в фазу раннего наполнения и фазу предсердной систолы (аМ, аТ), время изоволюмической релаксации ЛЖ (ВИРЛЖ–ТД), рассчитывали отношение еМ / аМ, еТ / аТ , ЕМ / еМ, ЕТ / еТ.
Статистическая обработка проводилась с использованием пакета Statistica 8.0. Нормальность распределения проверялась с помощью критерия Колмогорова–Смирнова. Поскольку для большинства количественных переменных распределение отличалось от нормального, данные представлены в виде медианы и верхнего и нижнего квартилей (Me [LQ, UQ]). Оценка достоверности различий между группами с разным прогнозом проводилась с использованием критерия Манна–Уитни. Для оценки влияния различных факторов на годовой прогноз проводили однофакторный дисперсионный анализ. В многофакторный анализ включались переменные, для которых критерий статистической значимости при однофакторном анализе составлял меньше 0,1. Многофакторный анализ выполнялся методом пошагового включения. Первоначально выделялся признак, наиболее тесно связанный с изучаемым исходом. Включение последующих переменных происходило только в случае, если их добавление к уже отобранным факторам демонстрировало значимость вклада на уровне ??0,1. Различия считались достоверными при р<0,05.
Результаты
При сопоставлении клинико-анамнестических данных (табл. 1) можно отметить, что существенные различия между группами были только по двум показателям: длительности анамнеза АГ (10 лет при неблагоприятном годовом прогнозе и 5 лет – при благоприятном,; р=0,042) и наличию многососудистого поражения коронарных артерий (73,9 и 43,4 % соответственно, р=0,034). Также отмечалась тенденция к меньшей частоте приема β-АБ в группе с неблагоприятным прогнозом (91,3 %) по сравнению с группой благоприятного прогноза (100 %, р=0,080). В остальном различий между группами в терапии госпитального этапа не отмечалось. Число курящих пациентов было несколько меньше в группе с неблагоприятным прогнозом (р=0,045), что, вероятно, связано с тем, что в этой группе было больше женщин.
Таблица 1. Клинико-лабораторные данные госпитального периода у больных с благоприятным и неблагоприятным годовым прогнозом после ЧКВ в рамках ОКСпST
| Показатели | Группа благоприятного прогноза (n=46) | Группа неблагоприятного прогноза (n=23) | p |
| Мужской пол | 39 (84,7 %) | 15 (65,2 %) | 0,251 |
| Возраст (лет) | 58,0 (50,0; 62,0) | 55,0 (50,5; 62,0) | 0,651 |
| Артериальная гипертензия | 34 (73,9 %) | 20 (86,9 %) | 0,421 |
| Анамнез артериальной гипертензии (лет) | 5,0 (1,0; 10,0) | 10,0 (3,0; 15,0) | 0,042 |
| Сахарный диабет | 11 (23,9 %) | 6 (26 %) | 0,814 |
| Хроническая обструктивная болезнь легких | 7 (15,2 %) | 2 (8,69 %) | 0,725 |
| Курение | 29 (63 %) | 8 (34,7 %) | 0,045 |
| Время от начала симптомов до восстановления кровотока в КА (мин) | 90 (30; 180) | 75,0 (30,0;210,0) | 0,736 |
| Класс СН по Killip ≥2 | 2 (4,3 %) | 1 (4,34 %) | 0,754 |
| Многососудистое поражение КА (≥2) | 20 (43,4 %) | 17 (73,9 %) | 0,034 |
| Стеноз ствола левой КА | 5 (10,8 %) | 1 (4,34 %) | 0,098 |
| Передний ИМ | 31 (67,3 %) | 12 (52 %) | 0,221 |
| Нижний ИМ | 21 (45,6 %) | 12 (52 %) | 0,513 |
| Максимальный уровень КФК-МВ (МЕ / л) | 64,7 (22,0; 143,0) | 48,5 (18,4; 123) | 0,675 |
| Аневризма ЛЖ | 3 (6,5 %) | 1 (4,34 %) | 0,251 |
| Регургитация на митральном клапане ≥2 | 2 (4,34 %) | 1 (4,34 %) | 0,569 |
| Прием β-АБ | 46 (100 %) | 21 (91,3 %) | 0,080 |
| Прием ингибиторов АПФ | 36 (78,2 %) | 17 (73,9 %) | 0,608 |
| Прием кордарона | 0 | 1 (4,34 %) | 0,221 |
| Прием ACa2+ | 36 (78,2 %) | 19 (82,6 %) | 0,785 |
| Прием статинов | 36 (78,2 %) | 18 (78,2 %) | 0,895 |
| Прием диуретиков | 19 (41,3 %) | 10 (43,4 %) | 0,826 |
| Общий ХС (ммоль / л) | 5,72 (4,53; 6,5) | 5,38 (4,74; 5,93) | 0,636 |
| Триглицериды (ммоль / л) | 2,25 (1,63; 2,54) | 2,70 (1,47;3,76) | 0,697 |
| Холестерин ЛПНП (ммоль / л) | 3,40 (2,52; 4,07) | 3,05 (2,5; 3,74) | 0,584 |
| Холестерин ЛПВП (ммоль / л) | 1,29 (0,99; 1,37) | 1,17 (0,97; 1,31) | 0,516 |
| Индекс атерогенности (ммоль / л) | 4,18 (3,05; 4,55) | 3,83 (3,2; 5,0) | 0,898 |
По локализации ИМ, времени от начала симптомов до восстановления коронарного кровотока группы достоверно не различались. По выраженности СН, оцениваемой по классификации Killip, группы не различались между собой, причем у подавляющего числа больных она была не выше 1 класса. Стеноз ствола левой коронарной артерии (ЛКА) несколько чаще встречался в группе с благоприятным прогнозом, но это различие было статистически незначимым. Лабораторные показатели в группах также не различались.
Показатели диастолической функции ЛЖ в 1-е сутки заболевания в группах были сопоставимы (табл. 2). К 12-му дню заболевания отмечены следующие различия между группами: при неблагоприятном годовом прогнозе отмечено повышение отношения ЕМ / еМ (р=0,051), сопровождающееся снижением еМ (р=0,084) по сравнению с группой благоприятного прогноза. Эти различия можно, по-видимому, объяснить повышением давления в полости ЛЖ у больных с неблагоприятным прогнозом [12]. Хотя межгрупповых различий показателя ВЗЕ не отмечалось ни в первый, ни на 12-й дни заболевания; прирост этого показателя был заметно выше в группе неблагоприятного прогноза (на 22 %), чем в группе благоприятного прогноза (на 4,7 %) (табл. 2).
Таблица 2. Показатели диастолической функции ЛЖ в 1-е и 12-е сутки заболевания в группах с различным годовым прогнозом после ЧКВ у больных ИМпST
| Показатели | Группа благоприятного прогноза (n=46) | Группа неблагоприятного прогноза (n=23) | p1 | p2 | ||
| 1-й день | 12-й день | 1-й день | 12-й день | |||
| ЕМ, см / с | 55,1 (44; 62) | 61,9 (49; 73) | 57,2 (47; 65) | 60,5 (50; 70) | 0,322 | 0,845 |
| АМ, см / с | 59,7 (49; 68,5) | 61,0 (48; 70,6) | 60,4 (45; 73) | 63,8 (47; 76) | 0,909 | 0,815 |
| ЕМ / АМ | 0,98 (0,71; 1,16) | 1,12 (0,71; 1,42) | 1,02 (0,71; 1,25) | 1,01 (0,75; 1,15) | 0,733 | 0,550 |
| ВИРЛЖ, мс | 90,6 (72; 108) | 85,9 (66; 90) | 90,9 (78; 102) | 84,5 (72; 102) | 0,836 | 0,341 |
| ВЗЕМ, мс | 155,1 (126; 180) | 162,4 (138; 192) | 144,2 (120; 156) | 176 (144; 192) | 0,156 | 0,169 |
| eМ, см / с | 7,49 (6; 9,3) | 8,75 (6,9; 10,1) | 7,43 (6,1; 8,7) | 7,99 (6,0; 8,6) | 0,723 | 0,084 |
| aМ, см / с | 9,45 (7,9; 10,5) | 9,57 (8,3; 11,2) | 9,39 (7,9; 10,6) | 8,76 (8,0; 9,6) | 0,875 | 0,192 |
| еМ / аМ | 0,83 (0,57; 0,94) | 0,97 (0,73; 1,20) | 0,83 (0,62; 1,01) | 0,98 (0,68; 1,12) | 0,643 | 0,479 |
| ВИРЛЖ–ТД , м с | 79,3 (72; 90) | 78,2 (66; 90) | 82,1 (66; 96) | 77,3 (66; 90) | 0,870 | 0,926 |
| ЕМ / еМ | 7,83 (6,54; 9,19) | 7,4 (6,57; 8,80) | 8,28 (6,15; 8,87) | 8,14 (7,50; 10,83) | 0,802 | 0,051 |
| СРМП, см / с | 39,8 (31; 46,3) | 39,5 (33; 43,6) | 43,2 (38; 48) | 42,9 (37,9; 47,5) | 0,119 | 0,199 |
| ЕМ / СРМП | 1,43 (1,16; 1,64) | 1,63 (1,24; 1,85) | 1,35 (1,09; 1,46) | 1,46 (1,18; 1,74) | 0,276 | 0,218 |
Похожая ситуация отмечалась для показателей диастолической функции ПЖ: в первые сутки заболевания различий не выявлено, на 12-е сутки они появлялись. Так, отмечено увеличение ВИРПЖ в группе неблагоприятного прогноза по сравнению с пациентами с благоприятным годовым прогнозом (р=0,0039) (табл. 3).
Таблица 3. Показатели диастолической функции ПЖ в 1-е и 12-е сутки заболевания в группах с различным годовым прогнозом после ЧКВ у больных ИМпST
| Показатели | Группа благоприятного прогноза (n=46) | Группа неблагоприятного прогноза (n=23) | p1 | p2 | ||
| 1-й день | 12-й день | 1-й день | 12-й день | |||
| ЕТ, см / с | 44,5 (37,4; 51) | 49,9 (43; 56) | 44,2 (36; 52) | 46,4 (42; 51) | 0,906 | 0,245 |
| АТ, см / с | 43,3 (34; 49) | 44,7 (34; 55) | 42,3 (36,5; 48) | 40,3 (33; 45) | 0,639 | 0,175 |
| ВЗЕТ, мс | 158,3 (132; 174) | 171,3 (144; 198) | 157,2 (128,5; 190) | 165,5 (149; 186) | 0,612 | 0,538 |
| еТ, см / с | 9,0 (6,9; 10,2) | 9,96 (8,6; 11,9) | 8,25 (7,2; 8,7) | 10,08 (7,1; 12,3) | 0,319 | 0,884 |
| аТ, см / с | 11,8 (9,7; 13,3) | 13,6 (12,1; 15,2) | 11,8 (10,5; 12,5) | 14,3 (11,8; 16,7) | 0,659 | 0,721 |
| еТ / аТ | 0,79 (0,59; 0,87) | 0,75 (0,64; 0,76) | 0,71 (0,59; 0,76) | 0,71 (0,61; 0,81) | 0,257 | 0,657 |
| ВИРПЖ–ТД , м с | 71,5 (60; 90) | 73,9 (60; 90) | 73,8 (66; 84) | 84,8 (72; 96) | 0,539 | 0,039 |
| ЕТ / еТ | 5,34 (3,91; 6,57) | 5,19 (4,2; 6,0) | 5,61 (4,19; 6,87) | 4,96 (3,91; 5,81) | 0,514 | 0,565 |
| СРТП, см / с | 37,6 (32;41) | 35,6 (31; 39,4) | 37,64 (32,1;43) | 36,9 (31,7; 40,7) | 0,879 | 0,492 |
| ЕТ / СРТП | 1,27 (0,99; 1,47) | 1,45 (1,16; 1,67) | 1,21 (0,96; 1,43) | 1,31 (1,13; 1,49) | 0,906 | 0,223 |
Для структурных показателей ПЖ и ЛЖ статистически значимых различий между группами не выявлено ни в первые, ни на 12-е сутки заболевания (табл. 4). Можно только отметить тенденцию к меньшим размерам ПЖ в группе неблагоприятного прогноза по сравнению с пациентами благоприятного прогноза (для КДРПЖ значение р=0,080, для КСРПЖ – р=0,07). По-видимому, данная тенденция может быть объяснена относительным преобладанием женщин в группе неблагоприятного прогноза.
Таблица 4. Показатели систолической функции и геометрии левого и ПЖ в 1-е и 12-е сутки заболевания в группах с различным годовым прогнозом после ЧКВ у больных ИМпST
| Показатели | Группа благоприятного прогноза (n=46) | Группа неблагоприятного прогноза (n=23) | p1 | p2 | ||
| 1-й день | 12-й день | 1-й день | 12-й день | |||
| КДОЛЖ, мл | 157,9 (124; 186) | 162,7 (131; 186) | 151,2 (126; 180) | 151,8 (125; 164) | 0,549 | 0,381 |
| КСОЛЖ, мл | 82,7 (63; 96) | 69,9 (52; 77) | 76,6 (62; 92) | 68,2 (53; 76) | 0,549 | 0,746 |
| ФВ ЛЖ, % | 48,1 (44; 52) | 57,5 (52; 64) | 49,3 (46; 53) | 55,2 (50; 58) | 0,514 | 0,179 |
| ЛП, мм | 38,7 (36; 41) | 39,9 (38; 44) | 38,1 (36; 41) | 40,5 (37; 44) | 0,663 | 0,655 |
| LЛЖ–Д, мм | 79,9 (76; 84) | 76,8 (71; 83) | 80,3 (76; 85) | 77,0 (74; 81) | 0,831 | 0,840 |
| LЛЖ-С, мм | 72,6 (68; 77) | 69,4 (64; 75) | 73,1 (68; 79) | 69,8 (66; 73) | 0,866 | 0,989 |
| ИСФД | 0,72 (0,65; 0,77) | 0,75 (0,69; 0,79) | 0,69 (0,63; 0,75) | 0,72 (0,68; 0,76) | 0,482 | 0,678 |
| ИСИР | 68,6 (60,2; 76,5) | 78,1 (71,6; 85,3) | 72,2 (61,0; 78,9) | 76,9 (70,9; 84,9) | 0,396 | 0,534 |
| КДРПЖ, мм | 16,4 (12; 18) | 18,8 (16; 21) | 15,7 (13; 18) | 16,8 (15; 18) | 0,711 | 0,089 |
| КСРПЖ, мм | 13,8 (10; 15) | 14,8 (12; 18) | 13,0 (11; 15) | 13,1 (11; 15) | 0,740 | 0,070 |
| ФУПЖ | 18,4 (12,5; 25) | 21,3 (11,8; 29,4) | 16,7 (10,5; 22,2) | 21,3 (13,3; 27,8) | 0,415 | 0,994 |
| ПП1, мм | 36,2 (34; 39) | 36,9 (33; 38) | 33,9 (32; 37) | 36,8 (34,5; 37) | 0,184 | 0,947 |
| ПП2, мм | 46,8 (44; 48) | 47,1 (44; 49) | 44,8 (42; 49) | 45,9 (43; 48,5) | 0,609 | 0,785 |
Для выявления прогностически значимых факторов проведен логистический регрессионный анализ с включением в него как клинических показателей, так и данных ЭхоКГ (табл. 5). Статистически значимую связь с неблагоприятным прогнозом имели следующие факторы: курение (р=0,040), длительность анамнеза АГ (р=0,024), многососудистое поражение коронарных артерий (р=0,035) и динамика показателя ВЗЕМ в ходе стационарного лечения (р=0,009). При многофакторном анализе только последний показатель имел независимую ассоциативную связь с развитием неблагоприятного прогноза (ОР 1,023; 95 % ДИ 1,001–1,045; р=0,038) (табл. 5).
Таблица 5. Факторы, ассоциированные с неблагоприятным годовым прогнозом после ЧКВ у больных ИМпST
| Показатели | ОР | 95 % ДИ | р |
| Однофакторный логистический регрессионный анализ | |||
| Курение | 0,310 | 0,099–0,965 | 0,040 |
| Длительность АГ | 1,109 | 1,012–1,216 | 0,024 |
| Многососудистое поражение КА (≥2) | 2,036 | 1,041–3,983 | 0,035 |
| Показатели ЭхоКГ на 12-й день | |||
| ВЗЕМ | 1,01 | 0,996–1,03 | 0,119 |
| ВИРЛЖ–ТД | 1,02 | 0,998–1,047 | 0,073 |
| ЕМ / еМ | 1,299 | 0,98–1,72 | 0,060 |
| ЕТ / СРТП | 4,23 | 0,825–21,70 | 0,079 |
| Динамика показателей ЭхоКГ в ходе лечения (1–12 день) | |||
| ФВ ЛЖ | 0,934 | 0,869–1,003 | 0,056 |
| КДОЛЖ | 0,973 | 0,943–1,004 | 0,076 |
| ВЗЕМ | 1,023 | 1,005–1,041 | 0,009 |
| аМ | 0,763 | 0,581–1,003 | 0,047 |
| Многофакторный логистический регрессионный анализ | |||
| ВЗЕМ | 1,023 | 1,001–1,045 | 0,038 |
Обсуждение
В настоящем исследовании показано, что сердечнососудистые события при наблюдении в течение года возникали у 33 % больных. Увеличивали риск неблагоприятного прогноза такие факторы, как многососудистое поражение коронарных артерий, длительность анамнеза АГ, а также динамика в ходе стационарного лечения ВЗЕМ.
После первичного ЧКВ отдаленный прогноз у больных ИМ существенно лучше, чем при других способах реваскуляризации миокарда. Так, при проспективном наблюдении в течение 30 мес смертность среди данной категории пациентов в неселективной выборке составила 6 % [10]. В настоящем исследовании уровень смертности оказался еще меньше, что объясняется меньшим сроком наблюдения и невключением в исследование наиболее тяжелой категории пациентов с выраженными явлениями СН. С другой стороны, максимальная частота сердечно-сосудстых событий смещается в сторону нефатальных осложнений – они и преобладали в настоящем исследовании. Если же рассматривать частоту развития комбинированной конечной точки (смерти, ИМ, повторной реваскуляризации), то в опубликованных исследованиях она сопоставима с нашими данными. Так, она отмечена у 22,6 % больных в течение полутора лет после первичного ЧКВ при остром ИМ [13]. В то же время без первичного ЧКВ отдаленные результаты заметно хуже – в достаточно давнем уже когортном исследовании, включавшем больных острым ИМ после тромболитической терапии и даже без реперфузии, уровень смертности составил 32 % при наблюдении в течение двух лет [3].
После первичного ЧКВ в настоящем исследовании наиболее частыми сердечно-сосудистыми событиями явились повторные ИМ и процедуры реваскуляризации миокарда, которые чаще встречались у лиц с многососудистым поражением коронарных артерий (как и следовало ожидать). Следует отметить, что наряду с другими клиническими показателями этот фактор входил в модель стратификации риска у больных после первичного ЧКВ при остром ИМ и в других исследованиях [10, 13].
Поскольку первичное ЧКВ в максимальной степени способствует сохранению жизнеспособного миокарда [14] по сравнению с тромболитической терапией (и тем более – при отсутствии реперфузии) то вовсе не удивительно, что после ЧКВ процессы постинфарктного ремоделирования выражены в меньшей степени [15]. Соответственно, можно ожидать изменения прогностической значимости отдельных показателей, в том числе ЭхоКГ. Не вызывает сомнений взаимосвязь показателей систолической функции ЛЖ после ИМ с прогнозом. Тем не менее у больных после первичного ЧКВ наибольшей прогностической ценностью обладали новые маркеры систолической дисфункции. Значения таких показателей, как глобальная деформация (global strain) и скорость деформации (strain rate) ЛЖ выше, чем –15,1 % и –1,06 сек–1, повышали риск смертности от всех причин в 4,5 раза (95 % ДИ 2,1–9,7) и в 4,4 раза (95 % ДИ 2,0–9,5), соответственно [2]. Нам не удалось выявить подобных закономерностей: по-видимому, это было связано с тем, что в настоящее исследование не включены пациенты с неуспешным первичным ЧКВ (то есть те, у кого не достигнут удовлетворительный ангиографический результат процедуры). Как показано, именно этот клинический показатель наряду со снижением ФВ ЛЖ имел существенное прогностическое значение [13].
Диастолическая дисфункция ЛЖ активно изучается в исследованиях последних лет, как прогностический маркер при остром ИМ, поскольку она является динамичным параметром в острых ситуациях и может быстрее развиваться при патологическом процессе [12]. Ввиду сложности процессов, происходящих в период наполнения желудочков сердца, обычно используется комплексная оценка диастолической функции с использованием нескольких маркеров. В разных клинических ситуациях те или иные показатели диастолической функции имеют неодинаковое клиническое и прогностическое значение [12]. Неудивительно, что практически для каждого из показателей удается найти исследования, подтверждающие их прогностическую значимость у больных ИМ. Так, она показана для таких традиционных показателей трансмитрального кровотока, как отношение Е / А и ВЗЕ [4, 16–19], для показателей тканевой допплерографии митрального клапана [20], внутрижелудочковых потоков наполнения [3, 21]. Мета-анализ 12 исследований также показал, что рестриктивные показатели диастолической функции у больных после ИМ связаны с неблагоприятным прогнозом при последующем наблюдении [4]. В настоящем исследовании все вышеперечисленные маркеры при оценке их в 1-й и 12-й дни от начала заболевания не имели прогностического значения по влиянию на развитие комбинированной конечной точки при наблюдении за больными в течение года после выполнения ЧКВ при ИМпST. Причины этого могут быть следующие. Во-первых, преобладание повторных ИМ и реваскуляризаций миокарда (а не летальных исходов и развития СН) среди конечных точек выдвигает на первый прогностический план наличие многососудистого поражения коронарных артерий, а не гемодинамические показатели. Во-вторых, в настоящее исследование были включены пациенты после успешного первичного ЧКВ, что имело также большое значение. Так, развитие синдрома «no-reflow» после стентирования коронарной артерии было связано с последующим ремоделированием ЛЖ и неблагоприятным прогнозом [22]. С другой стороны, распространение внутрижелудочковых потоков наполнения зависит от объема некротизированного миокарда [23], поэтому при относительно небольших размерах ИМ после успешной ЧКВ изменения этих показателей могут быть менее выраженными, что и отмечено в настоящей работе. Также недавно было показано, что неблагоприятные процессы ремоделирования в ранние сроки после ИМ связаны с развитием в последующем выраженной диастолической дисфункции и неблагоприятного прогноза [24]. В настоящем исследовании не наблюдалось такого ремоделирования ЛЖ. Задержка с проведением ЧКВ у больных ИМ приводит к выраженной диастолической дисфункции миокарда ЛЖ уже на третьи сутки заболевания [25]. У нас такой картины не наблюдалось вследствие своевременности выполнения процедуры. Кроме того, в данном исследовании было мало больных с выраженными признаками острой СН (подавляющее число больных имели выраженность СН 1 степени по классификации Killip), прогноз у этой категории больных был существенно лучше, чем в других обследованных когортах.
Только динамика показателя ВЗЕ в ходе стационарного лечения имела независимое прогностическое значение, превышающее таковое других, в том числе клинических, факторов. В последнее время для повышения прогностического значения стали применяться новые маркеры функции ЛЖ, оцениваемые с использованием технологии «speckle tracking» [13, 26]. Наши данные свидетельствуют, что с той же целью можно использовать и оценку в динамике более привычных показателей диастолической функции ЛЖ. Это предположение требует подтверждения в дальнейших исследованиях.
В ЭхоКГ подисследовании крупного исследования VALIANT [27] показано, что снижение систолической функции ПЖ было независимо связано с повышением риска общей и кардио-васкулярной смертности, развития внезапной смерти и СН. Снижение такого показателя, как изменение фракционной площади ПЖ на каждые 5 % было ассоциировано с повышением риска развития сердечно-сосудистых событий в 1,53 раза (95 % ДИ 1,24–1,88) [27]. У больных после первичного ЧКВ также удалось показать зависимость прогноза от показателей функции ПЖ. Неблагоприятный госпитальный прогноз был ассоциирован со снижением максимальной систолической скорости движения стенки ПЖ в режиме тканевой допплерографии [8]. Такие параметры, как процент снижения площади ПЖ и напряжение ПЖ, независимо предсказывали развитие комплексной конечной точки (наряду с такими показателями, как класс СН по Killip, многососудистое поражение, максимальный уровень тропонина Т, ФВ ЛЖ) при последующем 2-летнем наблюдении [28]. В настоящей работе только отдельные показатели имели ассоциацию с прогнозом, как правило, не достигавшую статистической значимости. Если прогностическое значение систолической дисфункции ПЖ при ИМ установлено, то для показателей диастолической функции ПЖ это еще предстоит изучить. Хотя есть данные, что с наличием поражения ПЖ при ИМ была ассоциирована диастолическая скорость движения стенки ПЖ в режиме тканевой допплерографии [8], влияние его на прогноз неизвестно. Поскольку ранее было показано, что изучение диастолической функции ПЖ может быть более информативно, чем оценка его систолической функции, в определенных клинических ситуациях (например, при развитии легочной гипертензии [29]), требуется дальнейшее изучение прогностического значения нарушений наполнения ПЖ. Не исключено, что при этом необходимо будет учитывать локализацию ИМ, степень вовлеченности ПЖ в некротический процесс. Вполне возможно, что для этого потребуется проведение дальнейших исследований.
Следует признать, что постоянно появляющиеся новые ЭхоКГ показатели также заслуживают изучения в плане улучшения прогностических возможностей у больных ИМ. Например, в работе Shanks M. с соавт. [13] было показано, что при проведении ЭхоКГ в течение 48 ч от развития острого ИМ показатель «strain rate» верхушки ЛЖ во время изоволюмической релаксации оказался наиболее чувствительным из всех ЭхоКГ параметров в определении больных с риском развития комбинированной конечной точки в течение последующих 17 месяцев наблюдения (наряду со снижением ФВ ЛЖ, наличием многососудистого поражения коронарных артерий и кровотока TIMI 0–1 после ЧКВ) [13]. Кроме того, перспективным выглядит использование комбинированных показателей. Известно, что индекс миокардиальной производительности (индекс Теи), оценивающий в комплексе систолическую и диастолическую функцию желудочка, существенно выше у больных после первичного ЧКВ, чем после тромболитической терапии [30]. Данный индекс неплохо зарекомендовал себя в качестве прогностического индикатора при нормальной ФВ ЛЖ [31], но у других категорий больных его прогностическое значение еще предстоит уточнить [32]. Кроме того, недавно предложен так называемый FIT-индекс, интегрирующий функциональную оценку уже обоих желудочков сердца. Этот показатель вычисляется, как отношение скорости систолического движения трикуспидального клапана к показателю E / e’ ЛЖ [33]. В пилотном исследовании с участием ограниченного числа пациентов этот индекс коррелировал с показателями инвазивной гемодинамики (сердечным индексом, давлением заклинивания легочной артерии), а значения данного индекса <1,0 были существенным предиктором неблагоприятного исхода при остром ИМ [33]. Насколько данные маркеры способны улучшить прогностическое значение ЭхоКГ показателей, выяснится только в дальнейших исследованиях.
Итак, при наблюдении в течение года после ЧКВ у больных ИМпST летальный исход имел место в 1 (1,36 %) случае, наличие хотя бы одного сердечнососудистого события – у 23 (31,5 %) больных. Отмечена статистически значимая ассоциация неблагоприятного прогноза с числом пораженных коронарных артерий, длительностью АГ, динамикой показателя ВЗЕМ в ходе стационарного лечения. Эхокардиографические показатели на 12-й день заболевания не имели связи с прогнозом в обследованной когорте пациентов. Таким образом, первичное ЧКВ у больных ИМпST не только улучшает годичный прогноз, но и модерирует прогностическое значение ЭхоКГ показателей у данной категории пациентов.
Список литературы
