Тактика мукоактивной терапии при воспалительных заболеваниях в оториноларингологии
СтатьиОпубликовано в журнале:
«Педиатрия», Том 07, №2, 2005, приложение Consilium-medicum, с. 47-50
Г.Д.Тарасова
ФГУ Научно-клинический центр оториноларингологии Росздрава (дир.– проф. Н.А.Дайхес), Москва
Одним из основых барьеров защиты слизистой оболочки верхних дыхательных путей является наличие мукоцилиарного клиренса и секреция мерцательным эпителием секреторного иммуноглобулина А, лактоферрина и лизоцима. Процесс слизеобразования является физиологическим для слизистой оболочки дыхательных путей, при этом формируется двухфазная по структуре слизь, состоящая из слоя золя – перицилиарный слой, в котором реснички совершают две фазы своего движения – эффективный удар и распрямление, и более поверхностного слоя геля, который лежит над ресничками. Золь действует как вспомогательная смазка, координирующая движение ресничек, которые транспортируют слой геля. Реснички совершают двухфазное движение: эффективный удар, во время которого они достигают слоя геля и перемещают его, затем следует распрямление. Таким образом, реснички и слизь на поверхности эпителия образуют единый функциональный комплекс [1–4].
Существует оптимальная концентрация молекул муцина в отделяемом респираторного тракта, необходимая для полноценного выполнения транспортной, увлажняющей, фильтрационной и антибактериальной функций.
Регуляция гидратации слизи необходима для эффективности мукоцилиарного клиренса, ее контролируют ионный состав, рН и осмолярность. Степень диффузии или всасывающая способность слизистой оболочки поддерживает ее эффективность как фильтрационного барьера против бактерий и контаминирующих агентов.
В то же время адгезия к эпителию, снижение мукоцилиарного клиренса – мукостаз и продукция экскреторных энзимов помогают бактериям противостоять мукоцилиарному клиренсу. Так называемые адгезины находятся на поверхности бактерий и обеспечивают их сцепление со слизистой оболочкой. Затем патогены размножаются и “запускают” местную воспалительную реакцию.
Воспалительные заболевания, особенно хронические, в органах дыхания, которые покрыты реснитчатым эпителием, сопровождаются изменением реологических свойств (деструктуризацией) вырабатываемой им слизи и нередко избыточной ее продукцией (гиперкринией). Нарушение реологических и физических свойств слизи приводит к ее застою вследствие нарушения экспекторации (свободного отделения). При этом наблюдают расстройство функций и структуры ресничек эпителия.
Известно, что основными механизмами очистки дыхательных путей являются мукоцилиарный транспорт, чиханье и кашель. Но вырабатываемую при этом деструктурированную слизь нередко организм не в состоянии эвакуировать самостоятельно, что приводит к ее застою и скоплению в полостях организма и прежде всего при ЛОР-заболеваниях: в полостях околоносовых пазух и среднего уха [5–8].
При небольшом увеличении вязкости улучшается мукоцилиарный клиренс, но до определенного предела. При гиперсекреции кашель может давать очищение более чем на 50%, компенсируя этим возможные нарушения мукоцилиарного транспорта. Но при значительном повышении вязкости выключаются и клиренс, и кашель, т.е. механизмы собственной защиты [1, 9–11]. Так, при инфекционном воспалении на 60–80% уменьшается или останавливается мукоцилиарный транспорт. Большинство респираторных патогенов продуцируют экзотоксины, нарушающие функцию различных защитных механизмов, и в первую очередь мукоцилиарный клиренс. Одновременно повышается вязкость, адгезивность и уменьшение эластичности слизи.
В связи с этим в комплексную терапию воспалительных заболеваний верхних дыхательных путей и уха рационально включать мукоактивные препараты. В настоящее время эта группа препаратов внесена в разработанный стандарт лечения синусита в России. В задачи муколитической терапии входят: стимуляция выведения слизи, разжижение слизи, уменьшение внутриклеточного образования слизи, регидратация. В оториноларингологии используют несколько групп мукоактивных препаратов, обладающих различными механизмами действия (см. таблицу) [5, 6, 8, 12, 13]. Выбирая муколитический препарат, следует руководствоваться присущим ему особенностям действия и индивидуальной ситуацией.
Среди мукоактивных средств, прямо воздействующих на процесс слизеобразования, выделяют производные алколоида визицина (бензиламины). Они представлены препаратами “Бромгексин”, “Амброксол” или входят в состав комбинированных лекарственных средств (“Зедекс” и “Бронхосан”), которые лишь разжижают и уменьшают вязкость секрета. Их целесообразно использовать при заболеваниях, сопровождающихся сухим непродуктивным кашлем.
Муколитические ферменты – трипсин, химотрипсин, рибонуклеаза, дезоксирибонуклеаза используют в оториноларингологии давно, но имеют ряд выраженных побочных эффектов, которые ограничивают возможность их широкого распространения, и к тому же их не используют в детском возрасте [6, 10, 13].
Препараты резорбтивного прямого действия (способствующие регидратации), такие как соли натрия и калия (йодиды), гидрокарбонат натрия, гипохлорид аммония (нашатырно-анисовые капли), амония хлорид, стимулируют бронхиальную секрецию, разжижают мокроту, усиливают перистальтику мерцательного эпителия, но их эффект почти не проявляется на уровне полости носа и околоносовых пазух, поэтому их назначают при трахеитах и бронхитах.
Синтетические соединения – терпингидрат и ликорин действуют посредством гастропульмонального рефлекса через рвотный центр продолговатого мозга, вызывают рефлекторную стимуляцию секреции бронхиальных и слюнных желез, усиливают перистальтику мерцательного эпителия. У детей их следует применять с осторожностью, так как избыточная стимуляция рвотного и кашлевого центров может привести к рвоте и аспирации. Поэтому препараты этой группы имеют ограниченное применение [13].
Симпатомиметики – стимуляторы b2-адренорецепторов (b2-агонисты) – тербуталин, теофиллин, активизируют механизмы мерцательного эпителия, но их чаще применяют при воспалительных заболеваниях бронхов и бронхиальной астме.
К муколитикам прямого действия относят препараты-носители сульфгидрильных групп (разрывающие полимеры секрета) – ацетилцистеин и месна. В России их используют достаточно широко. В основе действия производных ацетилцистеина лежит восстановление свойств слизи путем разрыва дисульфидных связей мукополисахаридов мокроты – молекулы деполимеризуются и мокрота становится менее вязкой и адгезивной. Однако им присущи множественные побочные реакции (диспепсии, шум в ушах, носовые кровотечения, аллергические реакции), развивающиеся как при местном, так и при системном их применении, а также имеют достаточно широкие противопоказания (болезни печени, почек, дисфункция надпочечников, склонность к кровотечениям, периоды кормления и беременности).
Классификация мукоактивных препаратов по механизму действия
| Прямое действие | ||
| Препараты, разрывающие полимеры секрета | Тиолитики – производные цистеина | Ацетилцистеин, цистеин, месна, метилцистеин, этилцистеин, L-цистеин, гуайфенезин, имозимаза, террилитин |
| Производные алколоида визина (бензиламины) | Бромгексин, амброксол, лазолван | |
| Протеолитические ферменты | Трипсин, химотрипсин, химопсин, рибонуклеаза, дезоксирибонуклеаза | |
| Препараты, способствующие регидратации секрета | Неорганический йод, соли натрия и калия, гипертонические солевые растворы | |
| Непрямое действие | ||
| Препараты, стимулирующие гастропульмональный рефлекс | Фитопрепараты | Препараты термопсиса, алтея, солодки, истода, эфирные масла |
| Синтетические соединения | терпингидрат, ликорин | |
| Препараты, регулирующие выработку секрета | Производные карбоцистеина | Карбоцистеина лизиновая соль, карбоцистеин |
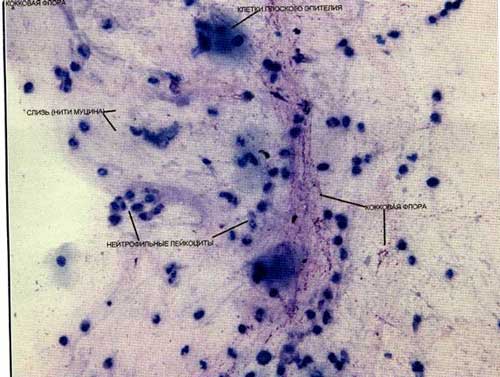
Назальный секрет (гнойный характер) у ребенка с хроническим инфекционным ринитом (до лечения).
Существуют фитопрепараты, нередко комбинированные, выпускаемые, как правило, в виде сиропов (гербион, стоптуссин, проспан, гликодин, и др.), которым также свойственно непрямое воздействие на процесс слизеобразования через стимуляцию гастропульмонального рефлекса. В их состав обычно входят такие растения, как солодка, термопсис, истод, алтей и др. Эфирные масла некоторых растений также обладают секретолитическим эффектом. Они являются основой ряда препаратов, например геломиртола. Кроме того, выпускают фитопрепараты, обладающие секретолитическими свойствами, содержащие экстракты нескольких трав [2]. Одним из них является синупрет. Однако при назначении фитопрепаратов с муколитической активностью нельзя забывать о возможности развития аллергической реакции на их компоненты.
Мукоактивными средствами непрямого действия являются производные карбоцистеина. Механизм действия карбоцистеина связан с активацией сиаловой трансферазы – фермента бокаловидных клеток слизистой оболочки. Он нормализует количественное соотношение кислых и нейтральных гликопептидов, что восстанавливает вязкость и эластичность слизи. При этом происходит замещение патологической слизи реструктуризированной, которая располагается между патологическим секретом и слизистой оболочкой. Таким образом, деструктурированная слизь как бы приподнимается, а пульсация ресничек осуществляется уже в контакте с физиологической слизью [11].
Нами накоплен опыт по применению препарата “Флюдитек” (карбоцистеин), производимого в виде 2% сиропа для детей и 5% сиропа для взрослых.
Основной целью нашего исследования явилась оценка терапевтической эффективности карбоцистеина на основании клинических критериев с учетом цитологического анализа назального секрета.
Материал и методы
Методы включали помимо общепринятых (сбор и анализ данных анамнеза, оториноларингологический осмотр) морфологическую методику – эксфолиативный цитологический анализ назального секрета.
Объектом исследования были 64 ребенка в возрасте с 3 до 8 лет, находящиеся на санаторном этапе реабилитации. Основным критерием включения было наличие клиники инфекционного ринита с сопутствующим хроническим аденоидитом, установленное при оториноларингологическом обследовании. К критериям исключения были отнесены: наличие на момент включения в исследования у ребенка острой респираторной вирусной инфекции и другого острого или обострения хронического заболевания.
Контрольная группа включала 22 ребенка, комплекс терапии которых был традиционным и состоял из ирригации полости носа 0,01% раствором мирамистина и ингаляционной терапии минеральной водой “Ессентуки-4”. Основную группу составили 42 ребенка, в комплекс лечения которых наряду с перечисленными средствами был включен карбоцистеин в возрастной дозировке курсом от 8 до 10 дней.
Цитологический анализ назального секрета проводили до лечения и через 14 дней от начала лечения в основной и контрольной группах. На рисунке отражен наиболее характерный вид назального секрета до лечения.
В результате проведенного исследования было выявлено более раннее выздоровление детей в основной группе по сравнению с контрольной. При этом раньше купировался кашель, более быстро восстанавливалось носовое дыхание и уменьшался отек слизистой оболочки. Особые различия у больных этих групп отмечены при оценке количества, длительности и характера назального секрета. Так, в основной группе на 2–3-й день от начала терапии у большинства детей количество отделяемого увеличилось, а с 3–4-го дня стал меняться его видимый характер и уменьшаться его количество. Выделения становились менее густыми и лучше удалялись при отсмаркивании и при промывании. Кашель почти у всех детей (у 88,2%) этой группы купировался к 7-му дню лечения.
В контрольной группе характер отделяемого видимо стал меняться лишь на 5–6-й день от начала лечения. Уменьшение же его интенсивности наблюдали с 6–7-го дня.
Эксфолиативный анализ цитологии назального секрета у большинства больных до лечения показал низкий цитоз реснитчатого эпителия, превалирование плоского эпителия, высокие цифры нейтрофилов, большое количество слизи и наличие в большом количестве разнообразной микрофлоры, преимущественно кокковой.
Эксфолиативные цитограммы по окончании лечения у 64,7% детей в основной группе свидетельствовали об урегулировании процесса фагоцитоза при отсутствии подавления экссудации с одновременным уменьшением количества микроорганизмов. В контрольной группе подобные изменения имели место лишь у 36,4% пациентов и были менее выраженными.
Полученные результаты свидетельствуют об эффективности использования карбоцистеина “Флюдитека” в комплексном лечении воспалительных заболеваний верхних дыхательных путей. Терапевтическую эффективность применения мукоактивных препаратов целесообразно оценивать на основании результатов методики эксфолиативной цитологии назального секрета.
Следует отметить, что оценка состояния секреции слизистой оболочкой при воспалительном процессе в динамике в нашей стране проведена впервые. Результаты исследования позволяют широко рекомендовать применение мукоактивного средства “Флюдитек” в детской практике при воспалительных заболеваниях ЛОР-органов, сопровождающихся нарушением секреции. В то же время эффективность других подобных препаратов мы можем лишь предполагать.
ЛИТЕРАТУРА
1. Полевщиков А.В. Риносинуситы: механизмы развития воспаления слизистых оболочек и пути воздействия на него. Матер. ХV1 съезда оториноларингологов РФ, Сочи, 2001.
2. Рязанцев С.В. Роль мукоактивной терапии в комплексном лечении острых и хронических синуситов. Рос. оториноларингол. 2005; 5 (18): 123–6.
3. Bals R. Cells types of respiratory epithelium: morphology, molecularbiology and clinical significance. Pneumologie 1997; 51: 142–9.
4. Toremalm NG. The mucociliary apparatus. Rhinology 1983; 21: 197–202.
5. Гаращенко Т.И., Богомильский М.Р. Мукоактивные препараты в лечении заболеваний верхних дыхательных путей. Ринология. 2002; 2: 28–39.
6. Зайцева О.В. Лечение кашля у детей и подростков: рациональный выбор терапии. Consilium medicum 2003; 5 (4): 204–7.
7. Catalano GB, Mallanino NA, Serra A. La carbocisteina nella patologia flogistica cronica rinosinusale. Otorinolaringologia. 1981; 31: 1–11.
8. Chalumeau M, Cheron G, Assathiany R et al. Mucolitic agents for acute respiratory tract infections in infants: a pharmacoepidemiologic problem? Arch Pediatr 2002; 9: 1128–36.
9. Овчаренко С.И. Муколитические (мукорегуляторные) препараты в лечении хронической обструктивной болезни легких. РМЖ. 2002; 10 (4): 153–7.
10. Синопальников А.И., Клячкина И.Л. Место муколитических препаратов в комплексной терапии болезней органов дыхания. Рос. мед. вести. 1997; 2 (4): 9–18.
11. Bron J. Relative biovailability of carbocysteine from three dosage forms. Investigated in healthy volunteers. Biopharm Drug Disposit 1988; 9: 97–111.
12. Рязанцев С.В. Роль муколитических, секретолитических и секретомоторных препаратов в лечении острых и хронических синуситов у детей. Новости оториноларингол. и логопатол. 2002; 1 (29): 129–32.
13. Самсыгина Г.А., Зайцева О.В. Бронхиты у детей. Отхаркивающая и муколитическая терапия. Пособие для врачей. М., 1999.
