Пробиотическая коррекция антибиотик-ассоциированного дисбактериоза кишечника у детей
СтатьиОпубликовано в журнале:
«Вопросы современной педиатрии» 2007, ТОМ №6, № 3, с. 38-42
С.В. Бельмер1, Н.Е. Щиголева1, А.И. Хавкин2, А.В. Горелов3, С.Ф. Блат2, Е.В. Каннер3, М.А. Ратникова3, О.А. Кондракова3, Е.В. Семенова1, Р.Р. Мустафина3
1 Российский государственный медицинский университет, Москва
2 Московский НИИ педиатрии и детской хирургии Росздрава
3 Московская медицинская академия им. И.М. Сеченова
В открытом сравнительном рандомизированном исследовании проведена оценка эффективности пробиотической терапии у 59 детей в возрасте от 6 до 17 лет препаратом, содержащим лиофилизированные штаммы Bifidobacterium infantis v. Liberorum, Lactobacillus acidophilus и Streptococcus faecium (Линекс, Лек, Словения) антибиотик-ассоциированного дисбактериоза кишечника, развившегося на фоне антихеликобактерной терапии. Основную группу составили 38 пациентов, группу сравнения — 21 ребенок. Пациенты обеих групп были сопоставимы по демографическим и клиническим характеристикам. В ходе исследования анализировались клинические данные, а также результаты исследования состава кишечной микрофлоры и летучих жирных кислот. Проведенное исследование показало, что у большинства пациентов антихеликобактерная терапия сопровождается развитием антибиотик-ассоциированного дисбактериоза кишечника. Однако назначение препарата, содержащего лиофилизированные штаммы Bifidobacterium infantis v. Liberorum, Lacto-bacillus acidophilus и Streptococcus faecium снижает риск развития антибиотик-ассоциированного дисбактериоза кишечника, а его эффект проявляется клиническим улучшением, нормализацией состава микрофлоры кишечника и восстановлением ее метаболической активности. Ключевые слова: антибиотик-ассоциированный дисбактериоз, дети, пробиотики, лечение, профилактика.
Многочисленная кишечная микрофлора, заселяющая практически все отделы желудочно-кишечного тракта (максимально представленная в толстой кишке), выполняет жизненно важные для макроорганизма функции, обеспечивая его питательными веществами, витаминами, поддерживая функциональную активность иммунной системы и многое другие. Под воздействием эндогенных и/или экзогенных факторов состав кишечной микрофлоры может меняться, что нарушает нормальное течение физиологических процессов, а в отдельных случаях — приводит к тяжелым патологическим состояниям. Причиной нарушения кишечного микробиоценоза может стать практически любое заболевание органов пищеварения, в первую очередь — заболевания, сопровождающиеся нарушениями процессов переваривания и всасывания, вследствие чего меняется состав внутренней среды в кишке и условия существования кишечных микроорганизмов. Другая возможная причина развития дисбактериоза кишечника — применение антибиотиков, которые прямо влияют на микроорганизмы и существенно изменяют «микробный пейзаж» желудочно-кишечного тракта.
Для обозначения комплекса изменений в кишечнике и соответствующих клинических проявлений, связанных с дисбактериозом на фоне применения антибиотиков, в зарубежной литературе часто используется термин антибиотик-ассоциированная диарея (antibiotic associated diarrhea), эквивалентом которого, по существу, является термин «антибиотик-ассоциированный дисбактериоз кишечника». Частота этого состояния, по данным различных авторов, колеблется от 5 до 39%.
Так, было показано, что ампициллин существенно подавляет рост как аэробной, так и анаэробной флоры. Амоксициллин в меньшей степени подавляет нормальную микрофлору, хотя и приводит к некоторому увеличению популяции представителей семейства Enterobacteriaceae, при этом не способствуют размножению грибов и Clostridium difficile [1]. Сходным образом на микробиоценоз кишечника влияет комбинированный препарат амоксициллина и клавулановой кислоты. Большинство цефалоспоринов способствует росту численности энтерококков и С. difficile. Фторхинолоны в значительной степени угнетают рост микробов семейства Enterobacteriaceae и, в меньшей степени — энтерококков и анаэробных микроорганизмов, не способствуя при этом росту грибов и С. difficile [1].
Одними из наиболее тяжелых и угрожающих жизни состояний являются так называемые С. difficile-ассоциированный колит и его крайнее проявление — псевдомембранозный колит. Эти процессы связаны с избыточным размножением в кишечнике С. difficile. При бактериологическом исследовании С. difficile выявляют лишь у 1-3% здоровых лиц, но более чем у 20% пациентов, получающих антибактериальную терапию. В отдельных случаях, на фоне угнетения нормальной флоры происходит лавинообразный рост популяции С. difficile с изменением его токсигенных свойств: что проявляется повышением синтеза энтеротоксина А и цитотоксина В и приводит к тяжелому поражению слизистой оболочки толстой кишки. Чаще всего С. difficile-ассоциированный колит развивается при применении клиндамицина или линкомицина, полусинтетических пенициллинов, реже — цефалоспоринов с широким спектром антибактериального действия. Наиболее тяжелой формой С. difficile-ассоциированного колита является псевдомембранозный колит, летальность при развитии которого, достигает 30% [2-4].
Псевдомембранозный колит в типичных случаях характеризуется сильными болями в животе, подъемом температуры тела до 40°С, частым (10-20 раз в сут) жидким стулом с примесью слизи и крови. Клинически часто наблюдаются признаки тяжелого эндотоксикоза, а в общем анализе крови выявляются лейкоцитоз и увеличение СОЭ. В толстой кишке обнаруживаются гиперемия слизистой оболочки и фибринозные пленки, образовавшиеся на участках некроза, в виде бледных серовато-желтых бляшек размером 0,5-2,0 см в диаметре на слегка приподнятом основании. Гистологически выявляются участки некроза слизистой оболочки толстой кишки, отек подслизистого слоя, круглоклеточная инфильтрация собственной пластинки и фокальные экстравазаты эритроцитов. Наиболее доступным диагностическим тестом при псевдомембранозном колите является определение в фекалиях токсина А С. difficile методом латекс-агглютинации.
Одной из проблем, возникших в последние годы, является развитие антибиотик-ассоциированного дисбактериоза кишечника на фоне эрадикации H. pylori. В состав антихеликобактерных схем в различных комбинациях могут входить различные антибактериальные препараты, такие как амоксициллин, макролиды (кларитромицин, рокситромицин, азитромицин), метронидазол, фуразолидон, нифурател, висмута трикалия дицитрат, а также современные лекарственные средства, снижающие желудочную секрецию (блокаторы протонного насоса или блокаторы Н2-гистаминовых рецепторов), также способные, хотя и косвенно, снизить резистентность естественной кишечной микрофлоры. Многочисленные исследования свидетельствуют о необходимости включения в комплексную терапию хеликобактер-ассоциированных заболеваний верхних отделов пищеварительного тракта биопрепаратов, в частности, бифидумсодержащих, что позволяет уменьшить частоту развития и глубину выраженности дисбиотических изменений и, как следствие, уменьшить выраженность и длительность сохранения болевого абдоминального и диспепсического синдромов у детей [5].
Профилактика и коррекция антибиотик-ассоциированного дисбактериоза кишечника является достаточно трудной задачей, особенно у детей первого года жизни. Задача становится особенно сложной, если антибактериальную терапию следует продолжить. Основой профилактики дисбактериоза кишечника является рациональная антибиотикотерапия и исключение необоснованных случаев назначения антибактериальных средств. У детей первого года жизни важным фактором профилактики является сохранение грудного вскармливания или, при невозможности, использование смесей с пребиотиками. Кроме того, в любом возрасте клинически обосновано сочетанное назначение антибиотиков с препаратами-пробиотиками. Коррекция антибиотик-ассоциированного дисбактериоза включает в себя назначение энтеросорбентов и пробиотических препаратов.
Лечение псевдомембранозного колита является особенно сложной задачей, требующей отдельного рассмотрения. После отмены проводимой ранее антибактериальной терапии (клиндамицина, ампициллина, цефалоспоринов, аминогликозидов, линкомицина и др.) больному назначают препараты, направленные на эрадикацию С. difficile в кишечнике, к которым относятся метронидазол или ванкомицин в сочетании с энтеросорбентами. Кроме того, проводят коррекцию водно-электролитных нарушений и симптоматическую терапию. По мере восстановления состояния кишечника в терапию включают биопрепараты для восстановления микробиоценоза толстой кишки.
В настоящее время широко используются препараты, содержащие в том или ином виде различные штаммы бифидо- и/или лактобактерий, а также некоторые другие микроорганизмы, например, Saccharomyces boulardii. Многочисленными исследованиями была показана эффективность использования препаратов на основе перечисленных микроорганизмов для лечения гастроинтестинальных осложнений антибиотикотерапии как изолированно, так и в сочетании с пребиотиками и энтеросорбентами.
C целью оценить эффективность пробиотической терапии антибиотик-ассоциированного дисбактериоза кишечника, развившегося на фоне антихеликобактерной терапии, было проведено открытое сравнительное рандомизированное исследование, в котором приняли участие 59 детей в возрасте от 6 до 17 лет (средний возраст — 11,8 лет).
Исследование проводилось в Москве на базах Российского государственного медицинского университета (Российская детская клиническая больница), Московского НИИ педиатрии и детской хирургии Росздрава и Московской медицинской академии им. И.И. Сеченова.
Все дети случайным образом были разделены на две группы — основную (38 пациентов) и группу сравнения (21 ребенок). Пациенты обеих групп получали антихеликобактерную терапию и были сопоставимы по демографическим и клиническим характеристикам. В качестве лекарственного препарата-пробиотика в работе был использован Линекс (Лек, Словения). Препарат содержит не менее 1,2х107 живых лиофилизированных штаммов бактерий Bifidobacterium infantis v. liberorum, Lactobacillus acidophilus и Streptococcus faecium устойчивых к антибиотикам, химиотерапевтическим средствам и кислой среде.
Всем детям перед началом исследования было проведено клиническое и лабораторное обследование (1-й осмотр). В дальнейшем пациентам основной группы был назначен препарат Линекс в возрастной дозировке. Длительность курса лечения составила 1 нед. После окончания курса антихеликобактерной терапии в течение 1-й нед дети обеих групп были обследованы повторно (2-й осмотр), а, спустя 1 мес — обследованы в третий раз (3-й осмотр). Критериями исключения из исследования и прекращения приема препарата были непереносимость препарата, отказ от его приема, необходимость дополнительного на значения других препаратов, влияющих на состав кишеч ной микрофлоры.
В ходе исследования анализировались клинические данные (характер и консистенция стула, наличие болей в животе), а также результаты изучения состава кишечной микрофлоры стандартным микробиологическим исследованием и летучих жирных кислот в фекалиях методом высокоэффективной жидкостной хроматографии. В группе сравнения примерно у половины детей стул оставался оформленным в течение всех трех осмотров (52,38, 42,86 и 47,06% в 1-й, 2-й и 3-й осмотры соответственно). Иная ситуация наблюдалась в основной группе, где первоначально оформленный стул был у 63,16% пациентов, а затем происходило постепенное увеличение доли таких детей до 74,35 и 84,38%, при 2-м и 3-м осмотрах соответственно.
Цвет стула у детей группы сравнения, так и основной групп практически всегда был нормальным, однако в группе сравнения к 3-му осмотру у 5,88% детей (p При оценке численности бифидо- и лактобактерий было отмечено, что у детей обеих групп средний уровень численности этих микроорганизмов был ниже минимального значения нормальных показателей. В группе сравнения первоначально низкое среднее значение их содержания еще больше снижалось ко 2-му осмотру, а к 3-му осмотру происходило некоторое увеличение среднего значения до нижней границы возрастной нормы. В основной группе отмечалось увеличение числа бифидобактерий ко 2-му осмотру и некоторое их снижение к третьему. Такая же закономерность прослеживалась и в отношении лактобактерий.
Среднее значение E. coli у всех детей в ходе проведения исследования колебалось от 211,238 до 293,771 млн/г. У детей группы сравнения ее количество повышалось, в основной снижалось: при 1-м осмотре среднее значение E. coli в группе составляло 211,238, при 2-м осмотре — 214,107, при 3-м осмотре — 285,941 млн/г; в то время как у детей основной группы — 293,771, 223,712, 257,875 млн/г, соответственно (рис. 1). Из условно-патогенной микрофлоры высевались лактозонегатиная кишечная палочка, гемолизирующая кишечная палочка, кишечная палочка со слабо выраженными ферментирующими свойствами; кокковые формы в общей сумме микроорганизмов, негемолитический стафилококк, коагулазонегативный стафилококк, энтерококки, протей, цитробактер, энтеробактер, псевдомонас, клебсиелла и ряд неферментирующих грамотрицательных микроорганизмов, а также дрожжеподобные грибы.
Рис 1. Результаты исследование микробиоценоза кишечника в основной и группе сравнения
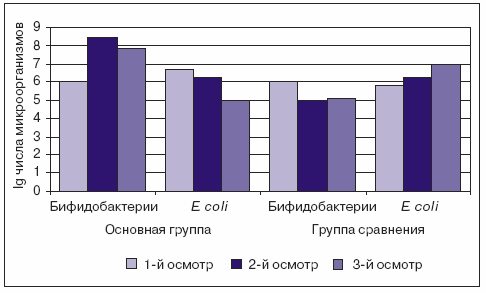
Следует отметить, что в группе сравнения достаточно стабильно высевалась гемолизирующая E. coli (в 23,81%, 14,29 (p Некоторые особенности микробиоценоза ко второму осмотру представлены на рис. 2.
Рис. 2. Некоторые особенности микробиоценоза ко второму осмотру
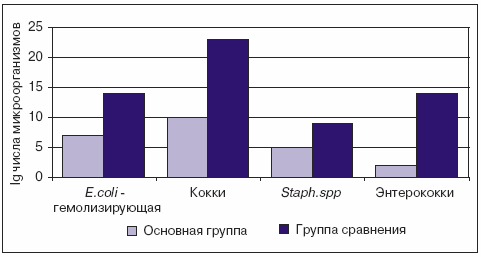
Общий уровень летучих жирных кислот в кале в группе сравнения во время всего исследования был ниже нормы — 6,83 мг/г при 1-м осмотре, 4,3966 мг/г при 2-м, 6,48 мг/г при 3-м (при норме 10,63 мг/г). В основной группе наблюдалась противоположная ситуация: при 1-м осмотре общий уровень ЛЖК был ниже нормы и составлял 7,61 мг/г, ко 2-му осмотру он достигал нормальных показателей (10,63 мг/г; p Рис. 3. Динамика общего уровня летучих жирных кислот в основной группе и группе сравнения
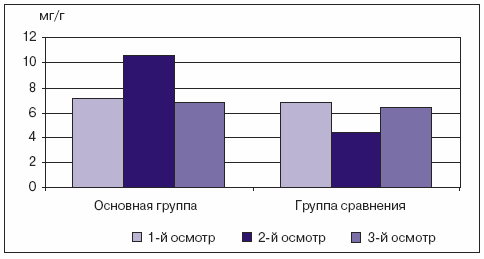
Среднее абсолютное значение отдельных кислот в группе сравнения не поддавалось каким-либо закономерностям, в отличие от основной группы, в которой среднее абсолютное значение отдельных кислот имело общие тенденции к увеличению ко 2-му осмотру до нормального уровня, но снижению до исходных значений к 3-му осмотру.
Так, у детей группы сравнения средние абсолютные значения масляной и капроновой кислот не поднимались до нормального уровня и составляли: масляная кислота — 0,864 мг/г во время 1-го осмотра, 0,666 мг/г во время 2-го и 1,0194 мг/г во время 3-го при норме 1,77 мг/г; капроновая кислота — 0,0116, 0,0008 (p В основной группе эти показатели вели себя следующим образом: среднее абсолютное значение масляной кислоты сначала составляло 1,136 мг/г, затем увеличивалось до 1,77 мг/г (p Соотношение ЛЖК в норме составляет 20% (масляная кислота): 16% (пропионовая кислота): 64% (уксусная кислота).
В группе сравнения соотношение во время 1-го осмотра составляло 17,29 : 18,24 : 64,52%; во время 2-го — 18,6 : 20,75 : 60,8%; во время 3-го — 19 : 19,53 : 61,18%, соответственно.
В основной группе соотношение ЛЖК при 1-м осмотре было 18,37 : 21,13 (p В целом лишь у детей основной группы соотношение ЛЖК приходило к норме.
Среднее значение индекса изокислот в группе сравнения в ходе всего исследования составило 0,3005 при 1-м осмотре, 0,2929 — при 2-м, 0,3211 — при 3-м. В то время как у детей основной группы среднее значение индекса изокислот при 1-м осмотре составил 0,4292 (p Рис. 4. Динамика индекса изокислот в основной группе и группе сравнения
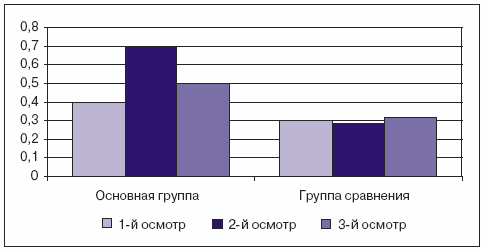
На основании проведенного исследования можно сделать следующие выводы.
- Антихеликобактерная терапия сопровождается развитием антибиотик-ассоциированного дисбактериоза кишечника у большинства пациентов
- Назначение препарата пробиотика, содержащего лиофилизированные штаммы Bifidobacterium infantis v. liberorum, Lactobacillus acidophilus и Streptococcus faecium, снижает риск развития антибиотик-ассоциированного дисбактериоза кишечника
- Эффект препарата пробиотика, содержащего лиофилизированные штаммы Bifidobacterium infantis v. liberorum, Lactobacillus acidophilus и Streptococcus faecium, проявляется клиническим улучшением, нормализацией состава микрофлоры кишечника, а также восстановлением ее метаболической активности
Таким образом, пациентам, получающим антихеликобактерную терапию, рекомендуется параллельное назначение препаратов пробиотиков с целью предотвращения развития антибиотик-ассоциированного дисбактериоза кишечника или уменьшения степени его тяжести.
ЛИТЕРАТУРА
1. Edlund C., Nord C.E. Effect on the human normal microflora of oral antibiotics for treatment of urinary tract infection // J. Antimicrob. Chemoter. — 2000. — V. 46. — 41 p.
2. Ерюхин И.А., Шляпников С.А., Лебедев В.Ф., Иванов Г.А. Псевдомембранозный колит и «кишечный сепсис» — следствие дисбактериоза, вызванного антибиотиками // Вестник хирургии им. И.И. Грекова. — 1997. — Т. 156, № 2. — С. 108–111.
3. Sullivan A., Edlund C., Nord C.E. Effect of antimicrobial agents on the ecological balance of human microflora // Lancet Infect. Dis. — 2001. — V. 1, № 2. — P. 101–114.
4. McFarland L.V. Risk factor for antibiotic-associated diarrhea // Ann. Med. Intern. (Paris). — 1998. — V. 149, № 5. — P. 261–266.
5. Цветкова Л.Н., Щербаков П.Л., Салмова В.С., Вартапетова Е.Е. Результаты биокоррекционной поддержки у детей, получавших антигеликобактерную терапию // Детская гастроэнтерология. — 2002. — С. 482–484.
