Вегетокорригирующее и анксиолитическое действие тофизопама в предклимактерическом периоде
Статьи
Опубликовано в журнале Врач, 2010; 5: 52-57 ИА Грибачева1, Н.Г. Жукова2
1 Новосибирский государственный медицинский университет
2 Сибирский государственный медицинский университет
В предклимактерический период выработка яичниками эстрогена и прогестерона начинает существенно сокращаться. Эстрогены модулируют электрическую возбудимость нейронов, функционирование синапсов и нейрональные морфологические черты. Они способны увеличивать нейрональную пластичность (способность нейронов менять свои функциональные свойства в зависимости от условий среды), что приобретает особую значимость в процессе старения головного мозга [1]. Взаимодействие геномных и негеномных механизмов определяет широкий спектр и многообразие воздействия половых стероидов на основные структуры головного мозга, обеспечивающие интегративные функции и осуществляющие взаимодействие специализированных систем (моторных, сенсорных, вегетативных). Однако с возрастом этот приспособительный механизм регуляции адаптивной деятельности нарушается. Приблизительно в 40-летнем возрасте в организме большинства современных женщин начинаются почти незаметные и неуловимые перемены. Это время и называется предклимактерический периодом.
Изменения гормонального гомеостаза связаны с гормонами яичников и, возможно, с соотношением эстрогена и прогестерона. Возникающий в организме женщины гормональный дисбаланс приводит к ряду неприятных и ярких вегетативно-соматических и болезненных симптомов. Наиболее частыми (у 70% женщин) становятся жалобы на приливы жара, озноб, повышенную потливость, волнение, сердцебиение, гипервентиляционные расстройства, головную боль, апатию, астению. Среди других жалоб, о которых сообщают почти 50% женщин, отмечаются резкая смена настроения, часто подавленное состояние, тревожно-депрессивные мысли, нарушения сна, увеличение массы тела, раздражительность и беспокойство.
Особое значение в предклимактерическом периоде у женщин имеют эмоционально-аффективные расстройства, приносящие много неприятных ощущений и отрицательно воздействующие на качество жизни. Терапия таких расстройств - важная задача неврологов, терапевтов, кардиологов, гинекологов, эндокринологов. Таким образом, эта проблема приобретает междисциплинарный характер. Препаратом выбора, эффективно купирующим психовегетативные расстройства и не обладающим недостатками, присущими типичным бензодиазепинам, может быть бензодиазепиновый транквилизатор Грандаксин (тофизопам) [4].
Главной особенностью тофизопама является место расположения нитрогенной группы. Если у традиционных бензодиазепинов нитрогенная группа находится в положении 1-4, то у тофизопама она расположена в положении 2-3, в связи с чем его обычно обозначают как 2-3-бензодиазепин. Как и все транквилизаторы бензодиазепинового ряда, он оказывает влияние на основной неспецифический тормозной медиатор - ГАМК, что и обусловливает широкий спектр влияний как на эмоциональную сферу (уменьшение тревоги, страха, напряжения), так и на вегетативные функции организма (вегетостабилизирующий эффект) [2]. В то же время, являясь атипичным транквилизатором, тофизопам обладает следующими уникальными свойствами: не развивается физическая зависимость к нему; он не обладает седативными и миорелаксирующими эффектами; не потенцирует действие алкоголя; не ухудшает когнитивные функции (в частности, не нарушает внимание); не обладает кардиотоксическим эффектом (напротив, показано благоприятное его влияние на коронарный кровоток и потребность миокарда в кислороде); оказывает умеренное стимулирующее действие и поэтому относится к группе "дневных" транквилизаторов [3].
Целью настоящего исследования было определение клинической эффективности и безопасности применения Грандаксина в комбинации с базисной терапией при лечении больных с начальными проявлениями артериальной гипертензии (АГ) в предклимактерическом периоде с синдромом тревожных и психовегетативных расстройств. Для этого нами оценены:
влияние Грандаксина на уровень тревожных и депрессивных расстройств у больных с начальными проявлениями АГ в предклимактерическом периоде; психовегетативный статус и показатели ежедневной жизненной активности, а также динамика субъективных и объективных неврологических нарушений у обследованных; селективное анксиолитическое и вегетокорректирующее действие Грандаксина у участвовавших в исследовании больных; безопасность применения препарата Грандаксин при начальных проявлениях АГ в предклимактерическом периоде с синдромом тревожных и психовегетативных нарушений. Работа проведена в рамках открытого несравнительного неконтролируемого проспективного мультицентрового клинического исследования. В ней приняли участие неврологические клиники из 11 городов России: Красноярска, Комсомольска-на-Амуре, Уфы, Хабаровска, Вологды, Самары, Москвы, Санкт-Петербурга, Новосибирска, Томска, Краснодара. В исследование включали женщин 45-50 лет с начальными проявлениями АГ в предклимактерическом периоде с синдромом тревожных и психовегетативных расстройств при следующих критериях: частота и выраженность указанных расстройств, а также нарушение трудоспособности достигают средней и высокой степени (по анамнезу); нерезко выражены головная боль и проявления астенических состояний (по анамнезу); в клинической картине доминируют тревожные расстройства непсихотического уровня; психовегетативные расстройства психофизиологической природы, когнитивные расстройства, которые снижают профессиональную и социальную адаптацию больных; пациенты с АГ I степени согласно классификации Европейского общества гипертонии (ESH) и Европейского общества кардиологов (ESC) 2007 г.: систолическое АД (САД) 140-159 мм рт.ст. и (или) диастолическое АД (ДАД) 90-99 мм рт.ст.; отсутствуют клинические проявления развернутого климактерического синдрома (по данным анамнеза и обследования у гинеколога). Критерии исключения: возраст моложе 45 лет и старше 50 лет; ограничения по каким-либо причинам к приему препарата внутрь; установленный диагноз АГ II и III степени и неконтролируемая АГ к моменту начала наблюдения; наличие выраженного климактерического синдрома (по анамнезу и заключению гинеколога); наличие острой или обостренной тяжелой неврологической и (или) соматической патологии; изменение режима дозирования заместительной терапии гормонами щитовидной железы в течение 4 нед до включения в исследование; тяжелая депрессия; непереносимость Грандаксина (по анамнезу или медицинским документам); выраженная форма ИБС, включая инфаркт миокарда в анамнезе; выраженная сердечная недостаточность и аритмия, включая мерцание предсердий и патологию клапанов сердца; тяжелая форма сахарного диабета; беременность; наличие других клинически значимых (кроме синдрома тревожных, психовегетативных расстройств) неврологических или психических нарушений - таких как рассеянный склероз, опухоль головного мозга, нейроинфекция, дисметаболические поражения базальных ганглиев, нормотензивная гидроцефалия, алкоголизм и пристрастие к употреблению психоактивных веществ, шизофрения, маниакально-депрессивный психоз, униполярное аффективное расстройство, другие психотические состояния, эпилепсия, а также любые другие состояния, которые сопровождаются выраженными когнитивными и эмоционально-аффективными нарушениями. Специальными критериями исключения пациентов из наблюдения были серьезные нежелательные явления в связи с приемом препарата; выявление скрытых заболеваний, которые соответствуют критериям исключения; решение пациентки выбыть из наблюдения; развитие непереносимости к препарату в дозе 50 мг 2 раза в сутки; низкая (<90%) комплаентность пациентки, выражающаяся в нежелании принимать тестируемый препарат; решение врача-исследователя вывести пациента из наблюдения по объективным причинам. Общая продолжительность наблюдения и лечения составила 8 нед (с обследованием больных неврологическими и психологическими методами в начале и в конце лечения). Всего в основной группе обследованы 99 женщин в возрасте 45-50 лет с начальными проявлениями АГ в предклимактерическом периоде с синдромом тревожных и психовегетативных расстройств. В окончательную обработку не вошли 5 пациенток (причина - неполное соответствие критериям включения, некорректное заполнение протоколов). Контрольную группу составили 28 женщин, которым проводилось только базисное лечение. Пациенткам основной группы в дополнение к традиционной гипотензивной, нейрометаболической, сосудистой, дезагрегантной и антиоксидантной терапии был назначен транквилизатор Грандаксин в суточной дозе 100 мг- по 1 таблетке 2 раза в сутки (утром и днем - до 18 ч). Прием каких-либо психотропных препаратов на момент исследования в обеих группах исключался. По окончании терапевтической фазы программы оценивали динамику психовегетативного состояния женщин и фиксировали побочные эффекты лечения. Критериями эффективности считалось изменение в группах неврологического и психовегетативного статуса после 8 нед лечения по сравнению с исходными данными. В начале исследования проводили клинический и неврологический осмотр, запись ЭКГ в покое, компьютерную или магнитно-резонансную томографию (по показаниям), лабораторные исследования (общий анализ крови и мочи, содержание липидов). В динамике (в начале лечения и по его окончании) оценивали неврологический статус и изучали психовегетативный статус. Для оценки психовегетативного статуса использовали: опросник для выявления признаков вегетативных изменений; схему исследования для выявления признаков вегетативных нарушений; вегетативный индекс Кердо; исследование минутного объема крови (по Лилье-Штрандеру и Цандеру); ортоклиностатическую пробу (переход из вертикального положения в горизонтальное); клиноортостатическую пробу (переход из горизонтального положения в вертикальное); пробу с дозированной физической нагрузкой (подъем ног, лежа в горизонтальном положении, на 30-40° - до 10 раз за 3 мин). Тревожно-депрессивные расстройства оценивали с помощью: Госпитальной шкалы оценки тревоги и депрессии (HADS) (предназначена для скринингового выявления тревоги/депрессии у пациентов соматического стационара и амбулаторных больных): 0-7 баллов - норма (отсутствие достоверно выраженных симптомов тревоги/депрессии); 8-10 баллов - субклинически выраженная тревога/депрессия; 11 и более баллов - клинически выраженная тревога/депрессия; Шкалы Монтгомери-Асберга для оценки депрессии (MADRS) (предназначена для быстрой и точной оценки тяжести депрессии и изменения тяжести состояния в результате терапии): 0-7 баллов - отсутствие депрессивного состояния; 8-16 баллов -легкое депрессивное расстройство; 17-27 баллов-умеренное депрессивное расстройство; свыше 27 баллов - тяжелое депрессивное расстройство; Шкалы Гамильтона для оценки депрессии (HARS) (предназначена для объективной оценки тяжести симптомов депрессии, а также их динамики на фоне лечения): 0-7 баллов - отсутствие депрессивного состояния; 8-16 баллов - легкое депрессивное расстройство; 17-27 баллов - умеренное депрессивное расстройство; свыше 27 баллов - тяжелое депрессивное расстройство. Качество жизни пациенток оценивали на основании обобщенных данных о динамике неврологического и психологического статуса. Статистическую обработку результатов проводили с использованием пакета прикладных программ SPSS 11.5 for Windows. В исследовании приняли участие 122 женщины (94 - основная группа и 28 - контрольная). Средний возраст женщин в основной группе составил 48,3±3,2 года, в контрольной - 49,7±4,1 года. Две трети обследованных составили служащие, ИТР и творческие работники, при этом группы по данному показателю достоверно не различались (р>0,05). Уровень образования также был сопоставим: в основной группе высшее и среднее специальное образование имели 89,3%, в контрольной - 85,7%, что объясняло высокую комплаентность при проведении исследования. Обращал на себя внимание тот факт, что только у 54,3 и 57,1% обследованных, соответственно, в основной и контрольной группах имелась устроенная личная жизнь, что, вероятно, отчасти объясняло широкую распространенность психовегетативных и тревожнодепрессивных расстройств. Основными у пациенток обеих групп были жалобы на эмоциональную лабильность, снижение работоспособности, неполноценный сон, повышение АГ, тревогу, апатию, астению, потливость, озноб, учащенное сердцебиение, наличие приливов жара и др., однако динамика жалоб под воздействием лечения существенно различалась. Если в контрольной группе улучшение большинства показателей под воздействием базисной комплексной терапии не достигало статистически значимых значений (рис. 1), то в основной группе по всем показателям была отмечена достоверная положительная динамика (рис. 2). 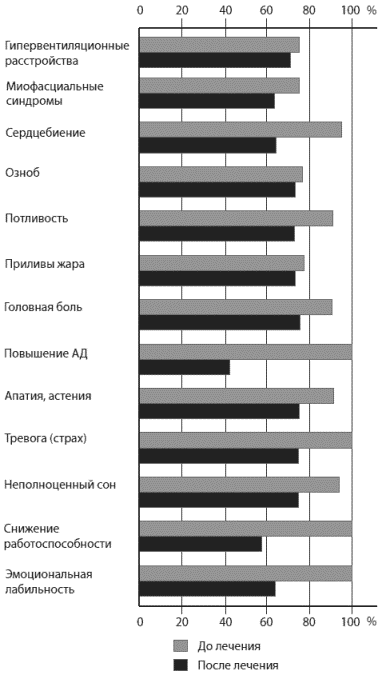 Рис. 1. Динамика клинических проявлений у обследованных контрольной группы
Рис. 1. Динамика клинических проявлений у обследованных контрольной группы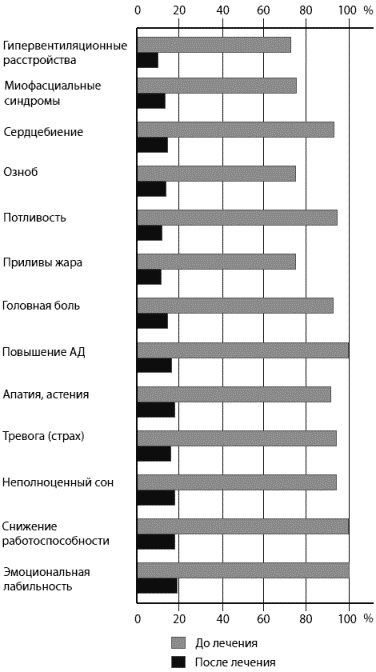 Рис. 2. Динамика клинических проявлений у больных основной группыПоскольку основным критерием включения в исследование было наличие у пациенток пограничной АГ, нами изучена динамика АД в процессе лечения. Как видно из табл. 1, в ходе исследования отмечена тенденция к нормализации АД (как САД, так и ДАД), более выраженная в основной группе. Таблица 1. Показатели САД и ДАД до и после лечения в основной и контрольной группах
Рис. 2. Динамика клинических проявлений у больных основной группыПоскольку основным критерием включения в исследование было наличие у пациенток пограничной АГ, нами изучена динамика АД в процессе лечения. Как видно из табл. 1, в ходе исследования отмечена тенденция к нормализации АД (как САД, так и ДАД), более выраженная в основной группе. Таблица 1. Показатели САД и ДАД до и после лечения в основной и контрольной группах| Показатель | Основная группа | Контрольная группа |
| До лечения | После лечения | До лечения | После лечения |
| САДСР., мм рт.ст. | 138,54±2,21 | 129,94±3,33 | 139,72±3,02 | 135,81±2,94 |
| ДАДСР., мм рт.ст. | 88,21±2,61 | 79,43±1,62 | 88,81±2,92 | 84,33±1,29 |
| ЧСС, уд. в мин | 83,04±1,93 | 69,89±1,81 | 81,84±2,04 | 76,92±2,01 |
Исследование вегетативного обеспечения различных форм деятельности дает важную информацию о состоянии вегетативной нервной системы, так как вегетативные компоненты являются обязательным сопровождением любой деятельности. Регистрацию их мы называем исследованием вегетативного обеспечения деятельности [1]. В клинической физиологии исследование вегетативного обеспечения производится с помощью экспериментального моделирования деятельности. При проведении орто-клиностатической пробы нами выявлены признаки избыточного и недостаточного вегетативного обеспечения. В контрольной группе в начале исследования у 64,3% женщин выявлялись признаки избыточного вегетативного обеспечения; к завершению наблюдения этот показатель изменился несущественно (60,7%). В то же время, в основной группе в начале лечения пациентки с избыточным вегетативным обеспечением составляли 75,5% (больше, чем в контрольной группе), а через 8 нед приема Грандаксина этот показатель уменьшился почти вдвое (42,6%), при этом значительно увеличилось число больных с нормальным вегетативным обеспечением (с 5,2 до 39,4%). По результатам ортоклиностатической пробы (табл. 2) и пробы с дозированной физической нагрузкой (табл. 3) на фоне лечения происходило изменение вегетативного обеспечения в сторону нормализации, причем в основной группе достоверное. Таблица 2. Результаты выполнения ортоклиностатической пробы (М±m)| Показатель | Основная группа | Контрольная группа |
| До лечения | После лечения | До лечения | После лечения |
Исходно:
САД, мм рт.ст.
ДАД, мм рт.ст.
ЧСС, в минуту |
138,54±2,21
88,21±2,61
83,04±1,93 |
129,94±3,33
79,43±1,62
69,89±1,81* |
137,72±3,02
88,81±2,92
81,84±2,0 |
135,81±2,94
84,33±1,29
76,92±2,01 |
При вставании:
САД, мм рт.ст.
ДАД, мм рт.ст.
ЧСС, в минуту |
162,31±8,21
94,27±1,84
96,16±1,92 |
144,26±3,04*
82,63±1,72*
79,34±1,92* |
163,17±2,74
94,84±2,16
97,04±1,70 |
152,22±3,07
88,74±2,64
93,29±2,17 |
При возвращении к исходному положению:
САД, мм рт.ст.
ДАД, мм рт.ст.
ЧСС, в минуту |
147,64±9,33
92,24±1,46
89,12±1,74 |
132,60+2,07*
82,67±2,19
72,14±2,23* |
155,42±2,61
92,68±2,23
88,77±2,14 |
151,14±2,22
90,22±2,41
84,39±2,39 |
*p<0,01Таблица 3. Результаты пробы с дозированной физической нагрузкой (М±m)| Показатель | Основная группа | Контрольпая группа |
| До лечения | После лечения | До лечения | После лечения |
САД, мм рт.ст.:
до пробы
после пробы |
138,54±2,21
162,19±2,61 |
129,94±3,33
142,44±2,64* |
139,72±3,02
161,29±2,21 |
135,81±2,94
154,19±2,91 |
ДАД, мм рт.ст.:
до пробы
после пробы |
88,21±2,61
108,31±2,14 |
79,43±1,62
98,17±1,90 |
88,81±2,92
11,22±3,04 |
84,33±1,29
104,71±2,87 |
ЧСС, в минуту:
до пробы
после пробы |
83,04±1,93
101,14±3,33 |
69,89+1,81*
90,52±2,64 |
81,84±2,04
100,67±3,13 |
76,92±2,01
96,92±3,04 |
*p<0,01Поскольку обеспечение деятельности осуществляется преимущественно эрготропной системой, о состоянии эрготропных препаратов судили по степени отклонения от исходных данных данных. При расчете вегетативного индекса Кердо результаты в обеих группах в начале исследования достоверно не различались (соответственно, 6,9±1,01 и 6,6±0,84; р>0,01), а по его окончании достоверные изменения отмечены только в основной группе (3,2±0,64 и 6,1 ±0,73; р<0,05). Исследование минутного объема крови (по Лилье Штрандеру и Цандеру) показало: в начале исследования при повышении симпатического тонуса в той и другой группе рос и минутный объем. На момент завершения наблюдения показатель в контрольной группе (соответственно, 4984,3±791,7 и 4713,2±815,6 мл/мин) практически не изменился, а в основной наблюдалось изменение в сторону вегетативного равновесия - эйтонии (5115,8+836,1 и4219,1±769,2 мл/мин). При изучении вегетативных нарушений с использованием опросников для выявления субъективных (заполняет пациент) и объективных (заполняет врач) признаков получены следующие результаты. Если учесть, что у здоровых полученная сумма баллов не должна превышать 15, то в начале исследования можно говорить о наличии вегето-сосудистой дистонии у больных как в основной, так и в контрольной группе (соответственно, 46,22±2,39 и 44,70±2,92; р>0,05). К завершению лечения в основной группе этот показатель снизился почти до нормы (16,34±1,17 балла), чего не произошло в контрольной группе (39,80±2,31 балла), хотя и здесь наметилась положительная тенденция. При оценке по схеме исследования для выявления признаков вегетативных нарушений (заполняется врачом) получены аналогичные результаты. При нормальном показателе 25 баллов в начале исследования в основной группе он составил 66,3±2,19 балла, в контрольной - 65,9±3,92 балла (р>0,05), а к моменту его завершения в основной группе отмечены достоверные изменения показателя в сторону нормализации (29,8±1,18 балла) при достаточно высоком его уровне в контрольной группе (59,9±3,27 балла). Средняя длительность тревожно-депрессивных расстройств (предклимактерического периода) составила 3,7±3,0 года; группы достоверно не различались по возрасту больных, длительности заболевания и основному диагнозу. Анализ динамики тревожно-депрессивных расстройств
В начале обследования основная и контрольная группы по уровню тревоги и депрессии достоверно не различались (рис. 3). 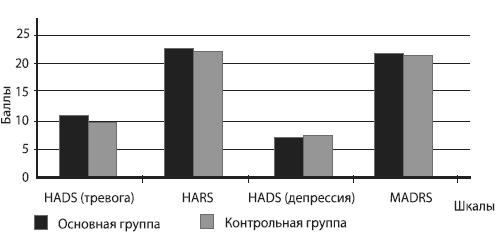 Рис. 3. Уровень тревоги и депрессии у пациентов до лечения При оценке по Шкале HADS оказалось, что до лечения средний показатель тревоги у женщин основной группы составил 10,9±3,7 балла, контрольной - 10,7±4,6, что соответствует субклинической степени выраженности тревоги. Однако в обеих группах несколько превалировали женщины с клинически выраженными тревожными проявлениями. Уровень депрессии по Шкале HADS до лечения составил в основной группы 8,5±4,4 балла, в контрольной - 9,0±3,6, что также соответствует субклиническому уровню депрессии. Однако соотношение женщин в зависимости от выраженности депрессии в группах было различным. Так, в основной группе отмечалось примерно одинаковое распределение пациенток в зависимости от выраженности депрессии, тогда как в контрольной значительно преобладали женщины с клинически выраженными симптомами депрессии и совсем не было пациенток без депрессии. По Шкале MADRS до начала лечения уровень депрессии составил в основной группе 21,1 ±11,4 балла, в контрольной - 19,1 ±9,8 балла, что соответствует умеренному депрессивному расстройству. В каждой группе превалировали женщины с тяжелыми депрессивными симптомами. При оценке депрессии по Шкале HARS оказалось, что у всех обследуемых был умеренный ее уровень (22,6±8,8 балла в основной и 20,3±6,6 - в контрольной группе) при примерно одинаковом распределении женщин в зависимости от выраженности депрессии. К 8-й неделе лечения показатели тревоги и депрессии достоверно снизились в обеих группах (рис. 4), однако степень этих изменений была существенно больше в основной группе.
Рис. 3. Уровень тревоги и депрессии у пациентов до лечения При оценке по Шкале HADS оказалось, что до лечения средний показатель тревоги у женщин основной группы составил 10,9±3,7 балла, контрольной - 10,7±4,6, что соответствует субклинической степени выраженности тревоги. Однако в обеих группах несколько превалировали женщины с клинически выраженными тревожными проявлениями. Уровень депрессии по Шкале HADS до лечения составил в основной группы 8,5±4,4 балла, в контрольной - 9,0±3,6, что также соответствует субклиническому уровню депрессии. Однако соотношение женщин в зависимости от выраженности депрессии в группах было различным. Так, в основной группе отмечалось примерно одинаковое распределение пациенток в зависимости от выраженности депрессии, тогда как в контрольной значительно преобладали женщины с клинически выраженными симптомами депрессии и совсем не было пациенток без депрессии. По Шкале MADRS до начала лечения уровень депрессии составил в основной группе 21,1 ±11,4 балла, в контрольной - 19,1 ±9,8 балла, что соответствует умеренному депрессивному расстройству. В каждой группе превалировали женщины с тяжелыми депрессивными симптомами. При оценке депрессии по Шкале HARS оказалось, что у всех обследуемых был умеренный ее уровень (22,6±8,8 балла в основной и 20,3±6,6 - в контрольной группе) при примерно одинаковом распределении женщин в зависимости от выраженности депрессии. К 8-й неделе лечения показатели тревоги и депрессии достоверно снизились в обеих группах (рис. 4), однако степень этих изменений была существенно больше в основной группе. 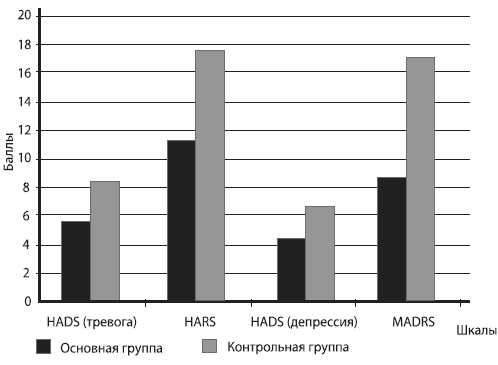 Рис. 4. Уровень тревоги и депрессии у пациентов после лечения Так, после лечения Грандаксином, по Шкале HADS, уровень тревоги достиг в основной группе 6,3±2,8 балла, в контрольной - 9,3±3,7. Таким образом, этот показатель улучшился в основной группе в 1,7 раза и в контрольной - в 1,2 раза. Анализ соотношения наблюдаемых показал уменьшение количества женщин с клинически выраженными тревожными проявлениями в основной группе - в 14,8 раза, в контрольной - в 4,7. На фоне приема Грандаксина существенно (в 2,5 раза) увеличилось число женщин, отрицающих у себя тревожные мысли (в контрольной группе эта категория женщин даже уменьшилась в 5,5 раз). Кроме того, значительно возросло число женщин без депрессии (в 39,4 раза) и уменьшилось - с выраженными ее симптомами (в 2,5 раза); в контрольной группе отмечено увеличение числа больных с выраженными депрессивными проявлениями. Анализ проявлений депрессии по Шкале MADRS показал, что на фоне приема Грандаксина произошло снижение этого показателя в 2,2 раза (до 9,6±8,7 балла), а в контрольной группе изменения были незначительными (с 19,1 ±9,8 до 17,6±6,5 балла). Оценка выраженности депрессии по Шкале HARS зафиксировала снижение этого показателя в основной группе в 1,9 раза (22,6±8,8 до 12,2±7,9 балла до лечения), при снижении показателя депрессии существенных изменений в контрольной группе не было (с 20,3±6,6 до 18,3±8,7 балла). Таким образом, к окончанию лечения тревожно-депрессивных симптомов у женщин с начальными проявлениями АГ в предклимактерическом периоде выраженность депрессии достоверно понизилась как в основной, так и в контрольной группе, однако в большей степени эти изменения были выражены при приеме Грандаксина. Подобная тенденция в группах наблюдалась при оценке тревоги. Исследование переносимости грандаксина
Рис. 4. Уровень тревоги и депрессии у пациентов после лечения Так, после лечения Грандаксином, по Шкале HADS, уровень тревоги достиг в основной группе 6,3±2,8 балла, в контрольной - 9,3±3,7. Таким образом, этот показатель улучшился в основной группе в 1,7 раза и в контрольной - в 1,2 раза. Анализ соотношения наблюдаемых показал уменьшение количества женщин с клинически выраженными тревожными проявлениями в основной группе - в 14,8 раза, в контрольной - в 4,7. На фоне приема Грандаксина существенно (в 2,5 раза) увеличилось число женщин, отрицающих у себя тревожные мысли (в контрольной группе эта категория женщин даже уменьшилась в 5,5 раз). Кроме того, значительно возросло число женщин без депрессии (в 39,4 раза) и уменьшилось - с выраженными ее симптомами (в 2,5 раза); в контрольной группе отмечено увеличение числа больных с выраженными депрессивными проявлениями. Анализ проявлений депрессии по Шкале MADRS показал, что на фоне приема Грандаксина произошло снижение этого показателя в 2,2 раза (до 9,6±8,7 балла), а в контрольной группе изменения были незначительными (с 19,1 ±9,8 до 17,6±6,5 балла). Оценка выраженности депрессии по Шкале HARS зафиксировала снижение этого показателя в основной группе в 1,9 раза (22,6±8,8 до 12,2±7,9 балла до лечения), при снижении показателя депрессии существенных изменений в контрольной группе не было (с 20,3±6,6 до 18,3±8,7 балла). Таким образом, к окончанию лечения тревожно-депрессивных симптомов у женщин с начальными проявлениями АГ в предклимактерическом периоде выраженность депрессии достоверно понизилась как в основной, так и в контрольной группе, однако в большей степени эти изменения были выражены при приеме Грандаксина. Подобная тенденция в группах наблюдалась при оценке тревоги. Исследование переносимости грандаксина
По отчетам пациентов, в целом переносимость препарата, оценена как хорошая. За период наблюдения не было ни одного случая преждевременного прекращения приема препарата. Лишь у 1 пациентки через 3 дня приема препарата в дозе 100 мг/сут появились общее беспокойство, агрессивность. После снижения дозы до 50 мг/сут данные симптомы исчезли. Таким образом, проведенное исследование показало, что применение Грандаксина (тофизопама) у женщин с начальными проявлениями АГ в предклимактерическом периоде приводит к значимому улучшению состояния. Применение препарата в дозе 100 мг/сут (по 1 таблетке 50 мг утром и днем) в течение 8 нед у больных с психовегетативным синдромом в комбинации с базисной терапией (сосудистые, метаболические и ноотропные препараты) достоверно улучшает как показатели эмоционального статуса, так и симптомы вегетативной дисфункции. В основной группе достоверно быстрее и в значительно большей степени улучшалось состояние больных, купировался психовегетативный дисбаланс и повысилось качество сна. В положительную сторону изменялись не только субъективные ощущения, но и объективные показатели, зафиксированные врачом. Грандаксин (тофизопам) в суточной дозе 100 мг/сут показал хороший уровень безопасности и переносимости (не было ни одного случая преждевременного прекращения приема препарата). Литература
1. Вегетативные расстройства. Под ред. A.M. Вейна- М, 1998:748 с.
2. Дкжова Г.М, Саксонова Е.В., Голубев В.Л. Грандаксин в неврологической практике (мультицентровое исследование). Журн. неврол. и психиатр, им. С.С. Корсакова, 2009;9:44-48.
3. Лоуренс Д.Р., Бенитт П.Н. Клиническая фармакология. Т. 2. - М.: Медицина, 1991:700 с.
4. Ронаи Ш, Орос Ф., Болла К. Применение Грандаксина в амбулаторной практике. Венгер. фармакотер. 1975:4-10.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 Рис. 1. Динамика клинических проявлений у обследованных контрольной группы
Рис. 1. Динамика клинических проявлений у обследованных контрольной группы Рис. 2. Динамика клинических проявлений у больных основной группыПоскольку основным критерием включения в исследование было наличие у пациенток пограничной АГ, нами изучена динамика АД в процессе лечения. Как видно из табл. 1, в ходе исследования отмечена тенденция к нормализации АД (как САД, так и ДАД), более выраженная в основной группе. Таблица 1. Показатели САД и ДАД до и после лечения в основной и контрольной группах
Рис. 2. Динамика клинических проявлений у больных основной группыПоскольку основным критерием включения в исследование было наличие у пациенток пограничной АГ, нами изучена динамика АД в процессе лечения. Как видно из табл. 1, в ходе исследования отмечена тенденция к нормализации АД (как САД, так и ДАД), более выраженная в основной группе. Таблица 1. Показатели САД и ДАД до и после лечения в основной и контрольной группах Рис. 3. Уровень тревоги и депрессии у пациентов до лечения При оценке по Шкале HADS оказалось, что до лечения средний показатель тревоги у женщин основной группы составил 10,9±3,7 балла, контрольной - 10,7±4,6, что соответствует субклинической степени выраженности тревоги. Однако в обеих группах несколько превалировали женщины с клинически выраженными тревожными проявлениями. Уровень депрессии по Шкале HADS до лечения составил в основной группы 8,5±4,4 балла, в контрольной - 9,0±3,6, что также соответствует субклиническому уровню депрессии. Однако соотношение женщин в зависимости от выраженности депрессии в группах было различным. Так, в основной группе отмечалось примерно одинаковое распределение пациенток в зависимости от выраженности депрессии, тогда как в контрольной значительно преобладали женщины с клинически выраженными симптомами депрессии и совсем не было пациенток без депрессии. По Шкале MADRS до начала лечения уровень депрессии составил в основной группе 21,1 ±11,4 балла, в контрольной - 19,1 ±9,8 балла, что соответствует умеренному депрессивному расстройству. В каждой группе превалировали женщины с тяжелыми депрессивными симптомами. При оценке депрессии по Шкале HARS оказалось, что у всех обследуемых был умеренный ее уровень (22,6±8,8 балла в основной и 20,3±6,6 - в контрольной группе) при примерно одинаковом распределении женщин в зависимости от выраженности депрессии. К 8-й неделе лечения показатели тревоги и депрессии достоверно снизились в обеих группах (рис. 4), однако степень этих изменений была существенно больше в основной группе.
Рис. 3. Уровень тревоги и депрессии у пациентов до лечения При оценке по Шкале HADS оказалось, что до лечения средний показатель тревоги у женщин основной группы составил 10,9±3,7 балла, контрольной - 10,7±4,6, что соответствует субклинической степени выраженности тревоги. Однако в обеих группах несколько превалировали женщины с клинически выраженными тревожными проявлениями. Уровень депрессии по Шкале HADS до лечения составил в основной группы 8,5±4,4 балла, в контрольной - 9,0±3,6, что также соответствует субклиническому уровню депрессии. Однако соотношение женщин в зависимости от выраженности депрессии в группах было различным. Так, в основной группе отмечалось примерно одинаковое распределение пациенток в зависимости от выраженности депрессии, тогда как в контрольной значительно преобладали женщины с клинически выраженными симптомами депрессии и совсем не было пациенток без депрессии. По Шкале MADRS до начала лечения уровень депрессии составил в основной группе 21,1 ±11,4 балла, в контрольной - 19,1 ±9,8 балла, что соответствует умеренному депрессивному расстройству. В каждой группе превалировали женщины с тяжелыми депрессивными симптомами. При оценке депрессии по Шкале HARS оказалось, что у всех обследуемых был умеренный ее уровень (22,6±8,8 балла в основной и 20,3±6,6 - в контрольной группе) при примерно одинаковом распределении женщин в зависимости от выраженности депрессии. К 8-й неделе лечения показатели тревоги и депрессии достоверно снизились в обеих группах (рис. 4), однако степень этих изменений была существенно больше в основной группе.  Рис. 4. Уровень тревоги и депрессии у пациентов после лечения Так, после лечения Грандаксином, по Шкале HADS, уровень тревоги достиг в основной группе 6,3±2,8 балла, в контрольной - 9,3±3,7. Таким образом, этот показатель улучшился в основной группе в 1,7 раза и в контрольной - в 1,2 раза. Анализ соотношения наблюдаемых показал уменьшение количества женщин с клинически выраженными тревожными проявлениями в основной группе - в 14,8 раза, в контрольной - в 4,7. На фоне приема Грандаксина существенно (в 2,5 раза) увеличилось число женщин, отрицающих у себя тревожные мысли (в контрольной группе эта категория женщин даже уменьшилась в 5,5 раз). Кроме того, значительно возросло число женщин без депрессии (в 39,4 раза) и уменьшилось - с выраженными ее симптомами (в 2,5 раза); в контрольной группе отмечено увеличение числа больных с выраженными депрессивными проявлениями. Анализ проявлений депрессии по Шкале MADRS показал, что на фоне приема Грандаксина произошло снижение этого показателя в 2,2 раза (до 9,6±8,7 балла), а в контрольной группе изменения были незначительными (с 19,1 ±9,8 до 17,6±6,5 балла). Оценка выраженности депрессии по Шкале HARS зафиксировала снижение этого показателя в основной группе в 1,9 раза (22,6±8,8 до 12,2±7,9 балла до лечения), при снижении показателя депрессии существенных изменений в контрольной группе не было (с 20,3±6,6 до 18,3±8,7 балла). Таким образом, к окончанию лечения тревожно-депрессивных симптомов у женщин с начальными проявлениями АГ в предклимактерическом периоде выраженность депрессии достоверно понизилась как в основной, так и в контрольной группе, однако в большей степени эти изменения были выражены при приеме Грандаксина. Подобная тенденция в группах наблюдалась при оценке тревоги. Исследование переносимости грандаксина
Рис. 4. Уровень тревоги и депрессии у пациентов после лечения Так, после лечения Грандаксином, по Шкале HADS, уровень тревоги достиг в основной группе 6,3±2,8 балла, в контрольной - 9,3±3,7. Таким образом, этот показатель улучшился в основной группе в 1,7 раза и в контрольной - в 1,2 раза. Анализ соотношения наблюдаемых показал уменьшение количества женщин с клинически выраженными тревожными проявлениями в основной группе - в 14,8 раза, в контрольной - в 4,7. На фоне приема Грандаксина существенно (в 2,5 раза) увеличилось число женщин, отрицающих у себя тревожные мысли (в контрольной группе эта категория женщин даже уменьшилась в 5,5 раз). Кроме того, значительно возросло число женщин без депрессии (в 39,4 раза) и уменьшилось - с выраженными ее симптомами (в 2,5 раза); в контрольной группе отмечено увеличение числа больных с выраженными депрессивными проявлениями. Анализ проявлений депрессии по Шкале MADRS показал, что на фоне приема Грандаксина произошло снижение этого показателя в 2,2 раза (до 9,6±8,7 балла), а в контрольной группе изменения были незначительными (с 19,1 ±9,8 до 17,6±6,5 балла). Оценка выраженности депрессии по Шкале HARS зафиксировала снижение этого показателя в основной группе в 1,9 раза (22,6±8,8 до 12,2±7,9 балла до лечения), при снижении показателя депрессии существенных изменений в контрольной группе не было (с 20,3±6,6 до 18,3±8,7 балла). Таким образом, к окончанию лечения тревожно-депрессивных симптомов у женщин с начальными проявлениями АГ в предклимактерическом периоде выраженность депрессии достоверно понизилась как в основной, так и в контрольной группе, однако в большей степени эти изменения были выражены при приеме Грандаксина. Подобная тенденция в группах наблюдалась при оценке тревоги. Исследование переносимости грандаксина

