Инновационный метод терапии депрессий у пациентов с ишемической болезнью сердца
Статьи Опубликовано в :«ОБОЗРЕНИЕ ПСИХИАТРИИ И МЕДИЦИНСКОЙ ПСИХОЛОГИИ» »» № 3
В.Э.Медведев1, А.В.Епифанов2
1Кафедра психосоматической патологии РУДН, 2ГКБ № 71, Москва
Резюме
Проведено исследование эффективности и переносимости антидепрессанта с инновационным механизмом действия Вальдоксана при терапии депрессивных расстройств легкой и средней степени тяжести у больных (n=30), страдающих ишемической болезнью сердца.
Получены данные, свидетельствующие о том, что статистически значимая редукция психопатологических нарушений, наряду с улучшением самочувствия у большинства пациентов, при приеме Вальдоксана (25-50 мг на ночь) регистрируется с 14-го дня терапии.
Вальдоксан обладает благоприятным профилем переносимости и безопасности, не оказывает отрицательного влияния на течение ишемической болезни сердца и обеспечивает высокий уровень комплаентности пациентов.
Ключевые слова: депрессия, кардиология, Вальдоксан
Innovation method of depression treatment in patients with coronary artery disease
V.E.Medvedev, A.V.Epifanov
1People's Frienship University, 2State Clinical Hospital №71, Moscow
Summary
The study of efficacy and tolerability of Valdoxane (antidepressant with innovation mechanism of action) in depression of mild and moderate severity was performed in patients (n=30) with coronary artery disease.
Our data suggest that statistically significant reduction of psychopathological symptoms and improvement of patient's condition in most cases are registered from the 14th day of treatment (at the dose of 25-50mg for the night).
Valdoxane has good safety and tolerability profile and doesn't have negative impact on clinical course of coronary artery disease. Valdoxane provides high level of compliance.
Key words: depression, cardiology, Valdoxane.
По мнению экспертов ВОЗ, к 2030-му году депрессия станет самым частым заболеванием на планете [11]. Депрессии относятся к наиболее распространенным психическим расстройствам, наблюдающимся у больных ишемической болезнью сердца (ИБС). По данным J.Strik (2004 г.), частота депрессий среди пациентов с ИБС, наблюдающихся в стационаре, достигает 31%. Т.ВДовженко (2008 г.) отмечает, что симптомы депрессии и тревоги выявляются у 61,45% пациентов с ИБС.
Согласно обобщенным результатам нескольких отечественных исследований, среди больных ИБС доля пациентов с расстройствами депрессивного спектра (от 18 баллов и более по шкале CES-D) достигает 55,7%. Достаточно велика и доля пациентов с психопатологически завершенными депрессивными состояниями (33,1%) [2, 312].
Сходные данные получены в клинико-эпидемиологическом исследовании КОМПАС: среди пациентов общей соматической сети депрессивные расстройства при ИБС диагностируются в 34% наблюдений [5]. В диссертационной работе Т.В.Довженко (2008 г.) также приводятся данные автора о наибольшей частоте и выраженности гипотимии у больных ИБС (до 96% наблюдений).
Сочетание психической патологии и ИБС усложняет диагностику и процесс лечения обоих заболеваний и ухудшает прогноз [13]. Так, ИБС может явиться причиной развития и видоизменения течения депрессии (нозогенные, соматогенные - сосудистые депрессии). В свою очередь депрессии рассматриваются как независимый фактор риска ИБС и острого коронарного синдрома (ОКС), инфаркта миокарда (ИМ), нестабильной стенокардии. Аффективные расстройства могут не только провоцировать обострения ИБС (ОКС), но и оказывать неблагоприятное воздействие на формирование симптоматики и течение соматического страдания (рецидивирующие, продолжительные приступы стенокардии, нарушения сердечного ритма, высокая частота коронарных катастроф). Депрессивные расстройства рассматриваются в качестве важного фактора, повышающего смертность у больных ИБС. Так, при сравнении данных о летальности после ИМ у больных, не обнаруживающих аффективных расстройств, и у лиц, страдающих депрессией, оказывается, что превышение показателя смертности у больных с коморбидными ИМ и депрессиями над аналогичным показателем у пациентов без аффективных расстройств составляет 13,5% через 6 мес и 14% - через 18 мес после коронарной катастрофы [29].
Затруднения, возникающие при назначении психотропных средств для купирования и профилактики депрессивных расстройств у больных ИБС, связаны с неблагоприятным влиянием психофармакотерапевтических препаратов на функции сердечно-сосудистой системы, их взаимодействием с кардиотропными лекарственными формами и, наконец, с возрастом пациентов. Известно, что по мере процесса старения снижается активность цитохромов, определяющая метаболизм лекарственных средств. Одновременно повышается чувствительность рецепторов, причем в первую очередь холинолитических. Соответственно, и у больных ИБС пожилого и старческого возраста может наблюдаться быстрое истощение действия одних психотропных средств и повышение активности других [14]. Терапевтические мероприятия применительно к рассматриваемому контингенту больных требуют особенно тщательного наблюдения, а нередко и назначения дополнительных обследований (коронароангиография, нагрузочные пробы и др.).
Использование в комплексной терапии больных, наряду с кардиотропными препаратами, тимолептиков благоприятно отражается на течении и прогнозе ИБС [8, 13, 16]. При этом на первый план выдвигаются характеристики антидепрессанта, связанные с его переносимостью и безопасностью.
Препаратами выбора для терапии аффективных расстройств у больных кардиологического профиля до настоящего времени считались селективные антидепрессанты последних поколений (СИОЗС, ССОЗС и др.). По эффективности эти тимолептики сравнимы с трициклическими антидепрессантам. Однако наличие у препаратов данной группы спектра нежелательных кардиотропных эффектов (удлинение интервала Q-T, синусовая тахикардия, фибрилляция предсердий и др.) вносит существенные ограничения при назначении их больным с ИБС. Чаще всего назначения врачей общей практики, наиболее часто наблюдающих данную категорию больных, ограничиваются рекомендациями по приему «успокаивающих препаратов» растительного происхождения, ноотропов или витаминов.
Собственные клинические наблюдения и данные литературы [6, 15, 22, 30] указывают на высокую эффективность и хорошую переносимость у широкого круга больных антидепрессанта с инновационным механизмом действия - Вальдоксана (агомелатин). Агомелатин является агонистом МТ1- и МТ2-мелатониновых и антагонистом 5-НТ2С-серотониновых рецепторов [17, 28]. При этом агомелатин не обнаруживает значимого аффинитета к другим центральным рецепторам или мембранным переносчикам моноаминов, а также не влияет на уровень серотонина [25]. Инновационный механизм действия препарата реализуется ресинхронизацией нарушенных циркадианных ритмов1 (определяемых по изменению выраженности депрессивной симптоматики в течение суток), что приводит к нивелированию аффективного расстройства [7, 27, 30].
| 1Циркадианные ритмы генерируются их главным водителем, расположенным в супрахиазматических ядрах (СХЯ) в переднем гипоталамусе [24]. Индивидуальная генетически обусловленная предрасположенность к эндогенной периодичности требует ежедневной 24-часовой синхронизации с помощью экзогенных факторов. Свет является главным синхронизатором для СХЯ [18]. В темноте происходит усиление выработки норадреналина, который запускает синтез мелатонина эпифизом. Свет, воздействуя на эпифиз через рецепторы сетчатки, зрительный нерв и ядра гипоталамуса, прерывает синтез мелатонина, подчиненный суточному, месячному [1] и годовому ритмам освещенности [19, 21]. |
Фармакокинетика агомелатина характеризуется быстрым и хорошим всасыванием (более 80%). Максимальная концентрация вещества в плазме достигается через 1-2 ч после его приема. Концентрация препарата увеличивается пропорционально дозе. Связывание агомелатина с белками плазмы составляет 95%, независимо от концентрации препарата, возраста пациента или наличия почечной недостаточности. Биодоступность составляет около 3% и варьирует в зависимости от эффекта «первого прохождения» через печень и индивидуальных различий параметров активности CYP1A2. Прием пищи (как обычной, так и с высоким содержанием жиров) не влияет ни на биодоступность, ни на скорость всасывания [32]. В организме агомелатин подвергается быстрому окислению, в основном за счет CYP1A2 (90%) и CYP2C9 (10%). Основные метаболиты в виде гидроксилированного и деметилированного агомелатина не активны, быстро связываются и выводятся с мочой (80%).
В литературе широко представлены данные о положительных результатах использования мелатонинергического антидепрессанта Вальдоксана для кратковременной и продолжительной (0,5-2 года) терапии большого депрессивного эпизода [7, 9, 10, 15, 20, 22, 23, 26] у соматически здоровых пациентов. При этом информация относительно применения препарата для лечения депрессивных состояний у больных ИБС в реальных клинических условиях отсутствует. Кроме того, в проводившихся исследованиях практически вне поля зрения оставалось влияние Вальдоксана на основные гемодинамические показатели (уровень артериального давления, частоту сердечных сокращений - ЧСС, проводимость сердца).
Таблица 1. Социально-демографическая характеристика выборки (n=30)
| Характеристика | Число пациентов | |
| Абс. | % | |
| Пол | ||
| муж | 12 | 40,0 |
| жен | 18 | 60,0 |
| Профессиональный статус | ||
| работают/учатся | 23 | 76,7 |
| пенсионеры/инвалиды | 7 | 23,3 |
| Семейный статус | ||
| состоят в браке | 19 | 63,3 |
| одинокие [разведены, вдов(ц)ы] | 11 | 36,7 |
Таблица 2. Распределение пациентов по коморбидной соматической патологии (n=30)
| Диагноз соматического заболевания | Число пациентов | |
| Абс. | % | |
| ИБС, стенокардия I-II ФК, ПИКС | 30 | 100 |
| Гипертоническая болезнь I-II степени | 8 | 26,7 |
| Аритмии (экстрасистолия, тахиаритмия) | 2 | 6,7 |
Цель настоящего открытого психофармакотерапевтического исследования, являющегося частью программы кафедры психосоматической патологии РУДН по накоплению данных о возможности и особенностях использования психотропных препаратов разных классов для терапии психопатологических расстройств у пациентов с соматическими заболеваниями, - изучить терапевтическую эффективность и переносимость антидепрессанта Вальдоксана (агомелатина) при лечении депрессивных расстройств средней и легкой степени тяжести у пациентов с ИБС.
Материалы и методы
В исследование включали больных в возрасте до 65 лет, прошедших обследование и лечение в отделении неотложной кардиологии городской клинической больницы №71 г. Москвы с основным диагнозом - ИБС с/без постинфарктным кардиосклерозом (ПИКС).
Из исследования исключали больных с впервые выявленной ИБС, ОКС (острая и подострая стадии ИМ, нестабильная стенокардия), стенокардией напряжения III-IV функционального класса (ФК), вторичными формами артериальной гипертензии, сердечной недостаточностью или недостаточность кровообращения, клапанными пороками сердца, хроническими формами нарушения ритма и проводимости сердца (жизнеопасными аритмиями, внутрисердечными блокадами), тяжелыми эндокринными нарушениями, печеночной и/или почечной недостаточностью, онкологическими заболеваниями.
До назначения антидепрессанта и после окончания терапии проводили стандартную 12-канальную электрокардиограмму (ЭКГ) в покое, регистрацию ЧСС, систолического и диастолического артериального давления (АД) в положении сидя, ортостатическую пробу, клинический и биохимический анализы крови, коагулограмму. При наличие показаний назначали суточное мониторирование АД и ЭКГ по Холтеру.
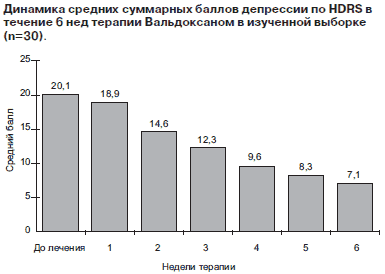
Рис. Динамика средних суммарных баллов депрессии по HDRS в течение 6 нед терапии Вальдоксаном в изученной выборке (n=30).
Вальдоксан назначали в начальной суточной дозе 25 мг на ночь. При недостаточной эффективности препарата с 14-го дня терапии предусматривалась возможность увеличения суточной дозы до 50 мг на ночь. Продолжительность курса терапии составляла 6 нед (42 дня).
Эффективность препарата оценивали еженедельно по шкалам депрессий Гамильтона (HDRS), общего клинического впечатления (CGI) и госпитальному опроснику тревоги и депрессии. В качестве респондеров рассматривали больных более чем с 50% снижением первоначальной суммы баллов.
Безопасность Вальдоксана в отношении сердечно-сосудистой системы оценивали как по спонтанным жалобам, регистрируемым побочным эффектам, так и по динамике ЭКГ, средних значений АД в дневное и ночное время. Для верификации побочных эффектов использовали шкалу побочных эффектов UKU.
Полученный материал обрабатывали с помощью программы «Statistica» («Статсофт, США»). Достоверность различий рассчитывали с помощью теста Колмогорова-Смирнова.
Результаты
Вальдоксан получали 30 пациентов (12 мужчин, 18 женщин; средний возраст 54,6±1,5 года). Полный курс лечения завершили все 30 пациентов, что косвенно указывает на хорошую переносимость препарата.
Социально-демографические характеристики изученных пациентов представлены в табл. 1, коморбидная соматическая патология - в табл. 2.
Все больные получали подобранную антиангинальную терапию и по необходимости антиаритмические и гипотензивные препараты (диуретики, ингибиторы ангиотензинпревращающего фермента - ИАПФ), антагонисты кальция, ß-блокаторы, ацетилсалициловую кислоту, пролонгированные нитраты и др.).
При клинико-психопатологическом обследовании у 25 (83,3%) пациентов диагностированы нозогенные депрессии (депрессивные реакции на совокупность ситуационных психотравмирующих факторов, связанных с соматическим заболеванием), у 3 (10%) - дистимическое расстройство, у 2 (6,7%) - эндогенные депрессии в рамках биполярного аффективного расстройства.
Синдромальная характеристика депрессивных состояний различалась. Наиболее часто наблюдались пациенты с тревожно-ипохондрическими депрессиями (23 случая, 76,7%), в 5 (16,7%) наблюдениях в структуре депрессивного состояния преобладали апатоадинамические проявления и в 2 (6,7%) - аффект тоски.
Ипохондрические представления реализовались мыслями о бесперспективности лечения, неблагоприятном исходе ИБС, ее непоправимых социальных последствиях.
При апатоадинамическом симптомокомплексе пациенты отмечали непривычную для их обычного состояния вялость, подавленность со стеснением в груди и ощущение внутреннего дискомфорта. В 9 (30%) наблюдениях обнаруживалась свойственная большинству витальных депрессий особенность: подверженность суточному ритму (наиболее тягостное самочувствие в утренние часы).
Значительное место в структуре аффективного синдрома занимали соматовегетативные проявления. Как правило, они выступали в виде гомономных (напоминающих симптомы сердечно-сосудистой патологии), полиморфных соматизированных и конверсионных симптомов.
Эффективная терапевтическая доза препарата составила 25 мг у 20 пациентов, 10 пациентов получали Вальдоксан в суточной дозе 50 мг.
Группа респондеров
К моменту завершения исследования клинически значимое улучшение (респондеры по принятым в исследовании критериям) зафиксировано у 24 (80%, средний возраст 54,2±1,3 года) из 30 пациентов, что подтверждается данными других исследователей [6, 7, 10, 20, 23].
У 17 (56,7%) больных отмечена полная редукция (ремиссия) психопатологических расстройств (ремиттеры).
Согласно шкале CGI-I, «существенное улучшение» также зафиксировано у 17 (56,7%), «выраженное улучшение» - у 7 (23,3%) пациентов.
Сходные результаты получены при анализе динамики тяжести психопатологических расстройств по шкале CGI-S. На момент завершающей оценки исходный средний балл CGI-S (4,3 балла) составлял не более 2 у 25 (83,3%) больных.
Выраженное клиническое действие Вальдоксана, установленное по критерию эффективности (шкалы CGI-I и CGI-S), подтверждается достоверной редукцией исходных баллов депрессии шкалы HDRS и Госпитального опросника депрессии и тревоги.
Начало действия Вальдоксана, фиксируемое по снижению баллов психометрических оценочных шкал и опросников, регистрировалось уже на 1-й неделе лечения. Статистически значимое (p<0,05) снижение суммы баллов по HDRS (см. рисунок) отмечалось к концу 2-й недели лечения и становилось более выраженным на фоне дальнейшей терапии с непрерывным улучшением показателей вплоть до 42-го дня (6 нед) терапии (p<0,001). При этом 5 из 24 больных являлись респондерами уже после 2 нед лечения.
В группе респондеров преобладали пациенты с психогенно провоцированными (22 наблюдения), впервые возникшими (19 наблюдений) депрессивными эпизодами, ранее не получавшие психофармакотерапии (23 наблюдения). Средняя длительность депрессии в этой группе пациентов составляла 2,1±0,4 мес.
К окончанию курса терапии наибольшая редукция психопатологической симптоматики зарегистрирована у пациентов с тревожно-ипохондрической (19 из 23 наблюдений) и апатоадинамической (4 из 5 наблюдени4) депрессией.
Клинически действие Вальдоксана проявлялось уменьшением выраженности гипотимии, редукцией депрессивного содержательного комплекса. Больные отмечали улучшение настроения с одновременным уменьшением вялости, подавленности, эмоциональной напряженности, раздражительности. Дезактуализировались ипохондрические идеи. Отмечая восстановление прежнего душевного равновесия, пациенты констатировали, что раньше слишком пессимистично оценивали ситуацию, «неосознанно» преувеличивали опасность ИБС и ее социальных последствий.
Эффективная суточная доза препарата составила 25 мг у 20 (67,7%) пациентов и 50 мг - у 4 (13,3%).
Группа нонреспондеров
К моменту окончания исследования клинически значимое улучшение по принятым в исследовании критериям не отмечено у 6 пациентов (средний возраст 55,1±1,7 года).
Группу нонреспондеров составили 4 пациента с психогенными депрессиями и 3 - с соматогенно провоцированными эндогенными депрессивными эпизодами. У 5 больных в анамнезе выявлялась одна депрессия и более. По этому поводу 3 пациентам проводилось лечение разными группами антидепрессантов (полициклическими, селективными, двойного действия). Средняя длительность актуальной депрессии среди нонреспондеров составила 6,2±0,5 мес.
Менее эффективным 6-недельный курс терапии Вальдоксаном оказался у больных с тоскливой депрессией, а также у 4 пациентов с ипохондрическим депрессивным состоянием. В 2 наблюдениях аффективное расстройство было квалифицировано как дистимия.
Переносимость и безопасность
Установлен благоприятный профиль безопасности препарата. Нежелательные явления на фоне приема Вальдоксана отмечались у 5 пациентов (головокружение - 2 наблюдения, головная боль, дневная сонливость, сухость во рту - по 1 наблюдению) преимущественно в течение первых 2 нед терапии и соответствовали описаниям, приводимым в литературе [7, 9, 26, 30]. В то же время, учитывая наличие у больных сердечно-сосудистой патологии, нельзя исключить влияния соматического заболевания на появление таких нежелательных явлений, как головная боль и головокружение.
В соответствии с целью исследования особое внимание уделялось влиянию Вальдоксана на основные гемодинамические показатели.
На фоне лечения Вальдоксаном в сочетании с кардиотропной терапией регистрировалось достоверное уменьшение частоты возникновения и продолжительности стенокардитических (с 4,7±1,3 раза в сутки 39,1±12,2 мин до 1,1±0,6 раза в день 15,2±6,7 мин) и апофатических (соматоформных, с 2,2±1,1 раза в сутки 12,3±1,5 мин до 0,7±0,2 раза в сутки 7,3±2,4 мин) алгий.
По результатам холтеровского мониторирования (4 наблюдения) можно отметить отсутствие достоверных отличий по показателям суправентрикулярной и вентрикулярной эктопической активности, а также динамики сегмента ST. Также следует подчеркнуть отсутствие динамики интервала Q-T и Q-Tc на фоне приема Вальдоксана, что важно в свете способности ряда традиционных (трициклических) и новых (двойного действия) антидепрессантов удлинять интервал Q-T и вызывать жизнеугрожающие желудочковые тахикардии типа «пируэт» (torsa-des de ро-intes).
На фоне приема Вальдоксана не отмечено явлений ортостатической гипотензии. Отмечено снижение среднего систолического АД в дневное время (с 8:00 до 23:00) с 145±2,1 до 129±2,3 (p<0,05) мм рт. ст., а в ночное (с 23:00 до 8:00) - с 128±112 до 119±2,5 мм рт. ст. (p<0,05). Аналогичные результаты получены и для диастолического АД: в дневное время с 89±1,4 до 73±0,9 мм рт. ст. (p<0,05), а в ночное (с 23:00 до 8:00) - с 76,7±2,1 до 70,7±1,2 мм рт. ст. (p<0,05).
На момент окончания терапии у больных изученной выборки не зафиксировано появлений аритмий и/или внутрисердечных блокад, а также значимых изменений ЧСС.
Отмена Вальдоксана по окончании периода исследования (23 наблюдения) не сопровождалась развитием признаков синдрома отмены (утомляемость, сонливость, головная боль, тошнота, рвота, анорексия, сухость во рту, головокружение, понос, бессонница, тревога, раздражимость, дезориентация, парестезии, потливость).
Обсуждение
В результате проведенного исследования получены достоверные доказательства эффективности Вальдоксана при терапии депрессивных расстройств легкой или средней степени тяжести у больных ИБС.
Препарат обеспечивает редукцию психопатологических состояний у пациентов с соматическими заболеваниями. Его терапевтический эффект реализуется быстро. Статистически значимая редукция психопатологических нарушений, наряду с улучшением самочувствия пациентов, регистрируется с 14-го дня терапии.
При терапии депрессивных расстройств у соматически больных Вальдоксан продемонстрировал благоприятный профиль переносимости и безопасности. Установлено, что у данных пациентов препарат не оказывает отрицательного влияния на течение соматической патологии и обеспечивает высокий уровень комплаентности.
В исследовании не отмечено признаков взаимодействия Вальдоксана в терапевтических дозах (25-50 мг на ночь) с современными препаратами, применяющимися для лечения сердечно-сосудистых заболеваний.
Таким образом, Вальдоксан является эффективным и безопасным препаратом, который может быть рекомендован для терапии депрессивных расстройств легкой или средней степени тяжести у больных ИБС.
Список использованной литературы
