Структурно-модифицирующая терапия неврологических проявлений остеохондроза позвоночника
СтатьиОпубликовано в журнале:
CONSILIUM MEDICUM | ТОМ 12 | № 9
В.А.Гориславец
Военно-медицинская академия им. С.М.Кирова, Санкт-Петербург
Вертеброневрология – междисциплинарная отрасль медицины, объединяющая интересы неврологов, нейрохирургов, ортопедов, терапевтов и других врачей-специалистов, изучающая неврологические заболевания, связанные с патологическими изменениями позвоночного столба.
Оказание качественной медицинской помощи требует от врачей первичного звена медицинской службы определенного объема знаний и практических навыков в диагностическом и лечебном процессе, умения быстро и правильно выбрать нужное решение по каждому конкретному пациенту и по проблеме в целом.
Умение комплексно, быстро и системно оценить состояние нуждающегося в помощи пациента определяет готовность и возможность медицинского работника работать в системе интегративной медицины, которая представляет собой «синтез специализированной и комплексной моделей медицинской помощи». По мнению авторов данной стратегии, Российское здравоохранение должно выйти на качественно новый уровень своего развития. Корни интегративной медицины мы находим в трудах Авиценны, И.М.Сеченова, Н.И.Пирогова, С.П.Боткина, В.М.Бехтерева, И.П.Павлова и других ученых-медиков. Рассматривая российскую систему взглядов на данную проблему, мы видим, что у нас акцент сделан на комплексную (сочетанную) патологию. Сделана попытка по-новому взглянуть «на взаимосвязь и взаимообусловленность патологических процессов при их всевозможном сочетании у пациента» [3].
Клиническая картина вертеброгенных заболеваний нервной системы предопределяется в значительной степени первичной спондилогенной патологией.
Причинами неврологических синдромов могут быть самые разные заболевания и повреждения позвоночника:
- дегенеративно-дистрофические (остеохондроз позвоночника, грыжа межпозвонковых дисков – МПД, спондилез, спондилоартроз и др.);
- травмы (растяжение или разрыв связок, переломы позвонков, травматическая грыжа межпозвонкового диска и др.);
- аномалии развития (врожденный стеноз позвоночного канала, полное или частичное сращение позвонков, спондилолиз, краниовертебральные аномалии, аномалии краниовертебрального стыка, поясничнокрестцового перехода и др.);
- дисплазии позвоночника (идиопатический сколиоз, остеохондропатии, фиброзная дисплазия и др.);
- метаболические заболевания, приводящие к развитию остеопороза (менопаузальный остеопороз, гиперпаратиреоз и др.);
- неинфекционные воспалительные спондилопатии – при диффузных заболеваниях соединительной ткани (ревматоидном артрите), серонегативных спондилоартропатиях (идиопатическом анкилозирующем спондилоартрите, синдроме Рейтера, псориатическом артрите), подагре;
- инфекционные и паразитарные заболевания (спондилиты, эхинококкоз позвоночника);
- нейрогенная спондилоартропатия (при сифилисе, сирингомиелии, сахарном диабете);
- первичные и метастатические опухоли.
В большинстве случаев вертеброневрологическая патология обусловлена дегенеративно-дистрофическими изменениями позвоночника. Благодаря использованию в диагностическом процессе компьютерной и магнитно-резонансной томографии (МРТ) установлено, что болевые синдромы и неврологическая симптоматика связаны не только с патологией межпозвонковых дисков, но и со спондилоартрозом, стенозом позвоночного канала и межпозвонковых отверстий, спондилолистезом, патологией мышц и связок.
Вертеброгенные неврологические синдромы в МКБ10 представлены в основном в подразделе «Дорсопатии» (М40–М54) раздела «Заболевания костно-мышечной системы и соединительной ткани». Неврологические осложнения вертебральной патологии указаны также в разделе «Заболевания нервной системы» (G00–G99).
Дорсопатия включает патологию не только позвоночника, но и мягких тканей спины – мышц, связок и т.д. Важнейшим признаком дорсопатии является дорсалгия. В зависимости от локализации боли выделяют следующие варианты дорсалгий: цервикалгию, цервикобрахиалгию, торакалгию, люмбалгию, люмбоишиалгию, сакралгию, кокцигодинию.
Кроме болевого синдрома, клиническая картина дорсопатии может включать:
- локальный вертебральный синдром, сопровождающийся деформацией, ограничением подвижности или нестабильностью одного или нескольких прилежащих позвоночных двигательных сегментов;
- вертебральный синдром на удалении, сопровождающийся изменением двигательного стереотипа и деформацией, патологической фиксацией выше- и нижележащих отделов позвоночника;
- рефлекторные (ирритативные) синдромы: отраженная боль (цервикобрахиалгия, цервикокраниалгия, люмбоишиалгия и т.д.), мышечно-тонические синдромы, нейродистрофические, реперкуссионные вегетативные нарушения с широким спектром вторичных проявлений (периартропатиями, миофасциальным симптомокомплексом, туннельным синдромом и т.д.);
- компрессионные (компрессионно-ишемические) корешковые синдромы: моно-, би-, мультирадикулярные;
- синдромы ишемии (сдавления) спинного мозга (вследствие грыжи МПД, стеноза позвоночного канала или межпозвонкового отверстия или других причин) [10].
Важное терапевтическое и прогностическое значение имеет дифференциация вертеброгенных симптомокомплексов.
В большинстве случаев вертеброневрологическая патология вызвана дегенеративными изменениями в тканях позвоночно-двигательного сегмента (ПДС) – дугоотростчатых суставах позвонков, в МПД, связках, сухожилиях, мышцах, фасциях [9].
Наиболее частой ее причиной у лиц среднего и пожилого возраста является остеоартроз (ОА) суставов позвоночника, остеохондроз [1, 4].
ОА возникает в результате воздействия механических и биологических факторов, нарушающих равновесие между процессами деградации и синтеза всех компонентов матрикса, прежде всего в суставном хряще [4, 10].
Гиалиновый хрящ межпозвонковых суставов и неповрежденное пульпозное ядро состоят из клеток – хондроцитов, синтезирующих протеогликаны (хондроитин-6-сульфат, кератана сульфат, гиалуроновая кислота и хондроитин-4-сульфат), которые совместно с коллагенами I и II типа входят в состав макромолекул межклеточного хрящевого матрикса. Хрящ МПД, подобно другим тканям, ремоделируется в течение роста и развития, т. е. в нем происходят процессы синтеза и деградации [4].
Метаболизм и структура протеогликанов фиброзного кольца и пульпозного ядра при старении и дегенерации подвергаются значительным изменениям [4, 6, 7].
Развитию спондилоартроза могут способствовать перегрузки задних отделов ПДС (например, в связи с нарушением статики позвоночника) в результате дегенерации и уменьшения высоты МПД при остеохондрозе, при котором происходит нарушение взаиморасположения суставных отростков с повышением нагрузки на них. Кроме того, заболевание может носить первичный характер и сочетаться с ОА периферических суставов [32], при этом процессы дегенерации в суставах принципиально не отличаются [27].
Важным механизмом боли при спондилоартрозе является развитие асептического воспаления. В процессе дегенерации суставного хряща в фасеточных суставах и прилегающих структурах ПДС возникают биохимические и иммунные реакции, которые завершаются формированием асептического нейрогенного воспаления в результате «цитокинового каскада» [10, 41], так как разрушение микроструктуры МПД является активным процессом, скорость которого регулируется цитокинами.
Цитокины являются ростовыми факторами, которые синтезируются в тканях сустава и выделяются в синовиальную жидкость. Они воздействуют на клетки как аутокринные и паракринные факторы. Многие цитокины в небольших количествах необходимы для поддержания гомеостаза [26, 40].
При ОА отсутствуют классические макроскопические признаки воспаления, нет выраженной инфильтрации воспалительных клеток в ткани сустава [30, 32]. Однако такие противовоспалительные цитокины, как интерлейкины (ИЛ) [29], в частности, ИЛ-1β, а также фактор некроза опухоли-α обнаруживаются в синовиальной жидкости больных ОА в повышенном количестве [4, 15, 16, 40].
Под воздействием ИЛ-1 хондроциты резко усиливают синтез металлопротеаз, прекращают синтез протеогликанов и коллагенов хряща [12, 13]. Кроме того, в ответ на стимуляцию ИЛ-1β хондроциты начинают синтезировать ферменты, необходимые для образования оксида азота (индуцибельную синтазу оксида азота) и простагландинов (циклооксигеназу-2) [34, 40].
Другой механизм, участвующий в формировании болевого синдрома, связан с раздражением нервных окончаний – ноцицепторов, локализованных в капсулах дугоотростчатых суставов и компонентах ПДС, в ответ на патологические изменения в них.
В процессе дегенерации диска нарушается синтез хондроцитами макромолекул матрикса, в первую очередь глюкозаминогликанов [4, 7, 8, 10]. Кроме того, увеличивается активность ферментов, участвующих в деструкции матрикса [10]. Использование в лечении хондроитин сульфата предполагает относительную компенсацию протеогликанов макромолекул внеклеточного матрикса [4].
Вопрос о роли хондроитин сульфата в патогенезе ОА обсуждался в литературе. Показано, что хондроциты человека очень чувствительны даже к незначительному снижению содержания хондроитин сульфата [1, 4, 5, 11], а при недостатке хондроитин сульфата нарушается синтез глюкозаминогликанов [4]. Высказано суждение, что нельзя полностью исключить положительные эффекты экзогенного хондроитин сульфата [17].
В данном случае речь идет о структурно-модифицирующей терапии, которая предполагает применение лекарственных средств, которые позволяют не только контролировать симптомы болезни, но и приостанавливать прогрессирование, а в идеале – добиться обратного развития ОА.
С «механистических» позиций введение «готовых к употреблению» единиц протеогликана, таких как хондроитин сульфат, позволяет ускорить синтез матрикса и обеспечить его восстановление.
В исследованиях in vitro хондроитина сульфат действительно захватывался хондроцитами и включался в состав матрикса [14].
В эксперименте отмечено противовоспалительное действие хондроитин сульфата [36], проявляющееся ингибированием протеаз и уменьшением распада матрикса [39, 42].
Хондроитин сульфат является «модификатором биологического ответа», уменьшает патологические проявления в хряще в ответ на нагрузку и повышает способность хряща к самовосстановлению [12, 13].
Целью исследования являлась оценка эффективности и переносимости хондроитин сульфата (Структума) при неврологических проявлениях остеохондроза позвоночника.
По дизайну это было 24-недельное клиническое испытание у больных с неврологическими проявлениями остеохондроза позвоночника. Структум использовался в дозе 1000 мг/сут.
Основной мерой эффективности являлись боль при выполнении повседневной активности. Вторичными мерами эффективности служили качество жизни и эффект последействия [4].
Материалы и методы исследования
Клиническая характеристика больных
Своевременная и точная дифференциальная диагностика неврологических проявлений остеохондроза позвоночника, размера протрузии и грыжи МПД важна для выбора тактики лечения таких пациентов. Идеальна постановка точного диагноза на основании результатов клинического исследования, лучевых методов диагностики [31, 34, 43].
Для реализации целей и задач настоящего исследования на базе клиники нервных болезней Военно-медицинской академии были пролечены 40 больных c вертеброневрологической патологией, получавших в течение 6 мес препарат Структум (хондроитин сульфат). Группа сравнения составила 30 человек, получивших традиционное лечение по поводу неврологических проявлений остеохондроза позвоночника без назначения хондропротекторов. Отбор больных проводился с учетом клинической картины заболевания и данных рентгенологического [31] и нейровизуализационного обследования МРТ [12]. Распределение пациентов представлено в табл. 1.
| Возраст, лет | Мужчины | Женщины | Всего | |||
| количество | % | количество | % | количество | % | |
| 20–30 | — | — | 2 | 5 | 2 | 5 |
| 30–40 | 2 | 5 | 2 | 5 | 4 | 10 |
| 40–50 | 2 | 5 | 2 | 5 | 4 | 10 |
| 50–60 | 9 | 22,5 | 12 | 30 | 21 | 52,5 |
| 60–70 | 1 | 2,5 | 4 | 10 | 5 | 12,5 |
| 70–80 | — | — | 4 | 10 | 4 | 10 |
| Всего... | 14 | 35 | 26 | 65 | 40 | 100 |
Методы обследования
Каждому пациенту было проведено полное клиническое обследование, включающее опрос жалоб, анамнеза, визуальный и мануальный осмотры.
Также исследовались кровь (общий анализ, биохимические показатели), моча. Проводилась рентгенография [31] (при необходимости при корешковых синдромах – МРТ) позвоночника, сопутствующих болезненных крупных и мелких суставов.
Магнитно-резонансное исследование
По результатам МРТ пояснично-крестцового отдела позвоночника определяли степень выраженности рубцово-спаечного эпидурита, мягкотканых нарушений межпозвоночного сегмента [12].
Нами исследовался преимущественно пораженный отдел позвоночника (табл. 2).
| Преимущественно пораженный отдел позвоночника | Мужчины | Женщины | Всего | |||
| количество | % | количество | % | количество | % | |
| Шейный | 5 | 36 | 6 | 23 | 11 | 27,5 |
| Грудной | 2 | 14 | 4 | 16 | 6 | 15 |
| Пояснично-крестцовый | 7 | 50 | 16 | 61 | 23 | 57,5 |
| Всего... | 14 | 100 | 26 | 100 | 40 | 100 |
Результаты МРТ позвоночника
По результатам МРТ-исследования, проведенного 10 (25%) больным с корешковыми синдромами остеохондроза, у всех были выявлены протрузии и грыжи МПД.
В зависимости от выраженности межпозвонковых грыж нами были взяты общепризнанные стандарты их размеров (табл. 3).
| Показатель | Количество | % |
| Отсутствие | 30 | 75 |
| Протрузии (до 0,5 мм) | 8 | 20 |
| Грыжи (более 0,5) | 2 | 5 |
| Всего... | 40 | 100 |
Наличие сопутствующей патологии суставов верхних и нижних конечностей (ОА) представлено в табл. 4.
| Локализация поражения | Количество | % |
| Плечевой сустав | 2 | 5 |
| Локтевой сустав | 2 | 5 |
| Прочие суставы верхних конечностей | 1 | 2,5 |
| Тазобедренный сустав | 4 | 10 |
| Коленный сустав | 4 | 10 |
| Другие суставы нижних конечностей | 1 | 2,5 |
| Без поражения суставов верхних и нижних конечностей | 26 | 65 |
| Всего... | 40 | 100 |
Результаты лечения
При оценке эффективности лечения снижение выраженности болевого синдрома отмечено у 37 (92,5%) пациентов. Все пациенты в период лечения сохраняли обычный режим труда, питания, отдыха.
При оценке эффективности лечения использовали:
- клинико-неврологическое обследование, включая наличие и выраженность болевого рефлекторного и корешкового синдрома;
- визуальную аналоговую шкалу боли (ВАШ) [4, 9];
- поясничный тест-индекс Schober [4];
- шкалу алготонуса Ф.А.Хабирова в модификации А.И.Федина;
- тест наклона и доставания пальцами рук до пола;
- функциональный индекс Лекена (Lequesne).
При неврологическом обследовании у 30 (75%) пациентов выявлен вертеброгенный болевой рефлекторный синдром, а у 10 (25%) – болевой корешковый синдром остеохондроза позвоночника.
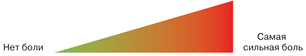
Каждый пациент и врач оценивали выраженность болевого синдрома до и после лечения, а также регистрировали дни уменьшения выраженности боли, которые оценивались по десятибалльной ВАШ, где интенсивность боли увеличивалась с 0 по 10 балл (рис. 1).
| Рис. 1. Визуальная аналоговая шкала. |
 |
Поясничный индекс Шобера исследовали у больных в положении стоя, при этом измеряли расстояние в сантиметрах по средней линии между остистыми отростками Lv-SI позвонков. При максимальном наклоне туловища вперед с фиксированными прямыми ногами производили повторное измерение этого расстояния. Индекс (К) определяли по следующей формуле: К=(10:Δ)×100, где К-индекс (в %), Δ-разница показателей двух измерений выше указанного расстояния. В норме К составляет 40–50%.
Шкала алготонуса состояла из оценки выраженности спонтанной боли, локального гипертонуса и пальпаторной болезненности мышц.
Тест наклона и доставания пальцами пола проводился при максимальном наклоне пациента вперед с вытянутыми руками и фиксированными разогнутыми ногами путем измерения расстояния в сантиметрах от кончика III пальца кисти до пола.
Больные при необходимости получали дополнительное медикаментозное лечение (антибактериальные, противовирусные препараты, сосудистые средства, анальгетики), физиотерапию, массаж, лечебную гимнастику, мануальную терапию.
В целом полученные результаты свидетельствуют о положительном лечебном эффекте хондроитин сульфата (Структума) в отношении основных клинических показателей вертеброневрологических заболеваний как миофасциального болевого рефлекторного симптомокомплекса, так и корешкового синдрома остеохондроза позвоночника.
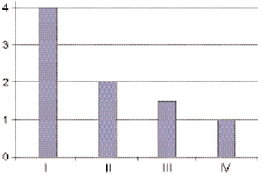
К началу 2-й недели приема препарата у 22 (55%) больных с болевым рефлекторным синдромом отмечено снижение интенсивности болевого синдрома на 1-2 балла, к концу 1-го месяца – у 25 (62,5%) пациентов на 2-3 балла по ВАШ (p
| Рис. 2. Динамика регресса болевого синдрома по ВАШ в течение года с регистрацией в конце 2-й недели (I), 1 (II), 3 (III) и 4 (IV) месяца на фоне приема препарата Структум. |
 |
Гипертонус паравертебральных мышц был пальпаторно снижен по отношению к исходному у всех пациентов, получавших Структум, начиная с 1-й недели приема препарата до окончания курса лечения (6 мес).
Среди лиц с начальными проявлениями венозной церебральной дисциркуляции у 4 (10%) пациентов отмечена стабилизация мозгового кровообращения (p
Вертеброгенный болевой корешковый синдром у 10 (25%) больных регрессировал постепенно на фоне приема Структума и комплексной терапии (лазеротерапия, фонофорез с гидрокортизоном и лидазой, сосудистые препараты, массаж, кинезитерапия и др.).
Снижение интенсивности болевого синдрома на 1 балл произошло у 2 (5%) пациентов (p
Обострений болевого синдрома спондилогенной природы во время приема препарата обследуемыми не выявлено.
Частота побочных эффектов Структума в клинических исследованиях сопоставима с таковой плацебо [17, 19, 28, 33].
У 2 (5%) больных, склонных к кратковременным аллергическим реакциям, отмечена крапивница.
Побочных эффектов Структума при курсовом 6-месячном лечении не выявлено. Общий анализ и биохимические показатели крови оказались в норме.
У 8 (20%) больных отмечено улучшение показателей сывороточного железа, что может явиться хорошим подспорьем использования препарата Структум при железодефицитной анемии.
Наиболее «чувствительным» оказалось исследование белковых фракций крови. Изменение показателей α1, α2, β и γ-глобулинов коррелировало. Повышалось при низких показателях и понижалось – при высоких (т.е. приближалось к нормальным параметрам) во время приема Структума.
Согласно данным рентгенологических исследований и МРТ позвоночника, в динамике отрицательной картины изменений не выявлено ни в ходе обследования, ни в течение заболевания, что указывает на высокое профилактическое действие препарата Структум в указанных дозах.
В период проведения лечения препаратом Структум у пациентов, имеющих сопутствующую патологию крупных и мелких суставов верхних и нижних конечностей (ОА), практически отсутствовали обострения.
Длительность терапевтического эффекта после курса лечения препаратом Структум составила 3-6 мес, в течение которых отмечено отсутствие обострений заболевания.
Заключение
Структум как базисный препарат структурно-модифицирующей терапии может с успехом использоваться при профилактике обострений неврологических проявлений остеохондроза позвоночника с сопутствующей патологией суставов верхних и нижних конечностей [2].
Литература
1. Алексеева Л.И., Архангельская Г.С., Давыдова А.Ф. и др. Отдаленные результаты применения Структума (по материалам многоцентрового исследования). Тер. арх. 2003Ф; 9: 82-6.
2. Гориславец В.А. Антикризисное управление и ценообразование в военной неврологии. СПб.: Изд-во НУ «Центр стратегических исследований», 2010.
3. Гориславец В.А., Лобзин С.В. Пропедевтика в мануальной медицине: Учебное пособие. СПб.: Изд-во НУ «Центр стратегических исследований», 2010.
4. Гориславец В.А. Структум – базисный препарат профилактики и лечения вертеброгенных заболеваний нервной системы. Леч. нервн. бол. 2009; 1 (27): 12.
5. Гориславец В.А. Хондроитин сульфат – базисный препарат профилактики и лечения вертеброгенных заболеваний нервной системы. Вестник Российской Военно-медицинской академии. Материалы IX Всероссийской научнопрактической конференции «Актуальные вопросы клиники, диагностики и лечения больных в многопрофильном лечебном учреждении». Ч. 2. СПб.: РВМедА, 2009; 1 (25): 6267.
6. Гориславец В.А. Оценка клинической эффективности хондропротектора Структум у больных с вертеброневрологической патологией. Поленовские чтения. Тезисы Всероссийской научно-практической конференции. Под ред. проф. В.П.Берснева. СПб.: Изд-во «Человек и его здоровье», 2009; с. 121-2.
7. Гориславец В.А. Базисная терапия вертеброневрологических заболеваний нервной системы с помощью хондропротектора Структум. Ежегодные Давиденковские чтения. Актуальные проблемы клинической неврологии. Материалы Всероссийской юбилейной научно-практической конференции. Под ред. проф. Н.М.Жулева. СПб.: Изд-во «Человек и его здоровье», 2009.
8. Гориславец В.А. Структум – стержень профилактики в вертеброневрологии. Поленовские чтения. Тезисы Всероссийской научно-практической конференции. Под ред. проф. В.П.Берснева. СПб.: Изд-во «Человек и его здоровье», 2010.
9. Мазуров В.И., Беляева И.Б. Применение Структума в комплексном лечении синдрома болей в нижней части спины. Структум 250 мг, 500 мг – хондроитин сульфат натрия. Новые возможности в лечении остеоартроза и остеохондроза. М., 2005; с. 21-4.
10. Шостак Н.А., Аксенова, Правдюк Д.А. и др. Боли в нижней части спины при остеохондрозе позвоночника: опыт применения хондропротективного препарата. Тер. арх. 2003; 8: 67-9.
11. Юнкеров В.И., Григорьев С.Г. Математико-статистическая обработка данных медицинских исследований. СПб.: ВМедА, 2002.
12. Abadie E, Ethgen D, Avouac B et al. (GREES). Recommendations for the use of new methods to assess the efficacy of disease modifying drugs in the treatment of osteoarthritis. Osteoarthritis Cartilage 2004; 12 (4): 263-8.
13. Altman R, Brandt K, Hochberg M et al. Design and conduct of clinical trial in patients with osteoarthritis: recommendations from task force of the Osteoarthritis Research Society. Osteoarthritis Cartilage 1996; 4: 217-43.
14. Bali J-P, Cousse H, Neuzil E. Biochemical basis of the pharmacological action of chondroitin sulfates on the osteoartricular system. Sem Arthritis Rheum 2001; 31: 58-68.
15. Andermann G, Dietz M. The influence of the route of administration on the bioavailability of an endogenous macromolecule: chondroitin sulphate (CSA). Eur J Drug Metab Pharmacokinet 1982; 7: 11-6.
16. Barnhill JG, Fye CL, Williams DW et al. Chondroitin product selection for the glucosamine/chondroitin arthritis intervention trial. J Am Pharm Assoc (Wash DC) 2006; 46 (1): 14-24.
17. Bourgeois P, Chales G, Dehais J et al. Efficacy and tolerability of chondroitin sulfate 1200 mg/day vs chondroitin sulfate 3x400 mg/day vs placebo. Osteoarthritis Cartilage 1998; 6 (Suppl. A): 25-30.
18. Bellamy N, Kirwan J, Boers M et al. Recommendations for a core set of outcome measure for future phase III clinical trial inn knee, hip and hand osteoarthritis. Consensus development at OMERAST III. J Rheumatol 1997; 24: 799-802.
19. Bucsi L, Poor G. Efficacy and tolerability of oral chondroitin sulfate as a symptomatic slow acting drug for osteoarthritis (SYSADOA) in the treatment of knee osteoarthritis. Osteoarth Cart 1998; 6 (Suppl. A): 39-46.
20. Cole TC, Ghosh P, Taylor TKF. Arteparon modifies proteoglican turnover in the intervertebral disk. J Bone J Sure 1998; 70B: 166.
21. Conte A, de Bernardi M, Palmieri L et al. Metabolic fate of exogenous chondroitin sulfate in man. Arzneimittelforschung 1991; 41: 768-72.
22. Conte A, Palmieri L, Segnini D, Ronca G. Metabolic fate of partially depolymerized chondroitin sulfate administered to the rat. Drugs Exp Clin Res 1991; 17: 27-33.
23. Davidson EA, Meyer K. Chondroitin, a new mucopolysaccharide. J Biol Chem 1954; 211 (2): 605-11.
24. Dettmer N. The therapeutic effect of glycosaminoglycan polysulfate (Arteparon) in arthroses depending on the mode of administration [German]. Z Rheumatol 1979; 38: 163-81.
25. Food and Drug Administration. Guidance for industry: Clinical development programs for drugs, devices, and biological products intended for the treatment of osteoarthritis, Washington, DC: FDA; 1999.
26. Group for the Respect of Ethics and Excellence in Science (GREES): Osteoarthritis Section. Recommendations for the registration of drugs used in the treatment of Osteoarthritis. Ann Rheum Dis 1996; 55: 552-7.
27. Hathcock JN, Shao A. Risk assessment for glucosamine and chondroitin sulfate. Regulatory Toxicol Pharmacol 2007; 47: 7883.
28. Jomphe C, Gabriac M, Hale TM et al. Chondroitin Sulfate Inhibits the Nuclear Translocation of Nuclear Factor-kappaB in Interleukin-1beta-Stimulated Chondrocytes. Basic Clin Pharmacol Toxicol 2007; 5.
29. Jordan KM, Arden NK. EULAR Recommendations 2003: an evidence based approach to the management of knee osteoarthritis: Report of a Task Force of the Standing Committee for International Clinical Studies Including Therapeutic Trials (ESCISIT). Ann Rheum Dis 2003; 62: 1145-55.
30. Кellgren JH, Lawrence JS. Radiological assessment of osteoarthrosis. Ann Rheum Dis 1957; 16 (4): 494-502. 31. Lawrence RC, Helmick CG, Arnett FC. Estimates of the prevalence of arthritis and selected musculoskeletal disorders in the USA. Arthritis Reumatism 1998; 12: 264-8.
32. Leeb BF et al. A metaanalysis of chondroitin sulfate in the treatment of osteoarthritis. J Rheumatol 2000; 27 (1): 205-11.
33. Mazzuca SA. Imaging and Osteoarthritis: What Is the Predictive Value? Cur Rheumatol Rep 2003; 5: 27-32.
34. Morreale P, Manopulo R, Galati M et al. Comparison of the anti-inflammatory efficacy of chondroitin sulfate and diclofenac sodium in patients with knee osteoarthritis. J Rheumatol 1996; 23: 1385-91.
35. Pavelka K, Bucsi L, Manopulo R. Double-blind, dose effect study of oral CS 4&6 1200 mg, 800 mg, 200 mg against placebo in the treatment of femoro-tibial osteoarthritis. Litera Rheumatol 1998; 24: 21-30.
36. Pratta MA, Tortorella MD, Arner E. Age related changes in aggregcan glycosylation affect cleavage by aggrecanase. J Biol Chem 2000; 275 (50): 39096-102.
37. Ronca F, Palmieri L, Panicucci P, Ronca G. Anti-inflammatory activity of chondroitin sulfate. Osteoarthritis Cartilage 1998; 6 (Suppl. A): 14-21.
38. Structure-modifying Drug for Osteoarthritis – The Role of Chondroitin 4&6 Sulfate. A report by IBSA, Institut Biochimique SA. Business Briefing: Europian Pharmaco Therapy – January 2003.
39. Sugimoto K, Takahashi M, Yamamoto Y et al. Identification of aggrecanase activity in medium of cartilage culture. J Biochem 1999; 126 (2): 449-55.
40. Uebelhart D et al. Intermittent treatment of knee osteoarthritis with oral chondroitin sulfate: a one-year, randomized, double-blind, multicenter study versus placebo. Osteoarthritis Cartilage 2004; 12 (4): 269-76.
41. Uebelhart D, Thonar EJ, Delmas PD et al. Effects of oral chondroitin sulfate on the progression of knee osteoarthritis: A pilot study. Osteoarthritis Cartilage 1998; 6 (Suppl. A): 3946.
42. Verbruggen G, Goemaere S, Veys EM. Chondroitin sulfate: S/DMOAD (structure/disease modifying anti-osteoarthritis drug) in the treatment of finger joint OA. Osteoarthritis Cartilage 1998; 6 (Suppl. A): 37-8.
43. Verg_s J, Castaneda-Hern_ndez G. On the bioavailability of oral chondroitin sulfate formulations: proposed criteria for bioequivalence studies. Proc West Pharmacol Soc 2004; 47: 50-3.
44. Wasiak R, Kim J, Pransky G. Work disability and costs caused by recurrence of low back pain: longer and more costly than in first episodes. Spine 2006; 31 (2): 219-25.
45. Zhang W, Moskowitz RW. OARSI recommendations for the management of hip and knee osteoarthritis, Part I: Critical appraisal of existing treatment guidelines and systematic review of current research evidence activity. Osteoart Cartil 2007; 15: 981-99.
