Залаин - монография для специалистов.: Клиническая эффективность
Статьи4.9. Клиническая эффективность
Клинические исследования новых лекарственных форм для интравагинального введения сертаконазола преследовали следующие цели:
- Изучить переносимость лекарственных форм препарата, вводимых интравагинально, оценить системную абсорбцию лекарства и выявить возможные побочные эффекты.
- Оценить эффективность препарата при однократном введении.
- Определить эффективность препарата в условиях, сходных с условиями рутинной клинической практики, с помощью многоцентровых рандомизированных контролируемых клинических исследований с использованием для сравнения в качестве стандартов сравнения эталонных лекарственных препаратов (миконазол, эконазол, клотримазол), а также с клинической и микологической оценкой эффективности.
Исследования были проведены в соответствии с современным законодательством по клиническим испытаниям и соответствующими этическими принципами.
Исследование фазы 1. Оценка безопасности сертаконазола в форме 2% крема (однократное и повторное применение) и вагинальной таблетки (однократное введение)
Характеристики изученной популяции
Задачами исследования на здоровых испытуемых являлись изучение местной и системной переносимости вагинальных дозированных форм препарата, оценка длительности нахождения препарата во влагалищных выделениях и количественное определение концентрации вещества в крови и моче после интравагинального введения.
В исследовании участвовали 12 женщин в возрасте от 21 до 35 лет со средним весом 57,3 кг (49-64 кг) и нормальным гинекологическим статусом. Изучавшимися дозированными формами сертаконазола являлись вагинальные таблетки, содержащие 500 мг препарата, и 2% крем. Последний применялся как однократно, так и повторно.
Методика
Данное исследование было двойным слепым перекрестным и контролируемым. В качестве контроля использовались вспомогательные ингредиенты вагинальных таблеток и вагинального крема. Исследование было подразделено на три этапа, которые были четко отграничены и отражены в плане: однократное применение крема, повторное введение крема и однократное использование вагинальной таблетки. Этапы исследования учитывали менструальные циклы испытуемых. Между разными этапами и последовательностями аппликации (активный ингредиент или плацебо) делались перерывы (периоды "отмывания") длительностью от 3 до 18 дней. Это позволяло адекватно устранять какие-либо "помехи" или возможные эффекты наложения (эффект "переноса остатка").
Для изучения безопасности и переносимости вещества, применяемого двумя различными способами, анализировали объективные и субъективные показатели. В течение периода наблюдения было выполнено следующее: больным предлагалось заполнить вопросник (список проверочных вопросов) по местным и системным побочным эффектам; проведение оценки переносимости лечения по 10-уровневой визуальной аналоговой шкале (ВАШ-100 мм; выполнялась испытуемыми); заполнение вопросника по эффектам, которые воспринимались испытуемыми как симптомы (18 пунктов); регистрация физиологических показателей (систолическое и диастолическое артериальное давление, частота сердечных сокращений, температура тела); оценка электрокардиограммы, анализы крови и мочи. Проводилось также тщательное гинекологическое обследование, которое включало изучение состояния слизистой оболочки влагалища, влагалищных выделений, рН среды влагалища, тест Папаниколау и кольпоскопию (это исследование всегда проводилось одним и тем же гинекологом, чтобы обеспечить максимальную воспроизводимость результатов).
Результаты, комментарии и обсуждение
Критерии отбора, установленные планом исследования, ясны и, хотя являются жесткими, вполне подходят для исследования фазы I.
Способ введения лекарства хорошо известен. Он был эффективным и однотипным, поскольку использовались сменные аппликаторы и испытуемые были должным образом проинструктированы. К концу исследования участницы исследования получили 2,1 г сертаконазола (80 г 2% геля и одну таблетку, содержащую 500 мг препарата).
Это исследование было санкционированно Комитетом по этике клинических испытаний госпиталя и Департаментом здравоохранения. Имелись информация для участников исследования и подписанные больными формы о согласии на участие в нем после полученной информации. Таким образом, исследование было проведено в соответствии с международными этическими рекомендациями.
Статистическая обработка данных проводилась независимой организацией (Centro de Calculo del al Universidad Autonoma de Barсelona (U.A.B.) c участием Phase I Unit of the Hospital de la Santa Cruz y San Pablo de Barcelona).
Определение концентраций вещества в моче, отделяемом из влагалища и в плазме крови проводили с помощью ЖХВД с УФ-детекцией. Этот метод позволял определять следующие наименьшие концентрации сертаконазола: 20 нг/мл в плазме крови, 25 нг/мл в моче и 80 нг/мл в отделяемом из влагалища. Процедура забора, обработка образцов, условия хроматографии, стандарты сравнения, реактивы и оборудование соответствовали хорошо известным методикам.
Анализ образцов плазмы крови после аппликации крема (однократное и повторное введение), а также после введения таблетки сертаконазола не обнаружил в них вещества.
Анализ образцов мочи показал наличие в них низких концентраций сертаконазола (х = 0,27% дозы в таблетке). Однако, поскольку это были случайные находки в образцах, полученных в разное время, обнаружение сертаконазола в моче могло быть следствием загрязнения этих образцов содержимым влагалища, чего трудно или невозможно избежать при использовании вагинальной таблетки препарата. Это объясняется фармацевтическим составом вагинальных таблеток сертаконазола, которые содержат вспомогательные ингредиенты, обеспечивающие биоадгезию и задержку содержимого таблеток на слизистой оболочке влагалища. При гинекологических обследованиях, проводившихся после каждого этапа исследования, не было обнаружено существенных изменений слизистой оболочки влагалища и выделений из влагалища (количество и рН). Наблюдавшиеся изменения являлись адаптивными изменениями слизистой оболочки влагалища в соответствии с менструальным циклом. Цитологические исследования не выявили каких-либо отклонений. Результаты лабораторных анализов (плазма крови и моча) были в пределах нормальных физиологических границ как при использовании плацебо, так и при применении сертаконазола. Физиологические показатели также были нормальными, а их колебания соответствовали типичным суточным изменениям.
По результатам ответов испытуемых с использованием визуальной аналоговой шкалы клинически существенных различий между сертаконазолом и плацебо не отмечалось.
Что касается безопасности препарата, о существенных побочных явлениях не сообщалось, и количество эффектов, оцененных больными как симптомы (12 в группе плацебо и 10 в группе сертаконазола), было очень небольшим. О данных симптомах сообщалось при использовании крема, но не таблеток сертаконазола. Эти симптомы (головная боль и сонливость) были умеренно выраженными и спонтанно исчезали.
Таким образом, методы и критерии для оценки побочных явлений соответствовали задачам исследования. Эти методы были хорошо структурированными и обладали высокой обнаруживающей и различающей способностями [57].
В целом, оценка данных по безопасности свидетельствует о том, что сертаконазол при использовании в форме вагинальных таблеток и в виде вагинального крема не подвергается системной абсорбции, безопасен и хорошо переносится:
- По данным, использующим визуальную аналоговую шкалу, не было выявлено каких-либо различий между сертаконазолом, вводимым в обеих лекарственных формах, и плацебо.
- Редко сообщалось о каких-либо эффектах, оцениваемых как симптомы, причем те симптомы, о которых сообщалось (только при использовании крема), возникали также при применении плацебо. Поэтому весьма вероятно, что причиной их возникновения являлась окружающая среда, а не применение препарата.
- Биохимические и гемодинамические показатели были в пределах нормы.
- Состояние слизистой оболочки влагалища, выделения из влагалища, их рН и результаты кольпоскопии не выявили различий между испытуемыми, которые получали сертаконазол или плацебо.
- Концентрации сертаконазола не были обнаружены ни в одном изученном образце плазмы ни у одной испытуемой. Поэтому, если следы вещества в образцах и имелись, они были меньше нижнего предела определения использованной аппаратуры. Невысокие концентрации препарата, обнаруженные в моче, были вариабельными и выявлялись без всякой закономерности.
Возможный терапевтический потенциал, который зависит от концентрации препарата в просвете влагалища, требует клинического подтверждения в исследованиях на больных кандидозом. Концентрации сертаконазола, достигавшиеся в просвете влагалища здоровых испытуемых при использовании обоих лекарственных форм препарата, были высокими и сохранялись длительное время. Это позволяет применять препарат однократно. Заслуживает внимания тот факт, что вагинальная таблетка обеспечивала создание значительно более высокой концентрации препарата, чем крем, как через 24, так и через 28 часов после аппликации. Концентрации препарата во влагалище, как при использовании крема, так и при применении таблетки, были значительно выше, чем минимальные ингибирующие концентрации (МИК) и фунгицидные концентрации сертаконазола по данным исследований in vitro в отношении C. albicans, C. glabrata и других грибов, не относящихся к роду Candida. Эти данные свидетельствуют о том, что, с практической точки зрения, разовое введение препарата может быть столь же эффективным, как по крайней мере 3-дневное лечение. Это обстоятельство добавляет преимущества сертаконазолу, уменьшая вероятность недисциплинированности пациенток в исполнении предписаний врача. Последнее является главной причиной неудачи лечения при данном способе терапии [58].
План и исполнение исследования соответствуют критериям исследования фазы I (начальный этап клинической фазы изучения препаратов). Оно адекватно определяет клиническую безопасность и потенциальную эффективность исследованных лекарственных форм сертаконазола. Исследование проводилось на здоровых испытуемых, а не на больных, что соответствует международным рекомендациям по клиническим испытаниям. Это устраняет влияние модифицирующих факторов, связанных с болезнью, возможные этические проблемы или отклонения от плана исследования из-за необходимости дополнительной медикаментозной терапии, которая может повлиять на результаты [59].
Большинство международных рекомендаций касается лекарственных средств, действующих системно, тогда как указаний по плану проведения оценки объективной и субъективной переносимости новых противогрибковых средств для интравагинального применения очень мало.
Гинекологические обследования и различные тесты, проведенные в данном исследовании, обеспечили получение ценных сведений о местной переносимости, а вопросники по побочным эффектам дали информацию о системной переносимости и безопасности лекарственных форм препарата. Определение концентраций вещества в плазме крови и просвете влагалища позволило оценить фармакокинетику сертаконазола при интравагинальном введении.
4.9.1. Гинекологические клинические испытания
Клиническое изучение
Оценивались результаты клинических исследований, проведенных для регистрации вагинальных лекарственных форм сертаконазола (вагинальные крем, таблетка и суппозиторий). В этих исследованиях приняли участие 1109 больных. 585 женщин получали лечение различными вагинальными дозированными формами сертаконазола. Число наблюдений увеличивается почти до 1400, если добавить больных, участвовавших в исследованиях других вагинальных дозированных форм препарата, в которых около 800 женщин получали лечение сертаконазолом в той или иной лекарственной форме.
Все оцениваемые исследования проводились в соответствии с правилами, регулирующими клинические испытания, и были одобрены Комитетом по этике клинических исследований и Главным управлением по продуктам фармации и медико-санитарной помощи. Эти организации в основном принимают во внимание этические и научные стандарты, рекомендованные современными инструкциями.
4.9.2. Исследования фазы III
Оценка эффективности и безопасности однократного применения Сертаконазола (вагинальной таблетки 500 мг) в сравнении с клотримазолом (вагинальная таблетка 500 мг) у больных с вульвовагинальным кандидозом
Место проведения. Отделения акушерства и гинекологии, многоцентровое клиническое исследование в Испании.
Больные. 582 больных (возраст 33±9 лет) были включены в это многоцентровое рандомизированное двойное слепое контролируемое клиническое исследование с использованием параллельных групп. 49,5% (288) больных получали сертаконазол, остальные (294) -клотримазол. Оба препарата использовали в форме вагинальных таблеток по 500 мг. Амбулаторные больные получали лечение в больницах и ведущих медицинских центрах или в обычных клиниках.
Клинический диагноз был подтвержден микологическими анализами (микроскопия и культура).
Исследование включало три посещения (дни 0, 7 и 14), во время которых проводились оценка изменений клинических признаков и симптомов (вульварных, вагинальных или цервикальных), изучение влагалищных выделений, микроскопический анализ (свод влагалища) и тестирование на культуру.
Терапевтическая эффективность. Клинический результат через 7 дней был лучше при применении сертаконазола (36,4%), чем при использовании клотримазола (30,9%).
При посещении через 14 дней полное клиническое излечение было достигнуто у 90,2% пациенток, получавших сертаконазол, и 86,2% пациенток, получавших клотримазол (Рис. 14).
Микробиологическое излечение наступало чаще в группе сертаконазола, чем в группе клотримазола (Рис. 15).
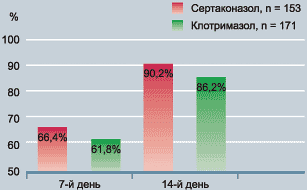 |
Рисунок 14. Процент клинического выздоровления на 7 и 14 день |
Безопасность. Результаты исследования свидетельствуют о хорошей безопасности обоих препаратов. Местные побочные явления были преимущественно легкими или умеренными, причем их трудно было отличить от симптомов заболевания. Наиболее частыми побочными явлениями в обеих группах являлись зуд и эритема. Сообщалось также о жжении, боли, повышенной чувствительности, отеке, покраснении, белях и мацерации. Сертаконазол превосходил клотримазол по способности уменьшать зуд и эритему в области вульвы и шейки матки, но это различие между препаратами не было статистически достоверным.
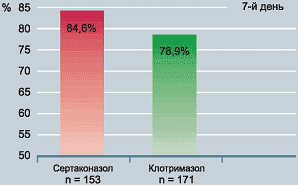 |
Рисунок 15. Процент отрицательных результатов общей микроскопии на 7 день |
Отмечалось небольшое количество системных нежелательных эффектов (головная боль, сонливость, тошнота, запор, диарея). Ни один из них не был выраженным, и ни один из исследователей не отнес их к эффектам, связанным с лечением.
Переносимость лекарственной формы сертаконазола была оценена как хорошая или очень хорошая 88% специалистов и 91% больных (Рис. 16).
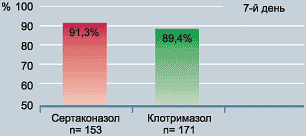 |
Рисунок 16. Процент хорошей и очень хорошей переносимости |
План и качество исследования. План исследования был типичным для испытания, целью которого является воспроизведение условий, сходных с таковыми в обычной клинической практике, за исключением слепого контроля и рандомизации больных, что важно для исключения необъективности оценок.
Из существующих препаратов клотримазол признан эффективным и безопасным препаратом для лечения кандидоза и считается хорошим эталоном для сравнительных исследований [60,61,62].
Критерии для оценки эффективности являлись объективными (микроскопия и культура). Кроме того, использовалось адекватное клиническое обследование.
Расчет величины популяции больных оправдан и удовлетворяет поставленным задачам. Критерии отбора больных соответствуют критериям, обычно используемым в клинических исследованиях, посвященных оценке эффективности и безопасности препаратов при этом заболевании. Анализ данных, тесты для их статистической обработки и возможности исследования описаны соответствующим образом. Данные статистически обрабатывались в Муниципальном институте медицинских исследований Барселоны.
Безопасность оценивалась с помощью вопросника для выявления нежелательных явлений. В нем отражены сведения о начале появления, длительности и выраженности нежелательных явлений, а также об их связи с применением лекарственного вещества. Последнее оценивалось с помощью алгоритма на причинную связь.
План исследования предусматривает наличие информационного листка для больных, подписанной больными формы о согласии на участие в исследовании и санкционирование исследования Комитетом по этике и Главным управлением по продуктам фармации и медико-санитарной помощи (no. 90/163. 1-14).
Сравнительное исследование терапевтической эффективности 2% вагинального крема сертаконазола и 2% вагинального крема миконазола у больных с вульвовагинальным кандидозом
Место проведения. Отделения акушерства и гинекологии. Многоцентровое клиническое исследование в Испании.
Больные. Двойное слепое контролируемое исследование на 456 больных с диагнозом вульвовагинальный кандидоз, подтвержденным выделением культуры гриба из влагалищных выделений. У 226 из них лечение проводили сертаконазолом. Сертаконазол и миконазол применяли в виде вагинального крема, который вводили 1 раз в день в течение одной недели. Клиническое, микроскопическое и микробиологическое исследования проводили в конце периода лечения, а также через 3 дня и 14 дней после его окончания.
В начале исследования различий между группами больных по таким параметрам, как возраст, вес, рост, сопутствующие заболевания, методы контрацепции, дополнительное лечение, не было. Одна больная из группы сертаконазола и шесть больных из группы миконазола были исключены из исследования из-за несоответствия критериям отбора (пять пациенток принимали антибиотики, у одной возникло интеркуррентное заболевание, и одна применяла неподходящее местное лечение). Исходный тест на культуру был отрицательным у 10 больных в группе сертаконазола и у 11 больных в группе миконазола. Эти больные были исключены из оценки эффективности терапии.
Терапевтическая эффективность. Излеченными по данным микологического тестирования через 3 дня после окончания терапии были 83,3% больных, получавших сертаконазол, и 84,1% больных, применявших миконазол. Относительное количество больных, у которых было достигнуто клиническое и микологическое излечение, при использовании сертаконазола и миконазола составляло соответственно 44,1% и 41,8%. Сходные результаты для обоих вариантов лечения были получены и по частоте рецидивов, которые отмечались менее чем у 3% больных.
Безопасность. Местная переносимость была удовлетворительной у 90% больных обеих групп. У больных, получавших лечение сертаконазолом, побочные явления отмечались реже (7,9%), чем у больных, применявших миконазол (11,3%) (Рис. 17).
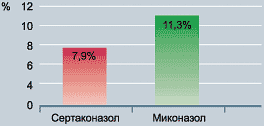 |
Рисунок 17. Процент побочных явлений при приеме сертаконазола и миконазола |
Изменений гематологических и биохимических показателей, а также показателей функции печени, что могло бы указывать на системное действие препаратов, не было обнаружено.
План и качество исследования. Использовались объективные диагностические критерии (тестирование культуры, прямое микроскопическое исследование). План исследования (контролируемое, рандомизированное, двойное слепое) и его осуществление соответствовали достижению поставленных целей. Эффективность терапии оценивалась подходящими структурированными методами, а для выявления причинной связи побочных эффектов с лечением использовался алгоритм Karch-Lasagna.
Размер выборки был адекватно рассчитан, и количество включенных в исследование больных удовлетворяло исходным статистическим требованиям. Статистическая обработка данных проводилась независимой организацией (Clinical Pharmacology Department of the Instituto Catalan de Farmacologia, U.A.B. Barcelona).
Использование в качестве препарата сравнения миконазола и его дозированной формы вполне оправданы, поскольку эффективность (51-88%) и безопасность этого лекарственного средства доказаны в клинических исследованиях [63].
Больные были проинформированы о характере исследования, и до включения в него от больных было получено подписанное ими согласие. Исследование было санкционировано Комитетами по этике участвующих центров и Департаментом здравоохранения (NO. 91/67.1-8).
Многоцентровое двойное слепое рандомизированное контролируемое сравнительное исследование эффективности и безопасности сертаконазола и эконазола (Gyno-Pevaril®) в форме вагинальных суппозиториев с длительным высвобождением препаратов при лечении вагинального кандидоза
Место проведения. Отделения акушерства и гинекологии. Многоцентровое клиническое исследование во Франции.
Больные. Это было многоцентровое двойное слепое рандомизированное контролируемое исследование Фазы III с использованием параллельных групп. В исследовании участвовали женщины, лечившиеся амбулаторно по поводу вульвовагинального кандидоза с исходным положительным тестом на культуру. Исследование включало максимально 4 посещения (дни 0, 7, 14, 37 или 44), во время которых проводились физические и гинекологические обследования, а также микробиологический анализ. Если излечение не достигалось, больным вводили второй суппозиторий. В этом случае клиническое и микологическое обследование проводили через неделю (на 14-й день). Все пациентки обследовались через 5 недель после введения последнего суппозитория (37-й или 44-й дни). Оценивались микологические и клинические показатели, а также показатели безопасности.
В исследовании участвовали 369 больных (возраст 32±0,55 лет), 183 из которых (49,6%) получали сертаконазол, а 186 (50,4%) -эконазол. Отрицательный исходный результат исследования на культуру был у 59 больных (у 33 в группе сертаконазола и у 26 в группе эконазола). Эффективность лечения была оценена у 310 больных (150 из группы сертаконазола и 160 из группы эконазола). Возбудителем заболевания у 95% больных являлась C. albicans. Обе группы больных были сходны по демографическим, клиническим и терапевтическим характеристикам, за исключением дизурических явлений и лечения антибиотиками. Последние различия не влияли на оценку эффективности и безопасности лечения.
Восемь больных не явились на обследование после лечения (пятеро в группе сертаконазола и трое в группе эконазола). Одна больная (группа эконазола) была исключена из исследования по причинам, не связанным с исследованием, а 11 больных выбыли из исследования по причинам, связанным с его планом (в группе сертако-назола: двое в связи с излечением и трое из-за неэффективности терапии; в группе эконазола: двое в связи с излечением и пятеро из-за неэффективности лечения). Ни одна больная не выбыла из исследования из-за возникновения побочных явлений.
Терапевтическая эффективность. Отрицательный результат теста на культуру был у 70,8% больных после однократного введения вагинального суппозитория с сертаконазолом и
у 64,7% больных, у которых использовали суппозиторий с эконазолом (Рис. 18).
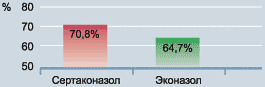 |
Рисунок 18. Процент отрицательных результатов на культуру |
Частота клинического излечения у больных, получавших лечение сертаконазолом или эконазолом, составляла соответственно 71,6% и 64,2% (Рис. 19).
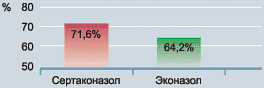 |
Рисунок 19. Частота клинического излечения при приеме сертаконазола и эконазола |
50 больных в группе сертаконазола и 56 больных в группе эконазола получили второй вагинальный суппозиторий. У этих больных микроскопическое исследование дало отрицательный результат в 94% случаев в обеих группах.
Прямое микроскопическое исследование, проведенное через один месяц после окончания лечения, дало отрицательный результат у 76,6% больных в группе сертаконазола и у 74,5% больных в группе эконазола. Тест на культуру был отрицательным у 64,5% больных, получавших сертаконазол, и только у 54,3% больных, лечение которых проводили эконазолом (Рис. 20).
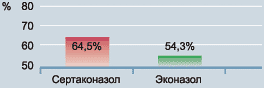 |
Рисунок 20. Процент отрицательных результатов на культуру через месяц после окончания лечения |
Частота клинического излечения составляла 65% при лечении обоими препаратами. Частота излечения у женщин, получивших лечение одним суппозиторием сертаконазола (67,4%), была выше по сравнению с таковой при использовании одного суппозитория эконазола (59%). Число рецидивов заболевания у больных, получавших сертаконазол, было меньшим, чем у женщин, использовавших эконазол (р <0,05) (Рис. 21).
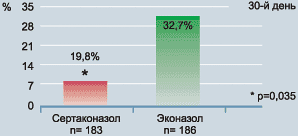 |
Рисунок 21. Процент рецидивирования на 30 день |
В целом, оценка эффективности была очень хорошей, поскольку эффективность была оценена как плохая только у 8,2% больных в группе сертаконазола и у 12,2% больных в группе эконазола.
Безопасность. Переносимость лечения обоими препаратами была оценена как хорошая больными и исследователями.
Менее часто местные побочные явления отмечали при использовании сертаконазола (8,7%), чем при применении эконазола (13,4%), однако это различие не достигало уровня статистической достоверности. Наиболее частыми нежелательными эффектами были зуд и чувство жжения, возможно обусловленные противогрибковым действием препаратов. Системные побочные эффекты (боли в тазовой области, мигрень, тошнота, рвота, генерализованный зуд, диарея и дискомфорт в области желудка) отметили шесть больных. Ни один из этих эффектов не был оценен, как имеющий четкую причинную связь с лечением.
План и качество исследования. В испытании участвовали более 79 исследователей в 50 центрах Франции. Исследование было проведено по стандартам GCP и включало 369 больных.
Выбор эталонного препарата (эконазол) был обусловлен тем, что это лекарственное средство широко используется во Франции при вульвовагинальном кандидозе в режиме однократного применения.
Критерии включения больных в исследование и исключения из него соответствовали, насколько это возможно, имитации условий обычной клинической практики. Популяция больных имела нормальный диапазон факторов риска.
4.9.3. Соотношение между положительным результатом и риском интравагинального применения сертаконазола
В клинических исследованиях, проводимых по правилам, определяется соотношение между успехом применения препарата и риском его использования при определенном способе введения. Это базируется на:
(а) Плане исследований:
- поисковые и направленные исследования (рандомизированные, двойные слепые с использованием параллельных или перекрестных групп);
- многоцентровые исследования. Три исследования фазы III должны быть проведены в различных центрах с широкой географией;
- контролируемые исследования с использованием эталонных препаратов (клотримазол, миконазол и эконазол).
(б) Критериях:
- четко определенные критерии включения в исследования и исключения из них, являются ли они рекомендованными при оценке новых препаратов для лечения вагинальных инфекций;
- оценка результатов: микроскопия, культура, клинические признаки и симптомы;
- переносимость и безопасность: список проверочных вопросов, открытые вопросы по побочным явлениям, эффекты, оцениваемые как симптомы, визуальные аналоговые шкалы, анализы крови и мочи.
(в) Исследуемой популяции:
- здоровые испытуемые и больные вульво-вагинальным кандидозом;
- возраст, локализация, динамика заболевания во времени и лечение, соответствующее рутинной клинической практике;
В целом результаты подобных исследований представляются точными и выявляют хорошую корреляцию между данными об эффективности, полученными с помощью микроскопических, микробиологических и клинических обследований.
Сертаконазол, применявшийся в любых вагинальных формах (крем, таблетки или суппозитории), был столь же эффективен, как эталонные препараты, а по некоторым показателям (клиническое улучшение или излечение, частота рецидивов после лечения) превосходил их. Во всех контролируемых исследованиях имелась тенденция к превосходству сертаконазола над другими препаратами. Важно отметить, что сертаконазол проявлял эффективность у больных с характеристиками, отличавшимися от основной группы пациенток (возраст от 18 до 65 лет, вульварная, вагинальная или вульвовагинальная локализация инфекции, возбудитель С. albicans или не albicans). Эта эффективность проявлялась в несколько первых дней лечения значительным ослаблением клинических проявлений и симптомов заболевания, а также отрицательными результатами первого микробиологического тестирования. Эффективность препарата доказывали длительные повторные отрицательные результаты микробиологического анализа, а также низкая частота рецидивов (исследования через 7, 14 и 28 дней после лечения). Быстрота развития эффекта сертаконазола благоприятствует его использованию больными, поскольку это важно для соблюдения ими режима лечения.
Было показано, что вагинальное введение сертаконазола является безопасным. Ни в одном клиническом исследовании применение препарата в любых дозированных лекарственных формах не было прекращено из-за побочных явлений. Не наблюдалось также изменений в анализах крови. Основные побочные явления были неспецифичными, и ни у одной больной их причинная связь с использованием препарата не была установлена. Местная переносимость сертаконазола была хорошей. Сообщалось об очень небольшом количестве местных нежелательных эффектов, к числу которых относились зуд, чувство жжения и эритема. Хотя статистически достоверных различий в двух исследованиях не наблюдалось (однократное введение препарата или повторное применение в виде крема в течение 7 дней), на 4% меньше местных побочных явлений отмечалось при использовании сертаконазола, чем при применении эталонных лекарственных средств.
Переносимость и безопасность сертаконазола определяют выполнение больными предписаний врача при лечении препаратом, а поэтому и хороший эффект терапии, снижающий в конечном счете ее стоимость.
Эти данные свидетельствуют о том, что сертаконазол при интравагинальном применении является ценной альтернативой другим препаратам, поскольку при его использовании возможны безопасные и эффективные варианты лечения, превосходящие по некоторым параметрам таковые для других лекарственных средств.
4.9.4. Полный анализ
Эффективность. Всего 1109 женщин (здоровые испытуемые и больные) приняли участие в изучении крема, таблеток и суппозиториев. 585 из них получали сертаконазол в той или иной лекарственной форме. Данные по эффективности были получены при клинических исследованиях вагинальных суппозиториев во Франции, в которых участвовали 369 больных, 183 из которых получали сертаконазол.
Контрольная группа больных получала лечение стандартными препаратами, что обеспечивает достоверность при сопоставлении результатов. В исследования были отобраны больные со сходными характеристиками с целью воспроизводимости данных по эффективности и безопасности.
Исследование фазы II подтвердило активность препарата, показанную в доклинических испытаниях. При однократном использовании в форме вагинальной таблетки сертаконазол проявлял высокую эффективность (частота микологического излечения через 7 и 14 дней соответственно 80% и 90%). Препарат устранял также признаки и симптомы кандидозной инфекции у 90% больных с поражениями в области вульвы и у 70% больных с поражениями влагалища.
Эффективность препарата подтвердили исследования фазы III, проведенные на большом количестве больных. Частота клинического излечения составляла 40% через несколько дней после введения таблетки, а в дальнейшем увеличивалась до 80%. Излечение по данным микологического исследования отмечалось более чем у 80% больных. Это различие в результатах терапии было обусловлено жесткими критериями для оценки клинического излечения. Из оценки эффективности терапии исключались пациентки с положительным анализом на культуру, но без симптомов заболевания, а также больные с симптомами заболевания, но с отрицательными результатами анализа на культуру.
Важным представляется выбор препарата сравнения. Клотримазол и миконазол являются общепризнанными средствами для местного применения, широко используемыми в США с 80-х годов. В сравнительных клинических исследованиях, продолжавшихся 10-14 дней, клотри-мазол и миконазол показали превосходную эффективность, обеспечивающую большую частоту излечений по сравнению с нистатином (70-80%). Эта высокая эффективность препаратов отмечалась даже при лечении, продолжавшемся меньше 14 дней (длительность лечения, рекомендованная при использовании нистатина). В таблице 10 представлены результаты об эффективности противогрибковых средств при вагинитах по данным некоторых опубликованных клинических исследований [64].
Ни в одном из проведенных исследований сертаконазол по эффективности не уступал препаратам сравнения (ни при определении статистической достоверности различий, ни при простой оценке этих различий). В целом, небольшое количество больных выбыло из исследований из-за неэффективности препарата.
Другим важным достоинством сертаконазола по данным клинического и микологического обследования является длительное сохранение его эффекта. Число рецидивов после лечения препаратом было небольшим, а в исследовании с эконазолом было достоверно меньшим, чем при использовании препарата сравнения. Во всех исследованиях для оценки клинической и микологической эффективности препаратов использовали адекватные периоды времени (7-14 дней).
Достоверные различия между видами терапии по частоте возникновения рецидивов выявлялись только при длительном после-лечебном наблюдении. В этом случае проявлялось преимущество сертаконазола. При более коротких периодах наблюдения после окончания терапии такие различия невозможно обнаружить. Для подтверждения этого благоприятного свойства сертаконазола необходимы дополнительные исследования.
Таблица 10. Исследования при кандидозном вульвовагините
| План исследования | Вещество/доза/ длительность применения | Полное излечение* | Микологическое излечение | Авторы |
| Двойное слепое, рандомизированное, многоцентровое | Кпотримазол 500 мг (× 1) Клотримазол 200 мг (× 3) | 75% (63-87) 71% (58-84) | 79% (68-91) 74% (62-87) | Fleurietal., 1985 [33] |
| Открытое, рандомизированное | Кпотримазол 500 мг (× 1) Клотримазол 100 мг (× 6) | - - | 82% (75-90) 85% (77-92) | Loendersloot et al., 1985 [35] |
| Многоцентровое без сопоставления | Клотримазол 500 мг (× 1) | - | 87% (80-94) | Goorsmans et al., 1982 [34] |
| Открытое, рандомизированное, многоцентровое | Миконазол 2% (× 14) Миконазол 2% (× 7) | 69% (53-84) 79% (67-91) | 74% (60-89) 88% (79-98) | Pascuale et al., 1979 [36] |
| Рандомизированное, многоцентровое | Терконазол 0,4% (× 7) Терконазол 0,8% (× 7) Миконазол 2% (× 7) | 71% (65-77) 72% (66-77) 68% (61-74) | - - - | Corson et al., 1991 [23] |
| Рандомизированное, двойное слепое | Терконазол 80 мг (× 3) Миконазол 2% (× 7) Плацебо (х 7) | 40% (0-83) 67% (36-97) 11% (0-32) | - - - | Thomason et al., 1990 [37] |
| Двойное слепое, рандомизированное, многоцентровое | Плацебо (× 3)(× 6) Бутоконазол 2% (× 3) Бутоконазол 2% (× 6) Миконазол 2% (× 6) | 23% (13-32) 52% (42-62) 58% (48-68) 54% (44-64) | 37% (25-48) 63% (53-73) 79% (71-88) 72% (62-81) | Brown et al., 1986 [32] |
Выбранные критерии оценки эффективности соответствуют таковым в литературных публикациях и критериям, рекомендованным Основными правилами по клинической оценке противомикробных лекарственных средств [65], изданными специализированными организациями (Американское общество по инфекционным заболеваниям, Управление по пищевым и лекарственным продуктам (FDA)).
Безопасность. 1478 женщин приняли участие в описанных в данном обзоре исследованиях. 768 из них получали лечение различными вагинальными лекарственными формами сертаконазола. В этих исследованиях для оценки безопасности препарата был использован широкий диапазон методов: структурированные и неструктурированные методы регистрации побочных явлений, гинекологическое обследование, анализы крови, плазмы крови и мочи для исключения системной абсорбции сертаконазола и оценки жизненных показателей.
Ни одна пациентка не была исключена из исследования из-за непереносимости или побочных эффектов препарата, тогда как двое больных, лечение которых проводили миконазолом и клотримазолом, были исключены из соответствующих исследований по этим причинам.
Местная переносимость сертаконазола при интравагинальном введении была хорошей. Сообщений о местных побочных явлениях было немного (примерно на 3-5% меньше, чем при лечении эталонными препаратами). Подавляющее большинство местных побочных явлений имело слабую или умеренную выраженность и не требовало лечения. Причинную связь этих явлений с использованием препарата было трудно установить из-за наличия у пациенток симптомов заболевания (зуд, жжение, боль, эритема и отек). В основном сообщалось о возникновении зуда и жжения, что типично для препаратов данного класса и отражает эффективность проводимого лечения. Этот тип местной реакции, особенно зуд, иногда встречается в первые несколько дней противогрибковой терапии (1-6%) и является реакцией на антиген, высвобождающийся вследствие цитолиза грибов [66].
Системная переносимость препарата во всех исследованиях была очень хорошей, а побочные явления, о которых сообщалось, не имели причинной связи с использованием препарата. Клинически существенных сдвигов в лабораторных показателях не отмечалось, что подтверждает отсутствие всасывания и попадания препарата в системную циркуляцию.
Данные, полученные в исследованиях, представляются убедительными и полностью согласуются с данными других литературных источников. Как правило, противогрибковые средства при местном применении безопасны. Только 0,2% больных, получавших сертаконазол, жаловались на головную боль и абдоминальный дискомфорт, хотя в некоторых исследованиях (например, при изучении терконазола) частота возникновения системных побочных эффектов достигала 10% [63]. В этой связи фармакологическая безопасность сертаконазола заслуживает внимания.
Местное лечение сертаконазолом при вульвовагинальном кандидозе можно рекомендовать как терапию выбора. Препараты для приема внутрь, несмотря на их эффективность, следует применять с осторожностью из-за их потенциальных побочных эффектов (желудочно-кишечные расстройства, гепатотоксичность). Некоторые из этих побочных эффектов редки, но опасны (ангионевротический отек, синдром Стивенс-Джонсона). Кроме того, в случае использования таких препаратов возможны взаимодействия с другими лекарственными средствами [69-71].
Сертаконазол при интравагинальном введении больным и здоровым испытуемым хорошо переносится и характеризуется высокой безопасностью. В связи с этим противопоказаний к применению препарата, за исключением индивидуальной непереносимости, нет, а его использование не требует специальных мер предосторожности. В сравнении с другими лекарственными средствами выявляется тенденция к меньшей частоте возникновения местных побочных явлений при использовании вагинальных препаратов сертаконазола и одобрению дозированных вагинальных форм сертаконазола большим числом больных (более 90% больных дали им хорошую или очень хорошую оценку).
Необходимо указать лишь обычные для этого класса соединений противопоказания к применению (такие как гиперчувствительность к производным азола или к вспомогательным ингредиентам лекарственных форм). Следует также обратить внимание на отсутствие исследований по эффективности и безопасности препарата у детей, женщин старше 70 лет, беременных, женщин, вскармливающих грудным молоком, и у больных с иммунодефицитными состояниями.
Комментарии
ПРАКТИКА ПЕДИАТРА
