Влияние разных видов лечения на эндотелиальную функцию у больных с эректильной дисфункцией и гипогонадизмом
СтатьиЕ.Б. Мазо, С.И. Гамидов, Е.М. Сотникова
Кафедра урологии и оперативной нефрологии ГОУ ВПО РГМУ Росздрава, Москва (зав. кафедрой – член -корр. РАМН, проф. Е.Б. Мазо)
Введение
Эректильная дисфункция (ЭД) у больных с гипогонадизмом не редкое явление и она имеет тенденцию к увеличению с возрастом. По разным данным, количество больных с ЭД и возрастным гипогонадизмом варьирует от 1.7% [1] до 35% [2]. Помимо индивидуальных особенностей и половой конституции значительный вклад в сроки наступления возрастного гипогонадизма оказывают соматические заболевания, которые могут ускорять наступление андропаузы на 5-7 лет. Среди хронических заболеваний, оказывающих влияние на уровень тестостерона крови, основное значение имеют: артериальная гипертония (АГ) [3], сахарный диабет (СД) [3-4], метаболический синдром (МС) [5] и ожирение. По данным Nieschlag и соавт. [6] хронический стресс, беспокойство и чрезмерные физические нагрузки могут вдвое снижать уровень тестостерона.
Негативное влияние низкого уровня тестостерона на эректильную функцию, может быть связано с развитием эндотелиальной дисфункции и атеросклерозом кавернозных сосудов [7], а также с угнетением ночных эрекций, имеющих важное трофическое значение для тканей полового члена [8]. Другими словами андрогены могут прямо контролировать экспрессию и активность NO синтазы в кавернозных телах человека [9-10].
Учитывая важное клиническое значение эндотелиальной дисфункции и её потенциальную обратимость, значительные усилия были направлены на разработку методов лечения данного состояния. В нескольких исследованиях показано, что коррекция неблагоприятных факторов образа жизни, в том числе отказ от курения [11], нормализация массы тела [12], регулярная физическая активность [13] сопровождаются улучшением эндотелиальной функции.
Однако неэффективность немедикаментозных методов лечения у больных с гипогонадизмом, часто требует проведения заместительной гормональной терапии андрогенами. Одни авторы продемонстрировали, что заместительная терапия тестостероном является эффективной при лечении ЭД, связанной с гипогонадизмом и может приводить к увеличению сосудистой реактивности, улучшать эректильную функцию и ответ к ингибиторам ФДЭ 5 [14-15]. С другой стороны, имеются немногочисленные исследования, которые показали, что при ЭД и гипогонадизме терапия только тестостероном не достаточна для восстановления общего сексуального удовлетворения [16], а средняя эффективность данного лечения варьирует от 35 до 40% [17]. В таких случаях, некоторые исследователи предлагают проведение комбинированной терапии с применением андрогенов и ингибиторов ФДЭ 5 типа [18].
Учитывая, что до сегодняшнего дня в литературе нет данных о влиянии андрогенов или их комбинации с ингибиторами ФДЭ 5 типа на эндотелиальную функцию у больных с ЭД и гипогонадизмом, мы сочли необходимым провести собственное исследование.
Материалы и методы
В исследование были включены 66 мужчин с органической ЭД и возрастным гипогонадизмом в возрасте от 34 до 72 лет (средний возраст в общей группе составил 54,25±2,03 лет).
Всем больным было проведено комплексное клиническое обследование, включавшее рутинные методы исследования (сбор анамнеза, осмотр, пальцевое ректальное исследование, клинический и биохимический анализы крови, общий простатоспецифический антиген (ПСА)) и специальные методы, предназначенные для диагностики ЭД и гипогонадизма. На этапе специального андрологического обследования для изучения патогенеза ЭД применялись следующие методы диагностики: анкетирование с использованием Международного Индекса Эректильной Функции (МИЭФ), опросник AMS (AMS опросник возрастных симптомов мужчины) для выявления клинических симптомов возрастного гипогонадизма, ультразвуковое исследование (УЗИ) полового члена, фармакодопплерография сосудов полового члена (ФДГ), в том числе с функциональными тестами.
Для оценки эндотелиальной функции мы применяли посткомпрессионные тесты на плечевой и кавернозных артериях, а также определяли уровень С-реактивного белка (СРБ) и гомоцистеина в крови. Посткомпрессионный тест на кавернозных артериях выполняли на ультразвуковом аппарате Technos MP фирмы Esaсote по модифицированной нами методике.
Проводилась оценка гормонального статуса крови (общий тестостерон, фолликулостимулирующий гормон (ФСГ), лютеинизирующий гормон (ЛГ), эстрадиол, пролактин, глобулин, связывающий половые гормоны, прогестерон) радиоиммунологическим методом. Уровень свободного тестостерона определяли расчетным способом.
В зависимости от получаемой терапии все больные в дальнейшем были разделены на 3 группы. Больным из 1 группы (n=20) назначали только заместительную андрогенную терапию. Во 2 группе (n=46) пациенты находились на комбинированной терапии (андрогены и ингибиторы ФДЭ 5 типа). Пациенты в 3 группе (n=31) получали только ингибиторы ФДЭ 5 типа.
Все группы исходно по сосудистым факторам риска (Таблица 1), по возрасту пациентов, по выраженности эндотелиальной и эректильной дисфункции были сопоставимы (Таблица 2).
В качестве заместительной андрогенной терапии в 1 и во 2 группе использовали тестостерона ундеканоат (Небидо, Шеринг) 1000 мг каждые 10-12 недель внутримышечно, но перерыв между первой и второй инъекциями составлял 6 недель. Из ингибиторов ФДЭ 5типа во 2 и 3 группе применяли варденафил (Левитра, Байер Шеринг Фарма) в дозе 20 мг. Пациенты принимали препарат по требованию за 1 час до полового акта, не менее 4 таб. в месяц в течение 6 месяцев.
Всем больным на фоне проводимой терапии проводили коррекцию неблагоприятных факторов образа жизни (отказ от курения, спиртных напитков, дозированная физическая нагрузка) и сопутствующих заболеваний. Пациентам из 1 и 2 группы перед назначением терапии, а далее каждые 3 месяца определяли уровень общего ПСА и проводили трансректальное ультразвуковое исследование простаты.
Эффективность проводимой терапии оценивалась через 1,3 и 6 мес. При этом мы изучали динамику показателей эректильной и эндотелиальной функции, а также лабораторные и клинические признаки гипогонадизма.
Анализ клинических данных производили с помощью стандартных методов статистики с использованием программного обеспечения для ПК Microsoft Excel и Statistica 6.0.
Результаты исследования
При контрольном обследовании через 1,3 и 6 месяцев в 1 и 2 группах отмечено достоверное снижение индекса массы тела (ИМТ) и окружности талии. Улучшение антропометрических показателей отмечали и у больных из 3 группы, но только после 6 мес. лечения. Более значимое снижение ИМТ регистрировались у больных, получающих комбинированную терапию. Этот факт можно объяснить более быстрым восстановлением сексуальной активности, которая является дополнительной физической нагрузкой и способствует снижению веса у мужчин в данной группе. (Рис.1) Прием андрогенов способствовал снижению показателей анкеты AMS и увеличению полового влечения МИЭФ у больных в 1 и во 2 группах уже через месяц терапии. (Таблица 3) Достоверное увеличение показателей либидо у больных из 3 группы было отмечено через 6 мес. и эти изменение были значительно меньше, чем в 1 и 2 группах. Следует отметить, что на фоне комбинированной терапии улучшение показателей эректильной функции МИЭФ во 2 группе происходило достоверно быстрее и эффективнее, чем в 1 и 3 группах. (Таблица 3)
Улучшение качества эрекции сопровождалось достоверным увеличением клинических и лабораторных показателей эндотелиальной функции. Наиболее выраженное повышение процентного увеличения диаметра кавернозных артерий (ПУДКА) (Рис. 2) и снижение уровня гомоцистеина (Рис. 3) отмечалось у больных из группы 2, и по сравнению с группами 1 и 3 эти больные достоверно раньше восстанавливали эндотелиальную функцию. Уровень СРБ не коррелировал с показателями эректильной функции МИЭФ и состоянием эндотелия.
С помощью гормональной терапии андрогенами у всех больных в 1 и во 2 группах удалось восстановить нормальный уровень общего и свободного тестостерона. Несмотря на то, что в 3 группе больные не получали андрогены, при контрольном обследовании через 6 мес. было отмечено достоверное увеличение уровня свободного тестостерона.
В целом терапия переносилась удовлетворительно, из числа побочных эффектов наблюдались головные боли, заложенность носа, гиперемия лица, гиперемия в месте инъекции, что не требовало проведения каких- либо специфических мероприятий и отмены лечения.
Обсуждение
Итак, патогенез ЭД у больных с возрастным гипогонадизмом многокомпонентный, и, как правило, к моменту возникновения гипогонадизма почти все они имеют артериогенную ЭД и другие сердечно-сосудистые заболевания такие как, ишемическая болезнь сердца, дислипидемия, гиперхолистеринемия, СД, АГ, ожирение, МС и др.
Литературные данные свидетельствуют о том, что низкий уровень тестостерона вызывает дегенеративные изменения в кавернозных телах (апоптоз, фиброз), приводит к отложению адипоцитов в подоболочечном пространстве полового члена и развитию вено-окклюзивной ЭД [7-9]. Следовательно только назначение андрогенов не может обеспечить больному быстрый эффект и устойчивую эрекцию, что подтверждают проведенные ранее исследования. По их данным на фоне монотерапии андрогенами улучшение эректильной функции отмечается в среднем у 50% больных и эффект наступает не раньше чем через 12-24 недель [19-20]. В связи с этим каждый неудачный половой акт еще больше увеличивает имеющиеся депрессивные нарушения и снижает доверие пациента к проводимой терапии, и качество жизни.
Полученные нами данные еще раз подтверждают необходимость комбинирования андрогенов с ингибиторами ФДЭ 5 типа у больных с ЭД и возрастным гипогонадизмом. Сочетание тестостерона с сосудистыми препаратами у данной категории больных по сравнению с монотерапией (как ингибиторами ФДЭ 5 типа, так и андрогенами) способствует достоверному улучшению показателей эректильной функции и при этом восстановление эрекции наступает относительно быстрее. Данный факт в первую очередь можно объяснить синергичным действием тестостерона и ингибиторов ФДЭ 5 типа на сосуды полового члена. Как известно, эти препараты активно участвуют в регуляции сосудистого тонуса (в том числе и полового члена) и улучшают состояние эндотелия. Значительное увеличение показателей ПУДКА и снижение уровня гомоцистеина на фоне комбинированной терапии лишний раз это доказывает. Быстрый и высокий успех от комбинированной терапии объясняется также благоприятным влиянием андрогенов на половое влечение, уровень липидов и обмен углеводов, что в свою очередь способствует улучшению кровоснабжения кавернозных тел.
Следует подчеркнуть то, что в 3 группе, где больные получали только ингибиторы ФДЭ 5 типа, мы также отмечали увеличение уровня тестостерона. Это, скорее всего, связано с улучшением антропометрических показателей пациентов (ИМТ, окружность талии) на фоне коррекции неблагоприятных факторов образа жизни. Подобные данные получены в работах других исследователей [21]. Однако, эти изменение наступают относительно в поздних сроках (через 6 мес.), что также снижает уверенность пациентов к проводимой терапии.
Заключение
Таким образом, все вышеперечисленные данные позволяют говорить о том, что комбинированная терапия (андрогены + ингибиторы ФДЭ 5) оказывает выраженный синергичный эффект на эндотелиальную и эректильную функцию у больных с ЭД и гипогонадизмом, и способствует раннему восстановлению эректильной функции у них. Поэтому, данная терапия может быть рекомендована как стартовая для этой категории пациентов.
Список литературы
Таблица 1. Распространенность сосудистых факторов риска в группах
| 1 группа | 2 группа | 3 группа | |
|---|---|---|---|
| Ожирение | 65% | 61% | 68% |
| Артериальная гипертония | 80% | 85% | 77,5% |
| ИБС | 60% | 50% | 55% |
| Сахарный диабет | 30% | 35% | 29% |
| Курение | 45% | 46% | 45,2% |
| Метаболический синдром | 75% | 80% | 71% |
| Дислипидемия | 95% | 90% | 90% |
Таблица 2. Основные возрастные, антропометрические, лабораторные характеристики, а также показатели эректильной и эндотелиальной функции до лечения в группах
| 1 группа | 2 группа | 3 группа | |
|---|---|---|---|
| Ср. возраст, лет | 53,6±2,07 | 53,98± 1,46 | 55,77±2,01 |
| ИМТ, кг/м2 | 31,6±0,88 | 31,8±0,55 | 31,5±0,72 |
| Либидо МИЭФ, баллы | 3,5±0,33 | 3,83±0,28 | 4,35±0,27 |
| ЭФ МИЭФ, баллы | 11,2±1,01 | 11,4±0,77 | 11,2±0,86 |
| AMS, баллы | 38,3±0,29 | 39,02±0,21 | 36,5±0,34 |
| ПУДКА, % | 19,55±2,88 | 19,51±1,28 | 19,34±1,93 |
| СРБ, мг/л | 5,0±0,72 | 4,99±0,41 | 5,11±0,58 |
| Гомоцистеин, мкмоль/л | 15,17±0,84 | 14,85±0,94 | 15±0,97 |
| Тестостерон общий, нмоль/л | 9,86±0,40 | 9,48±0,25 | 9,61±0,33 |
| Тестостерон свободный, пг/мл | 4,14±0,37 | 4,05±0,23 | 4,01±0,23 |
Таблица 3. Изменение показателей AMS, либидо МИЭФ и эректильной функции МИЭФ на фоне лечения
| До лечения | Через 1 мес | Через 3 мес | Через 6 мес | ||
|---|---|---|---|---|---|
| AMS, баллы | 1 группа | 38,3±0,29 | 32,8±0,65* | 30,6±0,05 | 29,2±0,32 |
| 2 группа | 39,02±0,21 | 30,4±0,49* | 29,9±0,62 | 28,6±0,95 | |
| 3 группа | 36,5±0,34 | 34,8±0,98 | 34,5±0,33 | 32,6±0,52 | |
| Либидо МИЭФ, баллы | 1 группа | 3,5±0,33 | 8,86±0,07* | 8,56±0,56 | 9,14±0,87 |
| 2 группа | 3,83±0,28 | 8,05±0,38* | 8,76±1,07 | 8,89±0,34 | |
| 3 группа | 4,35±0,27 | 5,87±0,45 | 6,02±0,22* | 7,55±0,72 | |
| ЭФ МИЭФ, баллы | 1 группа | 11,2±1,01 | 19,35±0,83 | 22,55±0,83* | 23,95±0,71 |
| 2 группа | 11,4±0,77 | 23,89±0,39* | 25,04±0,38 | 25,54±0,25 | |
| 3 группа | 11,2±0,86 | 22,74±0,45 | 23,03±0,56* | 23,35±0,68 |
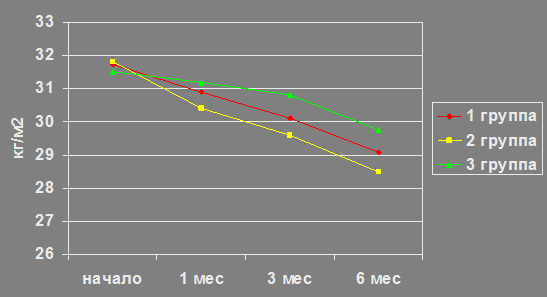
Рис. 1. Изменение индекса массы тела на фоне лечения в группах
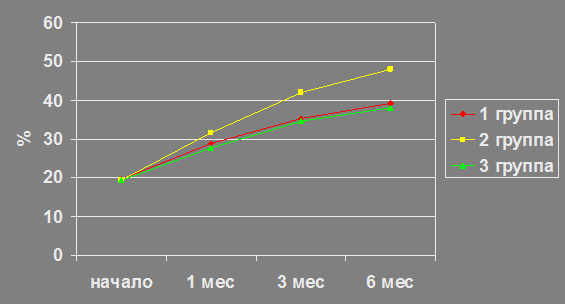
Рис. 2. Изменения процентного увеличения диаметра кавернозных артерий (ПУДКА) на фоне лечения в группах
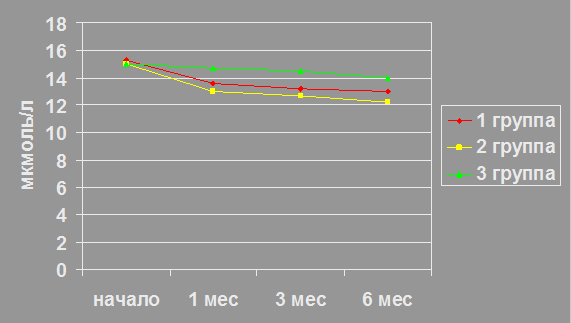
Рис. №3. Изменения гомоцистеина на фоне лечения в группах
Резюме
Цель исследования: Оценить влияние разных методов лечения на состояние эректильной и эндотелиальной функции у больных с ЭД и возрастным гипогонадизмом.
Материалы и методы: В исследование были включены 66 мужчин с ЭД, которые имели клинические и лабораторные признаки гипогонадизма. Всем больным проводили комплексное обследование и специальные методы диагностики ЭД и гипогонадизма (анкетирование с использованием эректильной функции международного индекса эректильной функции (ЭФ МИЭФ), опросник AMS, определение гормонального профиля крови). Для оценки эндотелиальной функции мы использовали посткомпрессионные тесты на кавернозных артериях, а также показатели гомоцистеина в крови. Все больные были разделены на 2 сопоставимые группы. В 1 группе состояло 20 мужчин, средний возраст 54,6±11,5 года, они получали только андрогены. В качестве заместительной терапии использовали тестостерона ундеканоат (Небидо, Шеринг) 1000 мг каждые 10-12 недель внутримышечно, но перерыв между первой и второй инъекциями составлял 6 недель. Во 2 группе было 46 мужчин, средний возраст 53,98±10,03 года, которые находились на комбинированной терапии (андрогены и ингибиторы ФДЭ 5). Из ингибиторов ФДЭ 5типа применяли варденафил (Левитра, Байер Шеринг Фарма) в дозе 20 мг. Длительность терапии составила 6 месяцев.
Результаты: У всех больных из обеих групп на фоне лечения отмечалось достоверное снижение баллов AMS (в 1 группе с 38,3±0,29 до 29,2±0,32 баллов; во 2 группе с 39,02±0,21 до 28,6±0,95 баллов) и увеличение уровня тестостерона (в 1 группе с 9,86±0,4 до 17,77±0,42 нмоль/л; во 2 группе с 9,35±0,25 до 17,21±0,63 нмоль/л). Динамика снижения уровня гомоцистеина у пациентов из 2 группы (с 15,03±0,94 до 12,2±0,33 мкмоль/л) была достоверно выражена, чем у пациентов из 1 группы (с 15,31±0,84 до 13,04±0,56 мкмоль/л). Комбинированная терапия оказывала достоверно выраженный эффект на показатели ЭФ МИЭФ у пациентов 2 группы (с 11,4±0,77 до 25,54±0,25 баллов), чем у больных из 1 группы (с 11,2±1,01 до 23,95±0,71 баллов), при этом улучшение эректильной функции у пациентов из 2 группы наступало раньше (3,4 против 13,7 нед, соответственно, рЗаключение: Таким образом, комбинированная терапия (андрогены + ингибиторы ФДЭ5) оказывает более быстрый и выраженный эффект на состояние эндотелиальной и эректильной функции, а также благоприятно влияет на уровень гомоцистеина в крови. Данная терапия может быть рекомендована как стартовая для больных с ЭД и возрастным гипогонадизмом.
Ключевые слова: Эректильная дисфункция (ЭД), гипогонадизм, комбинированная терапия, Андрогены, ингибиторы фосфодиэстеразы 5 типа (ФДЭ 5).
Комментарии
ПРАКТИКА ПЕДИАТРА
