Состояние микроценоза влагалища и способы коррекции его нарушений во время беременности
Статьи Опубликовано в журнале:Вопросы гинекологии, акушерства и перинатологии, 2007, т. 6, №5
А.Н.Стрижаков, П.В. Буданов
Московская медицинская академия имени И.М.Сеченова
В норме на протяжении беременности возрастает колонизационная резистентность влагалищного биотопа. В то же время нарушения микроценоза влагалища встречаются у каждой второй беременной. Ранняя своевременная безопасная коррекция вагинальной флоры позволяет снизить частоту связанных с инфекциями осложнений беременности, родов, послеродового периода и улучшить перинатальные показатели. Проведенное исследование показывает высокую эффективность Гексикона для лечения нарушений микроценоза влагалища у беременных. Гексикон не обладает отрицательным влиянием на количество лактобацилл и хорошо переносится. Высокую частоту рецидивов нарушений микроценоза влагалища удается предотвратить при комбинации местного лечения с повышением общей резистентности организма с помощью препаратов интерферонов (интерферон альфа-2) и Вобэнзима.
Ключевые слова: вульвовагинальные инфекции, бактериальный вагиноз, кандидоз, лечение, хлоргексидин, Вобэнзим, Гексикон The state of vaginal microcenosis and ways of correcting its disorders during pregnancy A.N.Strizhakov, P.V.Budanov I.M.Sechenov Moscow Medical Academy
Normally, during pregnancy colonizational resistance of the vaginal biotope increases. On the other hand, disorders of vaginal microcenosis occur in every second pregnant woman. Early safe correction of vaginal flora permits to decrease the incidence of complications of pregnancy, labor, and of the puerperium related to infection and to improve perinatal indices. The study demonstrates a high efficacy of Hexicon for treatment of disorders of vaginal microcenosis in pregnant women. Hexicon does not produce any negative effect on the amount of lactobacilli and has good tolerance. High incidence of relapses of disorders of vaginal microcenosis can be prevented by combining local treatment with an increase of general resistance of the body using interferon medications (interferon alpha-2) and Wobenzym.
Key words: vulvovaginal infections, bacterial vaginosis, candidiasis, treatment, chlorhexidine, Wobenzym, Hexicon
Нарушения микроценоза влагалища встречаются у 45-86% пациенток акушерских и гинекологических стационаров, приводят к инфекционным осложнениям после хирургических вмешательств на органах малого таза, способствуют возникновению воспалительных заболеваний внутренних половых органов, внутриутробной инфекции [1, 2, 10].
Нарушение колонизационной резистентности влагалищного биотопа в несколько раз увеличивает вероятность инфицирования возбудителями, передаваемыми половым путем. Подавляющее большинство инфекционных заболеваний влагалища и шейки матки являются вариантами нарушения микроценоза [2, 10, 11]. Так, бактериальный вагиноз (БВ), генитальный кандидоз (ГК) и трихомонадный вагинит составляют более 90% всех вагинальных инфекций [3, 10].
Инфекционные заболевания нижних отделов половых путей у беременных являются важной проблемой современного акушерства, в связи с высоким уровнем материнской и перинатальной заболеваемости, связанной с восходящим инфицированием фето-плацентарного комплекса [3].
В настоящее время подробное изучение культуральных и биохимических свойств представителей влагалищного биотопа привело к трансформации знаний о вариантах нарушений нормоценоза влагалища и его инфекционной патологии [9, 12, 13].
Термин "нормоценоз" отражает типичное состояние нормального биотопа влагалища (преобладание лактобактерий, отсутствие грамотрицательной микрофлоры, спор, мицелия, псевдогифов, лейкоцитов, неизмененные эпителиальные клетки). "Промежуточный тип" биоценоза влагалища является пограничным типом, редко сопровождается субъективными симптомами и клиническими проявлениями (сниженное количество лактобактерий, наличие грамположительных кокков, грамотрицательных палочек). "Дисбиоз" влагалища соответствует микробиологической картине бактериального вагиноза (минимальное количество или полное отсутствие лактобактерий, полиморфная грамотрицательная и грамположительная палочковая и кокковая микрофлора, наличие "ключевых клеток). "Вагинит" соответствует неспецифическому вагиниту (преобладание лейкоцитов над эпителиоцитами, повышенная эксфолиация эпителиоцитов, обнаружение трихомонад, псевдомицелия, спор грибов). При обнаружении трихомонад, мицелия, псевдогифов, спор определяется соответствующий этиологический диагноз [4].
Наряду с этим сопоставление бактериального вагиноза с неспецифическим кольпитом или промежуточным типом микроценоза влагалища и назначение антибактериальной терапии без учета патогенеза заболевания в большинстве случаев не дает положительного эффекта, а приводит к потенцированию патологического процесса [4, 5].
В понимании механизмов естественного барьера для инфекционных осложнений наиболее важен термин "колонизационная резистентность влагалищного биотопа". Это совокупность механизмов, поддерживающих стабильность популяционного и количественного состава компонентов нормального микроценоза [3, 6].
Собственный опыт диагностики, лечения, оценки эффективности и наблюдения отсроченных результатов различной терапии более 300 случаев бактериального вагиноза, генитального кандидоза, трихомониаза, уреаплазмоза и микоплазмоза в различных возрастных группах, в том числе у беременных женщин, показал, что частота положительных результатов лечения зависят не только от качества проведения этиотропной терапии и элиминации возбудителя, а, в основном, от нормализации и восстановления нормальной микрофлоры влагалища [4].
С целью выявления структуры нарушений микроценоза и выбора метода эффективного восстановления колонизационной резистентности влагалищного биотопа проведено обследование 486 беременных на протяжении гестации.
Из них 150 пациенток без инфекционной патологии половых органов составили контрольную группу. В основную группу включили 167 беременных с нарушениями микроценоза влагалища, которые были представлены бактериальным вагинозом, генитальным кандидозом, кольпитом и промежуточным типом микроценоза.
Обследование у всех женщин включало бактериологическое исследование содержимого влагалища, цервикального канала и кишечника. Причем, в контрольной группе подобные мероприятия выполнялись трижды - в каждом триместре беременности с целью изучения особенностей микроэкологии влагалища в зависимости от срока беременности. В ходе исследования у всех беременных были исключены сифилис, гонорея, ВИЧ-инфекция, гепатиты В и С.
Оценка состояния микроценоза родовых путей у беременных выполнялась в сроки до 12 нед, в 18-20 нед, 28-30 нед и в 37-38 нед. В процессе каждого эпизода обследования выполнялись тесты на бактериальный вагиноз, микроскопия мазков из влагалища, шейки матки и уретры. Обследование для выявления возбудителей инфекций, передающихся половым путем, проводилось до 12 нед, в 18-20 нед и в 37-38 нед.
Ни у одной из 150 пациенток контрольной группы не было обнаружено не только нарушений микроценоза родовых путей и специфических возбудителей, но и промежуточного типа микроценоза влагалища.
Нарушения микроценоза влагалища отмечены в 49,7% наблюдений. Преобладали бактериальный вагиноз и генитальный кандидоз, общая частота которых достигала 76% (рис. 1). Неспецифический кольпит диагностирован всего у 9 женщин. По нашему мнению неспецифический кольпит является результатом несовершенной лабораторной диагностики. Кроме того, у 18,6% беременных выявлялся промежуточный тип микроценоза влагалища.
Рис. 1. Структура нарушений микроценоза влагалища у беременных.
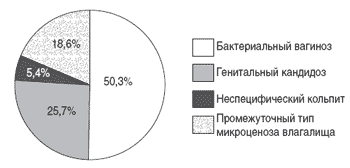
Структура нарушений микроценоза влагалища во время беременности изменялась в зависимости от срока гестации. Так, на рис. 2 представлено изменение частоты встречаемости инфекционной патологии влагалища во время беременности в зависимости от ее срока.
Рис. 2. Структура нарушений микроценоза влагалища в зависимости от срока беременности.
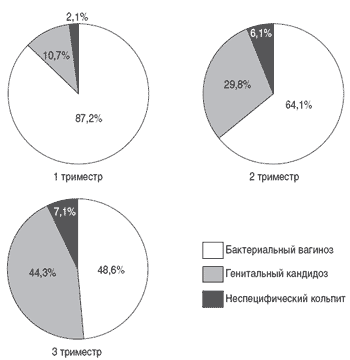
Пролонгированное наблюдение за беременными позволило установить, что в 1-м триместре беременности в подавляющем большинстве случаев развивается бактериальный вагиноз, а частота кандидозных поражений прогрессивно увеличивается со сроком гестации. Подобная динамика, вероятно, связана с уменьшением влияния эстрогенов во 2-м и 3-м триместрах беременности.
При этом независимо от срока беременности меняется состав вагинального отделяемого. В первую очередь повышается количество лейкоцитов, число которых преобладает над числом эпителиоцитов. Увеличивается количество слущенных эпителиальных клеток и повышается адгезия на них грибковых, а также различных бактериальных объектов. В 77,1% (81) имели место изменения микробного состава вагинального секрета, выражавшиеся в уменьшении количества лактобацилл и увеличении доли условно-патогенных микроорганизмов. Однако выраженное преобладание лейкоцитов над эпителиоцитами, отсутствие ключевых клеток и значительного повышения (на несколько порядков) общего количества микроорганизмов не позволяли квалифицировать данную картину как бактериальный вагиноз.
При анализе результатов микроскопии содержимого влагалища и шейки матки у беременных контрольной группы с отрицательными результатами посевов из канала шейки матки, количество лейкоцитов в вагинальном мазке составило 3,17 ± 0,72, а в мазке из цервикального канала - 6,73 ± 1,09, что в 2,12 раза больше (p < 0,01). Среди женщин с положительными результатами посевов из цервикального канала было отмечено, что количество лейкоцитов составило 4,66 ± 1,09 и 18,97 ± 1,99 (p < 0,001) в полях зрения соответственно. То есть, количество лейкоцитов у этих женщин в составе цервикальной слизи было в 4,07 раза больше. В основной группе средние количества лейкоцитов составили: при микроскопии содержимого влагалища - 28,32 ± 6,94, шейки матки -76,36 ± 11,99, т.е. в 2,69 раза больше.
При бактериологическом изучении содержимого влагалища было обнаружено, что вне зависимости от срока беременности у всех женщин контрольной группы доминирующим являлся род Lactobacillus. Однако полученные нами данные свидетельствуют о некоторых колебаниях количества лактобацилл на протяжении беременности (рис. 3).
Рис. 3. Динамика изменения количества Lactobacillus spp. в зависимости от срока беременности.
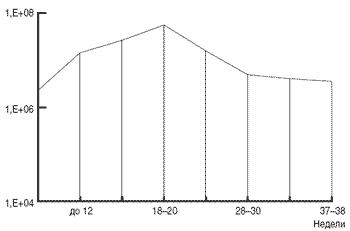
Другие представители нормального биотопа влагалища встречались в различных сочетаниях при количестве каждого вида, не превышавшем 101-102-3 КОЕ * мл-1. Отмечено, что с увеличением срока беременности увеличивалась частота выделения таких анаэробов как Fusobacterium nuclea-tum, F. mortiferum, Peptostreptococcus anaerobius, Campylobacter fetus, Е. coli, Bacteroides melaninogenicus, Eubacterium lentum, E. limosum, Propionibacterium granulosum. Так, по сравнению с первой половиной беременности (частота выделения - 17,3%) в сроке 37-38 нед эти микроорганизмы обнаруживались у 45,3% женщин, что в 2,6 раза чаще.
Почти всем (122) женщинам контрольной группы в 1, 2 и 3 триместрах беременности было проведено бактериологическое исследование содержимого верхней, средней и нижней трети цервикального канала. На протяжении всей беременности посевы 21 (17,2%) беременной не дали выделения бактериальной флоры. Меньшая часть обследованных -13,1% (16) пациенток имели только в нижней трети цервикального канала представителей Lactobacillus spp., Candida spp., Staphylococcus spp. Среди них только у 5 (31,25%) при повторном проведении посевов обнаруживались микроорганизмы. А в 3 триместре подобные данные были получены лишь у 2 женщин. Таким образом, с развитием беременности происходит процесс самоочищения цервикального канала, микроэкологическая подготовка родовых путей к родам.
В то же время, 85 (69,7%) женщин хотя бы однократно в содержимом канала шейки матки имели представительство различных групп микроорганизмов (рис. 4).
Рис. 4. Частота положительных и отрицательных результатов посевов из канала шейки матки у женщин контрольной группы.
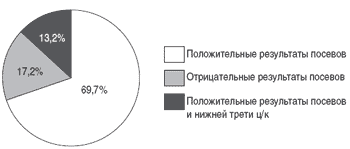
Следует отметить, что ни у одной женщины с отрицательным результатом посева из нижней трети цервикального канала не обнаруживались микроорганизмы и в других порциях материала из шейки матки.
Спектр микроорганизмов, выделенных из цервикального канала, соответствовал бактериальному спектру влагалища у каждой женщины. Все выделенные бактерии относились к группе условно-патогенных микроорганизмов.
При повторном исследовании микробной обсемененности содержимого цервикального канала только у 41 из 101 (в 2,5 раза меньше) женщины результаты посевов были положительными. При этом наблюдалась обратная отрицательная зависимость обсемененности цервикального канала от срока беременности. Последнее бактериологическое обследование, проведенное в 37-38 нед, показало, что микроорганизмы выделяются только из нижней трети канала шейки матки у 7 (6,93%) беременных, причем Proteus spp., Peptostreptococcus spp., Klebsiella spp., Lactobacillus spp., Bacteroides spp., Fusobacterium spp., Candida spp. в монокультуре или в ассоциациях занимали 92,3% среди всех обнаруженных штаммов.
В основной группе у 62 беременных было проведено 156 бактериологических посевов содержимого канала шейки матки. У всех женщин результаты посевов были положительными. Обнаружено, что у женщин с нарушениями микроценоза родовых путей отсутствовала тенденция уменьшения микробной обсемененности канала шейки матки с увеличением срока беременности. Напротив, при повторном микробиологическом исследовании отмечено увеличение количества патогенных штаммов в цервикальном секрете.
Из 36 женщин с бактериальным вагинозом и генитальным кандидозом у 34 (94,4%) уже при проведении первого посева имелась высокая обсемененность нижней трети, а у 12 (33,3%) патогенные биотопы определялись и в средней трети канала шейки матки (рис. 5).
Рис. 5. Количество положительных результатов бактериологических посевов содержимого канала шейки матки у беременных с нарушениями микроценоза родовых путей.
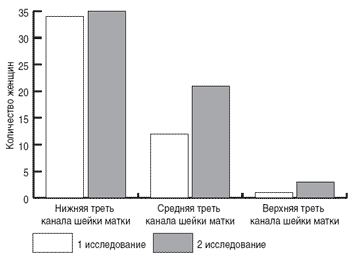
При повторном исследовании количество женщин с положительными результатами посевов из средней трети цервикального канала составило 61,8%. При этом общая концентрация выделяемых штаммов увеличилась в среднем на 1,33 * 103 КОЕ * мл-1 (р < 0,001). В верхней трети шеечного канала микроорганизмы были обнаружены у 11,1% беременных.
При наличии промежуточного типа микроценоза влагалища с увеличением срока беременности повышалась частота микробной обсемененности цервикального канала.
Следует отметить, что у 98,5% женщин с промежуточным типом микроценоза влагалища в дальнейшем развивались те или иные нозологические формы нарушений микроценоза влагалища. Это происходило в среднем через 1,99 ± 0,23 мес. после обнаружения промежуточного типа микроценоза.
Таким образом, у беременных с нормальным состоянием микроценоза влагалища с увеличением срока беременности происходит подготовка родовых путей, заключающаяся в снижении глубины и степени обсемененности канала шейки матки. При этом в видовом составе микроорганизмов, выделяемых из шейки матки перед родами, преобладают облигатные анаэробы, а на протяжении беременности - факультативные анаэробы, включая лактобактерии. Следует отметить, что во время беременности из цервикального канала с высокой частотой выделяются грибы рода Candida, причем их представительство в микробном составе цервикальной слизи увеличивается к концу беременности при отсутствии клинических и лабораторных признаков кандидоза. Подобные изменения происходят на фоне увеличения общей обсемененности влагалища, с преобладанием в его микробном составе молочнокислых палочек.
У беременных с генитальными инфекциями с увеличением срока беременности, длительности существования инфекционного процесса, повышается частота обнаружения бактериальных агентов в верхних отделах шейки матки. Наличие во время беременности промежуточного типа микроценоза влагалища приводит к возникновению нарушений микроценоза влагалища и увеличению микробной обсемененности шейки матки к сроку родов.
На втором этапе исследования, проводилось лечение, осуществлялась оценка клинической эффективности, лабораторный контроль за скоростью элиминации возбудителя, наличием рецидивирования и суперинфекции. Динамическое обследование беременных включало не менее 6 микроскопических исследований мазка вагинального отделяемого (по 2 в каждом триместре).
Рис. 6. Результаты лечения беременных с нарушением микроценоза влагалища.
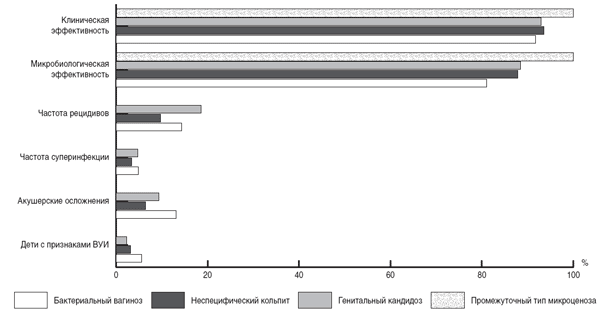
Вне зависимости от срока беременности при обнаружении любого варианта нарушения микроценоза влагалища применяли свечи, содержащие хлоргексидин (Гексикон), по 1 свече интравагинально 2 раза в сутки на протяжении 10 дней [6, 8].
Гексикон является эффективным антисептическим препаратом для самостоятельного интравагинального применения и обладает комплексной активностью относительно широкого спектра возбудителей генитальных инфекций. Во время беременности, особенно до завершения плацентации, значительно ограничен спектр безопасных препаратов даже для интравагинального введения. Для лечения вульвовагинальных инфекций использование антибактериальных препаратов для системного применения ведет к потенцированию явлений дисбактериоза, неэффективности лечения и развитию дополнительных осложнений (например, такого как дисбактериоз кишечника). Вместе с тем важным является наличие высокой эффективности препаратов относительно анаэробных микроорганизмов, отсутствие воздействия на лактобациллы и кислую среду влагалища, возможность их использования для экстренной профилактики перед хирургическим вмешательством или родоразрешением и безопасность использования во время беременности.
Гексикон представляет собой единственный препарат хлор-гексидина для самостоятельного применения пациенткой. Кроме того, к преимуществам использования Гексикона в акушерстве является отсутствие противопоказаний для применения у беременных, широкий спектр антибактериальной активности препарата, поддержание рН вагинального секрета.
Оценка эффективности проводимой терапии включала определение срока исчезновения жалоб, нормализации клинической картины, микробиологического выздоровления, частоты и времени возникновения рецидивов (рис. 6) [14].
Клиническая и микробиологическая эффективность лечения приближалась к 100%. Возникновение суперинфекции на фоне или после окончания терапии при использовании препаратов интерферона встречалось крайне редко. Частота ассоциированных с инфекционной патологией осложнений беременности, родов и послеродового периода, была меньше, чем общие показатели родильного дома.
Вне зависимости от варианта инфекционной патологии на фоне лечения Гексиконом в среднем жалобы и бели регрессировали к 4-5 сут, клинические проявления воспаления купировались к 5-7 сут терапии.
Уменьшение количества лейкоцитов, грибов и бактериальной обсемененности в вагинальном мазке при применении Гексикона начинается с 1-х сут лечения и достигает нормальных значений после 5 дней лечения. К 10 дню введения этого препарата количество лейкоцитов составляет не больше, чем 6-7 лейкоцитов в полях зрения светового микроскопа.
В 14,3% наблюдений после лечения бактериального вагиноза имелись рецидивы заболевания. При использовании Гексикона в сочетании с лактобациллами для интравагинального применения только в двух наблюдениях возник рецидив бактериального вагиноза через 2 и 6 нед после лечения. У этих пациенток в качестве антибактериального препарата при повторном лечении бактериального вагиноза был использован клиндамицин, после лечения которым, на протяжении беременности и 6 мес. после ее окончания не было выявлено никаких нарушений микроценоза.
Частота рецидивирования генитального кандидоза, по сравнению с другими инфекциями, была наиболее высокой во время беременности. Среди всех женщин с микотическим поражением, получавших лечение, повторное возникновение кандидоза наблюдалось у 18,6%.
При возникновении рецидивов бактериального вагиноза и генитального кандидоза проводилась терапия со сменой антибактериального/антимикотического препарата. Нарушения местного и общего иммунитета, выявляемые многими авторами при нарушениях микроценоза влагалища, привели к использованию методов иммунокоррекции в спектре лечения этой патологии. С этой целью широко используются препараты комбинированных ферментов желудочно-кишечного тракта и интерферона для системного воздействия. В настоящем исследовании лечение дополнялось сочетанием данных препаратов, повышающих общую иммунологическую резистентность (интерферон альфа-2, Вобэнзим).
Вобэнзим является комбинированным препаратом и представляет собой сочетание высокоактивных ферментов растительного и животного происхождения. Оказывает иммуномодулирующее, противовоспалительное, фибринолитическое, антиагрегантное и вторичное анальгезирующее действие [6].
Важным является действие Вобэнзима на ход воспалительного процесса: препарат ограничивает патологические проявления аутоиммунных и иммунокомплексных процессов, положительно влияет на показатели иммунологической реактивности организма. Стимулирует и регулирует функциональную активность моноцитов-макрофагов, естественных киллерных клеток, стимулирует противоопухолевый иммунитет, цитотоксические Т-лимфоциты, фагоцитарную активность клеток.
Под воздействием Вобэнзима снижается количество циркулирующих иммунных комплексов и происходит выведение мембранных депозитов иммунных комплексов из тканей.
Действие Вобэнзима на реологические показатели заключаются в снижении риска тромбофилических осложнений. Вобэнзим снижает концентрацию тромбоксана и агрегацию тромбоцитов. Регулирует адгезию клеток крови, повышает способность эритроцитов изменять свою форму, нормализует число нормальных эритроцитов и уменьшает общее число активированных форм тромбоцитов, нормализует вязкость крови, снижает общее число микроагрегатов. Таким образом нормализуется снабжение тканей кислородом и питательными веществами. Вобэнзим нормализует липидный обмен, снижает синтез эндогенного холестерина, повышает содержание липопротеинов высокой плотности, снижает уровень атерогенных липидов, улучшает всасывание полиненасыщенных жирных кислот.
Терапия полиферментными препаратами и интерфероном повышает эффективность антибиотикотерапии, увеличивая концентрацию антибиотиков в плазме крови и очаге воспаления, а также уменьшает побочные эффекты антибиотиков. Вобэнзим регулирует выработку интерферонов, тем самым, проявляя противовирусное и противомикробное действие.
Патогенетическим обоснованием применения полиферментного препарата Вобэнзим явилось его противовоспалительное, антипролиферативное, иммуномодулирующее, анальгезирующее действия.
Вобэнзим применялся по схеме: 7 драже 3 раза в день в течение 2-х мес, курсовая доза составила 1200 драже. Препарат хорошо переносился больными, побочных эффектов, потребовавших отмены препарата, не наблюдалось.
При использовании клиндамицин-вагинального крема в сочетании с Вобэнзимом и интерфероном альфа-2 только у одной женщины возник рецидив бактериального вагиноза через 6 нед после лечения. В качестве антибактериального препарата при повторном лечении бактериального вагиноза у данной пациентки был использован метронидазол, после лечения которым, на протяжении 6 месяцев не было выявлено никаких нарушений микроценоза.
После проведения повторных курсов терапии по поводу рецидивов кандидоза со сменой антимикотического препарата всего в двух наблюдениях были отмечены рецидивы заболевания (4,6%). У обеих пациенток подобное произошло в 3 триместре беременности.
Клиническая и микробиологическая эффективность обоих вариантов лечения приближалась к 100%. Возникновение суперинфекции на фоне или после окончания специфической терапии при использовании препаратов интерферона в сочетании с Вобэнзимом встречалось достоверно реже (p < 0,05). Частота рецидивов инфекции у этих женщин была в 2,4 раза меньше, а рождение детей с признаками внутриутробной инфекции встречалось в 2,5 раза реже.
Более чем у половины пациенток основной группы (61,1%) имелось сочетание нарушений микроценоза влагалища и кишечника, тогда как у пациенток контрольной группы только в 7,3%.
После проведения комбинированного лечения нормализация кишечного микробиоценоза была достигнута у 82,4% (84). Улучшение бактериологических показателей или уменьшение степени выраженности патологических изменений посева отмечено у 15,7% (16). Только у 2 пациенток была зарегистрирована неэффективность терапии дисбактериоза кишечника (1,96%).
На фоне применения Гексикона не было отмечено снижения количества лактобацилл по сравнению с исходным уровнем. Кроме того, общее количество Lactobacillus spp. достигало титра 105-107 КОЕ * мл-1 в среднем через 12,41 ± 4,4 сут. после окончания лечения без применения препаратов эубиотиков. То есть, подтверждено отсутствие влияния местного введения хлоргексидина на микроорганизмы, обеспечивающие колонизационную резистентность.
При проведении лечения по вышеописанным схемам, частота угрозы прерывания беременности снизилась в 2 раза, самопроизвольного выкидыша в 3,7 раза по сравнению с общими показателями родильного дома.
В группе женщин, получавших лечение, снизилась частота преждевременного излития вод и преждевременных родов - до 18,8% и 7,3%, соответственно. Не было ни одного случая возникновения хориоамнионита.
Проведение коррекции промежуточного типа влагалищного микроценоза с помощью препарата Гексикон позволило снизить частоту возникновения нарушений микроценоза родовых путей и инфекций, передающихся половым путем, у беременных женщин.
В ходе проведения исследования не было зарегистрировано побочных реакций на фоне интравагинального введения Гексикона и отказов от лечения.
Таким образом, нарушение микроценоза родовых путей приводит не только к резкому увеличению риска контаминации условно-патогенными возбудителями, но и повреждает биологический барьер секрета влагалища и канала шейки матки. Применение препарата хлоргексидина для самостоятельного использования пациенткой (Гексикон) высокоэффективно для лечения любых вариантов нарушения микроценоза влагалища. При рецидивирующих нарушениях микроценоза влагалища эффективность терапии повышает комплексное лечение, включающее препараты интерферона (интерферон альфа-2) и Вобэнзим. В отличие от антибактериальных препаратов Гексикон не оказывает отрицательного воздействия на количество лактобацилл. Литература
1. Байрамова Г.Р. Бактериальный вагиноз. Гинекология 2001; 3: (2): 52-4.
2. Буданов П.В., Баев О.Р., Пашков В.М. Нарушения микроценоза влагалища. Вопросы гинекологии, акушерства и перинатологии 2005; 4(2): 78-88.
3. Генитальные инфекции. Стрижаков А.Н., Давыдов А.И., Баев О.Р., Буданов П.В. М.: Издательский дом "Династия", Москва, 2003,140 с.
4. Никонов А.П., Асцатурова О.Р. Вульвовагиниты (в помощь практическому врачу). Гинекология 2002; 4(3): 122-5.
5. Покровский В.И. Медицинская микробиология. Москва: Гэотар-Медицина. 1998,1183.
6. Пестрикова Т.Ю., Молодцова Л.Ю. Принципы терапии бактериального вагиноза и вагинального кандидоза у беременных. Вопросы гинекологии, акушерства и перинатологии 2006; 5(6): 81^1.
7. Прилепская B.H. Особенности инфекционных процессов нижнего отдела половых путей. Возможности терапии препаратами для локального применения. Гинекология 2000; 2(2): 57-9.
8. Уварова Е.В., Латыпова H.X. Применение препарата Гексикон в лечении воспалительных заболеваний влагалища неспецифической этиологии. Репродуктивное здоровье детей и подростков. 2007; 4: 32-6.
9. Engberts М.К., Boon М.Е., van Haaften M., Heintz A.P. Symptomatic candidiasis: Using self sampled vaginal smears to establish the presence of Candida, lactobacilli, and Gardnerella vaginalis. Diagn Cytopathol. 2007 Oct; 35(10): 635-9.
10. Georgijevic A., Cjukic-lvancevic S., Bujko M. Bacterial vaginosis. Epidemiology and risk factors. Srp Arh Celok Lek 2000; 128:1-2: 29-33.
11. Hernandez G.E., Zamora P.F., Martinez A.M., et al. Epidemiologic, clinical and microbiological characteristics of nosocomial urinary infection in the spinal cord lesioned patient. Adas Urol Esp. 2007 Jul-Aug; 31(7): 764-70.
12. Hogan V.K., Culhane J.F., Hitti J., et al. Relative performance of three methods for diagnosing bacterial vaginosis during pregnancy. Matern Child Health J. 2007 Sep 15.
13. Raska M., Be'lakova J., Krupka M., Weigl E. Candidiasis-do we need to fight or to tolerate the Candida fungus? Folia Microbiol (Praha). 2007; 52(3): 297-312.
14. Tanaka Y., Naganawa M., Sakai M., Saito S. Fundamental study of a newly developed medium on detection of Lactobacillus. Rinsho Biseibutshu Jinsoku Shindan Kenkyukai Shi. 2006; 17(1): 23-32.
 invar.ru
invar.ru
