Кетанов в терапии абстинентного синдрома у больных опийной зависимостью: Описание метода
СтатьиВ ТЕРАПИИ АБСТИНЕНТНОГО СИНДРОМА У БОЛЬНЫХ ОПИЙНОЙ (ГЕРОИНОВОЙ) ЗАВИСИМОСТЬЮ
ОПИСАНИЕ МЕТОДА
1. Характеристика клинического материала
Было обследовано 56 больных героиновой зависимостью, мужчин, проходивших стационарный курс лечения в отделении клинической психофармакологии ННЦ наркологии МЗ РФ. В начале исследования больные случайным образом были разделены на две группы — основную и контрольную, клинико-динамические и социально-демографические показатели в группах практически не различались. Возраст больных составлял от 18 до 35 лет, средний возраст — 22,8+2,6.
Диагностика осевых синдромов зависимости проводилась по МКБ-10. Основные клинико-динамические показатели представлены в таблице 1.
Таблица 1.
Основные клинико-динамические показатели
|
Клинико-динамические характеристики заболевания |
Основная гр. |
Контрольная гр. |
||
|
Абс. |
% |
Абс. |
% |
|
|
Возраст начала употребления героина |
||||
|
13-16 |
8 |
27 |
12 |
46 |
|
16-19 |
16 |
53 |
14 |
54 |
|
старше 20 лет |
6 |
20 |
0 |
0 |
|
всего: |
30 |
100 |
26 |
100 |
|
Формирование абстинентного синдрома (от начала систематического употребления) |
||||
|
Менее 2-х недель |
5 |
17 |
5 |
19 |
|
До 3-х месяцев |
19 |
63 |
16 |
62 |
|
Свыше 3-х месяцев |
6 |
20 |
5 |
19 |
|
всего: |
30 |
100 |
26 |
100 |
|
Длительность заболевания (годы): |
||||
|
До 1,5 лет |
14 |
47 |
18 |
69 |
|
1,5-3 |
10 |
33 |
5 |
19 |
|
3-6 |
6 |
20 |
3 |
12 |
|
всего: |
30 |
100 |
26 |
100 |
|
Частота и длительность ремиссий в анамнезе |
||||
|
До 3-х месяцев |
8 |
27 |
4 |
15 |
|
3-6 |
5 |
17 |
4 |
15 |
|
6-12 |
1 |
3 |
0 |
0 |
|
Свыше 12 |
0 |
0 |
0 |
0 |
|
всего: |
14 |
47 |
8 |
30 |
Симптоматика опийного (героинового) абстинентного синдрома (ОАС) включала специфические соматоневрологические, болевые и психопатологические нарушения.
Пациенты поступали в клинику, в основном, с начальными проявлениями абстинентных нарушений. Развитие ОАС происходило, в среднем, через 4—12 часов после последнего употребления наркотика. Начальные проявления были представлены соматовегетативными нарушениями. В последующем присоединялись характерные болевые ощущения в мышцах и суставах верхних и нижних конечностей, спине. С усилением болевой симптоматики было связано и нарастание психопатологических нарушений, пациенты жаловались на осознанное влечение к наркотику, усиливались беспокойство, раздражительность, напряженность, проявлялась тревога, в некоторых случаях доходящая до степени ажитации, практически постоянно присутствовали расстройства сна. Эти проявления достигали своего максимума на 2—3 день пребывания в стационаре с постепенной редукцией симптоматики к 5—7 дню лечения. Степень тяжести опийного (героинового) абстинентного синдрома была квалифицирована как средняя у 39 и как тяжелая у 17 больных (таблица 2).
Таблица 2.
Динамика и балльная оценка опийного (героинового) абстинентного синдрома
|
Группы |
Тяжесть течения (М±т) |
Продолжительность ОАС |
||
|
Вегетативные проявления |
Алгические проявления |
Психопатологические проявления |
||
|
Основная |
1,4±0,3 |
2,2±0,8 |
2,1 ±0,8 |
5-6 дней (максимально до 8 дней) |
|
Контрольная |
1,2±0,4 |
2,4±0,5 |
2,3±0,5 |
|
Периодически возобновляющаяся болевая симптоматика наблюдалась и в постабстинентном состоянии. Связано это было, как правило, с обострением патологического влечения к наркотику (ПВН). Однако не всегда оказывалось успешным применение только средств, направленных на купирование ПВН (как правило, нейролептики, антидепрессанты, транквилизаторы). Более выраженный эффект давало сочетанное применение психотропных средств с обезболивающими.
Лечение абстинентного синдрома было комплексным. В качестве базисной терапии применялись антиконвульсанты (финлепсин — 400-600 мг), агонисты альфа-2-адренорецепторов (клофелин - 0,045-0,06 мг), обезболивающие средства (см. ниже); при выраженном влечении к наркотику, психомоторном возбуждении назначались нейролептики (аминазин -до 600-800 мг; галоперидол - до 10-15 мг; тиапридал - до 1000-1300 мг; неулептил - до 40 мг); при расстройствах сна - транквилизаторы (реланиум -до 40 мг; феназепам — до 6-8 мг). Применялась также общеукрепляющая, гепатотропная терапия.
В качестве обезболивающего средства в основной группе применялся кетанов (кеторолака трометамин), в контрольной группе — трамал (трамадола гидрохлорид).
Кетанов назначался с первого дня развития абстинентного синдрома в средней суточной дозе 90 мг, в более тяжелых случаях доза увеличивалась до 120 мг. В первые 4-5 дней препарат назначался в инъекциях (по 1.0 мл 3-4 раза в сутки). В дальнейшем препарат назначался внутрь в средней суточной дозе 60 мг, максимальная доза составляла 90 мг (по 1 табл. 2-3 раза в сутки) до полного купирования болевой симптоматики. Общая длительность применения препарата не превышала 10 дней (в среднем - 5—7 дней).
В группе сравнения в качестве обезболивающего средства назначался трамал в первые дни в инъекциях в суточной дозе 400-600 мг. На пике болевой активности доза могла достигать 800 мг. Снижение доз и отмена анальгетика происходила к 5-7 дню лечения.
Следует подчеркнуть, что используемая психотропная терапия в двух группах не отличалась, дозы препаратов подбирались индивидуально, лечение было направлено на купирование психопатологической симптоматики: патологического влечения к наркотику, связанных с ним поведенческих, аффективных расстройств, нарушений сна.
Обследование больных осуществлялось в день поступления (0 день), в дальнейшем - ежедневно до купирования болевого симптомокомплекса.
Кроме обычного клинического психопатологического исследования в работе использовались: индивидуальная карта больного, включавшая в себя основные клинические характеристики заболевания, выраженность личностных особенностей, а также сведения об объеме проводимой терапии; шкала оценки интенсивности боли; шкала общего клинического впечатления.
Статистическая обработка полученных результатов проводилась с использованием компьютерной программы Microsoft Excel 2000, проводилось внутригрупповое и межгрупповое сравнение. Проверялась достоверность изменения болевой симптоматики под влиянием кетанова в сравнении с трамалом. Критерием достоверности считалось достижение уровня р=0.05 и меньше.
Эффект признавался хорошим, если достигалась редукция болевой симптоматики по шкале оценке интенсивности боли на 50% к 3 дню лечения, а показатели шкалы общего клинического впечатления не превышали 2 баллов на 7 день исследования.
2. Результаты исследования
Оценка терапевтической эффективности кетанова производилась по следующим параметрам:
1. скорость наступления терапевтического эффекта;
2. выраженность анальгетического действия;
3. длительность действия препарата;
4. проявление общих или местных побочных эффектов
5. взаимодействие с другими препаратами и оценка его безопасности.
Итак, клинические исследования препарата кетанов позволили сделать следующие выводы. При внутримышечном введении препарат начинал действовать через 15-20 минут (17,1 ±2,9). В контрольной группе обезболивающий эффект развивался быстрее — через 5-10 минут (8,5±2,1). Как видно по представленным результатам, статистически достоверного результата между группами в этом параметре выявлено не было (рисунок 1).
Рисунок 1.
Динамика болевых расстройств при использовании разовой дозы КЕТАНОВА в сравнении с ТРАМАЛОМ (средние показатели) основная группа N=30; контрольная группа N= 26
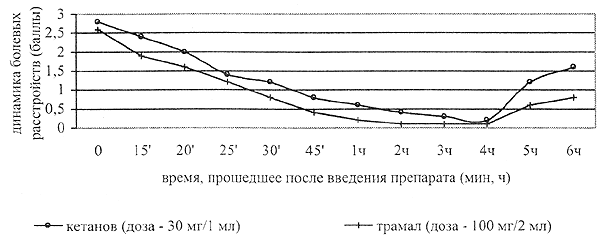
Длительность анальгетической активности кетанова в минимальной разовой дозе 30 мг (1 мл) составляла в среднем 4,5-5,5 часа (4,4+1). При использовании трамала длительность анальгезии в среднем составляла 4-6 часов (5,1 ±0,7). В данном случае достоверной разницы между группами также не было. Поэтому, в первые 4—5 дней кетанов вводился внутримышечно 4 раза в день через каждые 4 часа в дозе 30 мг (1.0). Установленная доза (120 мг в день) была достаточной и адекватной для стойкого купирования болевой симптоматики в рамках героинового абстинентного синдрома. Анальгетический эффект кетанова был оценен как высокий, сравнимый с анальгетическим эффектом трамала (рисунок 2).
Рисунок 2.
Сравнительная характеристика кетанова и трамала при купировании болевых расстройств в рамках опийного (героинового) абстинентного синдрома
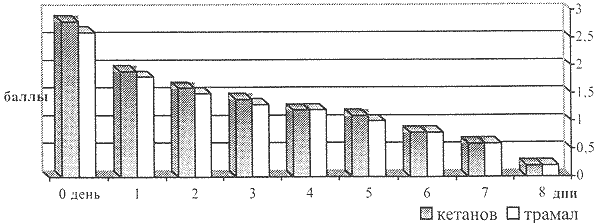
Но анальгетический эффект кетанова не во всех случаях проявлялся одинаково. При выборе тактики лечения многое зависело от выраженности болевого компонента опийного (героинового) абстинентного синдрома. При умеренной болевой симптоматике (20 пациентов - 67%) влияния одного кетанова было достаточно. При выраженных проявлениях (10 пациентов — 33%) в схему лечения добавлялся трамал (таблица 4).
Таблица 4.
Распределение доз при сочетанием использовании кетанова и трамала в случаях выраженного болевого компонента (основная группа)
|
Дни терапии |
Препараты, дозы, время приема (10,00 – 14,00 – 18,00 – 22,00) |
|
|
кетанов 1.0-30 мг |
трамал 1.0-50 мг |
|
|
1 |
1.0 - 0 - 1.0 - 1.0 |
0 - 0 - 0 - 0 |
|
2 |
1.0 - 1.0 - 1.0 - 1.0 |
0 - 0 - 0 - 2.0 |
|
3 |
1.0 - 1.0 - 1.0 - 1.0 |
0 - 0 - 0 - 2.0 |
|
4 |
1.0 - 0 - 1.0 - 1.0 |
0 - 0 - 0 - 2.0 |
|
5 |
1.0 - 0 - 0 - 1.0 |
0 - 0 - 0 - 0 |
|
6 |
Переход на таблетированную форму кетанова |
|
Как уже отмечалось выше, максимальная выраженность всех проявлений опийного (героинового) абстинентного синдрома отмечалась на 2—3 день отнятия наркотика. При этом, как правило, у больных отмечалась и суточная динамика состояния: усиление тревожной, дисфорической, алгической симптоматики наблюдалось в вечернее время. Именно адекватные терапевтические мероприятия, направленные на купирование болей, снижение тревоги, предупреждение бессонницы во многом определяли успешность проводимого лечения. В таких случаях хороший эффект наблюдался при сочетанном применении кетанова и трамала (таблица 4). При использовании такой тактики наблюдалось потенцирование анальгетического действия, что в свою очередь оказывало положительное влияние на общее состояние пациентов: они становились спокойнее, достаточно быстро засыпали на плановых назначениях, сон был продолжительным, глубоким, без пробуждений в течение ночи и без возобновления болевых ощущений. Такая же тактика применялась и в тех случаях, когда наблюдались картины «развернутого» абстинентного синдрома с превалированием болевой симптоматики в течение дня.
Немаловажным в наркологической практике является вопрос развития постинъекционных инфильтратов после введения определенных групп препартов или их больших количеств. При использовании кетанова таких осложнений не наблюдалось, при внутримышечном введении препарат быстро всасывался, не было отмечено и местно-раздражающего действия.
Кетанов использовался и в постабстинентном состоянии, при возобновлении болевой симптоматики, сопровождающей, как правило, актуализацию патологического влечения к наркотику. В таких случаях пациенты предъявляли жалобы на «непонятные, тянущие», «подкручивающие» боли в мышцах и суставах конечностей, отмечали, что не могут найти удобное место, уточняли, что при движениях боль усиливается. Препарат применялся в комплексе с психотропными препаратами, в основном, в таблетках в дозе 10-30 мг до 2-3 раз в день. Клинический эффект наблюдался через 20-25 минут, длительность действия колебалась от 4 до 6 часов.
На протяжении всего периода применения кетанова каких-либо побочных действий или осложнений не наблюдалось. Возможно, это связано с коротким курсом назначения препарата. Случаев привыкания к препарату также отмечено не было.
При взаимодействии кетанова с другими психотропными препаратами не было отмечено ни усиления действия последних, ни его ослабления.
Использование шкалы общего клинического впечатления позволило подтвердить значительный терапевтический эффект кетанова, не уступающий трамалу (рисунок 3).
Рисунок 3.
Шкала общего клинического впечатления (степень терапевтической эффективности)
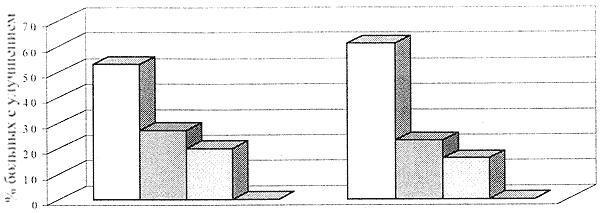
Примечание. Баллы отражают степень терапевтической эффективности препарата в процессе всего курса лечения:
1 — значительный терапевтический эффект
2 — умеренный
3 — минимальный
4 — изменений нет или ухудшение
Далее: »» ЭФФЕКТИВНОСТЬ ИСПОЛЬЗОВАНИЯ МЕТОДА
Комментарии
ПРАКТИКА ПЕДИАТРА
