Эффективность комплексной терапии с применением инъекционной формы хондроитина сульфата и гиалуроната натрия при остеоартрите коленного сустава.
СтатьиОпубликовано в журнале Терапевтический архив . 2019; 05: 96-102
Беляева Е.А., Авдеева О.С.
ФГБОУ ВО «Тульский государственный университет», медицинский институт
Аннотация: Проведено исследование эффективности комплексной терапии ОА коленного сустава в реальной клинической практике. В исследовании приняли участие 125 пациентов в возрасте от 50 до 70 лет, из них 25 мужчин и 100 женщин, с диагнозом ОА коленного сустава, 3 рентгенологической стадии по Келлгрену-Лоуренсу. Средний возраст пациентов составлял 62±3,21 лет, средняя продолжительность заболевания 9,4±2,8 лет. Пациенты были рандомизированы на три группы по 35 человек, одна группа – 20 человек стала контрольной. Группа 1 – 35 человек: получала НПВП+ Инъектран 200 мг в/м через день № 25. Группа 2 – 35 человек :- НПВП + Ферматрон 1 % 2 мл с интервалом 7 дней в/с № 3. Группа 3 – 35 человек: - НПВП+ Инъектран 200 мг в/м через день № 25 + Ферматрон 1 % 2 мл с интервалом 7 дней в/с № 3. Контрольная группа: - 20 человек - получала только НПВП. Оценка симптомов заболевания проводилась при помощи индекса WOMAC до начала терапии, через 8 и 12 недель. Интенсивность боли при ходьбе оценивалась по ВАШ.
В группах, получавших один из препаратов Инъектран (группа 1) или Ферматрон (группа 2), динамика снижения боли при ходьбе была сопоставимой и составила чуть более 30 %, в обеих группах, это достоверные значения по сравнению с исходными (р<0,01). В группе 3, где применялись оба препарата Инъектран+Ферматрон, боль при движении уменьшилась более чем на 50 % от исходных значений, то есть совместное применение двух препаратов одновременно позволило улучшить результаты лечения в 1,5 раза. Также исследовалась потребность пациентов в НПВП до и после проведенной терапии. Во всех группах исследования пациенты смогли снизить дозу применяемых НПВП. В контрольной группе 80 % сохранили к 8 неделе прежнюю дозу НПВП, тогда как в группе И+Ф только 5,7 % в группе Ф 17.1 %, в группе И 11,5 %. Межгрупповые различия достоверны (р<0,001). Число пациентов, полностью отказавшихся от НПВП было наибольшим в группе И+Ф (22,8 %), что в 2 раза больше, чем в группе Ф (11,4%) и в 4 раза больше, чем в группе И (5,7 %), различия достоверны (р<0,01).
К окончанию терапии снижение суммарного индекса WOMAC в наибольшей степени отмечено в группе 3 (И+Ф) – более, чем на 50 %, в 1 (И) и 2 (Ф) группах – более, чем на 40%, в контрольной группе – на 20 %. Во всех группах через 12 недель отмечалась тенденция к сохранению и даже нарастанию эффекта от проведенной терапии.
Ключевые слова: остеоартрит, коленный сустав, хондроитина сульфат, гиалуронат натрия, комплексная терапия
Проблема терапии остеоартрита (ОА) коленного сустава имеет большое социально-экономическое значение в связи с высокой распространенностью этой патологии и прогнозируемым ростом в последующие годы. [1,2]. Поскольку по-прежнему ОА является частой причиной инвалидизации, а результаты его лечения во многих случаях не оправдывают ожидания, постоянно проводится поиск новых схем лечения, разрабатываются подходы к терапии, с учетом новых знаний об этом заболевании.
В 1911 г. T. Muller предложил выделить группу заболеваний суставов дегенеративно-дистрофической природы как «arthrosis deformans», где ОА отводилось ведущее место. Положение об ОА как о дистрофически-дегенеративном заболевании суставов полностью сформировалось в середине 1980-х годов, когда было определено, что хондроциты имеют низкую метаболическую активность и поэтому не способны восстановить поврежденный хрящ. Также считалось, что вследствие отсутствия васкуляризации хрящ не может ответить обычной воспалительной реакцией на раздражение [3].
Во второе десятилетие XXI века в связи с развитием молекулярной биологии стало возможным изучение патогенеза ОА на субклеточном уровне и это прояснило природу заболевания [4,5,6,7].
Четко доказано, что ОА не просто болезнь износа (болезнь «wear and tear»), а скорее аномальное ремоделирование суставных тканей, управляемое множеством провоспалительных факторов (доказано участие провоспалительных цитокинов: ИЛ-1, ИЛ-6, ФНО-альфа, а также матриксных металлопротеиназ, оксид азота и др.), продуцируемых, прежде всего, субхондральной костью и синовиальной оболочкой. Патологическое ремоделирование формирует функциональную дисфункцию всех суставных структур с развитием однотипных патобиохимических изменений и клинических проявлений. Местная продукция провоспалительных цитокинов оказывает влияние на инициацию и усугубление других возрастзависимых и метаболических заболеваний. Воспаление рассматривается как основной фактор развития и прогрессирования ОА [4,5,6,7,8].
Можно предполагать, что одновременное воздействие по трем направлениям (подавление воспаления, замедление деструкции – «хондропротекция» - сдвиг баланса в сторону анаболических процессов в хряще и вискосупплементация) позволит добиться не только симптоматического эффекта, но и воздействия на механизмы развития и прогрессирования ОА, что будет обеспечивать более высокую эффективность терапии.
Для разработки этой гипотезы на базе кафедры внутренних болезней медицинского института ТулГУ было предпринято исследование эффективности комплексной терапии ОА коленного сустава в реальной клинической практике. В качестве основных лекарственных препаратов использовались: хондроитина сульфат, инъекционная форма 100 мг в мл, 2 мл, торговое название «Инъектран» и гиалуронат натрия 1 % 2 мл в преднаполненном шприце, торговое название «Ферматрон».
Также все пациенты принимали НПВП в режиме по требованию. Исследование получило название ТРИО (фермаТРон + Инъектран при Остеоартрите коленного сустава).
Выбор препаратов был обусловлен наличием обширной доказательной базы по применению хондроитина сульфата и гиалуроната натрия при ОА. А также тем фактом, что данные препараты обладают хорошей переносимостью и рекомендованы ведущими международными экспертными организациями для лечения ОА [9-15].
В препарате «Инъектран» хондроитина сульфат представлен в виде гомогенизированной субстанции («БИОИБЕРИКА С.А.У.,» Испания) MV 7-13 kDa, получаемой из трахеи телят. Соотношение сульфатных групп в препарате (по данным клинических испытаний): Хондроитин 4 сульфат - 53,9%, Хондроитин 6 сульфат - 37,2%. Наилучшая абсорбция и биодоступность обеспечивается низким молекулярным весом. Наилучший эффект препарата - близким к составу хряща человека соотношением хондроитина сульфата-4/хондроитина сульфата-6 (61%:34%). Хондроитина сульфат (ХС) 4 типа – маркер «молодости» хряща. Современные исследования убедительно доказали, что с возрастом уменьшается содержание в хрящевой ткани ХС 4 типа и увеличивается содержание хондроитина сульфата ХС 6 типа. Хондроитина сульфата ХС 4 типа обладает лучшей способностью аккумулировать влагу и имеет лучшие амортизационные свойства [16].
«Ферматрон» относится к 4 поколению препаратов гиалуроновой кислоты, имеет оптимальный молекулярный вес 1,1-2,2 млн. Дальтон, примерно соответствующий молекулярному весу нормальной синовиальной жидкости, изготовлен путем бактериальной ферментации. Стерилизация препарата проводится по методу микромембранной фильтрации с сохранением максимальной нативности препарата, рН стабилизация осуществляется фосфатным буферным раствором, идентичным человеческому. Ферматрон в концентрации 1% был выбран, с одной стороны, из соображений экономической целесообразности. С другой стороны, мы предположили, что если положительный терапевтический эффект 1% формы выпуска будет обнаружен в ходе исследования, то эффект от более вязких и концентрированных форм гиалуроновой кислоты, будет как минимум сопоставимым.
Всего в исследовании приняли участие 125 пациентов в возрасте от 50 до 70 лет, из них 25 мужчин и 100 женщин. Критериями включения в исследование были: установленный диагноз первичного ОА коленного сустава, рентгенологическая стадия III по Келлгрену –Лоуренсу, боль не менее 40 мм по ВАШ, потребность в системном приеме НПВП. Критерии исключения были следующие: внутрисуставное введение препаратов гиалуроновой кислоты в течение 3 месяцев, предшествующих исследованию, прием глюкозамина сульфата или хондроитина сульфата за 1,5 мес. до исследования, вторичный ОА, оперативные вмешательства на коленном суставе, болезни крови, прием оральных антикоагулянтов и варфарина, онкозаболевания. Средний возраст пациентов составлял 62±3,21 лет, средняя продолжительность заболевания 9,4±2,8 лет. Соотношение мужчин и женщин в каждой группе было сопоставимо (таб.1). Пациенты были рандомизированы на три группы по 35 человек, одна группа стала контрольной.
Группа 1 – 35 человек: получала НПВП+ Инъектран 200 мг в/м через день № 25. Группа 2 – 35 человек :- НПВП + Ферматрон 1 % 2 мл с интервалом 7 дней в/с № 3
Группа 3 – 35 человек: - НПВП+ Инъектран 200 мг в/м через день № 25 + Ферматрон 1 % 2 мл с интервалом 7 дней в/с № 3
Контрольная группа: - 20 человек - получала только НПВП. Эта группа сформировалась из пациентов, которые по разным причинам не могли или не хотели применять другие препараты.
Табл.1. Характеристика пациентов, включенных в исследование.
| 1 группа (n=35) -И |
2 группа (n=35) -Ф |
3 группа (n=35) И+Ф |
Контрольная группа (n=20) |
|
| Средний возраст, лет | 63,0±3,5 | 61,1±4,8 | 63,8±4,1 | 62,2±2,3 |
| Пол, М/Ж | 8/27 | 6/29 | 7/28 | 4/16 |
| Средняя продолжительность заболевания, лет | 9,6±2,1 | 10,4±1,8 | 9,8±2,4 | 10,8±2,3 |
Оценка симптомов заболевания проводилась при помощи индекса WOMAC до начала терапии, через 8 и 12 недель. Интенсивность боли при ходьбе оценивалась по ВАШ. Также исследовалась потребность пациентов в НПВП до и после проведенной терапии. Этот критерий мы посчитали важным, так как в реальной клинической практике отмечалась высокая коморбидность, у 89 человек (71,2 %) имелось 2 и более заболевания, у большинства пациентов присутствовала сердечно-сосудистая и другая патология (таб.2), требующая минимизации системного применения НПВП для снижения риска нежелательных реакций.
Табл.2. Коморбидная патология
| Нозология | n=125, М-25, Ж-100: n (/%) |
| АГ | 121 (96,8%) |
| ИБС | 121 (96,8%) |
| ХБП ( СКФ>50) | 27 (21,6%) |
| СД б/инсулинпотребности | 43 (34,4%) |
| ЯБ в анамнезе | 32 (25,6%) |
| БА, ХОБЛ | 13 (10,4%) |
В исследовании был применен факторный протокол 2х2, чтобы оценить роль каждого исследуемого фактора (в нашем случае – лекарственного препарата) по отдельности и в комбинации, а также результаты отсутствия влияния обоих факторов.
Мы сознательно отбирали пациентов с 3 рентгенологической стадией ОА, чтобы оценить лечебные воздействия у больных с наиболее выраженными симптомами заболевания.
Лечение завершили все пациенты. У трех пациентов при введении Ферматрона были отмечены болевые ощущения в месте инъекции, самостоятельно исчезнувшие в течение суток. При применении Инъектрана нежелательных реакций не отмечено.
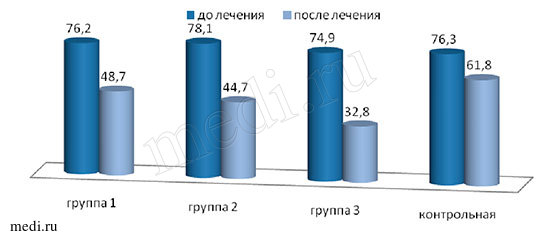
Оценка боли при ходьбе по ВАШ до начала терапии и сразу после ее окончания была выделена отдельно (рис 1), поскольку именно эта характеристика очень важна для врача и определяет готовность пациента расширять двигательную активность. Было выявлено, что уменьшение боли при ходьбе имело место во всех группах. В группах, получавших один из препаратов Инъектран (группа 1) или Ферматрон (группа 2), динамика снижения болевого синдрома была сопоставимой и составила чуть более 30 %, в обеих группах, это достоверные значения по сравнению с исходными (р<0,01). В группе 3, где применялись оба препарата Инъектран+Ферматрон, боль при движении уменьшилась более чем на 50 % от исходных значений, то есть совместное применение двух препаратов одновременно позволило улучшить результаты лечения в 1,5 раза. Межгрупповые различия достоверны (р<0,05). В контрольной группе этот показатель недостоверен.
Рис. 1. Динамика боли при ходьбе до лечения и через 8 недель
Боль в коленных суставах при ходьбе
Во всех группах исследования пациенты смогли снизить дозу применяемых НПВП (таб. 3). В контрольной группе 80 % пациентов сохранили к 8 неделе прежнюю дозу НПВП, тогда как в группе И+Ф только 5,7 % в группе Ф - 17.1 %, в группе И - 11,5 %. Межгрупповые различия достоверны (р<0,001). Число пациентов, отказавшихся от НПВП было наибольшим в группе И+Ф (22,8 %), что в 2 раза больше, чем в группе Ф (11,4%) и в 4 раза больше, чем в группе И (5,7 %), различия достоверны (р<0,01). Большинство больных во всех группах исследования, за исключением контрольной, смогли снизить дозу НПВП в 2 раза.
Таб.3. Потребность в НПВП через 8 недель после начала лечения
| 1 группа(И) (n=35) |
2 группа(Ф) (n=35) |
3 группа (И+Ф) (n=35) |
Контрольная группа (n=20) |
|
| Отказались от приема НПВП | 2 (5,7%) | 4 (11,4 %) | 8 (22,8%) | |
| Снизили дозу НПВП на 50 % и более | 16 (45,7%) | 16 (45,7%) | 21 (60%) | 1 (5%) |
| Снизили дозу НПВП на 25 % | 13 (37,1%) | 9 (25,8%) | 3 (8,5%) | 3 (15%) |
| Сохранили прежнюю дозу НПВП | 4 (11,5%) | 6 (17,1%) | 2 (5,7%) | 16 (80%) |
К окончанию терапии снижение суммарного индекса WOMAC в наибольшей степени отмечено в группе 3 (И+Ф) – более, чем на 50 %, в 1 (И) и 2 (Ф) группах – более, чем на 40%, в контрольной группе – на 20 %. Во всех группах через 12 недель отмечалась тенденция к сохранению и даже нарастанию эффекта от проведенной терапии (рис.2). Таким образом, наблюдается эффект последействия, достигающий наибольшей выраженности при совместном применении Инъектрана и Ферматрона в группе 3. Межгрупповые различия (между 1 и 3, 2 и 3 группами) к 12 неделе наблюдения достоверны, р<0,05.
Рис.2. Значения суммарного индекса WOMAC до лечения, через 8 и 12 недель от начала терапии
Значение суммарного индекса WOMAC

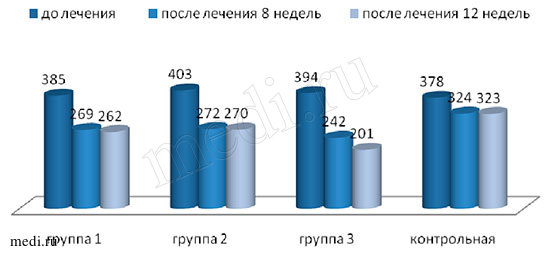
Применение каждого из препаратов (Инъектрана и Ферматрона) по отдельности имело высокую эффективность в отношении влияния на ведущие симптомы ОА у пациентов с тяжелым течением заболевания и 3 рентгенологической стадией по Келлгрену. Однако, совместное применение двух препаратов потенцировало лечебное действие каждого из них, о чем свидетельствует динамика таких показателей как боль, скованность, функциональная недостаточность в группе 3, получавшей Ферматрон и Инъектран одновременно (рис.3,4,5).
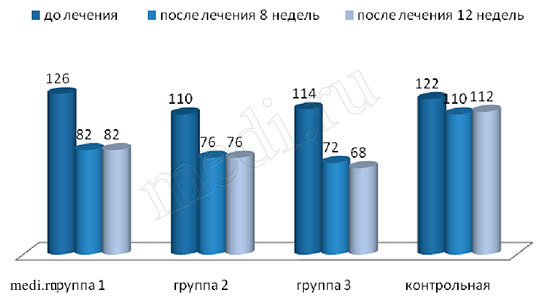
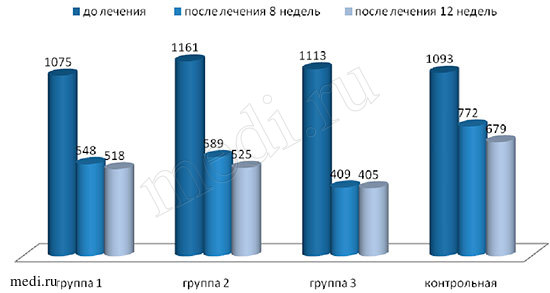
После завершения курса лечения в 3 группе (И+Ф) показатели боли уменьшились в 2 раза, в 1 (И) и 2 (Ф) группах более, чем на 30 %. В контрольной группе результат существенно ниже – 15 %. Функциональные нарушения при совместном применении И+Ф в 3 группе регрессировали на 64 % от исходного уровня, в группе 1 (И) уменьшились на 52 %, в группе 2 (Ф) – на 47 %, а в контрольной группе – менее, чем на 30 %. Показатели скованности в третьей группе (И+Ф) уменьшились на 41 %, во второй (Ф) – на 31 %, в первой (И) на 35 %, в контрольной – на 9 % от начальных значений.
Рис.3,4,5. Динамика показателей боли, скованности и функциональной способности по WOMAC
Боль по WOMAC
Скованность по WOMAC
Функциональная способность по WOMAC
Пациенты с 3 рентгенологической стадией и высокой интенсивностью болевого синдрома часто становятся кандидатами на эндопротезирование коленного сустава. Успешная терапия боли и воспаления у этой группы больных способна отсрочить эндопротезирование или сохранить сустав. Также важно понимать, что всегда есть пациенты с противопоказаниями к проведению эндопротезирования, которые нуждаются в облегчении симптомов заболевания методами консервативной терапии.
Особого внимания заслуживает тот факт, что во всех исследуемых группах у большей части пациентов удалось снизить суммарную недельную дозу системных НПВП на 25 % и 50 %, а в некоторых случаях больные смогли полностью отказаться от приема препаратов этой группы. Наряду с уменьшением клинических проявлений заболевания, ограничение приема системных НПВП является важнейшим результатом, влияющим на качество жизни пациентов, поскольку в нашем исследовании и в реальной клинической практике большинство из них имеют сердечно-сосудистую патологию, при которой применение НПВП в высоких и средних дозах в постоянном режиме нежелательно из-за угрозы дестабилизации АД, прогрессирования ХСН и ХБП и повышения риска сердечно-сосудистых событий. В условиях коморбидности это имеет большое значение, так как позволяет уменьшить вероятность лекарственных взаимодействий и снизить риски нежелательных реакций.
Основным симптомами, ухудшающими качество жизни при ОА коленного сустава, являются боль и нарушение функции. Облегчение этих симптомов ассоциируется у пациента с эффективностью проводимой терапии. Для врача отсутствие боли и прогрессирующих функциональных нарушений означает, что пациент отвечает на проводимое лечение и имеет возможность сохранить сустав.
Результаты лечения самими пациентами в целом были оценены положительно, без выраженных межгрупповых различий (Рис.6,7,8). Преобладали хорошие и отличные оценки терапии, это связано с оправданием ожиданий пациентов в плане уменьшения болей в суставе в покое и при движении. Неудовлетворительные и удовлетворительные результаты были преимущественно у лиц с нейропатической болью и депрессивными проявлениями. Таким пациентам в дальнейшем может быть рекомендовано применение дулоксетина, прегабалина и габапентина, низких доз трамадола. При неэффектитвности всех использованных медикаментозных методов лечения данная категория больных может быть направлена на эндопротезирование сустава.
Рис.6,7,8. Оценка эффективности лечения пациентами.
Группа 1
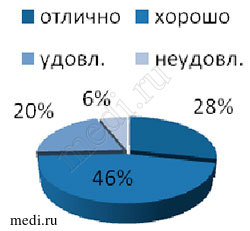
Группа 2
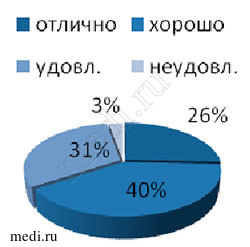
Группа 3
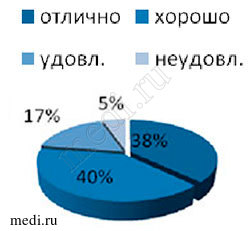
Согласно результатам проведенного исследования сочетанное применение Инъектрана и Ферматрона позволяет к 8 неделе лечения уменьшить болевой синдром более, чем на 50 %, способствует сокращению скованности на 41 % и приводит к уменьшению функциональных нарушений на 64 % от исходных показателей и расширению двигательной активности у пациентов с ОА коленного сустава. К 12 неделе наблюдения, через месяц после окончания применения препаратов положительный эффект не только сохраняется, но и нарастает, продолжается регресс клинической симптоматики. Эта тенденция отмечается во всех трех основных группах исследования.
Результативность комплексной терапии с применением Ферматрона и Инъектрана оказалась выше, чем применение каждого из препаратов по отдельности, также показавшее хорошую эффективность.
Каждый из использованных в исследовании препаратов (И и Ф) оказывает не только симптоматическое, но и патогенетическое действие.
Гиалуронат натрия влияет на синовиальный гомеостаз путем восстановления вязкоэластичных свойств синовиальной жидкости, стабилизации коллагеновых волокон капсулы и лигаментарного аппарата, восстановления скорости транспорта метаболитов от клеток через синовиальную среду в лимфатические сосуды и поддержания нормального уровня транссиновиального обмена за счет барьерной и механической функции гиалуроновой кислоты (ГК), а на микроуровне происходит восстановление вязкоэластичного окружения клеточных структур синовиальной оболочки, ноцицепторов, угнетение миграции, фагоцитоза и высвобождения простагландинов под действием ГК и стимуляция выработки сoбственной ГК синовиоцитами [17-19].
Хондроитина сульфат согласно данным многочисленных исследований повышает эластичность и механическую прочность хряща, обеспечивает гидратацию и накопление гиалуроновой кислоты, повышает секрецию внеклеточного матрикса (коллаген, аннексин, агрекан) и факторов роста (PENK, CTGF) соединительной ткани, тормозит деградацию хряща путем блокирования протеаз (SERPINA3, SERPIN1), повышает активность хондроитинсульфатных гликозилтрансферраз, отвечающих за реконструкцию соединительной ткани [9, 20-22].
Противовоспалительное действие его реализуется путем связывания с рецептором СD44 и снижения транскрипции провоспалительного сигнального фактора NF- ᴋB, снижения активации провоспалительных цитокинов (ИЛ1,6, ФНО), ингибирования синтеза ММР и простагландина Е, подавления синтеза ИЛ1-индуцированной экспрессии СОХ2 и повышение уровня тромбоспондина-1 – ингибитора ангиогенеза [9, 13, 20-22].
Причиной успеха комплексной терапии может быть взаимодействие хондроитина сульфата и гиалуронана, при котором хондроитина сульфат защищает гиалуроновую кислоту от воздействия гиалуронидазы путем угнетения ее активности и потенцирования противовоспалительного действия и регуляторного эффекта на метаболизм хряща.
ЛИТЕРАТУРА
- Балабанова Р.М., Эрдес Ш.Ф. Распространеность ревматических заболеваний в Росии в 2012-2013гг./ Научно-практическая ревматология, 2015, 53(2), С. 120-124.
- Фаломеева О.Н., Галушка Е.А., Эрдес Ш.Ф. Распространенность ревматических заболеваний в Росии и США/ Научно-практическая ревматология, 2008. 46 (4), С. 4-13.
- Шумада И.В. Диагностика и лечение дегенеративно-дистрофических поражений суставов. Здоров’я, Київ, 1990
- Xia B, Di Chen, Zhang J et al. Osteoarthritis pathogenesis: a review of molecular mechanisms/Calcif.Tissue Int.2014,95 (6);495-505
- Berenbaum F. (2013) Osteoarthritis as an inflammatory disease (osteoarthritis is not osteoarthrosis!). Osteoarthritis Cartilage, 21: 16–21.
- Дубиков А.И. Остеоартроз: старая болезнь, новые подходы. Совр. ревматология,2013,№ 2: С.82–88.
- Каратеев А.И., Лила А.М. Остеоартрит: современная клиническая концепция и некоторые перспективные терапевтические подходы/Научно-практическая ревматология, 2018 (56), 1, С. 70-81.
- Robinson, Lepus CM, wang Q et al. Low-grade inflammation as a key mediator of the pathogenesis of osteoarthritis/ Nat rev Rheumatol, 2016, 12 (10), 580-592
- Лила А.М., Громова О.А., Торшин И.Ю., Назаренко А.Г., Гоголев А.Ю. Молекулярные эффекты хондрогарда при остеоартрите и грыжах межпозвоночного диска/Неврология. Нейропсихиатрия, психосоматика, 2017, 9 (3), С. 88-97.
- «Ступенчатая» терапия хондроитина сульфатом у больных остеоартритом на поликлиническом этапе/ Современная ревматология, 2017. 11 (3), с.77-80
- Каратеев А.Е., Лила А.М. Российский опыт применения инъекционных форм хондроитина сульфата и глюкозамина сульфата: обзор клинических исследований/Современная ревматология, 201, 12 (1), с. 33-40.
- Иммаметдинова Г.Р, Чичасова Н.В.Хондроитина сульфат при заболеваниях опорно-двигательного аппарата: эффективность и безопасность с позиций доказательной медицины/ Русский медицинский журнал, 2016, (22), С.1481-1488.
- Ronca F., Palmieri L, Panicucci P, Ronca G. Antiinflammatori activity of chondroitin sulfate. Osteoarthritis Cartilage, 1998, may 6, Suppl A:14-21
- Bruyere O, Cooper CC, Pelletier JP et al. An algorithm recommendation for the management of knee osteoarthritis in Europe andinternationally: A report from a task force of the European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis (ESCEO)/Semin Arthritis Rheum, 2014. 44 (3). 253-263
- Bruyere O, Cooper CC, Pelletier JP et al.A consensus statement on the the European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis (ESCEO). Algorithm for the management of knee osteoarthritis – From evidence- based medicine to the real-life setting/. Semin Arthritis Rheum, 2016. 45 (4). 3-11.
- Епифанов В.А. Остеохондроз позвоночника: диагностика, лечение, профилактика :, М. :МЕДпресс-информ, 2004 – изд. 2.
- Федорищев И.А., Гиалуроновая кислота,, монография. М.: , 2011., 237 с.
- Henrotin Y, Raman R., Richette P et al. Consensus statement jn viscosupplementation with hyaluronic acid for the management of OA/ Semin Arthritis Rheum, 2015. 45 (2). 140-149.
- Yasui T., Acatsuca M., Tobetto K. et al. The effect of hyaluronan on interleukin-1 alpha- induced prostaglandin E2 production in human OA sinovial cells/Agents Actions.1992.37 (1-2); 155-156.
- Campo GM,Avenoso A, Campo S et al. Chondroitin-4-sulfate ingibits NF-ḱB translocation and caspase fctivation in collagen-induced arthritis in mice/ Osteoarthritis Cartilage, 2008, Dec.16 (12); 1474-1483/
- Volpi N. Anti-inflammatory activity of chondroitin sulfate: new functions from an old natural macromolecule// Inflammopharmacology. 2011, Dec.19(6):299-306/
- Imada K, Oka H, Kawasaki D. et al/ Antiarthritic action mechanisms of natural chondroitin sulfate in human articular chondrocytes and synovial fibroblasts/Biol Pharm Bull, 2010, 33 (3): 410-414/
