Геронтоинформационный анализ свойств молекулы мексидола
СтатьиОпубликовано в журнале:
«Неврология, нейропсихиатрия, психосоматика» № 9(4), 2017
Громова О.А.1,2, Торшин И.Ю.2, Федотова Л.Э. 1
1ФГБОУ ВО «Ивановская государственная медицинская академия», Иваново, Россия;
2ФГБУ «Федеральный исследовательский центр «Информатика и управление» РАН, Москва, Россия
1153000, Иваново, Шереметевский пр., 8; 2119333, Москва, ул. Вавилова, 40
Цель исследования — комплексная оценка посредством фармакоинформационного профилирования всех возможных эффектов молекул мексидола, холина альфосцерата, пирацетама, глицина, семакса в соответствии с анатомо-терапевтическо-химической классификацией.
Материал и методы. Хемореактомный, фармакоинформационный и геронтоинформационный анализы свойств молекул основаны на хемореактомной методологии. Для хемореактомного анализа использована информация из баз данных PubChem, HMDB и String; для фармакоинформационного анализа — информация из международной классификации АТХ и объединенная выборка данных из баз TTD (Therapeutic target database), SuperTarget, MATADOR (Manually Annotated Targets and Drugs Online Resource) и PDTD (Potential Drug Target Database); для геронтоинформационного анализа — данные о геропротективном действии отдельных веществ из базы PubChem и данные литературы о геропротекции из базы PubMed, собранные посредством системы искусственного интеллекта.
Результаты и обсуждение. Мексидол характеризуется максимальным набором положительных эффектов (препарат для лечения заболеваний ЦНС, сердечно-сосудистой патологии, метаболических нарушений, имеющий противовоспалительные и антиинфекционные свойства, и др.). У мексидола и глицина прогнозируются наименьшие частоты таких побочных эффектов, как зуд, запор, парестезии, рвота и др. Геронтоинформационные оценки изменения продолжительности жизни модельных организмов показали, что мексидол способствует увеличению средней продолжительности жизни C. elegans (на 22,7±10%), дрозофилы (на 14,4±15%) и мышей (на 14,6±3%, контрольные препараты — не более 6,1%).
Заключение. Результаты исследования указывают на высокий потенциал мексидола для использования в качестве геропротектора.
Ключевые слова: геропротекция; побочные эффекты; мексидол; фармакоинформатика; системы искусственного интеллекта.
Geriatric information analysis of the molecular properties of mexidole
Gromova O.A.1,2, Torshin I.Yu.2, Fedotova L.E.12Federal Research Center «Informatics and Control», Russian Academy of Sciences, Moscow, Russia
18, Sheremetevsky Pr., Ivanovo 153000; 240, Vavilov St., Moscow 119333
Objective: by using the pharmacoinformation profiling, to comprehensively assess all possible effects of the molecules of mexidol, choline alfos-cerate, piracetam, glycine, and semax in accordance with the anatomical therapeutic and chemical (ATC) classification system.
Material and methods. Chemoreactomic, pharmacoinformation, and geriatric information analyses of the properties of the molecules are based on chemoreactomic methodology. The chemoreactomic analysis uses the information from the PubChem, HMDB, and String databases; the pharmacoinformation analysis applies the information from the international ATC classification and a combined sample of data from the Therapeutic Target Database (TTD), SuperTarget, Manually Annotated Targets and Drugs Online Resource (MATADOR), and Potential Drug Target Database (PDTD); geriatric information analysis employs the data on the geroprotective effect of individual substances from the PubChem database and the data available in the literature data on geroprotection from the PubMed database, which have been collected through the artificial intelligence system.
Results and discussion. Mexidol is characterized by the maximum set of positive effects (the drug is used to treat CNS and cardiovascular diseases and metabolic disorders and has anti-inflammatory and anti-infective properties, etc.). Mexidol and glycine are predicted to cause the lowest frequency of adverse reactions, such as itching, constipation, paresthesia, vomiting, etc. Geriatric information assessments of changes in the life span of model organisms have shown that mexidol contributes to the higher life expectancy of C. elegans (by 22.7±10%), Drosophila (by 14.4±15%), and mice (by 14.6±3%); the control drugs do by no more than 6.1%.
Conclusion. The results of the study indicate that mexidol has a high potential to be used as a geroprotector.
Keywords: geroprotection; adverse reactions; mexidol; pharmacoinformatics; artificial intelligence systems.
Геропротекторы (дословно — «защищающие от старости») — группа препаратов, увеличивающих продолжительность и качество жизни. Препараты с геропротективными свойствами способствуют замедлению темпов старения, отдалению возникновения заболеваний, обычно ассоциируемых с пожилым возрастом. Поэтому для геропротекции важны не только адекватная диета и двигательная активность, но и рациональный выбор препаратов, которые позволяют и сохранить здоровье, и продлить жизнь.
С точки зрения фармакологии препараты, назначаемые пациентам пожилого возраста, обязательно должны отвечать следующим трем принципам: 1) максимальное число разнообразных положительных эффектов (мультитаргетность действия), что позволит избежать полипрагмазии; 2) минимальный спектр побочных эффектов; 3) способность увеличивать продолжительность жизни (геропротекция).
К сожалению, у подавляющего большинства имеющихся на рынке препаратов описаны преимущественно побочные эффекты. Собственно геропротекторные эффекты (увеличение продолжительности жизни) исследованы лишь у единичных препаратов (например, у метформина, который используется как стандартный контроль при изучении геропротекторных свойств молекул-кандидатов [1]). Информация о полном наборе положительных свойств препарата в подавляющем большинстве случаев разнесена по большому числу научных публикаций и далеко не всегда входит в официальную инструкцию к препарату. Например, препараты витамина D относятся к одному классу по анатомо-терапевтическо-химической (АТХ) классификации (A11CC05 — колекальциферол) и считаются принадлежащими к одной фармакологической группе (витамины и витаминоподобные средства). Долгое время препараты витамина D назначали при чрезвычайно узком круге нозологий (E55.0 — Рахит активный, M81.4 — Лекарственный остеопороз, M83 — Остеомаляция у взрослых) и только в последнее время к вошедшим в инструкции показаниям стали добавлять, например, A15-A19 — Туберкулез и L40 — Псориаз. В то же время спектр уже установленных и доказанных фармакологических эффектов витамина D гораздо шире, что делает препараты на его основе интересными не только педиатрам, но и терапевтам, эндокринологам, акушерам-гинекологам, неврологам, геронтологам, специалистам по восстановительной и профилактической медицине [2].
Данный пример показывает, что у большинства назначаемых пожилым пациентам препаратов недостаточно изучены геропротективные свойства, это затрудняет рациональный выбор лекарственного средства для конкретного больного в соответствии с указанными выше тремя принципами. Одним из решений данной проблемы может стать использование хемоинформатики в форме хемореактомного, фармакоинформационного и геронтоинформационного анализов свойств молекул, которые являются действующими началами уже известных препаратов.
Цель исследования — оценка результатов применения этого комплексного подхода к молекуле мексидола в сравнении с контрольными молекулами (холина альфосцерат, пирацетам, глицин, семакс).
В нашей стране мексидол (этилметилгидроксипиридина сукцинат, PubChem CID 122298) используется в комплексной терапии цереброваскулярных заболеваний. Молекула мексидола стимулирует повышение синтеза аденозин-трифосфата, проявляет антиоксидантный, антигипоксический и ноотропный эффект, модулирует активность бензодиазепинового, ацетилхолинового и ГАМК*-рецепторных комплексов, характеризуется транквилизирующим, антистрессорным, антиатерогенным, противовоспалительным, антитромботическим действием [3, 4]. Весьма широкий спектр фармакологических эффектов мексидола, важных для терапии цереброваскулярной и сердечно-сосудистой патологии [5], делает его перспективным для использования в геропротекции.
Проведенный нами ранее хемореактомный анализ молекулы мексидола не только подтвердил комплекс его нейропротективных и ангиопротективных свойств, но и позволил сформулировать механизмы осуществления этих эффектов на уровне определенных белков-рецепторов (таргетные белки мексидола — ацетилхолиновые и ГАМК-рецепторы, ингибирование синтеза провоспалительных простагландинов и др.) [4]. От молекул сравнения мексидол отличается более высокой безопасностью (меньшая степень взаимодействия с «проаритмическими» каналами KCNH2, ферментами МАО и CYP1A1, более слабое влияние на серотониновые и опиоидные рецепторы).
Закономерным системно-биологическим продолжением хемореактомного анализа являются фармакоинформационный и геронтоинформационный анализы молекулы мексидола, которые позволяют перейти от рассмотрения эффектов мексидола на уровне реактома (т.е. совокупности всех химических реакций, которые запрограммированы в геноме клеток пациента) к их изучению на уровне организма пациента.
Фармакоинформационный анализ позволяет, во-первых, получить спектр всех вероятных показаний для назначения мексидола с количественной оценкой вероятности каждого из показаний; во-вторых, прогнозировать все классы АТХ, к которым потенциально может быть отнесен мексидол и молекулы сравнения; в-третьих, оценить частоту различных побочных эффектов исследуемых молекул.
Геронтоинформационный анализ — еще одно важное направление применения методологии фармакоинформационного анализа. В результате геронтоинформационного анализа можно получить оценки воздействия мексидола на продолжительность жизни модельных организмов, повсеместно исследуемых в экспериментальной геронтологии (C. elegans, Drosophila Melanogaster, Mus Musculus, Rattus Norvegicus).
Материал и методы. Хемореактомный, фармакоинформационный и геронтоинформационный анализы свойств молекул основаны на хемореактомной методологии — новейшем направлении приложения систем искусственного интеллекта в области постгеномной фармакологии. В рамках постгеномной парадигмы молекула любого лекарственного средства мимикрирует под определенные метаболиты (вследствие наличия определенных сходств химической структуры) и, связываясь с теми или иными белками протеома, оказывает соответствующие данному лекарству эффекты (как позитивные, так и негативные) [6].
Анализ фармакологических «возможностей» молекул в рамках хемореактомной методологии проводится посредством сравнения химической структуры исследуемой молекулы со структурами миллионов других молекул, молекулярно-фармакологические свойства которых уже были изучены в экспериментальных и клинических исследованиях. «Обучение» алгоритмов искусственного интеллекта проводится на основе информации типа big data, представленной в базах данных UMLS, PubMed, PubChem, PharmGKB.
Хемореактомная методология основана на новейших технологиях искусственного интеллекта [7—9]. В рамках комбинаторной теории разрешимости вводится функция расстояния, отражающая «химическое расстояние» между двумя произвольными молекулами [4].
При проведении хемореактомного анализа используется информация, извлеченная из баз данных PubChem [10], HMDB [11] и String [12]. Результаты хемореактомного анализа молекулы мексидола опубликованы ранее [4].
Для фармакоинформационного анализа необходимы информация из международной классификации АТХ и объединенная выборка данных из баз TTD (Therapeutic target database), SuperTarget, MATADOR (Manually Annotated Targets and Drugs Online Resource) и PDTD (Potential Drug Target Database) [13]. Результатами ФИА являются оценки вероятностей отнесения исследуемой молекулы к тому или иному классу препаратов по АТХ, оценки вероятностей для различных показаний и оценки частот встречаемости возможных побочных эффектов.
Геронтоинформационный анализ основан на данных о геропротективном действии отдельных веществ, представленных в базе PubChem [10], и данных литературы о геропротекции в базе PubMed, собранных посредством системы искусственного интеллекта [9]. Нами разработана база данных GRPROT, включающая информацию о 520 веществах, у которых были экспериментально измерены геропротекторные свойства. В результате геронтоинформационного анализа можно получить оценки увеличения средней и максимальной продолжительности жизни модельных организмов (C. elegans, Drosophila Melanogaster, Mus Musculus, Rattus Norvegicus) при применении мексидола и контрольных молекул.
Результаты и обсуждение. Полученные в результате фармакоинформационного анализа показания для назначения мексидола и молекул сравнения (табл. 1) свидетельствуют о перспективности его использования при сердечно-сосудистой патологии (хроническая сердечная недостаточность, артериосклероз, гипертриглицеридемия, инфаркт миокарда, тахикардия), заболеваниях, ассоциированных с хроническим воспалением и/или аллергией (энтерит, отек, лекарственная аллергия, ревматоидный артрит, анкилозирующий спондилит, сенная лихорадка), инфекционных заболеваниях (в том числе при кандидозе) и других патологических состояниях (спастичность мышц, рвота, дисфункция печени, затрудненное дыхание, астения, приливы). Заметим, что дисфункция печени, затрудненное дыхание, астения как показания для потенциального назначения мексидола могут, в частности, относиться и к симптомам сердечно-сосудистых заболеваний. Кроме того, для всех перечисленных выше патологических состояний оценки вероятности приемлемости назначения мексидола были выше, чем для других препаратов.
Таблица 1.
Фармакоинформационные оценки показаний для назначения мексидола и молекул сравнения
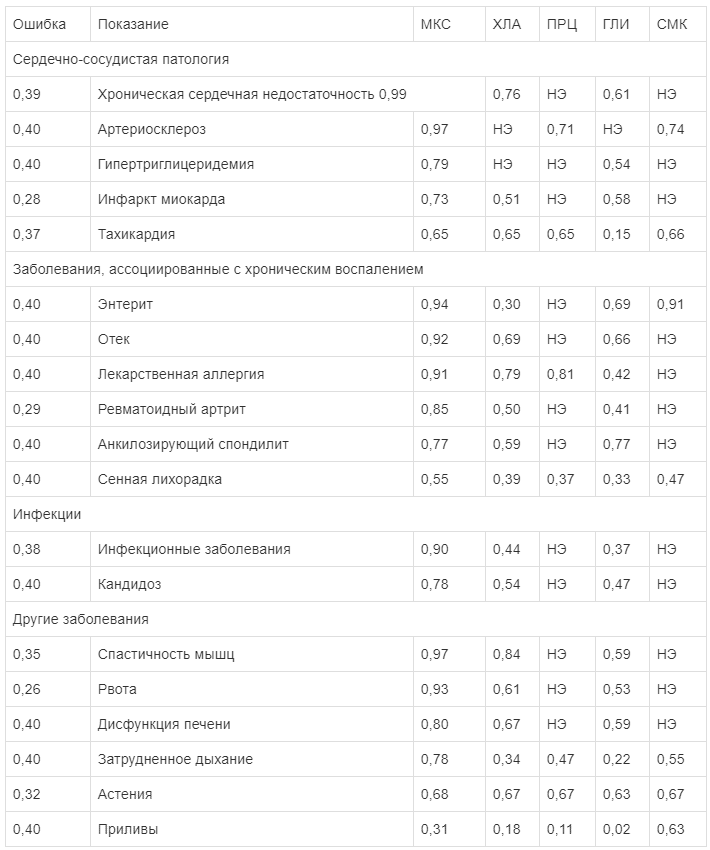 Примечание. Для каждой молекулы представлены оценки вероятности того, что она имеет фармакологический эффект, важный для терапии соответствующей патологии (здесь и в табл. 2). Ошибка — погрешность значения параметра; МКС — мексидол; ХЛА — холина альфосцерат; ПРЦ — пирацетам; ГЛИ — глицин; СМК — семакс; НЭ — нет эффекта (здесь и в табл. 2—4).
Примечание. Для каждой молекулы представлены оценки вероятности того, что она имеет фармакологический эффект, важный для терапии соответствующей патологии (здесь и в табл. 2). Ошибка — погрешность значения параметра; МКС — мексидол; ХЛА — холина альфосцерат; ПРЦ — пирацетам; ГЛИ — глицин; СМК — семакс; НЭ — нет эффекта (здесь и в табл. 2—4). Результаты фармакоинформационного профилирования мексидола в соответствии с классификацией АТХ (табл. 2) подтверждают и существенно дополняют результаты фармакоинформационных показаний для его назначения. Во-первых, фармакоинформационный анализ мексидола по АТХ подтвердил основное направление применения этого препарата — лечение заболеваний ЦНС. Во-вторых, этот анализ показал возможность использования мексидола для лечения сердечнососудистой патологии, коррекции метаболических нарушений (ожирение и сахарный диабет), а также его противовоспалительные и антиинфекционные свойства, что во многом согласуется с опубликованными ранее результатами хемореактомного анализа мексидола [4].
I — препараты, действующие на ЦНС; II — препараты для лечения сердечно-сосудистых заболеваний; III — препараты для лечения метаболических нарушений; IV — противовоспалительные препараты; V — противовоспалительные препараты для использования в дерматологии; VI — антиинфекционные препараты. Различия достоверны при сравнении мексидола со всеми остальными молекулами: *р<0,001; **р<0,05
По данным проведенного нами ранее хемореактомного анализа, молекула мексидола имеет свойства: 1) агониста ацетилхолиновых и ГАМКА-рецепторов; 2) противовоспалительные; 3) нейропротективные; 4) ингибитора коагуляции; 5) сахароснижающие и 6) гиполипидемические [4]. Эти прогнозируемые эффекты молекулы мексидола во многом подтверждаются представленными в настоящей работе результатами фармакоинформационного анализа (см. табл. 2, рис. 1).
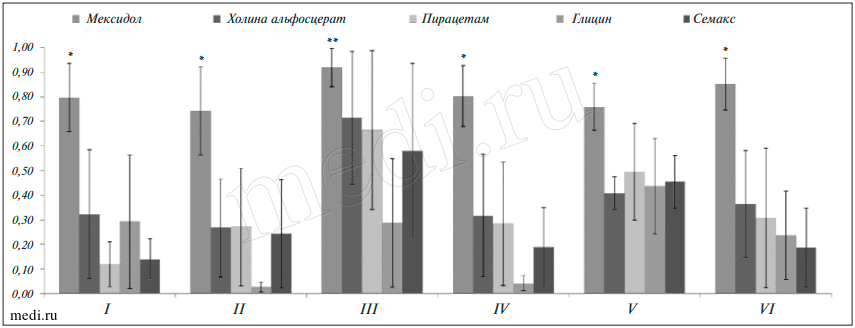 Рис. 1. Средняя вероятность проявления фармакологического эффекта по АТХ. Проведено усреднение по соответствующим разделам табл. 2.
Рис. 1. Средняя вероятность проявления фармакологического эффекта по АТХ. Проведено усреднение по соответствующим разделам табл. 2.
Так, с высокими значениями вероятности (0,80±0,14) мексидол может быть отнесен к разделам АТХ, описывающим препараты, действующие на ЦНС (анестетики, противоэпилептические препараты, анксиолитики, снотворные и седативные средства, антидепрессанты, препараты для лечения деменции, парасимпатомиметики, лекарственные средства, используемые в терапии болезней привыкания, см. табл. 2). Анксиолитические, антидепрессантные, парасимпатомиметические и нейропротективные свойства мексидола имеют непосредственное отношение к тому, что он может активировать ацетилхолиновые и ГАМК-рецепторы. Активация мускариновых рецепторов ацетилхолина приводит к стимуляции пути выживания нейронов ERK1/2, нормализует процессы пре- и постсинаптического возбуждения холинергических синапсов. Ингибирование М4-мускариновых рецепторов молекулой мексидола способствует ГАМКергической трансмиссии, что усиливает воздействие препарата на ГАМК-рецепторы [4].
Отнесение мексидола к классу N03 (противоэпилептические препараты) соответствует противосудорожной активности его молекулы, оцененной в результате хемореактомного анализа. Например, ингибирование фенилхинон-индуцированных судорог у мышей может осуществляться на 93% при использовании мексидола, на 36% — пирацетама и только на 11% — семакса [4]. Отнесение мексидола к классу N06D (препараты для лечения деменции) полностью соответствует результату хемореактомного анализа: молекула мексидола может ингибировать образование и агрегацию бета-амилоида, а также стимулировать рост нейритов и регенерацию нервной ткани [4].
Интересным и неожиданным результатом является отнесение мексидола к классам N07B (препараты, применяемые при психологических и физиологических зависимостях от различных веществ; с вероятностью 0,97±0,0167) и N07BC (средства для лечения опиатной зависимости; с вероятностью 0,59±3*10-9). Важно подчеркнуть не только достаточно высокие значения вероятности (и нулевые значения для контрольных молекул), но и крайне низкие уровни ошибок. Потенциальный механизм этого фармакологического эффекта мексидола пока не вполне понятен и требует отдельного изучения.
Отнесение молекулы мексидола к группам препаратов для лечения сердечно-сосудистой патологии (ингибиторы агрегации тромбоцитов, сердечные гликозиды, альфа-адреноблокаторы, бета-адреноблокаторы, ингибиторы АПФ) соответствует более выраженному гемодинамическому потенциалу молекулы мексидола по сравнению с контрольными молекулами, установленному в результате хемореактомного анализа. В частности, расчеты показали, что ингибирование коллаген-индуцированной агрегации тромбоцитов мексидолом осуществляется при гораздо более низких концентрациях вещества (IC50=462 нМ), чем в случае семакса (IC50=4295 нМ) [4]. Фармакоинформационное моделирование указывает на такой физиологический механизм антитромботического действия мексидола, как антагонизм к витамину К — отнесение к классу B01AA (антагонисты витамина К) с вероятностью 0,81±0,075. Потенциальные свойства мексидола как антагониста альфа-адренорецепторов, бета-адреноблокатора и/или ингибитора АПФ также заслуживают дальнейшего изучения.
Фармакоинформационное профилирование мексидола как препарата для коррекции метаболических нарушений (A08AA — препараты для лечения ожирения центрального действия; А10 — средства для лечения сахарного диабета; A14 — анаболические препараты для системного использования) также подтверждается результатами хемореактомного анализа, показавшего, что мексидол может снижать повышенный уровень глюкозы на 34%, в то время как холина альфосцерат — на 8%, а пирацетам — всего на 4%. Улучшение метаболизма глюкозы клетками при участии мексидола может осуществляться за счет активации фермента глюкокиназы и рецептора PPAR-гамма, что способствует нормализации уровня глюкозы в крови а также снижению содержания холестерина и триглицеридов. Отметим и весьма малое химическое расстояние (dx=0,08) между молекулой мексидола и дигидроксинортропаном — алкалоидом шелковицы, проявляющим гипогликемический эффект [4].
Фармакоинформационное профилирование мексидола как противовоспалительного препарата (группа коксибов, препараты для лечения обструктивных заболеваний дыхательных путей, антигистаминные средства), в том числе дерматологической направленности (топические средства для лечения псориаза, акне), опять же подтверждается данными хемореактомного анализа. При этом молекулярные механизмы, установленные в ходе этого анализа, полностью соответствуют результатам профилирования.
Так, хемореактомный анализ мексидола показал частичное ингибирование ферментов 5-липоксигеназы и циклооксигеназы 2 (например, ЦОГ2 — на 46±17%), для молекул сравнения этот показатель был значительно ниже (не более чем на 23±17%) [4]. Фармакоинформационный анализ с вероятностью 0,79±0,31 позволил отнести мексидол к группе M01AH (коксибы), которые являются специфическими ингибиторами ЦОГ2. В отличие от коксибов мексидол частично ингибирует ЦОГ2, что может потенциально снижать риск формирования геморрагических осложнений.
Хемореактомное моделирование также установило ингибирование молекулой мексидола секреции гистамина (на 43±9%), у молекул сравнения такого эффекта не отмечено [4]. При фармакоинформационном профилировании выявлено, что мексидол относится к группе R06AX (другие антигистаминные препараты для системного применения) с вероятностью 0,71±0,36.
Мексидол действительно проявляет противовоспалительные свойства. Например, использование его в комплексном лечении ревматоидного артрита у женщин (n=62) способствовало регрессу активности ревматоидного воспаления, улучшению функционального статуса и уменьшению выраженности депрессивной симптоматики [14]. Внутрисуставное введение мексидола при экспериментальном посттравматическом артрите приводило к активации процессов биосинтеза коллагена и репарации хряща, уменьшало выраженность воспалительных изменений в суставе [15].
Интересным результатом фармакоинформационного анализа является профилирование мексидола как противовоспалительного препарата дерматологической направленности (хотя и с невысокими значениями вероятности — от 0,64±0,40 до 0,88±0,40), который может быть эффективен при местной терапии псориаза и акне (D05 — препараты для лечения псориаза; D10 — препараты для лечения угревой сыпи). Эффект мексидола при этих заболеваниях будет осуществляться, вероятно, в соответствии с теми же противовоспалительными механизмами — ингибирование ЦОГ2, 5-липоксигеназы и секреции гистамина.
Другим неожиданным результатом фармакоинформационного профилирования является отнесение мексидола к противоинфекционным препаратам (противогрибковые средства, антибактериальные препараты для системного использования, тетрациклины, противовирусные препараты, см. табл. 2). Молекулярные механизмы для этого действия мексидола не очевидны, хотя в ходе хемореактомного анализа была установлена достаточно высокая степень сходства (dx=0,25) между молекулами мексидола и этамбутола, являющегося антимикобактериальным антибиотиком. Кроме того, молекула мексидола, имитируя D-кольцо тетрациклина [16], может являться неспецифичным ингибитором бактериальных рибосом.
Таблица 2.
Фармакоинформационные оценки вероятности отнесения мексидола и молекул сравнения к различным группам препаратов по классификации АТХ
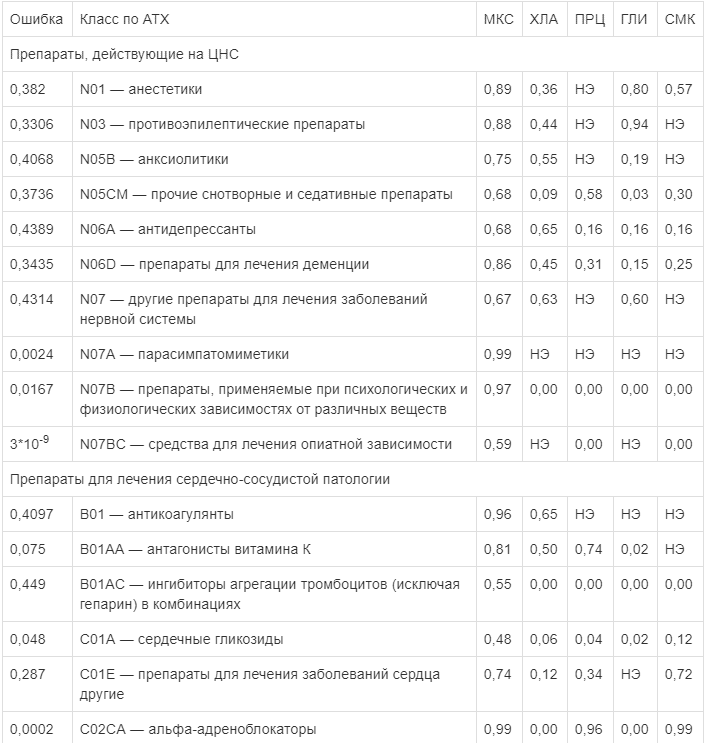
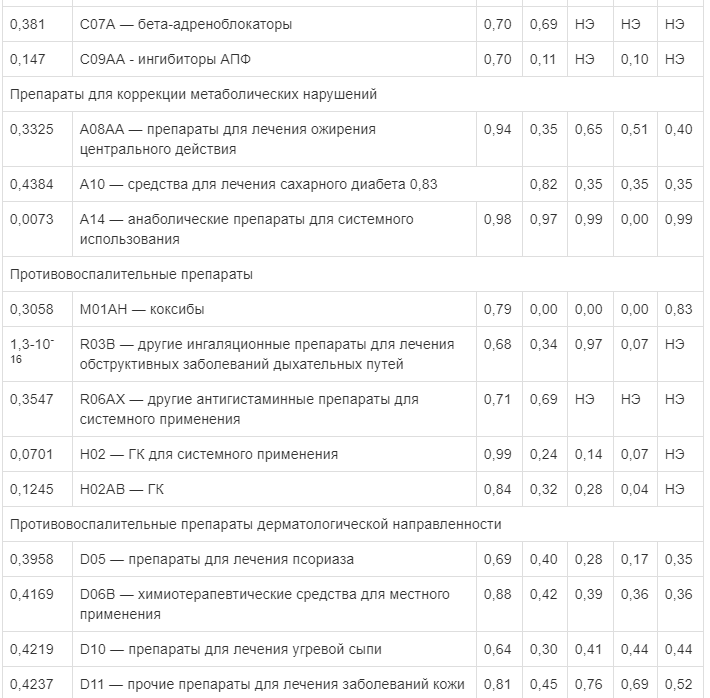
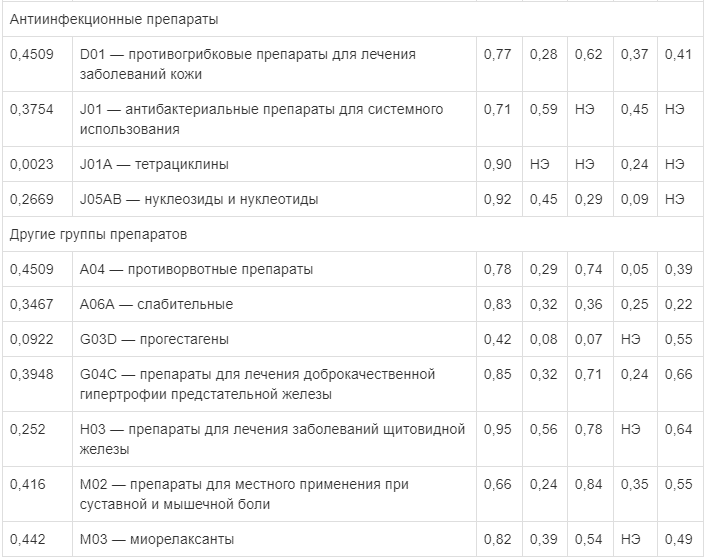 Примечание. Результаты упорядочены в соответствии с разделами классификации АТХ. Ингибиторы АПФ — ингибиторы ангиотензин-превращающего фермента; ГК — глюкокортикоиды.
Примечание. Результаты упорядочены в соответствии с разделами классификации АТХ. Ингибиторы АПФ — ингибиторы ангиотензин-превращающего фермента; ГК — глюкокортикоиды. Мексидол действительно способствует лечению инфекционных заболеваний: при ополаскивании полости рта раствором мексидола отмечено умеренное противомикробное действие, наиболее выраженное в отношении аммиак-продуцирующей микрофлоры. Ротовые ванночки с ополаскивателем, содержащим мексидол, приводят к достоверно выраженному и быстрому купированию явлений воспаления в десне, что может являться полезным при профилактике и лечении гингивита [17, 18].
Таким образом, фармакоинформационное профилирование исследованных молекул в соответствии с АТХ показывает, что мексидол вполне отвечает первому принципу назначения препаратов пациентам пожилого возраста и является препаратом с максимальным числом положительных эффектов.
Фармакоинформационный анализ также выявил соответствие мексидола и второму принципу лечения пожилых больных — минимальный спектр побочных эффектов. Кроме того, при оценке частот встречаемости побочных эффектов (табл. 3) показано, что побочные эффекты, связанные с нарушениями водно-минерального баланса (усиление мочеиспускания, гипокалиемия, гиперкальциемия, гематурия) и нежелательным воздействием на сердечно-сосудистую систему (синкопе, повышенный уровень холестерина в крови, кардиомиопатия, атриовентрикулярный блок, тромбофлебит), были весьма редкими для всех исследованных препаратов.
Таблица 3.
Фармакоинформационные оценки частот встречаемости побочных эффектов (в %), потенциально связанных с исследуемыми молекулами
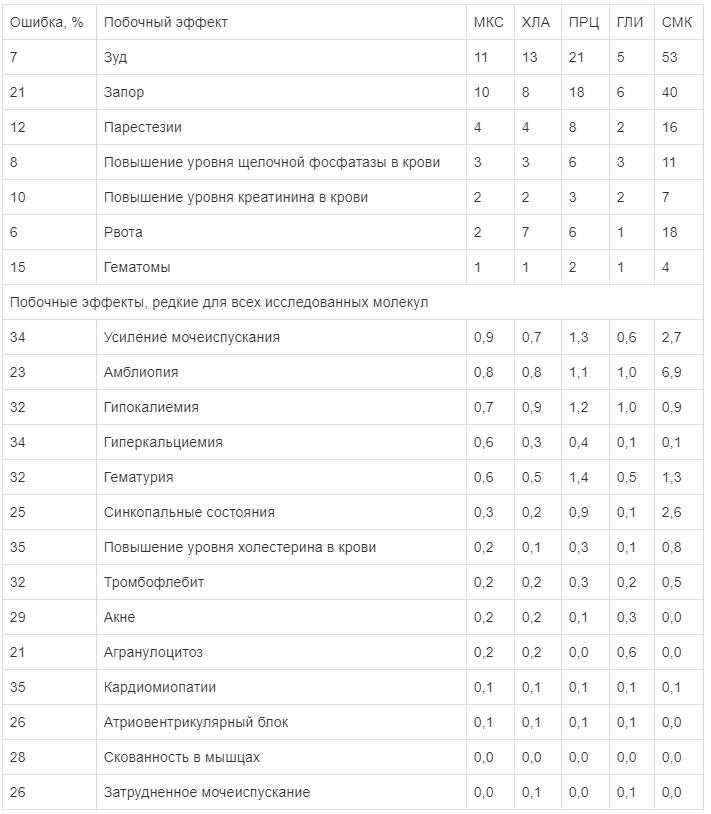 Примечание. Побочные эффекты упорядочены по убыванию частот их встречаемости для мексидола.
Примечание. Побочные эффекты упорядочены по убыванию частот их встречаемости для мексидола. Из всех изученных препаратов мексидол и глицин характеризовались наименьшей частотой возникновения зуда (11%), запора (10%), парестезий (4%), повышения уровня в крови щелочной фосфатазы (3%) и креатинина (2%), а также рвоты (2%), гематом (1%). Заметим, что указанные частоты встречаемости сравнимы с результатами для групп плацебо.
Мексидол отвечает и третьему принципу назначения препаратов пациентам пожилого возраста — способствовать максимальному увеличению продолжительности жизни. Под влиянием мексидола наблюдается среднее увеличение продолжительности жизни C. elegans (на 22,7±10%), дрозофилы (на 14,4±15%) и мышей (на 14,6±3%). Интересно отметить, что все препараты сравнения в той или иной степени увеличивали продолжительность жизни более простых организмов (C. elegans и мушки-дрозофилы), но только мексидол оказывал выраженное действие на увеличение продолжительности жизни мышей (на 14,6±3%, контрольные препараты — 1,0—6,1%; табл. 4, рис. 2).
Таблица 4.
Геронтоинформационные оценки увеличения продолжительности жизни (в %) модельных организмов при использовании мексидола и контрольных молекул
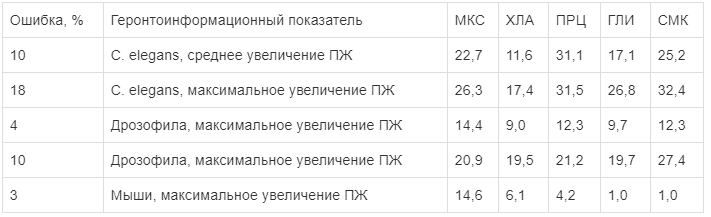 Примечание. ПЖ — продолжительность жизни.
Примечание. ПЖ — продолжительность жизни. 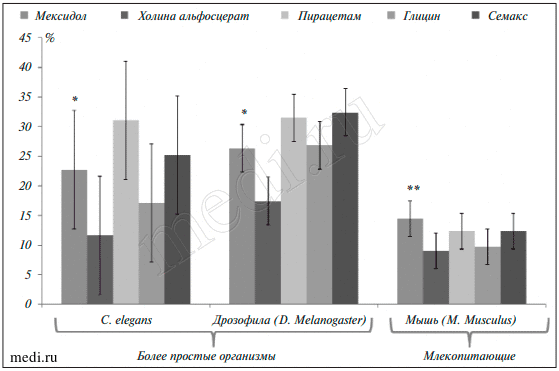 Рис. 2. Среднее увеличение продолжительности жизни (в %) модельных организмов для исследованных молекул: основные результаты геронтоинформационного анализа. *р<0,01 при сравнении мексидола с холина альфосцератом; **р<0,05 при сравнении мексидола со всеми остальными молекулами.
Рис. 2. Среднее увеличение продолжительности жизни (в %) модельных организмов для исследованных молекул: основные результаты геронтоинформационного анализа. *р<0,01 при сравнении мексидола с холина альфосцератом; **р<0,05 при сравнении мексидола со всеми остальными молекулами.
Заключение. Рациональный персонализированный выбор фармакологических препаратов для пожилых пациентов создает условия для увеличения продолжительности жизни и замедления темпов старения. Препараты, назначаемые пациентам пожилого возраста, должны характеризоваться: 1) максимальным числом положительных эффектов; 2) минимальным числом побочных эффектов; 3) способностью увеличивать продолжительность жизни. Фармакоинформационное профилирование исследованных молекул в соответствии с АТХ показывает, что мексидол является препаратом с максимальным числом положительных эффектов (препарат для лечения заболеваний ЦНС, сердечно-сосудистой патологии, метаболических нарушений, имеющий противовоспалительные и антиинфекционные свойства и др.). Из всех исследованных препаратов мексидол и глицин характеризовались наименьшей частотой побочных эффектов (зуд, запор, парестезии, рвота и др.). Геронтоинформационные оценки изменения продолжительности жизни модельных организмов показали, что мексидол способствует среднему увеличению продолжительности жизни C. elegans (на 22,7±10%), дрозофилы (на 14,4±15%) и мышей (на 14,6±3%, контрольные препараты — не более 6,1%). Таким образом, результаты исследования указывают на высокий потенциал мексидола как геропротектора.
ЛИТЕРАТУРА
1. Folch J, Busquets O, Sanchez-Lopez ME, et al. Experimental models for aging and their potential for novel drug discovery. Curr Neuropharmacol. 2017 Jul 7. doi: 10.2174/1570159X15666170707155345. [Epub ahead of print]
2. Громова ОА, Торшин ИЮ. Витамин D: смена парадигмы. Москва: ГЭОТАР Медиа; 2016. [Gromova OA, Torshin IYu. Vitamin D: smena paradigmy [Vitamin D: a paradigm shift]. Moscow: GEOTAR Media; 2016.]
3. Воронина ТА. Мексидол: спектр фармакологических эффектов. Журнал неврологии и психиатрии им. C.C. Корсакова. 2012;112(12):86-90. [Voronina TA. Mexidol: spectrum of pharmacological effects. Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2012;112(12):86-90. (In Russ.)].
4. Торшин ИЮ, Громова ОА, Сардарян ИС, Федотова ЛЭ. Сравнительный хемореактомный анализ мексидола. Журнал неврологии и психиатрии им. C.C. Корсакова. 2017;117(1-2):75-83. [Torshin IYu, Gromova OA, Sardaryan IS, Fedotova LE. A comparative chemoreactome analysis of mexidol. Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2017;117(1-2):75-83. (In Russ.)].
5. Стаховская ЛВ, Шамалов НА, Хасанова ДР и др. Результаты рандомизированного двойного слепого мультицентрового плацебо-контролируемого в параллельных группах исследования эффективности и безопасности мексидола при длительной последовательной терапии у пациентов в остром и раннем восстановительном периодах полушарного ишемического инсульта (ЭПИКА). Журнал неврологии и психиатрии им. C.C. Корсакова. 2017;117(3-2):55-65. [Stakhovskaya IV, Shamalov NA, Khasanova DR, et al. Results of a randomized double blind multicenter placebo-controlled, in parallel groups trial of the efficacy and safety of prolonged sequential therapy with mexidol in the acute and early recovery stages of hemispheric ischemic stroke (EPICA). Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2017;117 (3-2):55-65. (In Russ.)].
6. Torshin IYu. Bioinformatics in the postgenomic era: physiology and medicine. New York: NovaBiomedicalBooks; 2007.
7. Журавлeв ЮИ, Рудаков КВ, Торшин ИЮ. Алгебраические критерии локальной разрешимости и регулярности как инструмент исследования морфологии аминокислотных последовательностей. Труды МФТИ. 2011;3(4):67-76. [Zhuravlev YuI, Rudakov KV, Torshin IYu. Algebraic criteria for local solvability and regularity as a tool to investigate the morphology of amino acid sequences. Trudy MFTI. 2011;3(4):67-76. (In Russ.)].
8. Рудаков КВ, Торшин ИЮ. Об отборе информативных значений признаков на базе критериев разрешимости в задаче распознавания вторичной структуры белка. ДАН. 2011;(1):1-5. [Rudakov KV, Torshin IYu. On the selection of informative characteristic values on the basis of criteria of solvability in the problem of protein secondary structure recognition. DAN. 2011;(1):1-5. (In Russ.)].
9. Торшин ИЮ, Громова ОА. Экспертный анализ данных в молекулярной фармакологии. Москва: МЦНМО; 2012. 768 с. [Torshin IYu, Gromova OA. Ekspertnyi analiz dannykh v molekulyarnoi farmakologii [Expert data analysis in molecular pharmacology]. Moscow: MTsNMO; 2012. 768 p.]
10. Bolton E, Wang Y, Thiessen PA, Bryant SH. PubChem: Integrated Platform of Small Molecules and Biological Activities. In: Annual Reports in Computational Chemistry. Volume 4. Washington, DC: American Chemical Society; 2008.
11. Wishart DS, Tzur D, Knox C, et al. HMDB: the Human Metabolome Database. Nucleic Acids Res. 2007 Jan;35(Database issue):D521-6.
12. Mering C, Jensen L, Snel B, et al. STRING: known and predicted protein-protein associations, integrated and transferred across organisms. Nucleic Acids Res. 2005;33(Database issue):D433-7.
13. Chen X, Yan C, Zhang X. Drug-target interaction prediction: databases, web servers and computational models. Brief Bioinform.2016 Jul;17(4):696-712. doi: 10.1093/bib/bbv066. Epub 2015 Aug 17.
14. Синеглазова АВ, Волчегорский ИА. Влияние мексидола на качество жизни и депрессивную симптоматику у женщин, пациентов с ревматоидным артритом. Экспериментальная и клиническая фармакология. 2013;76(1):7-10. [Sineglazova AV, Volchegorskii IA. The effect of Mexidol on the quality of life and depressive symptoms in women patients with rheumatoid arthritis. Eksperimental'naya i klinicheskaya farmakologiya. 2013;76(1):7-10. (In Russ.)].
15. Шутова МИ, Козлов СА, Захватов АН и др. Экспериментальное обоснование эффективности антиоксидантной терапии посттравматического артрита. Бюллетень экспериментальной биологии и медицины. 2013;(2):148-50. [Shutova MI, Kozlov SA, Zakhvatov AN, et al. Experimental study of the effectiveness of antioxidant therapy for posttraumatic arthritis. Byulleten’ eksperimental’noi biologii i meditsiny. 2013;(2):148-50. (In Russ.)].
16. Arenz S, Wilson DN. Blast from the Past: Reassessing Forgotten Translation Inhibitors, Antibiotic Selectivity, and Resistance Mechanisms to Aid Drug Development. Mol Cell. 2016 Jan 7;61(1):3-14. doi: 10.1016/j.mol-cel.2015.10.019. Epub 2015 Nov 12.
17. Казарина ЛН, Вдовина ЛВ, Дубровская ЕН. Влияние препарата мексидол на состояние перекисного окисления липидов и активность антиоксидантной системы жидкости в полости рта у пациентов хроническим генерализованным пародонтитом и артериальной гипертензией. Стоматология. 2010;89(2):18-21. [Kazarina LN, Vdovina LV, Dubrovskaya EN. The influence of Mexidol on the state of lipid peroxidation and activity of antioxidant system of the liquid in the oral cavity in patients with chronic generalized periodontitis and hypertension. Stomatologiya. 2010;89(2):18-21. (In Russ.)].
18. Жигулина ВВ. Оценка эффективности мексидола в лечении экспериментального гингивита. Вестник Тверского государственного университета. 2015;(2):153-61. [Zhigulina VV. Assessment of efficacy of Mexidol in the treatment of experimental gingivitis. Vestnik Tverskogo gosudarstvennogo universiteta. 2015;(2):153-61. (In Russ.)].
