Терапия антиагрегантами и нестероидными противовоспалительными препаратами. Соотношение риска и пользы
Статьи Опубликовано в журнале:«РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ»; Неврология; ТОМ 15; № 23; 2007; стр. 1-5.
А. И. Каминный, доктор медицинских наук
НИИ кардиологии ФГУ РКНПК Росмедтехнологий, Москва
Нестероидные противовоспалительные препараты (НПВП), в том числе ацетилсалициловая кислота (АСК), в настоящее время широко применяются с целью облегчения боли, уменьшения воспаления и снижения температуры. Кроме того, низкие дозы АСК используются обычно с целью первичной и вторичной профилактики сердечно-сосудистых (ССЗ) и цереброваскулярных заболеваний. Это наиболее распространенный класс медикаментов, используемых в США. Чаще НПВП используются у пожилых больных. Опрос людей старше 65 лет показал, что 70% из них пользуются НПВП как минимум один раз в неделю, а 34% пациентов, из общего числа принимающих НПВП, пользуются ими ежедневно [1]. Среди НПВП, принимаемых один раз в неделю, преобладал АСК (60%). В 2004 г. в США было сделано более 111 миллионов назначений НПВП, причем большинство из них не пациентам с ССЗ, а больным с артритами и заболеваниями опорно-двигательного аппарата [2]. В 1990 г. в США выявлено 37,9 миллионов пациентов с артритами, что составляло 15% населения страны. К 2020 г. ожидается рост до 59,4 миллионов, т. е. на 57% по сравнению с 1990 г., вследствие чего ожидается рост приема НПВП [1].
Механизм действия НПВП заключается в ингибировании циклооксигеназы — фермента, участвующего в образовании простагландинов из арахидоновой кислоты.
Существуют две изоформы циклооксигеназы — циклооксигеназа-1 (ЦОГ-1) и циклооксигеназа-2 (ЦОГ-2). ЦОГ-1 присутствует практически во всех тканях. В тромбоцитах она обеспечивает превращение арахидовой кислоты в тромбоксан, а в стенках желудка и кишечника является источником защищающих слизистую цитопротективных простагландинов. ЦОГ-2 в норме присутствует в мозге, корковом слое почек и в клетках эндотелия, обеспечивая синтез простациклина [3]. В других тканях экспрессия гена ЦОГ-2 ассоциирована с воспалением, например, выявлено повышение содержания ЦОГ-2 в синовиальной жидкости суставов больных ревматоидным артритом.
Неселективные НПВП ингибируют обе изоформы ЦОГ. Считается, что основное терапевтическое действие этих средств обеспечивается влиянием на ЦОГ-2, тогда как подавление ЦОГ-1 способствует возникновению повреждений слизистой оболочки желудочно-кишечного тракта (ЖКТ).
Селективные ингибиторы ЦОГ-2 (коксибы) создавались для замены неселективных НПВП с целью достижения той же эффективности с меньшей частотой побочных желудочно-кишечных явлений. Ингибиторы ЦОГ влияют на образование важных регуляторов гемостаза — тромбоксана и простациклина. Тромбоксан образуется преимущественно в тромбоцитах, вызывая активацию тромбоцитов, вазоконстрикцию и пролиферацию гладкомышечных клеток. В тромбоцитах образуется только ЦОГ-1, поэтому средства, ингибирующие ЦОГ-1, способны повлиять на синтез в них тромбоксана. Простациклин вырабатывается клетками эндотелия сосудов и является не только ингибитором активации тромбоцитов, но и обладает вазодилятирующим эффектом. Клетки эндотелия сосудов могут экспрессировать обе изоформы ЦОГ. Активирование этих клеток воспалительными стимулами и напряжением сдвига потока крови приводит к экспрессии ЦОГ-2. В клетках эндотелия индуцируется выработка ЦОГ-2, что, в свою очередь, определяет уровень синтеза простациклина в организме [3].
Установлено, что ингибиторы ЦОГ-2 коксибы не влияют на агрегацию тромбоцитов, одновременно подавляя образование простациклина [3]. Исходя из этого, существует вероятность, что изменение соотношения тромбоксан/простациклин может способствовать возникновению тромбозов. У здоровых лиц возрастание риска тромбообразования невелико, так как эндотелий сосудов выделяет другие защитные вещества, в частности, оксид азота. Однако оно становится реальным при наличии различных сопутствующих заболеваний, при которых вероятность возникновения тромбозов также повышена. В связи с этим Британский комитет по безопасности лекарств рекомендовал при первой возможности перевести на альтернативное (не ЦОГ-2 селективное) лечение больных с ишемической болезнью сердца или цереброваскулярной болезнью, которые лечатся любым из ингибиторов ЦОГ-2. Такие же рекомендации, касающиеся использования селективных ингибиторов ЦОГ-2, выпустило FDA [4], отметив, что, согласно данным контролированных клинических испытаний, применение селективных ингибиторов ЦОГ-2 может быть связано с повышенным риском серьезных сердечно-сосудистых событий.
АСК в кардиопротективных дозах в основном необратимо ингибирует ЦОГ-1, вызывая ее ацетилирование, причем инактивированный фермент не может быть восполнен в не имеющих ядра тромбоцитах. Это является основой кардиопротективного клинического действия низких доз АСК.
Большое количество людей, принимающих АСК в кардиопротективной дозе, страдают от хронической боли, в связи с чем принимают как традиционные НПВП, так и селективные ингибиторы ЦОГ-2. Опрос пациентов, принимающих селективные ингибиторы ЦОГ-2, показал, что более 50% из них принимают АСК [5].
НПВП в комбинации с АСК — риск развития эрозивно-язвенных поражений со стороны ЖКТ
При применении всех НВПВ, включая ингибиторы ЦОГ-2 и традиционные НПВП в комбинации с АСК в кардиопротективных дозах, значительно возрастает риск возникновения язвенной болезни. Поэтому гастропротективную терапию следует применять у больных с повышенным риском согласно рекомендациям Консенсуса 2008 г. ACCF (American College of Cardiology Foundation)/ACG (American College of Gastroenterology)/AHA (American Heart Association). Различные неблагоприятные события со стороны ЖКТ и язвенные поражения встречаются у каждого двадцатого пациента при лечении НПВП, а в пожилом возрасте у 1 из 7 больных [6]. Диспепсия, абдоминальная боль или дискомфорт нередко возникают у больных при приеме НПВП, включая АСК. И хотя диспепсия не является четким предиктором язвенной болезни, она у таких пациентов встречается довольно часто. Ряд пациентов, принимающих НПВП, обращает внимание на учащение симптомов рефлюкс-эзофагита [7]. В течение года частота осложнений со стороны ЖКТ у этой категории больных составляет от 2% до 4,5% [6], а риск кровотечения и перфорации составляет 0,2—1,9% [8]. Только в США из-за таких осложнений госпитализируется ежегодно около 107 тыс. пациентов с артритами, из которых 16,5 тыс. госпитализаций заканчиваются летальным исходом [7]. В связи с этим рекомендовано использовать более низкие дозы НПВП, применять более «безопасные» НПВП и увеличивать использование ингибиторов протонной помпы (ИПП). У пожилых больных риск летальных исходов от осложнений со стороны органов ЖКТ повышен в три раза, даже если пациенту назначены меньшие дозы с учетом его возраста и состояния, а также, несмотря на прием селективных ингибиторов, ЦОГ-2 [9]. По данным, представленным Департаментом по делам ветеранов США, около 43% пожилых людей имеют высокий риск развития различных осложнений со стороны ЖКТ вследствие приема НПВП, а лица старше 65 лет составляют группу очень высокого риска (около 87%) [10]. Если смертность от осложнений со стороны ЖКТ вследствие приема НПВП выделить отдельно, то она занимала бы 15 место среди наиболее распространенных причин смертей в США [11]. Больные, принимающие НПВП в комбинации с АСК, представляют другую группу высокого риска. Когда неселективные НПВП комбинируются с АСК, ежегодный риск развития осложнений со стороны ЖКТ составляет 5,6%, а комбинация АСК с коксибами не только не обеспечивает дополнительной гастропротекции, но и увеличивает риск до 7,5% в год. Ряд обсервационных исследований подтвердил, что прием даже низких доз АСК в комбинации с НПВП повышает частоту развития осложнений со стороны органов ЖКТ в 2—4 раза. Так, например, частота ежегодных госпитализаций в скандинавских странах по этому поводу составляет 0,6% для больных, принимающих только один АСК в низких дозах, а комбинация этих же доз АСК с неселективными НПВП увеличивает этот показатель до 1,4% в год [12].
Исследования, в которых проводилась гастроскопия для контроля за состоянием больных, подтвердили возможность коксибов и неселективных НПВП усиливать ульцерогенный эффект АСК [13, 14]. Таким образом, выбор НПВП у пациентов должен сопровождаться обсуждением риска развития осложнений как со стороны ЖКТ, так и со стороны сердечнососудистой системы. Более полные данные о возможностях применения коксибов и неселективных НПВП будут получены после окончания крупного исследования PRECISION, и это, вероятно, внесет определенную ясность в вопросы эффективности и безопасности применения НПВП.
Применение АСК и риск интестинальных осложнений
Согласно рекомендациям ACCF/ACG/AHA для пациентов с риском неблагоприятных исходов рекомендуется назначение гастропротективной терапии. Риск развития осложнений со стороны органов ЖКТ увеличивается с увеличением дозы АСК, и для постоянного приема не следует без необходимости назначать АСК в дозе выше 81 мг/сут. Американская ассоциация кардиологов рекомендует использовать низкие дозы АСК у больных с 10-летним риском развития сердечно-сосудистых заболеваний более 10% [15]. С этой целью в США более 50 млн человек постоянно принимают АСК в дозах 325 мг в сутки и менее [16]. Использование низких доз АСК сопровождается 2-4-кратным увеличением риска развития осложнений со стороны органов ЖКТ [17, 18], причем применение кишечнорастворимых или забуференных форм препарата не уменьшает риск возникновения кровотечений [19, 20].
Была проведена оценка среднего риска развития осложнений со стороны ЖКТ при приеме кардиопротективных доз АСК. Она составила около 5 случаев на 1000 принимающих АСК больных в год. Среди пожилых больных отношение шансов возникновения кровотечения возрастало с увеличением дозы от 75, 150 до 300 мг в сутки, составив 2,3, 3,2 и 3,9 соответственно [17]. Уменьшение дозы АСК не приводило к уменьшению антитромботического эффекта, но ее увеличение сопровождалось повышением риска кровотечения [21]. Сложность выбора дозы возникает из-за противоречивых данных. К настоящему времени проведено более 14 рандомизированных, плацебо-контролируемых исследований с применением АСК в кардиопротективной дозе от 75 до 325 мг в сутки, в которых низкие дозы ассоциировались с возрастанием частоты осложнений. Обсервационные исследования также подтверждают, что АСК в более высоких дозах приводит к увеличению риска развития осложнений со стороны органов ЖКТ [17, 22]. Американская ассоциация кардиологов рекомендует снижать суточную дозу АСК с 325 мг до 81 мг у пациентов с высоким риском развития осложнений со стороны органов ЖКТ [1]. Однако некоторые эксперты предлагают применять АСК в суточной дозе 325 мг в течение одного месяца у больных после стентирования коронарных артерий, хотя нет четких данных о том, является ли эта доза действительно необходимой [1]. В настоящее время такой подход не имеет четких обоснований, т. к. отсутствуют данные о дополнительном положительном эффекте высоких доз АСК (если речь не идет об остром коронарном синдроме) на фоне возрастания гастроинтестинальных рисков. Ключевым моментом должна быть польза, которая заключается в уменьшении риска ЖК-кровотечений с уменьшением дозы. Неизвестна оптимальная доза АСК. Данные метаанализа Antithrombotic Trialists' Collaboration косвенно подтверждают, что высокие дозы АСК не являются более эффективными на уровне популяции [23]. Данные обсервационного исследования CURE (Clopidogrel in unstable angina to prevent recurrent events) свидетельствуют об отсутствии пользы высоких доз АСК и о повышении риска кровотечений на их фоне [24]. Использование кишечнорастворимых или забуференных форм препарата не уменьшает риск возникновения кровотечений [19, 20, 25], что предполагает наличие системного побочного действия АСК на ЖКТ
Наиболее высоким фактором риска развития осложнений со стороны органов ЖКТ является наличие в анамнезе язвенной болезни, особенно осложненной кровотечением. Возраст также является важным фактором риска, возрастающим начиная с 60-летнего возраста. Мужской пол хоть и не является важным фактором риска, но все же отмечено, что риск у мужчин немного выше, чем у женщин [26].
Комбинации антиагрегантов и антикоагулянтов
Риск развития осложнений, связанный с применением комбинации антиагрегантов и антикоагулянтов, хорошо известен.
Согласно рекомендациям ACCF/ACG/AHA комбинация АСК с антикоагулянтами (включая нефракционированный гепарин, низкомолекулярный гепарин и варфарин) связана со значительным повышением риска кровотечений, в большей степени желудочно-кишечных. Эту комбинацию следует использовать при тромбозах сосудов, аритмиях и заболеваниях клапанного аппарата, при этом пациенты должны получать сопутствующую терапию ИПП. При добавлении варфарина к АСК и клопидогрелю необходимо контролировать международное нормализованное отношение (МНО) в рамках от 2,0 до 2,5 [26].
Антиагрегантная терапия широко используется в лечении больных ишемической болезнью сердца (ИБС), в том числе и при остром коронарном синдроме (ОКС) [1]. Метаанализ четырех рандомизированных исследований, в которых сравнивалось лечение ОКС с помощью комбинации нефракционированного гепарина и АСК против одного АСК, выявил увеличение частоты больших кровотечений на 50% в группе комбинированной терапии по сравнению с группой больных, принимавших только АСК [27, 28]. Низкомолекулярный гепарин в комбинации с АСК при лечении ОКС также приводил к увеличению частоты больших кровотечений, как продемонстрировано в FRISC-1 (Fragmin during Instability in Coronary Artery Disease-1) [29] и CREATE (Clinical Trial of Reviparin and Metabolic Modulation in Acute Myocardial Infarction Treatment Evaluation) [30]. В сравнительном метаанализе с участием более 25 тысяч больных с ОКС лечение с использованием комбинации варфарина с АСК оказалось более предпочтительно, чем монотерапия АСК, однако это повышает риск больших кровотечений в два раза [31]. Наличие венозных тромбозов предполагает длительный прием антикоагулянтов, что может в свою очередь приводить к повышенному риску ЖК-кровотечений. Поэтому необходимо контролировать уровень МНО в рамках от 2,0 до 2,5, хотя у больных с механическими сердечными клапанами этот уровень может быть недостаточен и может быть рекомендовано его увеличение [26]. В связи с этим пациенты при тромбозах сосудов, аритмиях и заболеваниях клапанного аппарата должны получать сопутствующую терапию ИПП.
Лечение и профилактика эрозивно-язвенных поражений ЖКТ вследствие приема НПВП и АСК
Согласно рекомендациям ACCF/ACG/AHA ИПП являются препаратами выбора для терапии и профилактики гастроинтестинальных осложнений вследствие приема НПВП и АСК. Предлагаемые подходы к уменьшению риска гастроинтестинальных осложнений представлены на схеме.
В основе ульцерогенного действия НПВП лежит механизм истощения простагландинов, и заместительная терапия синтетическим простагландином мизопростолом должна уменьшать негативный эффект НПВП. В исследовании с участием здоровых добровольцев, принимающих АСК в дозе 300 мг в сутки, применение мизопростола в дозе 100 мг в сутки по данным контрольной фиброгастроскопии позволило достоверно уменьшить частоту возникновения эрозий в верхних отделах ЖКТ [32]. Кроме того, в плацебо-контролируемом исследовании мизопростол предотвращал появление рецидивирующих язв желудка среди пациентов, получающих низкие дозы АСК или другие НПВП [33]. Однако применение мизопростола связано с побочными эффектами, такими как кишечная непроходимость и диарея, из-за которых приходится прекращать его прием. Это наблюдали в крупном исследовании с участием более 8000 больных ревматоидным артритом. Около 20% больных, получающих мизопростол, выбыли из исследования из-за диареи в течение первого месяца исследования [34]. Именно поэтому в настоящее время этот препарат не нашел широкого применения с целью профилактики ульцерогенного действия НПВП.
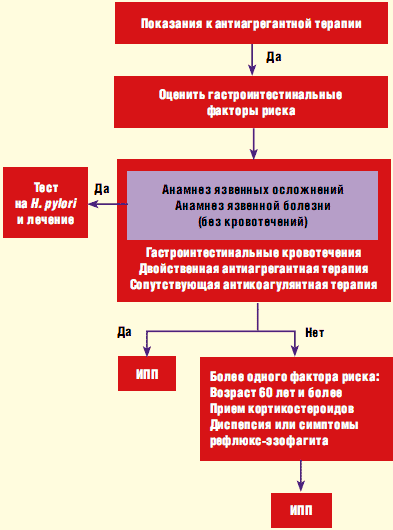
Схема. Алгоритм принятия решений с целью профилактики гастроинтестинальных кровотечений (ACCF/ACG/AHA)
Уменьшение уровня соляной кислоты с помощью традиционных доз антагонистов H2-рецепторов не приводит к профилактике большинства язв, связанных с приемом НПВП. До настоящего времени не проводилось крупных исследований по изучению комбинированного применения АСК с препаратами этой группы. В связи с этим применение препаратов из группы ИПП является разумной альтернативой. ИПП обеспечивают преимущество перед ранитидином и мизопростолом в профилактике НПВП-индуцированных язв и диспепсии. ИПП — лекарственные препараты, предназначенные для лечения кислотозависимых заболеваний ЖКТ за счет снижения продукции соляной кислоты посредством блокирования в париетальных клетках слизистой оболочки желудка протонного насоса — Н+/К+-АТФазы. В исследованиях с эндоскопическим контролем здоровые добровольцы принимали ланзопразол и омепразол, что способствовало уменьшению риска гастродуоденальных повреждений при приеме АСК в дозе 300 мг в сутки [35]. Эти данные были подтверждены результатами эпидемиологических исследований, в которых применение ИПП ассоциировалось со снижением гастроинтестинальных кровотечений среди пациентов, получавших низкие дозы АСК [36, 37]. Следует отметить, что наиболее выраженный положительный эффект с целью профилактики гастроинтестинальных осложнений при приеме АСК наблюдался в тех случаях, когда терапия ИПП сопровождалась эрадикацией Helicobacter pylori [38]. Применение АСК в комбинации с ИПП является наиболее предпочтительной тактикой в уменьшении риска повторных язвенных кровотечений у пациентов с высоким риском гастроинтестинальных осложнений, чем применение клопидогреля [39].
Если пациент не относится к группе высокого риска развития гастроинтестинальных осложнений, ему рекомендован прием клопидогреля в комбинации с АСК как минимум в течение одного месяца после перенесенного острого коронарного синдрома без подъема сегмента ST [1]. Лечение клопидогрелем в комбинации с АСК на протяжении одного года и более также рекомендовано всем больным после проведения транслюминальной коронарной ангиопластики с имплантацией стента, содержащего лекарственное покрытие [40]. Данные таких клинических исследований, как CURE [41], MATCH (Management of Atherothrombosis with Clopidogrel in High-Risk Patients) [42], CHARISMA (Clopidogrel for High Atherothrombotic Risk and Ischemic Stabilization, Management, and Avoidance) [43], доказывают возможность достоверного увеличения риска развития гастроинтестинальных осложнений в случае применения такой комбинации по сравнению с монотерапией только одним из них. Поэтому у пациентов с высоким риском развития кровотечений может быть более безопасным использование непокрытых стентов, т. к. в этом случае применение двойной антиагрегантной терапии может быть значительно менее продолжительным.
ИПП и клопидогрель
Следует отметить, что в настоящее время возможность применения ИПП с целью уменьшения риска развития гастроинтестинальных осложнений у больных, принимающих клопидогрель, ставится под сомнение в связи с появившимися публикациями об увеличении неблагоприятных сердечно-сосудистых событий. Так, на 32-м Ежегодном научном собрании Общества сердечно-сосудистой ангиографии и вмешательств (Society for Cardiovascular Angiography and Interventions — SCAI) было доложено, что одновременное использование клопидогреля и распространенных ИПП значительно повышает риск возникновения больших неблагоприятных сердечно-сосудистых событий, к которым относили инфаркт миокарда (ИМ), инсульт, нестабильную стенокардию, необходимость повторения коронарного вмешательства, коронарную смерть. В исследовании были использованы данные о пациентах, принимавших клопидогрель, полученные из базы данных Medco, содержащей информацию о 60 миллионах американцев. Целью было определение риска госпитализации с осложнениями пациентов со стентами при одновременном назначении ИПП и клопидогреля. Из 41 063 пациентов в базе данных Medco были выбраны пациенты, перенесшие транслюминальную коронарную ангиопластику со стентированием, из которых 9862 больных принимали одновременно ИПП и 6828 больных, не принимавших ИПП. Одновременный прием клопидогреля в дозе 75 мг/сут и ИПП составлял как минимум 293 дня. Ни у кого из пациентов не было в анамнезе желудочно-кишечных кровотечений. У пациентов, принимавших ИПП совместно с клопидогрелем, риск возникновения больших неблагоприятных сердечнососудистых событий составил 25%, в то время как у не принимавших ИПП пациентов риск был ниже и составлял 17,9%. В связи с этим SCAI выпустило официальное заявление, в котором говорится о необходимости дополнительного изучения данной темы. Аналогичное сообщение опубликовала FDA с указанием о возможном уменьшении эффекта клопидогреля при приеме ИПП (омепразола) и сообщением о нежелательном использовании такой комбинации лекарственных средств. Негативный эффект комбинации клопидогреля и ИПП связан с тем, что некоторые ИПП могут ингибировать цитохром P450 2C19, изменяя фармакокинетику клопидогреля [44]. Примером может служить омепразол, который метаболизируется в основном изоферментами CYP2C19 и CYP3A4. Исходное соединение обладает почти в 10 раз большей аффинностью к CYP2C19, чем к CYP3A4 [45]. Учитывая такую быструю и экстенсивную биотрансформацию, опосредованную изоферментами 2С19 и 3А4 системы CYP, представляется вполне вероятным взаимодействие омепразола с другими субстратами или ингибиторами обеих систем. Омепразол и эзомепразол (чистый S-энантиомер омепразола) подвержены одинаковым метаболическим превращениям. Несмотря на некоторые (количественные, но не качественные) различия в характере метаболических реакций обоих энантиомеров омепразола, потенциальная способность эзомепразола и рацемического омепразола участвовать в лекарственных взаимодействиях, по-видимому, значительно не отличается. Ланзопразол также метаболизируется преимущественно изоферментами CYP2C19 и CYP3A4 [46]. Результаты исследования in vitro свидетельствуют о сходной степени конкурентного ингибирования CYP2C19 при применении ланзопразола или омепразола, хотя клинические данные о возможности его взаимодействия с другими препаратами, метаболизирующимися с помощью CYP2C19, носят противоречивый характер. Еще один ИПП — пантопразол также метаболизируется с участием CYP2C19 и CYP3A4, но по сравнению с другими ИПП обладает меньшей аффинностью к этим ферментам [46]. В отличие от большинства продуктов, образующихся в фазе I биотрансформации других ИПП, первоначальный метаболит пантопразола, 4-гидроксипантопразол, образуемый в результате воздействия системы CYP, проходит затем вторичную (фаза II) биотрансформацию посредством конъюгации с сульфатом в цитозоле. Эту реакцию конъюгации, которая является относительно ненасыщаемым путем метаболизма лекарственных средств, часто расценивают как причину более низкой способности пантопразола вступать в лекарственные взаимодействия по сравнению с другими ИПП [46]. Таким образом, если пантопразол не ингибирует цитохром P450 2C19, он не должен влиять на метаболическую активацию клопидогрела, тогда как другие ИПП или их первичные метаболиты действительно ингибируют цитохром P450 2C19 и потенциально могут уменьшать положительные эффекты клопидогреля [46, 47]. Это подтверждается первыми данными популяционного исследования, проведенного среди жителей Онтарио старше 66 лет, находившихся на стационарном лечении по поводу острого ИМ (ОИМ) с 2002 по 2007 гг. [48]. В результате исследования были изучены следующие базы данных: «Ontario Public Drug Program» — содержит полные данные по поводу лечения больных; «Canadian Institute for Health Information Discharge Abstract Database» — отражает детализированную лечебно-диагностическую информацию о госпитализированных; «Ontario Health Insurance Plan» — содержит информацию о стационарных и амбулаторных услугах врачей. Основные демографические данные, включая дату смерти, были получены из «Registered Persons Database», которая содержит информацию о каждом когда-либо обращавшемся к врачу жителе Онтарио. Возможности этих баз данных позволяли изучить безопасность лекарственного средства, включая особенности взаимодействия лекарств и клинические последствия таких взаимодействий [48]. Наблюдение проводилось за пациентами, которые получали клопидогрель в течение 90 дней после выписки из стационара или до повторной госпитализации по поводу ОИМ. Была сформирована группа пациентов, которая длительное время (более одного года) принимала клопидогрель. За 69-месячный период исследования были проанализированы данные 13 636 пациентов. Из них 2682 пациента получали ИПП в течение 30 дней после выписки и 4224 — в течение 90 дней. Назначение пантопразола не было связано с частотой рецидивов ИМ для пациентов, получавших клопидогрель. Назначение других ИПП, напротив, сопровождалось 40% увеличением риска рецидива ИМ в течение 90 дней после выписки из стационара по сравнению с группой пациентов, которым эти ИПП не назначались (ОШ = 1,40; 95% ДИ = 1,10—1,77). Таким образом, среди пациентов, получавших клопидогрель после ОИМ, сопутствующее использование ИПП, ингибирующего цитохром P450 2C19 (омепразол, ланзопразол или рабепразол), увеличивает риск рецидива ИМ и, возможно, является результатом ингибирования метаболической биоактивации клопидогреля. Такой эффект не был замечен при сопутствующей терапии пантопразолом. Данное исследование объективизировало оценку взаимодействия лекарственных средств у популяции высокого риска рецидива коронарных событий. Как полагают авторы данной работы, проводимые в будущем исследования взаимодействий лекарственных средств с клопидогрелем покажут, что сопутствующая лечению клопидогрелем терапия ИПП, кроме пантопразола, должна быть минимизирована.
Следует отметить, что из широкого спектра препаратов группы ИПП в настоящее время наиболее подробно изучены особенности взаимодействия только двух из них — омепразола и пантопразола, в то время как особенности эзомепразола, ланзопразола и рабепразола установлены хуже. Особое внимание выбору ИПП следует уделять при их назначении больным, принимающим варфарин, т. к. омепразол и эзомепразол уменьшают его клиренс и это может привести к нежелательному повышению антикоагулянтного эффекта. Другие препараты из группы ИПП — пантопразол, ланзопразол и рабепразол не оказывают никакого влияния на клиренс варфарина и могут применяться в комбинации с ним. Однако необходимо учитывать, что особенности взаимодействия ланзопразола и рабепразола изучены в меньшей степени, чем пантопразола, поэтому в данном случае пантопразол обладает явным преимуществом при назначении ИПП таким пациентам.
Особо остро вопрос взаимодействия лекарственных препаратов поднимается у больных с желудочно-кишечным кровотечением на фоне приема антитромботических препаратов. В ряде случаев отмена этих препаратов связана с риском развития сердечно-сосудистых осложнений, например у больных, недавно перенесших имплантацию коронарного стента с лекарственным покрытием. В таких случаях в обязательном порядке должна проводиться стратификация индивидуализированных рисков. На основании согласованного мнения экспертов оргкомитета ACCF/ACG/AHA для лиц с хроническими кровотечениями и высоким риском сердечно-сосудистых осложнений, в частности, с недавно установленным стентом, двойная анти-тромбоцитарная терапия должна быть продолжена, как того требует высокий риск сердечно-сосудистых нарушений, при отсутствии явно выраженных противопоказаний [1]. При острых состояниях, сопровождаемых серьезными кровотечениями из ЖКТ, представляется обоснованным, после обсуждения со специалистами, прервать на короткое время антитромбоцитарную терапию до остановки кровотечения. В настоящее время отсутствуют четкие рекомендации о необходимости отмены антиагрегантов и сроках возобновления этой терапии, однако чаще терапия возобновляется в сроки 3—7 дней после отсутствия клиники повторных кровотечений [1]. Вероятным развитием событий у таких пациентов является эндоскопическое лечение на фоне внутривенного введения ИПП, который должен назначаться с учетом лекарственного взаимодействия, в связи с чем в данной клинической ситуации пантопразол представляется препаратом выбора.
Большинство лекарственных взаимодействий и побочных явлений, ассоциированных с ИПП, предсказуемо, и их можно предупредить с помощью периодической переоценки схемы лечения и/или выбора препаратов с более низкой способностью к взаимодействиям. Клиническое значение лекарственных взаимодействий может иметь особое значение у лиц пожилого возраста, у которых высок риск взаимодействий в связи с одновременным приемом многих медикаментов, а также у пациентов, принимающих препараты с узким диапазоном терапевтического действия. В таких случаях необходимо отдавать предпочтение лекарству с низким риском взаимодействия и тщательно охарактеризованной способностью вступать в такие взаимодействия.
Литература 1. Bhatt et al. ACCF/ACG/AHA 2008 Expert Consensus Document on Reducing the Gastrointestinal Risks of Antiplatelet Therapy and NSAID Use. JACC. Vol. 52, № 18, 2008. Bhatt et al. 1503, October 28, 2008: 1502-1517.
2. Shaheen N. J., Hansen R. A., Morgan D. R. et al. The burden of gastrointestinal and liver diseases, 2006 // Am J Gastroenterol. 2006; 101: 2128-2138.
3. McAdam B. F., Catella-Lawson F., Mardini I. A., Kapoor S. et al. Systemic biosynthesis of prostacyclin by cyclooxygenase (COX)-2: the human pharmacology of a selective inhibitor of COX-2 // Proc Natl Acad Sci USA. 1999; 96: 272-277.
4. FDA. Public health advisory. Non-steroidal anti-inflammatory drug products (NSAIDS). Accessed on January, 2, 2005.
5. Cox E. R., Frisse M., Behm A., Fairman K. A. Over-the-counter pain reliever and aspirin use within a sample of long-term cyclooxygenase 2 users // Arch Intern Med. 2004; 164: 1243-1246.
6. Bombardier C., Laine L., Reicin A. et al. Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumatoid arthritis: VIGOR Study Group // N Engl J Med. 2000; 343: 1520-1528.
7. Hawkey C. J., Talley N. J., Scheiman J. M. et al. Maintenance treatment with esomeprazole following initial relief of non-steroidal antiinflammatory drug-associated upper gastrointestinal symptoms: the NASA2 and SPACE2 studies // Arthritis Res Ther. 2007; 9: R17.
8. Ofman J. J., MacLean C. H., Straus W. L. et al. A meta-analysis of severe upper gastrointestinal complications of nonsteroidal antiinflammatory drugs // J Rheumatol. 2002; 29: 804-812.
9. Abraham N. S., Castillo D. L., Hartman C. National mortality following upper gastrointestinal or cardiovascular events in older veterans with recent nonsteroidal anti-inflammatory drug use // Aliment Pharmacol Ther. 2008; 28: 97-106.
10. Abraham N. S., El-Serag H. B., Johnson M. L. et al. National adherence to evidence-based guidelines for the prescription of nonsteroidal antiinflammatory drugs // Gastroenterology. 2005; 129: 1171-1178.
11. Johnson D. A. Upper GI risks of NSAIDs and antiplatelet agents: key issues for the cardiologist // Rev Cardiovasc Med. 2005; 6, Suppl 4: S15-22.
12. Abraham N. S.., Hartman C, Castillo D., Richardson P., Smalley W. Effectiveness of national provider prescription of PPI gastroprotection among elderly NSAID users // Am J Gastroenterol. 2008; 103: 323-332.
13. Singh G, Triadafilopoulos G. Epidemiology of NSAID induced gastrointestinal complications // J Rheumatol Suppl. 1999; 56: 18-24.
14. Lanas A., Bajador E, Serrano P. et al. Nitrovasodilators, low-dose aspirin, other nonsteroidal antiinflammatory drugs, and the risk of upper gastrointestinal bleeding // N Engl J Med. 2000; 343: 834-839.
15. Pearson T. A, Blair S. N, Daniels S. R. et al. AHA guidelines for primary prevention of cardiovascular disease and stroke: 2002 update: Consensus Panel Guide to Comprehensive Risk Reduction for Adult Patients Without Coronary or Other Atherosclerotic Vascular Diseases // Circulation. 2002; 106: 388-391.
16. Chan F. K., Graham D. Y. Review article: prevention of non-steroidal anti-inflammatory drug gastrointestinal complications-review and recommendations based on risk assessment // Aliment Pharmacol Ther. 2004; 19: 1051-1061.
17. Weil J., Colin-Jones D., Langman M. et al. Prophylactic aspirin and risk of peptic ulcer bleeding // BMJ. 1995; 310: 827-830.
18. Yeomans N. D., Lanas A. I., Talley N. J. et al. Prevalence and incidence of gastroduodenal ulcers during treatment with vascular protective doses of aspirin // Aliment Pharmacol Ther. 2005; 22: 795-801.
19. De Abajo F. J., Garcia Rodriguez L. A. Risk of upper gastrointestinal bleeding and perforation associated with low-dose aspirin as plain and enteric-coated formulations // BMC Clin Pharmacol. 2001; 1: 1.
20. Kelly J. P., Kaufman D. W., Jurgelon J. M. et al. Risk of aspirin-associated major upper-gastrointestinal bleeding with enteric-coated or buffered product // Lancet. 1996; 348: 1413-1416.
21. Sorensen H. T., Mellemkjaer L., Blot W. J. et al. Risk of upper gastrointestinal bleeding associated with use of low-dose aspirin // Am J Gastroenterol. 2000; 95: 2218-2224.
22. Serebruany V. L., Steinhubl S. R., Berger P. B. et al. Analysis of risk of bleeding complications after different doses of aspirin in 192,036 patients enrolled in 31 randomized controlled trials // Am J Cardiol. 2005; 95: 1218-1222.
23. Antithrombotic Trialists' Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients // BMJ. 2002; 324: 71-86.
24. Peters R. J., Mehta S. R., Fox K. A. et al. Effects of aspirin dose when used alone or in combination with clopidogrel in patients with acute coronary syndromes: observations from the Clopidogrel in Unstable angina to prevent Recurrent Events (CURE) study // Circulation. 2003; 108: 1682-1687.
25. Garcia Rodriguez L. A., Hernandez-Diaz S., de Abajo F. J. Association between aspirin and upper gastrointestinal complications: systematic review of epidemiologic studies // Br J Clin Pharmacol. 2001; 52: 563-571.
26. Hernandez-Diaz S., Garcia Rodriguez L. A. Cardioprotective aspirin users and their excess risk of upper gastrointestinal complications // BMC Med. 2006; 4: 22.
27. Lanas A., Serrano P., Bajador E., Fuentes J., Sainz R. Risk of upper gastrointestinal bleeding associated with non-aspirin cardiovascular drugs, analgesics and nonsteroidal anti-inflammatory drugs // Eur J Gastroenterol Hepatol. 2003; 15: 173-178.
28. Taha A. S., Angerson W. J., Knill-Jones R. P., Blatchford O. Upper gastrointestinal haemorrhage associated with low-dose aspirin and antithrombotic drugs — a 6-year analysis and comparison with nonsteroidal anti-inflammatory drugs // Aliment Pharmacol Ther. 2005; 22: 285-289.
29. Fragmin during Instability in Coronary Artery Disease (FRISC) study group. Low-molecular-weight heparin during instability in coronary artery disease // Lancet. 1996; 347: 561-568.
30. Yusuf S., Mehta S. R., Xie C. et al. Effects of reviparin, a low-molecularweight heparin, on mortality, reinfarction, and strokes in patients with acute myocardial infarction presenting with ST-segment elevation // JAMA. 2005; 293: 427-435.
31. Andreotti F., Testa L., Biondi-Zoccai G. G., Crea F. Aspirin plus warfarin compared to aspirin alone after acute coronary syndromes: an updated and comprehensive meta-analysis of 25,307 patients // Eur Heart J. 2006; 27: 519-526.
32. Donnelly M. T., Goddard A. F., Filipowicz B., Morant S. V., Shield M. J., Hawkey C. J. Low-dose misoprostol for the prevention of low-dose aspirin-induced gastroduodenal injury // Aliment Pharmacol Ther. 2000; 14: 529-534.
33. Goldstein J. L., Huang B., Amer F., Christopoulos N. G. Ulcer recurrence in high-risk patients receiving nonsteroidal anti-inflammatory drugs plus low-dose aspirin: results of a post HOC subanalysis // Clin Ther. 2004; 26: 1637-1643.
34. Silverstein F. E., Graham D. Y., Senior J. R. et al. Misoprostol reduces serious gastrointestinal complications in patients with rheumatoid arthritis receiving nonsteroidal anti-inflammatory drugs: a randomized, double-blind, placebo-controlled trial // Ann Intern Med. 1995; 123: 241-249.
35. Berger J. S., Stebbins A., Granger C. B. et al. Initial aspirin dose and outcome among ST-elevation myocardial infarction patients treated with fibrinolytic therapy // Circulation. 2008; 117: 192-199.
36. Lanas A., Garcia-Rodriguez L. A., Arroyo M. T. et al. Effect of antisecretory drugs and nitrates on the risk of ulcer bleeding associated with nonsteroidal anti-inflammatory drugs, antiplatelet agents, and anticoagulants // Am J Gastroenterol. 2007; 102: 507-15.
37. Chin M. W., Yong G., Bulsara M. K., Rankin J., Forbes G. M. Predictive and protective factors associated with upper gastrointestinal bleeding after percutaneous coronary intervention: a case-control study // Am J Gastroenterol. 2007; 102: 2411-2416.
38. Lai K. C., Lam S. K., Chu K. M. et al. Lansoprazole for the prevention of recurrences of ulcer complications from long-term low-dose aspirin use // N Engl J Med. 2002; 346: 2033-2038.
39. Chan F. K., Ching J. Y., Hung L. C. et al. Clopidogrel versus aspirin and esomeprazole to prevent recurrent ulcer bleeding // N Engl J Med. 2005; 352: 238-244.
40. Grines C. L., Bonow R. O., Casey D. E. Jr. et al. Prevention of premature discontinuation of dual antiplatelet therapy in patients with coronary artery stents // Circulation. 2007; 115: 813-818.
41. Yusuf S., Zhao F., Mehta S. R., Chrolavicius S., Tognoni G., Fox K. K. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation // N Engl J Med. 2001; 345: 494-502.
42. Diener H. C., Bogousslavsky J., Brass L. M. et al. Aspirin and clopidogrel compared with clopidogrel alone after recent ischaemic stroke or transient ischaemic attack in high-risk patients (MATCH): randomised, double-blind, placebo-controlled trial // Lancet. 2004; 364: 331-337.
43. Bhatt D. L., Fox K.A., Hacke W. et al. Clopidogrel and aspirin versus aspirin alone for the prevention of atherothrombotic events // N Engl J Med. 2006; 354: 1706 -1717.
44. Gilard M., Arnaud B., Cornily J. C. et al. Influence of omeprazole on the antiplatelet action of clopidogrel associated with aspirin: the randomized, double-blind OCLA (Omeprazole CLopidogrel Aspirin) study // J Am Coll Cardiol. 2008; 51: 256-260.
45. Blume H., Donath F., Warnke A., Schug B. S. Pharmacokinetic Drug Interaction Profiles of Proton Pump Inhibitors // Drug Safety. 2006; 29 (9): 769-784.
46. Blume H., Donath F., Warnke A. Pharmacokinetic Drug Interaction Profiles of Proton Pump Inhibitors // Drug Safety. 2006; 29 (9): 769-784.
47. Li X. Q., Andersson T. B., Ahlstrom M. et al. Comparison of inhibitory effects of the proton pump-inhibiting drugs omeprazole, esomeprazole, lansoprazole, pantoprazole, and rabeprazole on human cytochrome P450 activities // Drug Metab Dispos. 2004; 32: 821-827.
48. Juurlink D. N., Gomes T, Ko D. T. A population-based study of the drug interaction between proton pump inhibitors and clopidogrel // CMAJ. 2009: 180 (7).
