Вакцинопрофилактика коклюша - итоги и перспективы
Статьи
 Тетракок
Тетракок
Адсорбированная вакцина для профилактики дифтерии, коклюша, столбняка и полиомиелита Д.Т.Кок
Пентаксим
|
№5 (35) сентябрь - октябрь 2004 г.
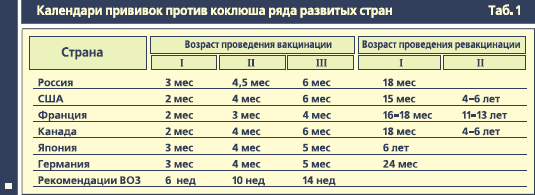
Вакцинопрофилактика коклюша - итоги и перспективы Н.А. Озерецковский, Р.П. Чупринина Вакцинация против коклюша включена в календари профилактических прививок практически всех стран мира. Схема вакцинации и возраст начала ее проведения в разных странах имеет определенные различия, тем не менее, во всех из них прививки АКДС-вакциной начинают не позже 3 месяцев жизни, а курс вакцинации включает не менее 3 инъекций препарата с минимальным 4-недельным интервалом между ними. Из 197 стран, о которых имеются данные, 129 начинают вакцинацию с возраста 6 недель - 2 месяцев с тем, чтобы быстрее защитить детей наиболее ранимого возраста. В большинстве стран проводят 3 прививки с 1 ревакцинацией, лишь в 79 странах курс вакцинации ограничивается тремя прививками, тогда как в 26 странах в календарь включены две ревакцинации. Необходимость второй ревакцинации объясняется тем, что иммунитет после первой ревакцинации сохраняется ограниченное число лет, так что в школьном возрасте восприимчивый контингент быстро увеличивается. Вторая ревакцинация, как правило, в 4-6 летнем возрасте, имеет целью защитить школьников от заболевания [4], однако ее проведение цельноклеточной коклюшной вакциной затруднено в связи с ее высокой реактогенностью. Практически во всех странах прививки АКДС-вакциной допускается осуществлять одновременно (в один день) с другими вакцинами Национального календаря прививок, все шире используются 4-, 5- и 6-компонентные вакцины, включающие КДС-компонент. Трехкратная вакцинация АКДС-вакциной, содержащей цельные микробные клетки B. pertussis при 82% охвате вакцинацией всех детей, проживающих на земном шаре, предотвращает ежегодно 85 млн заболеваний коклюшем и 762 тыс летальных исходов от коклюша у детей [4]. Миллионами исчисляются случаи предотвращенной инвалидности вследствие этой инфекции. Наибольший эффект был зарегистрирован в развитых странах, где заболеваемость клинически диагностированным коклюшем составила всего 3-10 случаев на 100 тыс населения, а в некоторых странах Европы (Бельгия, Болгария, Чешская республика, Исландия, Люксембург, Португалия) этот показатель был ниже 1 на 100 тыс [2]. Вместе с тем, несмотря на повсеместную вакцинацию препаратами, содержащими коклюшный компонент, в 1994 г. в мире коклюшем переболело около 40 млн человек, из которых у 5 млн заболевание осложнилось пневмонией, у 30 тыс - стойкими неврологическими осложнениями, а у 360 тыс наступил летальный исход. Причиной этого является как недостаточный охват прививками детей в развивающихся странах, так и несовершенство схемы вакцинации 4 дозами, при которой сохраняется восприимчивый контингент подростков и взрослых, среди которых происходит циркуляция возбудителя. При этом, заболевание протекает с нехарактерной клинической картиной, что препятствует проведению лечения и изоляции заболевших. Именно больные подростки и взрослые являются источником заражения грудных детей, которые остаются восприимчивыми до окончания первичной серии вакцинации, т.е. до возраста 4 месяцев, а в России - 6 месяцев жизни.
То, что коклюш еще не побежден окончательно, очевидно. Более того, в последние годы заболеваемость коклюшем имеет тенденцию к повышению. Так в США в 2001 г. коклюшем переболело 7580 человек, что в 2,8 раза превышает цифры 1991 г. (2719 человек) [9] и в 4 раза - 1980 г. (1730 человек). И в 2002 г. заболеваемость продолжала повышаться - 8296 случаев. За 2 десятилетия в США повысилась и смертность от коклюша - с 77 умерших в 1980-1989 гг. до 103 - в 1990-1999 гг. [10]. Подобная тенденция имеет место и в других странах. В России число случаев заболеваний коклюшем в 2003 г. (12523) в 2,3 раза превысило таковое в 2002 г. (5455). Серьезной проблемой является установление единых критериев коклюша, поскольку связывать диагноз только с бактериологическим подтверждением неправомерно. Так в подростковом возрасте и у взрослых при отсутствии типичных симптомов, просто при длительном кашле, естественно, бактериологическое исследование на коклюш не проводится. Да и само это исследование обладает далеко не 100%-ной чувствительностью. И по общей заболеваемости судить о ситуации с коклюшем малонадежно, поэтому пристальное внимание должна привлечь заболеваемость грудных детей, у которых спутать коклюш с другим заболеванием не так просто. И действительно, данные о повозрастном распределении случаев заболеваний весьма интересны. Так в США в 2001 г. на долю детей пришлось 65% из числа заболевших коклюшем (25% детей - в возрасте до 1 г.). В то же время в России в 2002 г. и 2003 г. дети составляли 96% и 95% из числа заболевших (13% и 11% - в возрасте до 1 г.) [3]. Анализ показывает, что абсолютное число заболевших коклюшем детей в возрасте до 1 года в США в 2001 г. (1895 случаев) имеет тот же порядок, что в России (1274 в 2001 г., 716 в 2002 г., 1363 в 2003 г.). Различия в удельном весе детей и взрослых среди заболевших коклюшем объяснимы, видимо, более целенаправленной диагностикой коклюша у подростков и взрослых в США; низкие цифры заболевания коклюшем в России у взрослых объясняются гиподиагностикой заболевания в данной возрастной группе. Приведенные данные позволяют думать также, что уже давно включенная в календарь прививок США вторая ревакцинация в начальной школе не оказала должного влияния на снижение заболеваемости подростков. В нашей стране разработка и организация выпуска коклюшной вакцины была осуществлена под руководством М.С. Захаровой [1]. Массовая вакцинация против коклюша была начата в 1957 г. - в год, когда число заболевших составило 476622 человека (415 на 100 тыс). В первые годы прививки осуществлялись коклюшной и коклюшно-дифтерийной вакцинами, а с 1964-65 гг. адсорбированной коклюшно-дифтерийно-столбнячной (АКДС) вакциной. Массовая вакцинопрофилактика коклюша привела к быстрому снижению заболеваемости, которая уже в 70-е годы составила 5,8-17,7 на 100 тыс при снижении смертности с 2,6 до 0,01 на 100 тыс. Коклюшный компонент отечественной АКДС-вакцины готовят из трех штаммов различных сероваров: 1.2.3, 1.2.0 и 1.0.3, взятых в равных соотношениях, которые в лабораторных тестах обладают средней токсичностью и высокой иммуногенной активностью. Отечественная АКДС-вакцина по всем компонентам соответствует требованиям ВОЗ. Сравнительная оценка иммуногенной активности коклюшного компонента АКДС-вакцины, свидетельствует, что выпускаемая отечественными предприятиями вакцина стандартна, а иммуногенная активность коклюшного компонента соответствует требованиям ВОЗ на протяжении всего срока годности препарата. Коклюшный компонент АКДС-вакцины также соответствует требованиям ВОЗ по критериям остаточной токсичности в тесте изменения массы тела мышей. В отличие от многих зарубежных препаратов в отечественной Инструкции по применению АКДС-вакцины определены более жесткие требования к допустимой частоте сильных общих поствакцинальных реакций (не более 1%). Однако цельноклеточная коклюшная вакцина при всех ее положительных свойствах является наиболее реактогенным препаратом из вакцин, включенных в Национальные календари прививок. Эти свойства препарата определяются, главным образом, эндотоксином. После ее применения развиваются и поствакцинальные осложнения, такие как фебрильные и афебрильные судороги, гипотонический гипореспонсивный синдром, синдром длительного непрерывного крика, анафилактический шок и другие формы аллергических реакций. Вместе с тем, наблюдения последних лет позволили исключить причинную связь с коклюшной вакцинацией таких грозных заболеваний, как стойкие длительные неврологические расстройства, развивающиеся вследствие "поствакцинального энцефалита", а также синдрома внезапной смерти (SIDS). Именно в связи с побочным действием препаратов, содержащих цельноклеточный коклюшный компонент, в ряде стран (Великобритания, Япония, ФРГ, Швеция) в 70-80-х годах прокатилась волна отказов от прививок против коклюша. Это явилось причиной резкого подъема заболеваемости этой инфекцией с увеличением числа тяжелых форм и появлением летальных исходов [7, 8]. В это же время в ряде стран была осуществлена разработка и внедрение в практику препарата бесклеточной коклюшной вакцины (БКВ), заменившей в составе АКДС-вакцины цельноклеточный (корпускулярный) коклюшный компонент. При разработке бесклеточного препарата исследователи исходили из серотипового состава коклюшных бактерий и роли отдельных компонентов в формировании специфического иммунитета (табл.2).
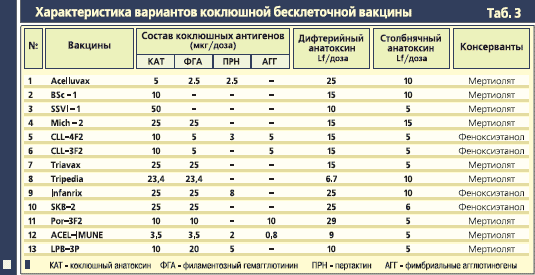
Первая БКВ была лицензирована в Японии в 1981 г. и в ассоциации с дифтерийным и столбнячным анатоксином была включена в календарь прививок для вакцинации детей с двухлетнего возраста, а с 1988 г. - с трехмесячного возраста. С 1990 по 1996 гг. проведено 8 полевых испытаний эффективности тринадцати БКВ (табл. 3), приготовленных разными производителями. Полученные в ходе этих исследований результаты свидетельствовали о высокой эффективности трех испытанных вакцин: четырехкомпонентной CCL-4F фирмы Pasteur Merieux Connaught, а также трехкомпонентных Infanrix фирмы SmithKline Beecham и Acelluvax фирмы Chiron Vaccines.
Высокая эффективность и низкая реактогенность АаКДС-вакцин (т.е. вакцины АКДС, содержащей бесклеточный коклюшный компонент) послужили основанием для их включения в Национальные календари прививок США, Новой Зеландии, Японии и ряда европейских стран как для вакцинации, так и для ревакцинации. После перехода на вакцинацию этими препаратами значительно уменьшилась частота развития побочных реакций (температурных, местных), и практически исчезли неврологические осложнения. Бесклеточная вакцина на порядок дороже цельноклеточной, поэтому ее применение - большая нагрузка на бюджет программ вакцинопрофилактики. Рассмотрев этот вопрос, ВОЗ рекомендовала продолжать использование цельноклеточных вакцин в программах массовой иммунизации как эффективных и безопасных; переход на бесклеточные вакцины может быть оправдан в тех ситуациях, когда опасения родителей и врачей в отношении реактогенности цельноклеточной вакцины способствуют снижению охвата населения прививками. Внедрение бесклеточной вакцины позволяет также ввести вторую ревакцинацию с перспективой снижения заболеваемости подростков. Сдерживающим фактором на этом пути является высокая цена бесклеточных вакцин и отсутствие местного производства. В России в НИИВС им. И.И. Мечникова на стадии завершения находится разработка бесклеточного коклюшного компонента АКДС-вакцины. Последний представляет собой протективный антигенный комплекс, выделенный из супернатанта среды культивирования коклюшных микробов. Он содержит основные протективные антигены - коклюшный токсин, филаментозный гемагглютинин и пертактин [2]. Ранее в НПО "Иммунопрепарат" (г. Уфа) В.Д. Смирновым была разработана технология производства коклюшного анатоксина, который был с успехом применен для вакцинации доноров с целью получения противококлюшного антитоксического иммуноглобулина - препарата, который, как показали Государственные испытания, обладал высокой терапевтической эффективностью при лечении коклюша у детей первого года жизни. К сожалению, до недавнего времени выпуск коклюшного анатоксина не был осуществлен. Применение бесклеточных коклюшных вакцин в рамках Национального календаря профилактических прививок позволит расширить охват ими, прежде всего, за счет детей с отягощенным анамнезом. Литература: © Н.А. Озерецковский, Р.П. Чупринина, 2004 |
Комментарии
ПРАКТИКА ПЕДИАТРА