Менингококковая инфекция у детей
СтатьиОпубликовано в журнале:
Практика педиатра
Декабрь, 2007
Ф.С. Харламова, профессор кафедры инфекционных болезней у детей ГОУ ВПО «Российский государственный медицинский университет» Росздрава, д-р мед. наук
Среди инфекционных болезней одной из опасных для жизни и непредсказуемых по молниеносности течения является менингококковая инфекция (МИ). Актуальность проблемы заключается в том, что при возникновении МИ требуется особый подход к организации диагностики и оказания скорой и неотложной медицинской помощи, ввиду того, что генерализованные формы МИ (наиболее часто встречающиеся в детском возрасте) при поздно начатом лечении могут приводить к смертельным исходам.
Для отечественных педиатров проблема МИ имеет особо значение, так как уровень заболеваемости среди детей всегда превышает таковую у взрослых в несколько раз, достигая 8–11 случаев на 100 тыс. населения. Более 50% от общего числа заболевших составляют дети до 5 лет (табл.1) [1]. Именно у детей высока частота развития генерализованных форм МИ. В значительной степени риск летального исхода при МИ зависит от возраста ребенка: чем он младше, тем выше вероятность неблагоприятного исхода. До 75% от числа умерших при МИ составляют дети до 2 лет, при этом доля детей первого года жизни достигает 40% (табл.2) [1].
Таблица 1
Возрастное распределение заболевших 2002–2004 годы
n=4972 (36 регионов РФ)
| 1–11 мес. | 1 г. | 2–4 г. | 5–9 л. | 10–14 л. | 15–19 л. | 20–24 л. | 25–44 л. | 45–64 л. | 65 л. + | Всего | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2002 | 0,13 | 18,8 | 12,4 | 16,9 | 10,1 | 10,4 | 9,3 | 4,8 | 8,4 | 6,9 | 1,8 | 100 |
| 2003 | – | 23,5 | 11,9 | 15,2 | 9,7 | 8,3 | 8,2 | 3,8 | 8,4 | 8,6 | 2,5 | 100 |
| 2004 | 0,2 | 1,3 | 13,2 | 15,8 | 8,13 | 5,4 | 10,4 | 4,6 | 9,8 | 8,7 | 2,4 | 100 |
| Всего | 0,1 | 21,5 | 2,4 | 15,9 | 9,3 | 8,0 | 9,2 | 4,3 | 8,8 | 8,1 | 2,3 | 100 |
Таблица 2
Возрастное распределение летальных случаев 2002–2004 годы
n=582 (36 регионов РФ)
| 1–11 мес. | 1 г. | 2–4 г. | 5–9 л. | 10–14 л. | 15–19 л. | 20–24 л. | 25–44 л. | 45–64 л. | 65 л. + | Всего | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2002 | 0,6 | 28,4 | 12,3 | 16,7 | 0,7 | 3,7 | 4,9 | 1,9 | 7,4 | 14,2 | 6,2 | 100 |
| 2003 | – | 30,4 | 12,1 | 9,2 | 3,8 | 4,6 | 5,4 | 0,4 | 10,4 | 18,3 | 5,4 | 100 |
| 2004 | 0,6 | 26,1 | 17,8 | 12,2 | 3,9 | 1,7 | 5 | 1,1 | 11,1 | 14,4 | 6,1 | 100 |
| Всего | 0,3 | 28,5 | 13,9 | 12,2 | 3,8 | 3,4 | 5,2 | 1,0 | 9,8 | 16,0 | 5,8 | 100 |
Эпидемиология
С 1962 года в ряде стран Европы и Азии, Канаде и США, а с 1968 года – и в нашей стране отмечается подъем заболеваемости МИ. Данные анализа глобальной эпидобстановки в 2005 году свидетельствуют о том, что в странах субсахарной Африки показатели заболеваемости МИ в целом колеблются от 100 до 800 случаев на 100 тыс. населения, а летальности – до 14%; предоминирует серогруппа менингококка А. На Европейском континенте наиболее высокий уровень заболеваемости МИ регистрировался в Исландии и Ирландии – 5–6,6 случаев на 100 тыс. населения, где предоминирует серогруппа В. А в странах Океании (Новая Зеландия) показатель заболеваемости МИ составил в этот период 14,5 случаев на 100 тыс. населения. В России с 1999 года в Астраханской, Пермской, Челябинской, Кемеровской, Новосибирской, Омской областях, в Хабаровском крае произошел значительный прирост МИ – на 22–40% – и составил 8,2 случая на 100 тыс. населения. В целом в 40 регионах страны в последние годы наблюдается снижение показателей заболеваемости этой инфекцией (рис. 1) [2, 3]. В общей серогрупповой характеристике по стране преобладают менингококки серогруппы А.
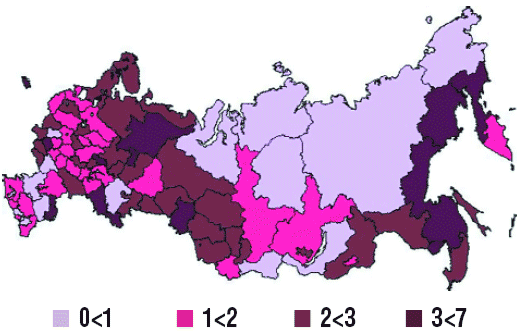
Рисунок 1
Территориальное распространение заболеваемости 2005 год.
n=2771 на 100000 населения
МИ характеризуется периодичностью – интервалы между отдельными подъемами заболеваемости составляют от 4 до 12–15 лет. Рост заболеваемости в эти периоды регистрируется в основном среди городского населения за счет скученности в транспорте и помещениях в холодное время года. Наиболее доказательна связь периодичности МИ с эпидемическими подъемами ОРВИ и гриппа с пиком в зимне-весенний период года.
Заболевают преимущественно дети и лица молодого возраста, чаще в закрытых коллективах.
Особенностью клинических форм МИ последних лет, в сравнении с прежними годами, является снижение частоты смешанных форм и менингококцемии без проявлений менингита на фоне увеличения частоты менингита, что, вероятно, является причиной диагностических ошибок. Об этом свидетельствуют данные НИИ детских инфекций (г. Санкт Петербург) и Морозовской детской клинической больницы (г. Москва) [7]. Так, в НИИ детских инфекций при менингите менингококковой этиологии в 83,2% случаев первично диагностировали ОРВИ. По данным Морозовской детской клинической больницы, в 2002–2004 годах диагноз «менингит» был поставлен только в 5 случаях из 31, первично диагностировали ОРВИ, острый аппендицит, менингококцемию без менингита, кому неясной этиологии, капилляротоксикоз, закрытую черепно-мозговую травму, тромбоцитопеническую пурпуру, острый гломерулонефрит, пневмонию и др. Другой особенностью последних лет является регистрация случаев заболевания МИ в течение года примерно с равной частотой, без четкой сезонности.
Источником распространения инфекции являются менингококконосители, больные назофарингитом и генерализованными формами инфекции. Путь передачи – воздушно-капельный, контактно бытовой. Входными воротами для инфекции служит слизистая оболочка верхних дыхательных путей.
Группой риска по развитию септических и гипертоксических форм МИ являются дети раннего возраста.
Установлена генетическая предрасположенность к заболеванию МИ и ее рецидивов у лиц, имеющих HLA антигены В12, В16, дефицит факторов комплемента С2–С8, пропердина, IgG2 и IgM [Самуэльс М., 1997]. Популяционная устойчивость к МИ, по мнению ряда исследователей, связана с локусом HLA–A1 антигена гистосовместимости.
Этиология
МИ является типичным антропонозом. Возбудитель – Neisseria meningitidis, грам-отрицательный диплококк, вырабатывающий экзо-и эндотоксин, который очень неустойчив во внешней среде.
Выделяют более 13 серотипов менингококка, при этом иммунитет – типоспецифический. По капсульным полисахаридам бактерии разделяют на серологические группы А, В, С, D43, D44, X, Y, Z, 29Е, W-135. По антигенам в мембранных протеинах различают более 20 серотипов и субтипов менингококка. По иммунотипам липополисахарида – более 11 иммунотипов. Доказана способность менингококков образовывать L-формы, которые вероятно могут обусловливать затяжные варианты менингита.
Патогенез
В развитии МИ ведущую роль играют три фактора: возбудитель, его эндотоксин и аллергизирующая субстанция. В месте входных ворот чаще всего не возникают воспалительные изменения, но при этом менингококк вегетирует, возникает менингококконосительство. Лишь в 10–15% случаев при снижении резистентности организма возможно развитие воспалительного процесса в носоглотке в виде менингококкового назофарингита. Если менингококки преодолевают местные защитные барьеры, распространение их происходит по лимфатическим путям в кровь. Менингококки в виде бактериальных эмболов заносятся в различные органы и ткани. В тех случаях, когда преодолевается гемато-энцефалический барьер, развивается гнойный менингит или менингоэнцефалит. При этом возможно проникновение возбудителя в оболочки мозга, минуя гематогенное распространение – через решетчатую кость по лимфатическим путям и влагалищам нервных волокон. Такой вариант возможен в случаях дефекта решетчатой кости или черепно-мозговой травмы. Сверхострый менингококковый сепсис развивается в результате массовой бактериемии и эндотоксинемии. При массовом распаде менингококков высвобождаемый эндотоксин воздействует на эндотелий сосудов и мембраны клеток крови, приводя к расстройству микроциркуляции [8]. В результате генерализованного повреждения эндотелия сосудов происходит закрытие дефектов тромбоцитами, агрегация которых провоцирует высвобождение тромбоксана и угнетение синтеза простациклина. Нарушаются реологические свойства крови: происходит агрегация форменных элементов, на которых фиксируется фибрин. Кроме того, важное значение имеет воздействие липида А эндотоксина на моноциты макрофаги, которые активизируясь выбрасывают ФНО-α – первичный медиатор токсических эффектов при токсическом шоке. Кроме него, в развитии септического шока колоссальную роль играют оксид азота, простагландины, факторы комплемента, гистамин, лейкотриены, фактор активации тромбоцитов и ИЛ-1, 2, 6, 8. Высвобождается избыточное количество биологически активных веществ (катехоламины, серотонин, гистамин), активизируются системы фактора Хагемана, калликреин-кининовая, свертывающая и в последующем фибринолитическая. Из печени мощно выбрасываются протромбин, калликреин и др., что в конечном счете приводит к гиперкоагуляции с образованием большого количества бактериальных тромбов в мелких сосудах (тромбогеморрагический синдром с бактериальной эмболией).
Утилизация факторов свертывающей системы приводит к коагулопатии потребления – гипокоагуляции, в результате которой возникают массивные кровоизлияния в ткани и различные органы. Чрезмерная активация плазминовой системы калликреином проводит к неуправляемой кровоточивости (симптом «кровавых слез»). Смена гипер- на гипокоагуляцию при сверхостром менингококковом сепсисе может происходить в считанные часы. Под воздействием калликреина чрезмерно образуется брадикинин, при этом системно расширяются сосуды и падает АД; компенсаторно активизируется ренин-ангиотензиновая система, что ведет к образованию самого сильного вазопрессора организма – ангиотензина-2, который совместно с катехоламинами приводит к спазму мелких артерий, централизации кровообращения, нарушению микроциркуляции. Помимо прямого действия эндотоксина, цитокинов, метаболического ацидоза и уменьшения коронарного кровотока, одной из причин нарушения функции миокарда при токсическом шоке является миокардиоугнетающий фактор (МУФ), при достижении критического уровня которого возникает дилятация левого желудочка и максимальное снижение фракции изгнания (ФИ).
Таким образом, септический шок при МИ имеет одновременно признаки гиповолемического (недостаток объема крови), распределительного (нарушение сосудистого тонуса) и кардиогенного (недостаточность сердечного выброса) шока. Существует стадийность в его развитии.
- Фаза «теплой нормотонии». Начальные проявления шока сопровождаются гипердинамическим режимом кровообращения в сочетании с вазодилятацией периферических сосудов, когда под воздействием эндотоксина увеличивается сердечный выброс, в том числе при накоплении цитокинов, резко уменьшается сосудистый тонус. Развивается относительная гиповолемия, в ответ на которую развивается гиперкатехолемия, приводящая к вазоконстрикции.
- Фаза «теплой гипотонии». Обусловлена сосудистым спазмом, гипоксией и ацидозом, при которых снижается сердечный выброс и усиливается относительная гиповолемия.
- Фаза «холодной гипотонии». Сопровождается потребностью ауторегуляции сосудов сохранить производительность сердца на достаточном уровне ценой периферической вазоконстрикции, ведущей к синдрому малого выброса, гипоперфузии и артериальной гипотензии.
- Фаза декомпенсации. АД не реагирует на увеличение ОЦК, тканевая перфузия неадекватна.
Клинические проявления
МИ представлена разнообразными клиническими формами – от локализованных (назофарингита и менингококконосительства) до генерализованных, среди которых – молниеносные, крайне тяжелые, чаще приводящие к летальному исходу в течение нескольких часов.
Диагностировать менингококковый назофарингит на основании клинической картины, без указания на соответствующий эпиданамнез, затруднительно. До 80% всех форм МИ составляет менингококковый назофарингит. В клинической картине заболевания наиболее типичными симптомами являются заложенность носа, першение в горле, гиперемия и отечность задней стенки глотки с гипертрофией лимфоидных образований на ней, отечность боковых валиков и слизь в небольшом количестве. Гиперемия имеет синюшный оттенок. Распространено мнение о легком характере течения этой формы МИ. В зависимости от уровня лихорадки и выраженности интоксикации различают легкую, среднетяжелую и тяжелую формы болезни. При тяжелой форме доминирует гипертермический синдром, менингизм, у детей первых лет жизни – судорожный синдром. Чаще такие пациенты расцениваются как больные ОРВИ с судорожным синдромом или серозным менингитом на момент госпитализации, и только высев менингококка позволяет адекватно верифицировать диагноз и проводить этиотропную терапию [9]. Нельзя забывать о том, что нередко у детей назофарингит предшествует развитию генерализованных форм болезни, в том числе и с летальным исходом.
Носительство менингококка в коллективах достигает более 40% (в зависимости от эпидситуации). У детей первых лет жизни менингококконосительство встречается редко.
Среди генерализованных форм различают менингококцемию (может протекать в легкой, среднетяжелой, тяжелой и молниеносной формах в виде менингококкового сепсиса), менингококковый менингит, менингоэнцефалит и смешанные формы (менингококцемия + менингит).
Для менингококцемии характерно острое, внезапное начало, критериями тяжести являются степень выраженности интоксикации, характер, величина, распространенность, наличие некрозов и продолжительность элементов сыпи, из которых может высеваться менингококк. При легкой форме элементы представлены розеолами, папулами, мелкими геморрагиями, которые бесследно исчезают к 3-му дню болезни. При среднетяжелой форме элементы преимущественно крупные, геморрагические, с поверхностным некрозом в центре. Сыпь более продолжительная – до 7–10 дней. Для тяжелых и септических молниеносных форм характерны обширные кровоизлияния на коже с глубокими некрозами и их отторжением, при которых могут формироваться косметические дефекты на теле. Эти формы часто сопровождаются маточными, носовыми, желудочно-кишечными кровотечениями, в том числе и на глазном дне. Отмечаются поражения сердца (эндокардит, миокардит, панкардит), суставов, легких, печени, почек, надпочечников.
Современными клиническими особенностями менингококкового менингита являются сомнительность (до 40%) или отсутствие (в 15%) менингеальных симптомов. При этом следует помнить об эквивалентной симптоматике, указывающей на вероятность менингита: спутанность сознания, бред, гиперестезию, упорство рвоты, не приносящей облегчения, «распирающего характера» головной боли, корешковые симптомы, провоцирующие картину «острого живота». У детей раннего возраста – выбухание большого родничка, срыгивания, рвота, диарейный синдром, судороги, положительный симптом Лессажа («подвешивания»).
На современном этапе выявлена зависимость ликворологических изменений (плеоцитоза и протеинрахии) от серогруппы. При заболевании, вызванном менингококком серогруппы С, эти показатели значительно выше, чем при МИ, вызванной менингококком В.
Среди больных МИ отдела нейроинфекций НИИ детских инфекций отмечено, что менингит развивался у лиц с дефектным преморбидным фоном со стороны ЦНС перинатального генеза [6]. Как наиболее частые неотложные состояния при менингококковом менингите в остром периоде заболевания регистрировались: отек головного мозга, внутричерепная гипертензия, инфекционно токсический шок, инфаркт мозга, субдуральный выпот, синдром неадекватной секреции антидиуретического гормона, диэнцефальная дисфункция и нейросенсорная тугоухость.
При менингоэнцефалите с первых дней болезни появляются очаговые симптомы на фоне нарушенного сознания, в виде поражения отдельных черепно-мозговых нервов, корковых и подкорковых парезов или параличей. Могут быть общие или локальные судороги. Характерны очень тяжелое течение, неблагоприятный прогноз – в исходе эпилепсия, гидроцефалия, грубая задержка психомоторного развития. Летальность высокая.
Диагностика
Верификация инфекции осуществляется бактериоскопическим (мазок и толстая капля крови, ликвор), бактериологическим (мазок слизи из носоглотки, посев крови, ликвора), серологическим (РНГА, РА, ИФА) и экспресс-методами (латекс агглютинации, ВИЭФ).
На современном этапе при менингите диагностический мониторинг включает НСГ для оценки состояния желудочков, субарахноидального пространства и цветовое доплеровское (дуплексное) картирование для дифференциации субарахноидального выпота от субдурального. Динамически оценивается ЭЭГ.
Лечебная тактика
На догоспитальном этапе при подозрении на менингококцемию (в том числе и смешанную форму МИ) терапию следует начинать немедленно, на дому, с последующей госпитализацией.
Проводится борьба с гипертермией в зависимости от варианта лихорадки. При «розовой» внутрь или ректально вводят Парацетамол в разовой дозе 10–15 мг/кг, при неэффективности – ибупрофен (Нурофен) в разовой дозе 5–10 мг/кг массы тела. Одновременно проводятся физические методы охлаждения, но не более 30 минут. При неэффективности внутримышечно вводят в возрастной дозе литическую смесь в составе: 50% раствор Анальгина + антигистаминный препарат. При «бледной» лихорадке больного согревают, вводят внутримышечно Папаверин, Но-шпу или Дибазол + литическую смесь. При выраженной централизации кровообращения в терапию добавляют 0,25% раствор дроперидола 0,1–0,2 мл/кг в сочетании с антипиретиками.
При судорожном синдроме (наряду с указанной терапией) вводят внутримышечно Реланиум из расчета 0,1 мл/кг. При отсутствии эффекта включают в терапию Дроперидол в сочетании с Ангальгином, оксибутират натрия. При дебюте менингита судорогами планово назначается длительная терапия препаратами вальпроевой кислоты (Конвулекс и др.), что снижает риск развития постменингитной эпилепсии.
Для предупреждения токсического шока вводят преднизолон (внутримышечно или внутривенно) в дозе 2 мг/кг. При выраженном менингеальном синдроме – 25% ную сернокислую магнезию (1 мл/год жизни) или Лазикс – 1–2 мг/кг внутримышечно.
Введение антибиотика в течение первого часа транспортировки не рекомендуется, а в случае длительной транспортировки стартовым препаратом является левомицетина сукцинат в разовой дозе 25 мг/кг, который вводится не более 2 суток.
Состояние больного оценивается под постоянным контролем АД, частоты пульса, дыхания, диуреза, окраски и температуры кожных покровов, нарастания количества и качества элементов экзантемы и сознания больного. При подозрении на молниеносный вариант генерализованной формы МИ госпитализация осуществляется реанимационной бригадой, которая проводит немедленные реанимационные мероприятия на дому в зависимости от степени септического шока (алгоритм действия перманентно осуществляется при транспортировке больного и продолжается в ОРИТ).
Важным в алгоритме оказания немедленной помощи при септическом шоке является нормализация гемодинамики, микроциркуляции, борьба с ацидозом и гипоксией. Противошоковый эффект достигается введением высоких доз гидрокортизона в сочетании с преднизолоном или его аналогами. Проводится инфузионная терапия, состав которой определяется показателями коллоидно-осмотического давления (альбумина 45–52 г/л и натрия 140–145 ммоль/л). Базовыми растворами являются 5% ная глюкоза, физиологический раствор или раствор Рингера. Соотношение вводимых коллоидов/кристаллоидов – 1:3. Физиологический раствор вводится с целью купирования гиповолемии, при резком падении АД – струйно, а при умеренном его снижении – внутривенно капельно. Под контролем КОС вводится 4%-ный раствор бикарбоната натрия внутривенно медленно, капельно по показателю дефицита оснований, в количестве, равном массе тела (в килограммах), умноженной на ВЕ : 2.
С учетом развития генерализованного васкулита с поражением эндотелия сосудов назначаются ангиопротекторы: Инстенон, Кавинтон, Актовегин, Весел Дуэ Ф (сулодексид).
Постоянно должна проводиться оксигенация, вплоть до ИВЛ, начиная с момента оказания помощи на дому.
После отмены левомицетина сукцината назначается пенициллин в дозе 300 тыс. ед/кг массы тела, 6 введений в сутки, а у детей до 3-месячного возраста – 500 тыс. ед/кг, 8 введений. Более комплаентным и альтернативным пенициллину препаратом является цефтриаксон (Роцефин), который вводится однократно в сутки внутривенно или внутримышечно в дозе 100–150 мг/кг массы в течение 5 дней при менингококцемии, а при менингите – до 10 дней. При тяжелом или затяжном менингите левомицетина сукцинат вводится эндолюмбально, в разовой дозе 10–15 мг.
При ДВС-синдроме назначаются при гиперкоагуляции – Трентал, реополиглюкин, коллоиды, а при гипокоагуляции – свежезаготовленная плазма, ингибиторы протеолиза. При отеке/набухании головного мозга после стабилизации центральной гемодинамики проводится постоянно дегидратационная терапия (Лазикс, Маннитол).
При клинико-ЭЭГ-мониторинге менингита с эпилептической симптоматикой проводится коррекция терапии антикольвунсантами. При неэффективности Конвулекса назначают топиромат (Топамакс).
С учетом длительности антибиотикотерапии в больших дозах, в последние годы предлагается хорошо зарекомендовавшая себя системная энзимотерапия Вобэнзимом, которая оказывает потенцирующий антибиотический, противовоспалительный, антитоксический, гепатопротективный и иммуномодулирующий эффекты, способствуя элиминации токсических субстанций, патогенных иммунных комплексов, иммунных депозитов из тканей, что укорачивает течение и уменьшает тяжесть генерализованных форм МИ [5, 6].
После выписки из стационара реконвалесценты генерализованных форм МИ находятся под диспансерным наблюдением педиатра и невропатолога, во время которого устраняются последствия болезни методами комплексной реабилитации.
При носительстве менингококка и нетяжелом назофарингите госпитализация проводится только по социально бытовым показаниям и из закрытых учреждений.
Назначаются ампициллин, левомицетин в возрастных дозировках в течение 4 дней или вводится внутримышечно Роцефин в течение 3 дней в дозе 125 мг (до 12 лет) и 250 мг у более старших. Спустя 3 дня проводится бактериологическое исследование, и при его отрицательном результате ребенок допускается в коллектив.
При длительном менингококконосительстве проводится повторный курс антибиотикотерапии в сочетании с препаратами иммунореабилитации.
С целью профилактики заболевания у лиц, контактировавших с больным МИ, проводится терапия, подобная лечению локализованных форм.
На коллектив накладывается карантин на 10 дней с момента изоляции больного, проводится наблюдение педиатра и лор-врача. В первые 5–10 дней проводится экстренная профилактика МИ вакцинами А или А+С детям старше года, подросткам и взрослым. Либо при выявлении других серогрупп менингококка в эти же сроки (не позже 7 дней от момента контакта) проводится пассивная профилактика нормальным иммуноглобулином.
После легкой формы МИ вакцинация детям согласно календарю прививок может проводиться спустя месяц после выздоровления. После тяжелых и смешанных форм МИ вакцинация (при отсутствии противопоказаний у невропатолога) может проводиться не ранее 3 месяцев после выздоровления.
Профилактика
В целях предупреждения распространения МИ необходимо проводить вакцинацию детей повышенного риска заражения в возрасте от 1,5 лет: посещающих детские дошкольные учреждения; находящихся в учреждениях с круглосуточным пребыванием (дома ребенка, детские дома); учащихся 1–2 классов общеобразовательных школ и школ–интернатов.
В России зарегистрированы отечественные вакцины менингококковые А и А+С (капсульные специфические полисахариды менингококков соответствующих серогрупп) и зарубежные: Менинго А+С (Франция) – очищенные лиофилизированные полисахариды менингококков серогрупп А и С; поливалентная менингококковая вакцина с полисахаридами групп A, C, Y и W-135 (Англия, США). Вакцины слабо реактогенны, иммунологически активны, вызывают нарастание защитного титра антител с 5 дня после однократного введения, с максимумом их накопления спустя 2 недели. Могут сочетаться в разных шприцах с другими вакцинами.
Список использованной литературы находится в редакции.

