Влияние острого повреждения почек на прогноз больных острой декомпенсацией хронической сердечной недостаточности
СтатьиСтатья публикуется по итогам конкурса молодых ученых в рамках конгресса «Сердечная недостаточность ‘2013»
Макеева Е. Р., Мензоров М. В., Шутов А. М., Серов В. А., Саенко Ю. В., Страхов А. А.
ФГБОУ ВПО «УлГУ», 432017, Ульяновск, ул. Л. Толстого, д. 42
Ключевые слова: декомпенсация кровообращения, острое повреждение почек, прогноз, ХСН
Keywords: circulatory decompensation, acute kidney injury, prognosis, CHF
Ссылка на эту статью: Макеева Е. Р., Мензоров М. В., Шутов А. М. и др. Влияние острого повреждения почек на прогноз больных острой декомпенсацией хронической сердечной недостаточности. Журнал Сердечная Недостаточность. 2014;82 (1):32–38.
Резюме
Актуальность. Частота и тяжесть острого повреждения почек (ОПП) у больных с острой декомпенсацией СН (ОДСН) изучены недостаточно. Цель. Оценить частоту и тяжесть ОПП у больных с ОДСН, а также уточнить связь ОПП с летальностью. Материалы и методы. В исследование включено 104 пациента с ОДСН: мужчин – 58 (56 %), женщин – 46 (44 %), средний возраст – 65,3±10,7 лет. Причиной СН у большинства больных – 82 (79 %) – была ИБС. Диагностику ОДСН осуществляли согласно Рекомендациям ВНОК. ОПП диагностировали и классифицировали согласно Рекомендациям KDIGO (2012). Результаты. ОПП по креатинину диагностировано у 76 (73 %) пациентов: у 61 (59 %) больного выявлена 1 стадия, у 13 (12 %) – 2 стадия и у 2 (2 %) – 3 стадия ОПП. В период госпитализации умерли 5 (5 %) больных. Все умершие имели ОПП. Вероятность внутригоспитальной летальности была выше у больных со 2–3 стадией ОПП, чем у остальных пациентов (ОР 11,2 при 95 % ДИ от 1,6 до 76,3). Заключение. Более половины больных с ОДСН имеют ОПП. У большинства больных (59 %) наблюдается 1 стадия ОПП. Среди пациентов с ОПП 2–3 стадий внутригоспитальная летальность выше, чем у больных без ОПП.
Summary
Background. Rate and severity of acute kidney injury (AKI) in patients with acute decompensated HF (ADHF) are understudied. Aim. To evaluate rate and severity of AKI in patients with ADHF and to specify the relationship of AKI with mortality. Materials and methods. The study included 104 patients with ADHF, 58 (56 %) males and 46 (44 %) females, mean age 65.3±10.7 years. In most of the patients (82, 79 %), HF was induced by IHD. ADHF was diagnosed according to Russian Society of Cardiology Guidelines. AKI was diagnosed and classified according to KDIGO Guidelines (2012). Results. AKI was diagnosed by creatinine level in 76 (73 %) patients. Stage 1 AKI was diagnosed in 61 (59 %) patients; stage 2 – in 13 (12 %) patients, stage 3 – in 2 (2 %) patients. Five (5 %) patients died during the hospitalization period. All dead patients had AKI. The probability of hospital mortality was higher for patients with stage 2–3 AKI than for other patients (OR, 11.2; 95 % CI 1.6–76.3). Conclusion. More than a half of ADHF patients have AKI. Most of the patients (59 %) have stage 1 AKI. Hospital mortality is higher for patients with stage 2–3 AKI than for patients without AKI.
Острое повреждение почек (ОПП) при острой декомпенсации ХСН (ОДСН) влияет на прогноз, а также увеличивает риск последующего развития хронической болезни почек (ХБП) [1]. ОПП диагностируется при увеличении сывороточного креатинина более чем на 50 %, однако некоторые исследования показали, что даже меньшее повышение уровня креатинина связано с увеличением внутригоспитальной летальности, а также частоты и длительности госпитализаций [2]. Частота ОПП при ОДСН составляет от 10 до 40 % [2–6], что зависит, в том числе, и от разных критериев, по которым диагностировали ОПП.
С целью стандартизации диагностики и оценки тяжести ОПП экспертами Acute Dialysis Quality Initiative (ADQI) group (2004) была предложена система стратификации тяжести ОПП – классификация RIFLE (Risk, Injury, Failure, Loss, End-stage renal disease) [7]. В 2007 году критерии RIFLE были модифицированы: предложены более мягкие критерии диагностики и деление ОПП на 3 стадии. Критерии получили название AKIN (Acute Kidney Injury Network) [8]. Обе системы критериев апробированы и применяются для диагностики, оценки тяжести и исходов ОПП при различных заболеваниях, травмах, экзогенных отравлениях [9–11].
В 2012 году были опубликованы Рекомендации KDIGO по диагностике и лечению ОПП (KDIGO Clinical Practice Guidelines for Acute Kidney Injury) [12], основой для которых стали хорошо зарекомендовавшие себя критерии RIFLE и AKIN. Весьма вероятно, что на ближайшие годы рекомендации KDIGO станут основными для диагностики ОПП. Настоящее исследование призвано обратить внимание на распространенность ОПП при ОДСН с использованием новых определений ОПП и изучить связь между тяжестью ОПП и клиническими исходами в течение госпитализации.
Материалы и методы
В исследование методом сплошной выборки включено 104 больных с ОДСН, которые были госпитализированы в отделение кардиологии Центральной городской клинической больницы г. Ульяновска. Мужчин было 58 (56 %), женщин – 46 (44 %), средний возраст больных составил 65,3±10,7 лет. Причинами СН были: ИБС – у 13 (12 %), АГ – у 4 (4 %), сочетание АГ и ИБС – у 69 (66 %), пороки сердца – у 15 (14 %), дилатационная кардиомиопатия – у 3 (3 %) больных. Характеристика больных представлена в таблице 1. Протокол обследования был утвержден этическим комитетом ГУЗ «Центральная городская клиническая больница г. Ульяновска» и соответствовал Хельсинкской декларации.
Таблица 1. Характеристика больных с острой декомпенсацией ХСН
| Показатель | Значение | ||||||||
| Больные Мужчины Женщины | 104 58 (56 %) 46 (44 %) | ||||||||
| Возраст, лет | 65,3±10,6 | ||||||||
Причины ХСН| 104 | 13 (12 %) 4 (4 %) 69 (66 %) 15 (14 %) 3 (3 %) Стадия ХСН | | 21 (20 %) 76 (73 %) 7 (7 %) САД, мм рт. ст. | 136,4±29,0 | ДАД, мм рт. ст. | 2,3±18,48 | Креатинин сыворотки, мкмоль / л | Скорость клубочковой фильтрации, мл / мин / 1,73 м² Скорость клубочковой фильтрации <60 мл/мин / 1,73 м² 122,0±44,8 | 61,0±18,9 54 (52%) |
Диагностику ОДСН осуществляли согласно Рекомендациям ВНОК (2006) [13]. ОПП диагностировали и классифицировали согласно Рекомендациям KDIGO (2012) [12]. Мы не располагали информацией об уровне креатинина сыворотки до заболевания, в этой связи исходным считали креатинин, соответствующий расчетной скорости клубочковой фильтрации (CКФ) 75 мл / мин / 1,73 м² (базальный креатинин) [14]. В случае повышения уровня креатинина сыворотки в 1,5–1,9 раза выше исходного уровня регистрировали 1 стадию ОПП, при увеличении в 2–2,9 раза – 2 стадию, в 3 и более раза или ?353,6 мкмоль / л – 3 стадию. Диагностика ОПП по диурезу была затруднена, поскольку ни у одного из пациентов не было показаний для катетеризации мочевого пузыря (по этой причине почасовой учет диуреза был невозможен). Первичной конечной точкой исследования была смертность от всех причин в период госпитализации.
Статистическая обработка данных проводилась с использованием программы Statistica for Windows 6.0. Достоверность различий между параметрами определяли при их нормальном распределении по критерию t Стьюдента для несвязанных переменных или MannWhitney U test, если распределение отличалось от нормального. Проводился однофакторный корреляционный анализ (в зависимости от вида распределения – Pearson или Kendall tau). Для сравнения двух групп по качественному признаку использовали χ² Пирсона. Для исследования связи бинарного признака с несколькими количественными и качественными признаками использовали многофакторный регрессионный анализ. Для прогнозирования вероятности развития события использовали логистический регрессионный анализ. В случае приближенно нормального распределения данные представлены в виде M±SD, где M – среднее арифметическое, SD – стандартное отклонение. В противном случае данные представлены в виде Me (ИКР), где Me – медиана, ИКР – интерквартильный размах: 25 процентиль – 75 процентиль. Различие считали достоверным при р<0,05.
Результаты
Все больные при поступлении имели картину застоя в малом круге кровообращения по результатам рентгенографии легких. Концентрация креатинина в сыворотке крови при поступлении составила 122,0±44,8 мкмоль / л. ОПП диагностировано у 76 (73 %) пациентов (рис. 1). У 61 (59 %) больного выявлена 1 стадия, у 13 (12 %) – 2 стадия и у 2 (2 %) – 3 стадия ОПП (рис. 2). Пациентов, нуждающихся в заместительной почечной терапии, не было. По возрасту пациенты с ОПП и без ОПП существенно не различались (65,1±9,8 и 67,7±11,6 лет; p=0,41).
Длительность госпитализации больных составила 12 (ИКР: 11–14) дней. В период госпитализации умерли 5 (5 %) больных. Все умершие больные имели ОПП. Частота ОПП 2–3 стадии составила 14 %. Вероятность внутригоспитальной летальности была выше у больных со 2–3-ей стадией ОПП, чем у остальных пациентов (относительный риск 11,2 при 95 %-м доверительном интервале от 1,6 до 76,3).
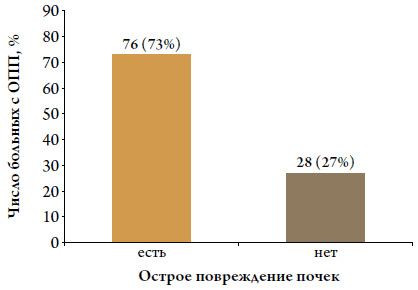
Рисунок 1. Частота острого повреждения почек у больных с острой декомпенсацией ХСН на основании рузультатов исследования уровня базального креатинина (критерии KDIGO)
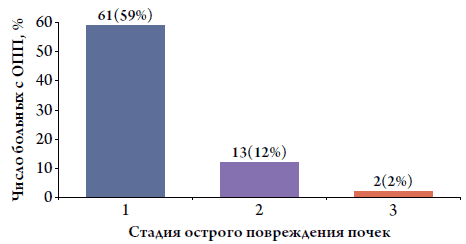
Рисунок 2. Тяжесть острого повреждения почек у больных с острой декомпенсацией ХСН по базальному креатинину (критерии KDIGO)
Обсуждение
Различные критерии, использовавшиеся ранее для диагностики ОПП, не позволяют сравнивать результаты, полученные при оценке частоты и тяжести нарушения функции почек в практике интенсивной терапии. Время развития ОПП является также важным, поскольку изменения уровня креатинина в различные сроки госпитализации отражают разные патофизиологические процессы. В первые дни ОДСН колебания уровня креатинина сыворотки крови отражают развитие 1 типа кардиоренального синдрома (КРС 1 тип) [15], который характеризуется почечной гипоперфузией, почечным венозным застоем [16]. В исследовании POSH медиана времени до диагностики ОПП составила 4 дня (1–12 дней), при этом 70 % пациентов имели ОПП в течение первых 7 дней [17]. В исследованиях Krumholz H. M. с соавт. [18], Forman D. E. с соавт. [19] ОПП развивалось на протяжении первых 7 суток у 90 и 80 % больных соответственно.
Частота ОПП по базальному креатинину у больных с ОДСН в нашем исследовании составила 73 %. В ряде публикаций приводятся значительно более низкие показатели частоты ОПП. Это связано с тем, что используя в диагностике одни и те же критерии, авторы не учитывают больных с 1 стадией ОПП («риск» по критериям RIFLE) [20]. Среди наших больных 2–3 стадию ОПП имели 14 % пациентов.
Критерии ОПП подразумевают оценку функции почек как по креатинину сыворотки, так и (или) по диурезу [7, 8]. Мнения о том, какой из двух способов предпочтительней, противоречивы. Так, при изучении возможностей диагностики ОПП по критерию «креатинин сыворотки» и по критерию «диурез» у больных реанимационного отделения (обязательным условием включения пациента в исследование было наличие постоянного катетера в мочевом пузыре) установлено, что при тщательном мониторировании почасового диуреза, диагностика ОПП по диурезу оказалась более точной. В то же время исследователи отмечают, что принятая в клинике оценка суточного диуреза не дает полного представления о почасовом диурезе [21].
Учитывая высокую частоту мочевой инфекции, ассоциированной c катетеризацией мочевого пузыря [22], диагностика ОПП по диурезу у больных без четких показаний к катетеризации мочевого пузыря затруднена. Более того, объем диуреза при нетяжелом ОПП в ряде случаев в большей степени зависит от состояния гидратации, чем от выраженности поражения почек. Кроме того, всем больным ОДСН вводятся диуретики, которые, увеличивая диурез, не улучшают прогноз ОПП [23].
Все вышеперечисленное заставляет осторожно относиться к возможностям ранней диагностики ОПП по диурезу у кардиологических больных, особенно с учетом того, что у большинства из них нет показаний для катетеризации мочевого пузыря. Проводить же катетеризацию мочевого пузыря только для измерения почасового диуреза вряд ли целесообразно. Ранее нами показано, что частота ОПП, диагностированного по диурезу, у больных ОИМпST почти вдвое меньше по сравнению с оценкой по креатинину, при этом прогностическая значимость критериев по диурезу оказалась выше [24].
Наибольшие трудности встречаются при диагностике 1 стадии ОПП [25]. При использовании базального креатинина ошибка в диагностике ОПП составляет 18 % [26]. Кроме того, сложности в ранней диагностике ОПП могут возникать и при попытке отделить больных ОПП от пациентов с ХБП, при этом у части больных ОПП может развиваться на фоне ХБП, что еще больше затрудняет постановку диагноза. В то же время наличие ХБП у кардиологических больных – не такая уж редкая ситуация. Так, частота ХБП у пациентов кардиологических отделений нашей клиники составляет 34 % [27]. В клинической практике креатинин сыворотки до заболевания часто не известен, особенно при впервые возникшей острой СН, поэтому дифференциальная диагностика между ХБП и ОПП во время госпитализации по поводу ОДСН сложна.
Следует отметить, что в большинстве исследований изучали прогностическое значение ухудшения функции почек, не дифференцируя ОПП и ХБП, и определяли только изменение уровня креатинина сыворотки крови ?26,5 мкмоль / л во время госпитализации [5, 17, 18]. Smith G. L. с соавт. показали, что повышение сывороточного креатинина даже на 9 мкмоль / л ухудшает прогноз пациентов с ОДСН [2]. В настоящем исследовании только 2 и 3-я стадии ОПП, которые характеризуются увеличением уровня креатинина более чем в 2 раза от базального, были связаны с увеличением смертности от любых причин. Известно, что ОПП ухудшает отдаленный прогноз больных, госпитализированных в отделения интенсивной терапии [2–6].
Таким образом, складывается впечатление, что «базальная почечная дисфункция», объединяющая как ОПП, так и ХБП, негативно влияет на клиническое течение ОДСН. Важно отметить, что увеличение сывороточного креатинина более чем в 1,5 раза от базального уровня негативно сказывается на клинических исходах. В исследовании Zhou Q. с соавт. увеличение сывороточного креатинина более чем в 1,5 раза от базального уровня в подгруппах с предсуществующей ХБП и ОПП было независимым фактором, влияющим на внутрибольничную летальность больных с ОДСН [3].
В течение многих десятилетий диагностика острой почечной недостаточности проводилась, основываясь на динамике уровня креатинина и мочевины сыворотки крови во время госпитализации [28, 29]. Серьезным недостатком такого подхода является невозможность ранней диагностики ОПП, поскольку необходимо время для того, чтобы проследить динамику уровня креатинина.
Вышеуказанные недостатки критериев диагностики ОПП стали основанием для поиска маркеров раннего повреждения почек, по аналогии с использованием биохимических маркеров некроза при ОКС. В последние годы широко обсуждается роль таких биомаркеров для диагностики и оценки прогноза ОПП, как интерлейкин 18, липокалин (NGAL), молекула повреждения почек-1 (KIM-1), цистатин С [30, 31]. Не останавливаясь на их диагностической и прогностической ценности, следует отметить, что клиническая ситуация при ОПП отличается от ситуации при ОКС, в случае которого повышение уровня тропонина является определяющим моментом в дальнейшей тактике ведения пациентов. При ОПП решение о заместительной почечной терапии будет основываться на клинических данных и вряд ли биомаркеры раннего повреждения почек повлияют на это решение. Тем не менее ранняя диагностика ОПП открывает возможности для вмешательства (оценка и коррекция гидратации, исключение нефротоксичных препаратов и т. д.). Трудности с интерпретацией результатов исследования биомаркеров связаны с тем, что их уровень может быть повышен у больных с ХБП [32].
Таким образом, более половины больных ОДСН имеют ОПП. У большинства больных наблюдается 1 стадия ОПП. Частота 2 и 3 стадии ОПП ниже – 14 %. Среди пациентов с ОПП 2–3 стадий внутригоспитальная летальность выше, чем у больных без ОПП.
Работа выполнена при поддержке ФЦП «Научные и научно-педагогические кадры инновационной России» (№14. B37.21.1119 от 14.09.12).
Список литературы
