Ротавирусная инфекция у детей: особенности иммунного ответа и опыт применения нового релиз-активного препарата
Статьи Опубликовано в журнале:
« МЕДИЦИНСКИЙ СОВЕТ » №07, 2016. Н.А. МАЛЫШЕВ1, д.м.н., профессор, О.А. САФОНОВА2
1 Московский государственный медико-стоматологический университет им. А.И. Евдокимова Минздрава России
2 Инфекционная клиническая больница №1 Департамента здравоохранения г. Москвы
В статье представлен обзор литературы по особенностям иммунопатогенеза ротавирусной инфекции у детей, а также современные подходы к ее терапии с описанием клинического случая, иллюстрирующего эффективность применения комбинированного противовирусного релиз-активного препарата Эргоферон. Полученные в ходе экспериментального и клинического исследования Эргоферона и его активных компонентов данные подтверждаются собственным опытом применения и свидетельствуют о возможности широкого использования препарата в комплексной терапии ротавирусной инфекции у детей уже с 6-месячного возраста. Клиническая эффективность Эргоферона обусловлена трехкомпонентным составом – аффинно очищенные антитела к интерферону-гамма, к гистамину и к CD4 в релиз-активной форме – и уникальным механизмом действия, позволяющим влиять на ключевые звенья иммунопатогенеза – функциональное состояние CD4+Т-клеток и синтез интерферонов. Противовирусное действие Эргоферона дополняется противовоспалительным и антигистаминным эффектами, что позволяет при ротавирусной инфекции обеспечить быстрое, уже на 2–3-й день терапии, купирование лихорадки, диспепсических расстройств, интоксикационных симптомов. Эргоферон эффективен при начале терапии даже со вторых суток, а его высокая безопасность позволяет минимизировать риск развития гиперстимуляции иммунной системы с последующей ее гипореактивностью.
Ключевые слова: ротавирус, ротавирусная инфекция острый ротавирусный гастроэнтерит острые кишечные инфекции релиз-активность Эргоферон
АКТУАЛЬНОСТЬ ПРОБЛЕМЫ
При последней экспертной оценке глобального бремени заболеваний за 2013 г. диарея по-прежнему остается весомой причиной смерти в детской популяции, входя в пятерку в возрасте до 5 лет и вызывая более 38 тыс. смертей у детей от 5 до 9 лет, особенно в странах с низким и средним уровнем дохода [1]. В последние годы наблюдается тенденция значительного снижения бактериальной этиологии острых кишечных инфекций (ОКИ) на фоне роста частоты их вирусного генеза с сохранением стабильно высокого уровня заболеваемости данной патологией [2]. Весомый вклад вносит ротавирусная инфекция, которая является значимой причиной ассоциированных с диареей смертей у детей младше 5 лет [3, 4]. Кроме того, ротавирусная инфекция – распространенная причина диареи, требующей госпитализации, даже в странах с низкой смертностью детства [3].
Согласно данным популяционных исследований, доля ротавирусных гастроэнтеритов у детей до 5 лет в странах Западной Европы максимальна в Норвегии и Швеции, составляя 63,5 и 52% соответственно, и минимальна в Греции, где их выявляется до 25,3%. Довольно большая часть таких пациентов госпитализируется – от 7 до 81% в зависимости от страны [5]. В РФ ротавирусная инфекция составляет 36% случаев всех ОКИ и остается главной причиной дегидратирующих диарей у детей [2, 6]. В отечественном исследовании 2010–2012 гг. с участием более 300 детей по данным полимеразной цепной реакции (ПЦР) установлено, что вирусная этиология ОКИ с диареей встречается более чем в 77% случаев. В группе детей до 3 лет доля вирусных диарей составила 45% при их ротавирусном генезе более чем у 40% детей, а в возрасте до 6 лет – 56% случаев.
Результаты данного исследования также свидетельствуют о том, что более чем в 80% случаев наблюдается средняя степень тяжести вирусных гастроэнтеритов, а их превалирующее осложнение – дегидратация 1–2-й степени [7].
РОТАВИРУСНАЯ ИНФЕКЦИЯ И ОСОБЕННОСТИ ИММУНОПАТОГЕНЕЗА У ДЕТЕЙ
Ротавирус – РНК-вирус семейства Reoviridae, которым впервые в возрасте до 5 лет заражается почти каждый ребенок в мире. Существует пять видов данного вируса, называемых группами A, B, C, D и E. Ротавирус А наиболее распространен и вызывает более чем 90% инфекций у людей [8]. Несколько его серотипов, вызывающих заболевание у людей, были идентифицированы и стали основой для разработки вакцин. Однако в последнее время в группе ротавирусов возросла этиологическая значимость серогруппы С, что, по мнению ряда ученых, может быть связано с распространением вирусных агентов из Китая, тогда как вакцина направлена на серогруппу А [2].
Ротавирус чрезвычайно устойчив во внешней среде. Иммунитет развивается при каждой перенесенной инфекции, поэтому последующие эпизоды инфицирования ротавирусом протекают менее выраженно клинически и взрослые люди поражаются значительно реже. Ротавирус размножается в зрелых эпителиальных клетках на кончиках ворсинок тонкого кишечника и передается фекально-оральным путем. Клинически ротавирусная инфекция чаще ограничена местными кишечными симптомами и приводит к водянистой диарее, рвоте, лихорадке, которая у трети детей достигает фебрильных значений. Наиболее тяжелое течение с выраженной дегидратацией чаще отмечается среди детей младшего возраста [6, 9]. Помимо поражений кишечника, ротавирусная инфекция также способна оказывать и системное действие – виремия может быть легко обнаружена после первичного инфицирования [10]. Соответственно, ротавирусная инфекция сопровождается местным и системным иммунным ответом. Иммунопатогенез ротавирусной инфекции до конца не изучен [6].
Известно, что первую линию защиты от ротавирусной инфекции в кишечнике представляет фактор гуморального иммунитета мукозальный иммуноглобулин А (IgA) наряду с факторами клеточного иммунитета – Т-клетками СD4+ и СD8+ [10]. Стоит отметить, что Т-лимфоциты – центральные клетки, участвующие в реализации реакций адаптивного иммунного ответа. А среди субпопуляций Т-лимфоцитов CD4+-Т-хелперы (Th) являются ключевыми, поскольку контролируют запуск как клеточно-, так и антитело-опосредованного (гуморального) адаптивного иммунного ответа [11].
Установлено, что и СD4+-Т-клетки, и антиротавирусные антитела играют ключевую роль в элиминации ротавируса из организма, однако Т-клетки опосредуют данный эффект быстрее [10]. Причем, согласно результатам недавно опубликованного исследования, доля участвующих в противовирусном ответе Т-клеток, включая CD4+, достоверно снижается у детей с ротавирусным энтеритом, что приводит к дисбалансу Т-хелперного ответа и, соответственно, нарушению выработки цитокинов [12].
На сегодняшний день существует понимание значимости CD4+-Т-клеток не только при первичном инфицировании ротавирусом, но и при повторной инфекции, и при вакцинации [13–15]. Установленным фактом, помогающим понять, почему дети только частично защищены после перенесенной ротавирусной инфекции или вакцинации, стали результаты изучения содержания вирус-специфических СD4+-Т-клеток, секретирующих интерферон-гамма (ИФН-гамма). Показано, что в отличие от взрослых дети с ротавирусной диареей имеют их крайне низкий уровень [14]. А циркулирующие ротавирус-специфические СD4+-Т-клетки имеют относительно слабый функциональный профиль, характеризующийся в т. ч. и снижением продукции ИФН-гамма [15].
Универсальная ранняя реакция врожденного иммунитета в ответ на вирусную инфекцию – выработка интерферонов (ИФН). Система ИФН с помощью всех 3 типов ИФН обеспечивает синергичный ответ на ротавирусную инфекцию [10]. ИФН-гамма – один из основных продуктов Тh1-СD4+клеток. К биологическим эффектам ИФН-гамма относятся потенцирование активности системы ИФН I типа (ИФН-альфа/бета), поляризация клеточного иммунного ответа в направлении Тh1, активация внутриклеточных противовирусных механизмов. Значимый результат активности ИФН-гамма – вызываемое им состояние противовирусной защиты, включая подавление синтеза белка и разрушение РНК-вируса [16].
In vitro установлено наличие противоротавирусного действия ИФН-гамма, продемонстрирована его роль в ограничении кишечных и внекишечных поражений, вызываемых рядом штаммов ротавируса [8, 17]. Также существуют экспериментальные доказательства того, что ИФН-гамма – единственный цитокин в стимулированных CD4+-Т-клетках иммунизированных животных, который ингиби-ровал репликацию ротавируса [18].
Ротавирус чрезвычайно устойчив во внешней среде. Иммунитет развивается при каждой перенесенной инфекции, поэтому последующие эпизоды инфицирования ротавирусом протекают менее выраженно клинически и взрослые люди поражаются значительно реже
В различных исследованиях было показано, что уровень ИФН-гамма повышен у инфицированных ротавирусом детей [8, 19]. Причем у детей с наличием рвоты выявлены статистически достоверно (р Известно, что экспрессию ИФН стимулирует сигнальный каскад в ответ на внедрение РНК-ротавируса в клетку. Однако в последние годы появились данные о возникновении у ряда штаммов ротавируса способности «ускользать» от действия иммунной системы, что, как правило, характеризуется низким уровнем экспрессии ИФН и, соответственно, подавлением создания противовирусного состояния в клетке [17].
Таким образом, в иммунопатогенезе ротавирусной инфекции у детей доказана высокая значимость СD4+-Т-клеток и ИФН-гамма для обеспечения полноценного иммунного ответа при ротавирусной инфекции.
РОТАВИРУС: РЕКОМЕНДАЦИИ ВОЗ И ОСОБЕННОСТИ РУТИННОЙ ПРАКТИКИ
Очевидно, что подходы к профилактике и терапии ротавирусной инфекции должны базироваться исключительно на данных доказательной медицины. На сегодняшний день в отношении ротавирусной инфекции существуют две ключевые стратегии с использованием вмешательств с доказанной эффективностью и рекомендованных Всемирной организацией здравоохранения (ВОЗ).
Во-первых, профилактическое применение ротавирусных вакцин. Ротавирусная инфекция ежегодно вызывала более полумиллиона смертей среди детей младше 5 лет и более 2 млн случаев госпитализации в год до введения вакцинации [20]. В настоящее время в мире существуют две лицензированные ротавирусные вакцины – одновалентная (RV1; Rotarix, GlaxoSmithKline Biologicals) и пятивалентная (RV5; RotaTeq, Merck & Co., Inc.). А также к использованию только в Китае разрешена ротавирус-ная вакцина, разработанная в Институте биомедицинских продуктов Ланьчжоу [3].
Во-вторых, при развернутой клинической картине ротавирусной инфекции чрезвычайно важно соблюдение рекомендаций ВОЗ по использованию пероральных регидратационных солевых растворов и/или домашнему выпаиванию.
Терапевтические вмешательства при ротавирусной инфекции включают диетотерапию: ограничение лактозы, оральную регидратацию, противовирусные препараты, энтеросорбенты, пробиотики и симптоматическую терапию
Однако с учетом нежелательных эффектов вакцинации, включая случаи инвагинации кишечника у детей раннего возраста, отсутствие охвата прививками детской популяции в должном объеме, особенности реакции иммунной системы ребенка на ротавирус и объективную недоступность верификации вирусных диарей в практической деятельности педиатра, проблема терапии ротавирусной инфекции по-прежнему остается чрезвычайно актуальной.
Терапевтические вмешательства при ротавирусной инфекции включают диетотерапию: ограничение лактозы, оральную регидратацию, противовирусные препараты, энтеросорбенты, пробиотики и симптоматическую терапию.
В сложившейся ситуации отсутствия специфической этиотропной терапии при ротавирусной инфекции наиболее значимым становится поиск лекарственного препарата, способного оказывать регулирующее действие для обеспечения полноценного противовирусного ответа без риска истощения иммунной системы, модулируя иммунный ответ в соответствии с текущими потребностями организма. В первую очередь, исходя из иммунопатогенетических особенностей ротавирусной инфекции у детей, необходимо использование лекарственного средства для оптимизации взаимодействия нативных ИФН с собственными рецепторами, повышения уровня синтеза ИФН в ответ на вирусную агрессию, а также активации функциональных способностей CD4+-Т-клеток.
С учетом вышеизложенного перспективным представляется использование нового комбинированного лекарственного препарата Эргоферон.
ЭРГОФЕРОН В ТЕРАПИИ РОТАВИРУСНОЙ ИНФЕКЦИИ: ДОКАЗАТЕЛЬСТВА ЭФФЕКТИВНОСТИ
Активные действующие вещества Эргоферона – аффинно очищенные антитела к ИФН-гамма, к гистамину и к CD4 в релиз-активной форме. Согласно действующей инструкции, одно из показаний к применению Эргоферона – профилактика и лечение ОКИ вирусной этиологии, включая ротавирусную.
Эргоферон влияет на функциональную активность взаимодействия ИФН-гамма, гистамина и CD4 с их рецепторами, оказывает регулирующее действие на молекулы-мишени (ИФН-гамма, ИФН-альфа, Т-хелперы, макрофаги, рецепторы к ИФН-гамма, рецепторы к гистамину, CD4-корецептор). Именно эта способность препарата обеспечивает комбинированный противовирусный, противовоспалительный и антигистаминный лечебный эффект.
В ходе экспериментальных исследований установлено, что мощное противовирусное действие Эргоферона достигается благодаря сочетанию воздействия на неспецифические и специфические звенья иммунитета с помощью релиз-активных антител к ИФН-гамма и СD4 [21]. Эргоферон влияет и на продукцию, и на рецепцию ИФН, что повышает эффективность работы системы ИФН. Стоит заметить, что регулирующее действие релиз-активных антител к CD4 приводит к повышению функциональной активности CD4-лимфоцитов и нормализации иммунорегуляторного индекса CD4/CD8, что также значимо с учетом данных об иммунопатогенезе ротавирусной инфекции у детей.
Влияние на систему ИФН в сочетании с активацией процессов распознавания вирусов системой CD4-клеток обеспечивает синергию в реализации их противовирусных эффектов и развитие полноценного противовирусного состояния в клетке. Помимо повышения вирус-индуцированной продукции ИФН-гамма и ИФН-альфа/бета и сопряженных с ними интерлейкинов (ИЛ-2, ИЛ-4, ИЛ-10 и др.), улучшения взаимодействия ИФН с его рецептором, важным преимуществом Эргоферона при ротавирусной инфекции, достигаемым благодаря входящим в его состав релиз-активным антителам к ИФН-гамма, представляется наличие способности восстанавливать баланс Th1/Th2-активностей иммунного ответа. А также повышение продукции защитных антител – IgG и IgA, в т. ч. секреторного sIgА, который усиливает местный, мукозальный, иммунитет.
В экспериментальных и клинических исследованиях доказана эффективность и Эргоферона, и его компонентов в отношении ротавирусной инфекции [22–26]. Эффективность Эргоферона в отношении ротавирусной инфекции доказана, например, в ходе плацебо-контролирумых исследований, проведенных в ФГБУ «ГНЦ Институт иммунологии ФМБА» под руководством профессора М.Р. Хаитова (данные готовятся к публикации).
Установлено, что Эргоферон демонстрирует достоверно превышающую контроль противовирусную активность в отношении кишечного ротавиру-са группы А, проявляющуюся снижением вирусной нагрузки в культуре клеток млекопитающих (МА-104).
В ходе экспериментальных исследований установлено, что мощное противовирусное действие Эргоферона достигается благодаря сочетанию воздействия на неспецифические и специфические звенья иммунитета с помощью релиз-активных антител к ИФН-гамма и СD4. Эргоферон влияет и на продукцию, и на рецепцию ИФН, что повышает эффективность работы системы ИФН
А противовирусная эффективность при ротавирусной инфекции у детей такого компонента Эргоферона, как релиз-активные антитела к ИФН-гамма, ранее широко изучена и доказана в ходе клинических исследований, включая «эталонные» по своему дизайну с точки зрения доказательной медицины многоцентровые рандомизированные двойные слепые плацебо-контролируемые (рис.) [22–23].
Например, в рандомизированном двойном слепом плацебо-контролируемом исследовании у детей в возрасте от 2 до 3 лет со среднетяжелой формой ротавирусного гастроэнтерита, проведенном в г. Краснодаре с участием 53 детей, была показана клиническая эффективность препарата, проявившаяся уже к концу первых суток терапии в виде уменьшения частоты стула, а также положительном влиянии на длительность и выраженность рвоты, диареи, метеоризма, болевого синдрома, лихорадки, других проявлений токсикоза и катаральных явлений в респираторном тракте в течение 5-дневного курса терапии. Авторами отмечено, что достигнутые клинические эффекты во многом связаны с элиминацией ротавируса из желудочно-кишечного тракта (ЖКТ) – у 90% детей на 5-е сутки лечения прекращалось вирусовыделение, тогда как в копро-фильтрате пациентов, получавших плацебо, антиген рота-вируса определялся у 40% пациентов [22].
Полученные данные были подтверждены и в других исследованиях эффективности и безопасности релиз-активных антител к ИФН-гамма при ротавирусной инфекции [23–26]. Так, например, в рандомизированном исследовании, выполненном с участием 82 детей в возрасте до 12 мес. в г. Красноярске, показано, что терапевтическая эффективность 7-дневного курса препарата релиз-активных антител к ИФН-гамма при ротавирусной инфекции проявлялась в достоверном уменьшении выраженности и более быстром купировании лихорадки, рвоты и диарейного синдрома. У детей, получавших данный препарат, наблюдалось более быстрое восстановление функции ЖКТ, отсутствовало вирусовыделение и значительно реже развивались постинфекционные нарушения [24].
Помимо противовирусного действия, Эргоферон обладает дополнительной лечебной активностью: оказывает противовоспалительное и антигистаминное действие.
Противовоспалительная активность Эргоферона обеспечивается результатами влияния релиз-активных антител к гистамину на гистамин-зависимые реакции, являющиеся компонентом воспалительного процесса, и релиз-активных антител к CD4 на цитокиновую сеть и регуляцией баланса продукции про- и противовоспалительных цитокинов [21, 27].
Таким образом, трехкомпонентный состав Эргоферона позволяет воздействовать на различные механизмы инфекционно-воспалительного процесса и формировать адекватный противовирусный ответ широкого спектра, включая ротавирусную инфекцию. Стоит отметить, что особенности фармакологического действия Эргоферона обусловливают единую лечебную схему, не зависящую от возраста пациента.
В ходе экспериментальных и клинических исследований пациента доказано, что уникальный механизм действия Эргоферона обеспечивает высокие показатели фармакологической безопасности: его активные компоненты модифицируют функции молекул-мишеней, без гиперстимуляции и развития гипореактивности организма. Благодаря высокому профилю безопасности, в РФ Эргоферон разрешен к применению у детей с 6 мес.
В нашей клинике накоплен достаточно большой позитивный опыт применения Эргоферона в терапии ротавирусной инфекции. В качестве его иллюстрации далее приведен один из клинических случаев.
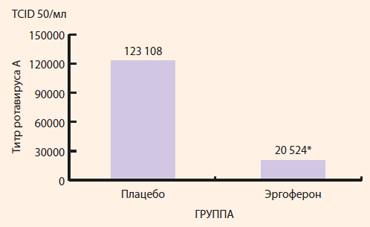
Рисунок. Противовирусная активность Эргоферона в отношении ротавируса группы А
* Отличие от плацебо достоверно, p Эффективность Эргоферона в отношении ротавирусной инфекции доказана в ходе плацебо-контролируемых исследований, проведенных в ФГБУ «ГНЦ Институт иммунологии ФМБА» под руководством профессора М.Р. Хаитова. Установлено, что Эргоферон демонстрирует достоверную по сравнению с плацебо-контролем противовирусную активность в отношении кишечного ротавируса группы А, проявляющуюся снижением вирусной нагрузки (титра вируса) в культуре клеток млекопитающих (МА-104).
КЛИНИЧЕСКИЙ СЛУЧАЙ: ОПЫТ ПРИМЕНЕНИЯ ЭРГОФЕРОНА ПРИ РОТАВИРУСНОЙ ИНФЕКЦИИ
Пациент Т., 2 года и 3 месяца.
Жалобы. Поступил в инфекционное отделение ЦКБ №1 с жалобами на выраженную тошноту, двукратную рвоту съеденной пищей и частый жидкий стул (трехкратно) в течение последних суток, умеренную боль, вздутие и урчание в животе, вялость, снижение аппетита, снижение подвижности, повышение температуры до 38 °С, затрудненное носовое дыхание.
Аnamnesis morbi.Болен 2-й день. Заболел остро. Вчера во второй половине дня после посещения детского развлекательного центра появились тошнота, жидкий стул, снижение аппетита, повышение температуры до 38 °С.
Родители давали двукратно диоктаэдрический смектит (Смекта) и парацетамол на ночь. Эффекта от проводимого лечения не наблюдалось. Ночью появилась рвота, участился стул, ребенок стал жаловаться на боль в животе, нарастали симптомы интоксикации – снизилась подвижность, ребенок стал вялым. Последнее мочеиспускание – 6 ч назад. Обратились в скорую помощь.
Госпитализирован в инфекционное отделение ЦКБ №1.
Anamnesis vitae. Родился в срок, без осложнений. Преморбидный фон не отягощен. Прививки по возрасту. Последнее взвешивание – 1 мес. назад, на профилактическом приеме в районной поликлинике. Вес 12,0 кг.
При осмотре: состояние средней степени тяжести, ребенок вялый, адинамичный. Носовое дыхание затруднено, отмечается заложенность носа, отделяемого нет, слизистая оболочка зева умеренно гиперемирована. Видимые кожные покровы чистые, бледные, с сероватым оттенком. Слизистые оболочки полости рта и нижнего века бледные. Язык бледно-розовый, у корня обложен серо-белым налетом.
Эластичность кожи и тургор снижены, кисти и стопы холодные. Температура тела в аксиллярной впадине 37,6 °С.
Рост 85,2 см. Вес 11,3 кг.
Помимо противовирусного действия, Эргоферон обладает дополнительной лечебной активностью: оказывает противовоспалительное и антигистаминное действие
Регионарные подкожные лимфоузлы не увеличены. В легких дыхание ритмичное, везикулярное (пуэрильное), хрипов нет. ЧДД – 26 в мин. Тоны сердца приглушены, ритм правильный, шумов в области сердца нет, ЧСС – 120 в мин, АД 100/60 мм рт. ст. Живот вздут, болезненный в эпигастрии и параумбиликальной области. Аускультативно над всей поверхностью живота выслушивается урчание и переливание. Печень у края реберной дуги по среднеключичной линии справа, край закруглен, безболезненный. Периферических отеков нет.
Общий анализ крови: эритроциты – 4,46 х 1012/л, Нв – 107 г/л, лейкоциты – 3,4 х 109/л, палочкоядерные – 4%, сегментоядерные – 45%, лимфоциты – 25%, моноциты – 26%, СОЭ – 19 мм/ч.
Общий анализ мочи: прозрачность полная, плотность – 1 009, реакция кислая, лейкоциты от 0 до 2, слизь «+» ПЦР: результат положительный – в кале обнаружена РНК Rotavirus А.
Диагноз: ротавирусная инфекция: острый гастроэнтерит средней степени тяжести, эксикоз 1-й степени, острый катаральный ринофарингит, ОДН 1.
Данный диагноз поставлен на основании типичной клинико-эпидемиологической картины, подтвержденной результатами ПЦР. Ротавирусная инфекция является контагиозной, передающейся фекально-оральным путем, что могло произойти при посещении ребенком детского развлекательного учреждения. Клинически для ротавирусной инфекции характерно острое начало с повышением температуры более 37,5 °С, появлением рвоты, диареи и нарастанием явлений эксикоза, наличием симптомов интоксикации (вялость, снижение аппетита, адинамия). Также характерно поражение слизистых оболочек носа и зева. Описанные симптомы наблюдались у данного пациента, что и позволило заподозрить ротавирусный гастроэнтерит.
В ходе сбора анамнеза и физикального обследования также получены дополнительные данные, соответствующие эксикозу 1-й степени – потеря массы тела 6–7%, снижение эластичности кожи и тургора тканей, бледность кожных покровов с сероватым оттенком, похолодание конечностей, тахикардия, приглушение сердечных тонов, урежение мочеиспусканий.
Проведенное лабораторное обследование окончательно подтвердило предварительный диагноз.
Данному пациенту была назначена терапия, включавшая следующее:
1. Санацию носовых ходов.
2. Дробное питье регидрона до 0,5 л/сут.
3. Эргоферон по схеме: 1-й день лечения 8 таблеток (1 таблетка каждые 30 мин в течение первых 2 ч, затем по 1 таблетке 3 раза в день с равными интервалами), начиная со 2-го дня до 7-го дня по 1 таблетке 3 раза в день. Растворять таблетку в небольшом количестве (1 столовая ложка) кипяченой воды комнатной температуры.
4. Мезим по ½ таблетки 3 раза в день.
5. Глюконат кальция по ½ таблетки 3 раза в день.
6. Sol. Analgini 0,2 + Dimedroli 0,2 внутримышечно (при повышении температуры тела выше 38,5 °С).
На фоне приема Эргоферона уже к утру второго дня терапии отмечена нормализация температуры тела – 36,4 °С (вечером она составила 36,6 °С) с сохранением нормальных значений до конца периода наблюдения. На 2-й день лечения, несмотря на сохранение общего среднетяжелого состояния, незначительной боли в животе и урчания, появилась тенденция к стабилизации витальных функций – ЧСС составляла 112 в минуту, уменьшились интоксикационные симптомы, перестали беспокоить тошнота и рвота, уменьшилась частота стула до 2 раз в сутки, он стал кашицеобразным.
К третьему дню лечения состояние пациента оценивалось как удовлетворительное, жалоб не было, показатели со стороны органов дыхания и кровообращения соответствовали возрастной норме, нормализовался стул – он был однократным, оформленным, купирован эксикоз. Параметры общего анализа крови также свидетельствовали о реконвалесценции: эритроциты – 5,6 х 1012/л, Нв – 126 г/л, лейкоциты – 6,5 х 109/л, палочкоядерные – 4%, сегментоядерные – 50%, лимфоциты – 37%, моноциты – 9%, СОЭ – 7 мм/ч.
При проведении контрольного анализа кала на рота-вирусную РНК с помощью ПЦР на 7-е сутки терапии получен отрицательный результат, что также стало свидетельством клинического выздоровления пациента.
Стоит заметить, что нежелательных явлений при приеме Эргоферона выявлено не было.
ВЫВОДЫ
Таким образом, наши наблюдения подтверждают полученные ранее данные об эффективности и безопасности применения Эргоферона при ротавирусной инфекции.
Накопленный опыт его применения позволяет рекомендовать Эргоферон к широкому использованию в комплексной терапии ротавирусной инфекции у детей начиная уже с 6 мес. Активные компоненты Эргоферона позволяют формировать эффективное противовирусное состояние в клетке, способствуя быстрой нормализации клинической симптоматики ротавирусного гастроэнтерита, включая диспепсические явления, симптомы интоксикации и сопутствующие внекишечные проявления со стороны верхних дыхательных путей.
Клинические результаты применения Эргоферона при ротавирусной инфекции обусловлены в первую очередь его противовирусной активностью, которая помимо влияния на продукцию и рецепцию ИФН, что повышает эффективность работы системы ИФН, усилена за счет воздействия на систему распознавания вирусов (система CD4+-клеток). Стоит отметить, что Эргоферон эффективен даже при начале на 2-е сутки заболевания, а его высокая безопасность позволяет минимизировать риск развития гиперстимуляции иммунной системы с последующей ее гипореактивностью.
ЛИТЕРАТУРА
1. Global Burden of Disease Pediatrics Collaboration. Global and National Burden of Diseases and Injuries Among Children and Adolescents Between 1990 and 2013: Findings From the Global Burden of Disease 2013 Study. JAMA Pediatr, 2016. doi:10.1001/jamapediat-rics.2015.4276.
2. Горелов А.В. Интерферонотерапия при острых кишечных инфекциях у детей (Актуальные вопросы интерферонотерапии в случае инфекционной патологии у детей). Эффективная фармакотерапия, 2015, 3: 49-50.
3. Soares-Weiser K, Maclehose H, Bergman H, Ben-Aharon I, Nagpal S, Goldberg E. et al. Vaccines for preventing rotavirus diarrhea: vaccines in use. Cochrane Database Syst Rev, 2012, 11: CD008521.
4. Das JK, Bhutta ZA. Global challenges in acute diarrhea. Curr Opin Gastroenterol, 2016, 32(1): 18-23.
5. Ogilvie I, Khoury H, Goetghebeur MM, El Khoury AC, Giaquinto C. Burden of community-acquired and nosocomial rotavirus gastroenteritis in the pediatric population of Western Europe: a scoping review. BMC Infectious Diseases, 2012, 12: 62. doi:10.1186/1471-2334-12-62.
6. Маянский Н.А., Маянский А.Н., Куличенко Т.В. Ротавирусная инфекция: эпидемиология, патология, вакцинопрофилактика. Вестник РАМН, 2015, 1: 47-55.
7. Лукьянова А.М., Бехтерева М.К., Птичникова Н.Н. Клинико-эпидемиологическая характеристика вирусных диарей у детей. Журнал инфектоло-гии, 2014, 6(1): 60-66.
8. Cho H, Kelsall BL. The role of type I interferons in intestinal infection, homeostasis, and inflammation. Immunol Rev, 2014, 260(1): 145-167.
9. Feng N, Kim B, Fenaux M, Nguyen H, Vo P, Omary MB et al. Role of Interferon in Homologous and Heterologous Rotavirus Infection in the Intestines and Extraintestinal Organs of Suckling Mice. J Virol, 2008, 82(15): 7578-7590.
10. Blutt SE, Conner ME. The Gastrointestinal Frontier: IgA and Viruses. Frontiers in immunology, 2013, 4: 402.
11. Swain SL, McKinstry KK, Strutt TM. Expanding roles for CD4+ T cells in immunity to viruses. Nature reviews Immunology, 2012, 12(2): 136-148.
12. Dong H, Qu S, Chen X, Zhu H, Tai X, Pan J. Changes in the cytokine expression of peripheral Treg and Th17 cells in children with rotavirus enteritis. Exp Ther Med, 2015, 10(2): 679-682.
13. Kim B., Feng N, Narváez CF, HeX-S, Eo SK, Lim CW et al. The Influence of CD4+ CD25+ Foxp3+ Regu la tory T Cells on the Immune Response to Rota virus Infection. Vaccine, 2008, 26(44): 5601-5611.
14. Jaimes MC, Rojas OL, González AM, Cajiao I, Charpilienne A, Pothier P, et al. Frequencies of virus-specific CD4(+) and CD8(+) T lymphocytes secreting gamma interferon after acute natural rotavirus infection in children and adults J Virol, 2002, 76(10): 4741-9.
15. Parra M, Herrera D, Jácome MF, Mesa MC Rodríguez LS, Guzmán C, et al. Circulating rota-virus-specific T cells have a poor functional profile. Virology, 2014, 468-470: 340-50.
16. Луцкий А.А., Жирков А.А., Лобзин Д.Ю., Рао М., Алексеева ЛА., Мейрер М. и др. Интерферон-у: биологическая функция и значение для диагностики клеточного иммунного ответа. Журнал инфектологии, 2015, 7(4): 10-22.
17. Arnold MM, Sen A, Greenberg HB, Patton JT. The Battle between Rotavirus and Its Host for Control of the Interferon Signaling Pathway. PLoS Pathog, 2013, 9(1): e1003064.
18. McNeal MM, Stone SC, Basu M, Clements JD, Choi AH, Ward RL. IFN-gamma is the only anti-rotavirus cytokine found after in vitro stimulation of memory CD4+ T cells from mice immunized with a chimeric VP6 protein. Viral Immunol, 2007, 20(4): 571-84.
19. Jiang B, Snipes-Magaldi L, Dennehy P, Keyserling H, Holman RC, Bresee J et al. Cytokines as mediators for or effectors against rotavirus disease in children. Clin Diagn Lab Immunol, 2003, 10(6): 995-1001.
20. Tate JE, Burton AH, Boschi-Pinto C, Steele AD, Duque J, Parashar UD. 2008 Estimate of world- wide rotavirus-associated mortality in children younger than 5 years before the introduction of universal rotavirus vaccination programmes: a systematic review and meta-analysis. Lancet Infect Dis, 2012, 12: 136-4110.
21. Дмитриев А.Н. Релиз-активные лекарственные препараты – новое направление в лечении острых респираторных вирусных инфекций (обзор литературы). Практическая медицина, 2014, 7(83): 14-20.
22. Тхакушинова Н.Х., Соболева Н.Г. Современные возможности эффективного лечения ротавирус-ной инфекции у детей раннего возраста (результаты двойного слепого плацебоконтролируемого исследования лечебной эффективности анаферона детского). Педиатрия, 2012, 91(1): 63-67.
23. Горелов А.В., Плоскирева А.А., Тхакушинова Н.Х. Клинико-вирусологическая оценка эффективности индуктора интерферона, содержащего антитела к гамма-интерферону в релиз-активной форме, в терапии острых вирусных кишечных инфекций. Инфекционные болезни, 2012, 10(3): 56-62.
24. Мартынова Г.П., Соловьева И.А., Кузнецова Н.Ф., Дорошенко Л.Г., Комарова Б.Л., Щеголева Ю.Е. и др. Ротавирусная инфекция: клинико-эпидемиологические особенности, опыт применения препарата Анаферон детский в комплексной терапии детей первого года жизни. Практическая медицина, 2015, 7(92): 138-144.
25. Калугина Т.В., Аверьянов О.Ю., Малявина Т.Е. Оценка клинической и санационной эффективности препарата «Анаферон детский» при назначении его в комплексной терапии у детей первого полугодия жизни с ротавирусным гастроэнтеритом. Поликлиника, 2012, 6: 1-2.
26. Николаева И.В. Опыт применения Анаферона детского в лечении ОРВИ с гастроинтести-нальным синдромом и вирусных диарей у детей. Обзор литературы. Эффективная фармакотерапия. Педиатрия, 2013, 1: 8-12.
27. Павлова Е.Б. Эффективная стратегия лечения ОРВИ: противовоспалительное действие нового противовирусного препарата. Internal Medicine. Clinical SleepMedicine (Доктор.Ру), 2014, 9(97): 20-24.


