Аргументы ЗА необходимость более совершенных прогностических факторов при РМЖ без поражения лимфатических узлов.
СтатьиК. Томссен и Ф. Енике
European Journal of Cancer 36 (2000) 293-306
Аргументы в пользу того, что нужны / См. также Аргументы против
1. Введение
Рак молочной железы характеризуется диссеминацией раковых клеток гематогенным путем уже на ранних стадиях заболевания. Поэтому помимо местного лечения (хирургическая операция и ренгенотерапия), больным проводится системная химиотерапия и/или эндокринная терапия. За последние 40 лет реальная польза от системного адъювантного лечения в плане улучшения показателей выживания без признаков заболевания и общего выживания была подтверждена многочисленными рандомизированными испытаниями [1, 2]. Однако, так как рак молочной железы является гетерогенным заболеванием, вопрос о том, целесообразно ли назначать адъювантную химиотерапию всем больным или только больным с высоким риском развития системного заболевания при первом выявлении, остается открытым.
2. На каком этапе мы находимся?
Согласно рекомендациям, разработанным в 1998 г. на Сент-Галленской конференции по адъювантной терапии при раке молочной железы, адъювантная терапия должна проводиться почти всем больным, как с негативными, так и с позитивными лимфатическими узлами [3, 4]. Эти рекомендации основаны на недавних разработках EBCTG (Early Breast Cancer Trialists Group), в соответствии с которыми адъювантная терапия дает преимущество почти у всех больных [1, 2]. Для большей части больных рекомендуется назначать вместе адъювантную химиотерапию и тамоксифен.
Эти общие лечебные рекомендации являются предметом спора, особенно в том, что касается рака молочной железы на ранних стадиях (с негативными лимфатическими узлами). Существует четыре гипотезы, на которых основываются рекомендации Сент-Галленской конференции.
2.1. Первая гипотеза: адъювантная терапия улучшает показатели выживания без признаков заболевания и общего выживания у больных раком молочной железы с негативными лимфатическими узлами
Исследования по адъювантной терапии, которые позволили прийти к этому заключению, а также соответствующий мета-анализ, были предназначены для того, чтобы на основании показателей выживания без признаков заболевания и общего выживания ответить на вопрос: проводить или не проводить адъювантную терапию. Высокая статистическая достоверность гарантировалась за счет огромного числа больных. Фактически, согласно результатам этих испытаний, адъювантная терапия, проводимая больным раком молочной железы на ранних стадиях (с негативными лимфатическими узлами) улучшает такие показатели, как выживание без признаков заболевания и общее выживание [1, 2].
Возражение: Результаты по больным высокого риска с ранними стадиями рака молочной железы (негативные лимфатические узлы) не должны распространяться на больных группы низкого риска.
В свете результатов мета-анализа, указывающих на значительную пользу от адъювантной терапии, исходный уровень риска для больных без лечения (выживание без признаков заболевания у больных до 50 лет составляет 58%, а после 50 лет - 59,9%) кажется довольно неблагоприятным. Можно ожидать, что адъювантная терапия окажется полезной и при более высоком риске. Однако, эти наблюдения предполагают наличие селективных эффектов:
- Больные раком молочной железы с негативными лимфатическими узлами, наблюдавшиеся в период с 1970 по 1990 гг., по своим характеристикам возможно будут отличаться от тех, которым диагноз ставится в настоящее время или будет поставлен в следующие десятилетия. Для этого имеются следующие причины:
- Все возрастающий охват программ скрининга увеличивает процент раннего выявления заболевания при небольших размерах опухоли и низком риске рецидивирования.
- Благодаря увеличению продолжительности жизни, также увеличится процент больных после менопаузы. Эффективность адъювантной терапии у таких больных вероятно будет более низкой.
- Критерии включения больных во многие исследования, на которых базируется мета-анализ, были сформулированы таким образом, чтобы набрать в испытание только больных с неблагоприятным прогнозом (отрицательный статус по рецепторам, более крупные опухоли). Так как эффект от лечения выше при рецептор-негативных формах, чем рецептор-позитивных, можно было ожидать, что лечение принесет определенную пользу.
2.2. Вторая гипотеза: каждый отдельный больной получает пользу от адъювантной терапии.
Учитывая результаты исследований, был сделан вывод, что исходя из среднестатистического снижения риска рецидивирования у всей группы больных можно говорить об индивидуальном снижении риска для каждого больного в отдельности, допуская при этом, что рак молочной железы на ранних стадиях (без вовлечения лимфатических узлов) является единообразным заболеванием.
Возражение: Семьдесят процентов больных раком молочной железы и негативными лимфатическими узлами излечивается исключительно хирургическими методами и поэтому не нуждается в адъювантной терапии.
Рак молочной железы – гетерогенное заболевание. На ранних стадиях заболевания с негативными лимфатическими узлами более 70% больных излечивается при использовании одной местной терапии и никогда не дадут рецидива. В идеале только 30% с негативными лимфатическими узлами должны получать адъювантную терапию. Поэтому не представляется разумным следовать унифицированным рекомендациям, скорее необходимо дифференцировать между больными с локализованным заболеванием и между больными со скрытым распространенным (системным) заболеванием при первичном выявлении. Это соображение было признано общим правилом на Сент-Галленской конференции: больным с очень маленькими, высокодифференцированными опухолями (G1) и положительным статусом по рецепторам стероидных гормонов, адъювантную химиотерапию можно не проводить. Однако, эти больные составляют лишь 10% от всех больных раком молочной железы с негативными лимфатическими узлами. Таким образом, на Сент-Галленской конференции не была достигнута цель определения адъювантной терапии, адаптированной для каждой степени риска. Поэтому необходимо улучшить методы выявления больных с очень низким риском рецидивирования, не нуждающихся в адъювантной терапии
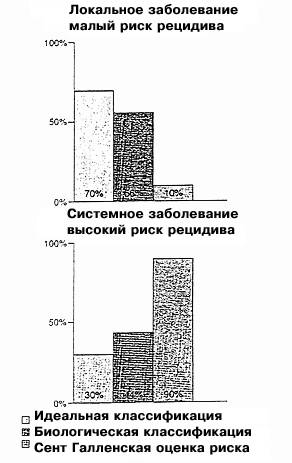 |
Рис. 1
Сравнение классификаций риска: левые столбики показывают реальную ситуацию (более 70% больных раком молочной железы с негативными лимфоузлами излечиваются только хирургическим путем, только у 30% будет рецидив), правые столбики: Сент-Галленская классификация (только 10% или менее больных с негативными лимфоузлами относятся к группе излечимых). Средний столбик показывает классификацию риска на основании новых прогностических факторов uPA и PAI-1: высокий процент (56%) больных оказывается в группе с очень низким риском рецидивирования (“излечимые”); больным этой группы назначать адъювантную терапию не следует. |
2.3. Третья гипотеза: традиционные прогностические факторы (размер опухоли, степень ее злокачественности и чувствительность к стероидным гормонам) дают достаточную информацию для прогнозирования
Комиссия в Сент-Галлене пыталась оценить риск рецидивирования рака молочной железы с негативными лимфатическими узлами, используя для этого традиционные прогностические факторы, такие как размер опухоли, степень ее злокачественности и чувствительность к стероидам. Были сформированы следующие группы риска – группа минимального риска, группа среднего риска, группа высокого риска при положительном статусе по гормональным рецепторам и группа высокого риска при отрицательном статусе. Для каждой из этих групп были разработаны рекомендации по адъювантному лечению, в большинстве случаев рекомендована химиотерапия плюс тамоксифен.
Возражение: Такие традиционные факторы, как размер опухоли, степень злокачественности и чувствительность к стероидным гормонам, не позволяют адекватно оценить риск при раке молочной железы на ранних стадиях заболевания (негативные лимфатические узлы). Чтобы дифференцировать больных с высоким и низким риском рецидивирования необходимы более эффективные прогностические факторы. Традиционные прогностические факторы (размер опухоли, гистологическая характеристика и статус по рецепторам к стероидным гормонам) являются неотъемлемой частью Сент-Галленской классификации степени риска, хотя ни один из этих показателей в отдельности не имеет большой прогностической значимости [5-7].
Размер опухоли коррелирует с вовлеченностью лимфоузлов и, следовательно, является прогностически значимым. Но, как это было показано в ходе ряда исследований по раку молочной железы с негативными лимфатическими узлами, прогностическое значение размера опухоли не доказано. Это можно объяснить тем, что большие опухоли, но без поражения подмышечных лимфатических узлов, могут иметь локальный рост и, следовательно, лучший прогноз [5].
Что же касается гистологической классификации, то ее прогностическая значимость для клинической практики не поддается однозначной оценке. Во-первых, учитывая значительную вариабельность наблюдений, трудно получить четкий результат. Во-вторых, большинство опухолей классифицируются как промежуточные формы (G2), и только 10% из них определены как хорошо дифференцированные (G1), с отличным прогнозом. Следовательно, безапелляционное использование данного вида классификации для оценки риска при раке молочной железы с негативными лимфоузлами также недопустимо [6].
Что же касается чувствительности опухоли к стероидным гормонам, то прогностическая значимость этого фактора была продемонстрирована многими авторами. Однако критический анализ этих данных показывает, что они были получены в ходе испытаний с коротким сроком наблюдения. После более длительных сроков наблюдения прогностическое значение чувствительности к стероидным гормонам становится менее заметным, так что больные с положительным статусом будут иметь почти такой же прогноз, как и рецептор-негативные.
Более того, даже эти традиционные прогностические факторы требуют стандартизованной оценки, гарантии качества и контроля качества для получения надежных гистопатологических и биохимических данных. На сегодняшний день программы обеспечения качества этих параметров выполнены только частично.
2.4. Четвертая гипотеза: Чем выше риск, тем агрессивнее терапия
Другая проблема, над которой работала Сент-Галленская группа, заключается в выборе типа адъювантного лечения; предполагается, что эффективность лечения зависит от степени риска рецидива. Согласно выработанным рекомендациям, больные с низким риском рецидива не нуждаются в терапии или в приеме только тамоксифена; больные со средней или высокой степенью риска нуждаются в более интенсивной адъювантной терапии (химиотерапия + тамоксифен).
Возражение: Риск рецидивирования не является прогностическим фактором в отношении чувствительности к терапии.
Эффективность лечения зависит от биологии каждой отдельной опухоли. Для назначения подходящей адъювантной терапии при индивидуализированном лечении необходимы прогностические факторы, основанные на биологии опухоли. Значение этого положения было продемонстрировано в ходе следующего наблюдения: адъювантная терапия тамоксифеном при раке молочной железы оказывается полезной только для больных с опухолями негативными по с-erb B-2. У больных с гиперэкспрессией с-erb B-2 тамоксифен оказывал даже неблагоприятное действие [10]. По всей видимости, эффективность адъювантной химиотерапии также зависит от статуса по с-erb B-2: у больных с с-erb B-2-негативными опухолями не наблюдается более высокий уровень выживаемости, когда они получают антрациклины вместо CMF, тогда как у больных с с-erbB-2-позитивными опухолями антрациклины могут оказаться более эффективными, чем CMF [11]. Таким образом, резистентность к лечению возможно определяется биологией опухоли, и это необходимо учитывать при выборе адъювантной терапии.
2.5. Вывод Сент-Галленской конференции 1998 г. по адъювантной терапии при раке молочной железы
Изложенные гипотезы привели к созданию хорошо известных рекомендаций и единому выводу о том, что почти все больные нуждаются в комбинированном лечении (химиотерапия плюс тамоксифен). Однако не было определено, в каких случаях назначать CMF, а в каких более предпочтительной является химиотерапия на основе антрациклина. Видимо, эти рекомендациии были даны на основании минимального консенсуса. Главный вопрос так и остается неразрешенным: а нужны ли нам улучшенные прогностические факторы при раке молочной железы без поражения лимфатических узлов (т.е. на ранних стадиях болезни).
3. Да, нам действительно нужны более совершенные прогностические факторы!
Мы знаем, что существуют больные с большими опухолями, у которых никогда не будет метастазов. У таких больных болезнь не повлияет на продолжительность их жизни. Напротив, у некоторых больных опухоли имеют очень маленькие размеры, иногда настолько маленькие, что они даже не обнаруживаются при первичном осмотре, но у них развиваются метастазы и они быстро погибают. Следовательно, как показывает клинический опыт, рак молочной железы представляет собой очень разнородное заболевание. Локализованную форму следует дифференцировать от незаметной системной формы заболевания.
Это ставит нас перед вопросом, может ли существовать единая форма лечения для столь разнородного заболевания. Тенденция к такой стратегии все больше и больше входит в практику [12]. Это началось в 1988 г., когда согласительная комиссия Национального института рака рекомендовала адъювантную терапию для рака молочной железы без поражения лимфоузлов, констатировав, что больные с уровнем смертности 30% (после 10-летнего наблюдения) должны получать адъювантную терапию. В 1995 г. на Сент-Галленской конференции это правило было распространено на группу больных, в которой смертность в течение 10 лет составляла более 10%. На согласительной конференции 1998 г. большинством специалистов была признана целесообразность распространить лечение даже на пациентов с низким риском (рецидив опухоли в течение 10 лет у 10%).
Было отмечено, что адъювантная терапия оказывается полезной только для 8% больных раком молочной железы с негативными лимфатическими узлами. У таких больных частота рецидивирования составляет 30%. Большинство больных (70%) излечивается исключительно хирургическим путем, и поэтому назначенная им химиотерапия не является необходимой. Из-за резистентности к химиотерапии у 22% всех больных с негативными лимфоузлами такая химиотерапия будет напрасной. Действительно, стоит ли напрасно подвергать химиотерапии 92 больных, чтобы улучшить прогноз всего лишь у восьми?
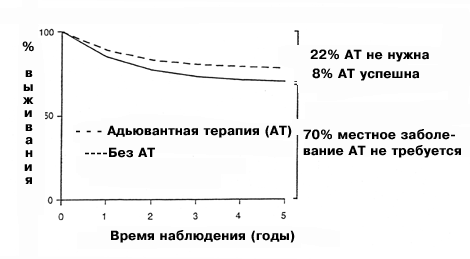 |
Рис. 2 Эффективность адъювантной терапии у больных раком молочной железы с негативными лимфоузлами. Из-за высокого процента больных с локализованным заболеванием (70%) и резистентности к химиотерапии (22%), адъювантная химиотерапия принесет пользу только 8% всех больных. |
Вышеописанная тенденция приведет к значительному перелечиванию, так как благодаря большей осведомленности женщин в том, что касается здоровья и скрининговых программ, сегодня удается диагностировать опухоли все более малого размера и, соответственно, возрастает процент выявления опухолей без поражения подмышечных лимфоузлов. Сегодня у 50-60% больных заболевание не затрагивает лимфоузлы, а в ближайшем будущем количество таких больных увеличится до 70-80%. Следовательно, в будущем для специалистов, занимающихся лечением рака молочной железы, риск перелечивания станет одной из главных проблем.
Итак, главный вопрос заключается в следующем: какие больные ничего не выигрывают от адъювантной терапии? При ведении каких больных следует избегать адъювантной терапии?
Для решения этих вопросов мы должны располагать не просто прогностическими факторами, но более совершенными прогностическими факторами.
4. Разработка прогностических факторов
Описано по крайней мере сто факторов, имеющих прогностическое значение при раке молочной железы с негативными лимфатическими узлами. Однако данные по большинству из этих факторов носят противоречивый характер. Часто они коррелируют с классическими прогностическими факторами при монопараметрическом анализе, но большинство из них не дает независимого прогностического вклада при мультипараметрическом анализе.
За последние 20 лет поиск клинически значимых прогностических факторов проводился в области биологии опухолей. Основные практические рекомендации на основании полученных в этих исследованиях результатов были разработаны МакГауйром и Кларком и модифицированы Енике и Грефом [13-15]. Для введения какого-то прогностического фактора в клиническую практику необходимы следующие условия:
- наличие биологической модели, подтверждающей возможную роль фактора
- простой и верифицированный метод определения фактора
- статистическое планирование анализов
- проведение проспективного исследования
- проведение моновариатного и мультивариатного анализа
- подтверждение на второй группе больных
- проспективное испытание для предварительной оценки прогностической значимости
(Рис. 1).
Чтобы подтвердить значимость этих новых факторов в оценке степени риска, было начато второе проспективное многоцентровое испытание [19].
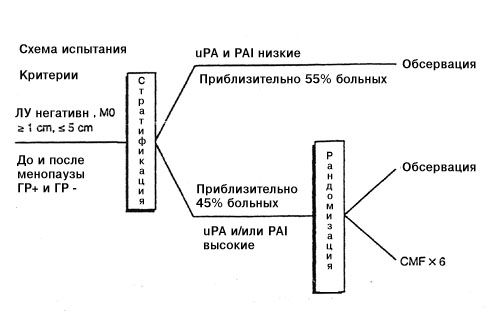 |
Рис. 3
Схема немецкого многоцентрового испытания по адаптированной к риску на основании биологических критериев опухоли (uPA, PAI-1) адьювантной химиотерапии у больных РМЖ с негативными ЛУ. CMF: циклофосфамид, метотрексат, 5-фтороурацил. |
Для этого исследования было отобрано более 650 больных раком молочной железы без поражения лимфоузлов. Данные первого промежуточного анализа будут опубликованы в ближайшем будущем. Кроме того, в этом многоцентровом исследовании была продемонстрирована возможность качественного определения уровня uPA и РАI-1 (GLP, надлежащая лабораторная практика), в исследовании была использована специальная программа контроля качества [20].
5. Заключение
5.1. Прогностические факторы
Существующие на сегодняшний день способы оценки степени риска у больных, страдающих раком молочной железы без поражения лифоузлов, неэффективны и недостаточны. Нужно проводить более тщательный отбор больных на химиотерапию, чтобы не проводить ее понапрасну тем, кто может быть излечен за счет только местного лечения (70% всех больных с негативными лимфатическими узлами). Так как рак молочной железы является гетерогенным заболеванием, общие лечебные рекомендации здесь неприемлемы. Во избежание риска перелечивания, правильнее оценивать риск рецидива для каждой опухоли (Таблица 1).
Следовательно, ответить на вопрос, поставленный в названии этой статьи, можно следующим образом: да, нам нужны более совершенные прогностические факторы при раке молочной железы с негативными лимфатическими узлами.
Таблица 1. Адъювантная терапия у больных раком молочной железы с негативными лимфатическими узлами: Подход, выработанный согласительной комиссией (Сент-Галлен, 1998) по сравнению с подходом, ориентированным на риск
| Адъювантная терапия согласно рекомендациям комиссии | Адъювантная терапия по оценке риска рецидива |
| У всех больных имеется риск рецидива | Следует различать больных с высоким и низким риском рецидива (пятилетняя выживаемость без признаков заболевания менее 10%) |
| Адъювантная терапия полезна для всех | Большинство (70%) больных с негативными лимфати-ческими узлами излечи-ваются только местным лечением |
| Тип терапии согласно риску рецидива (при низком риске тамоксифен; при высоком риске химиотерапия) | Требуется прогноз ответа каждой опухоли на лечение |
| Адъювантную терапию рекомендуется проводить всем больным | Большинству (70%) больных раком молочной железы с негативными лимфати-ческими узлами проводить адъювантную химиотерапию нецелесообразно |
5.2. Предсказательные факторы
Кроме того, для больных, имеющих реальный риск рецидива, необходимо оценивать предсказательные факторы. Тип и агрессивность адъювантной терапии могут быть выбраны на основе биологических данных о чувствительности или резистентности (Рис. 4).
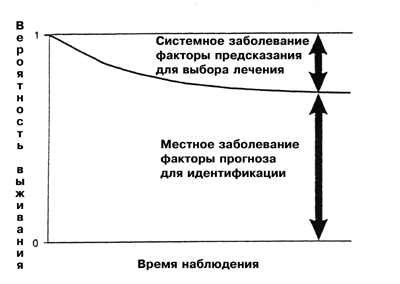 |
Рис. 4 Прогностические факторы необходимы для идентификации больных с локализованным заболеванием (и поэтому с очень низким риском рецидивирования), которым не требуется адъювантная химиотерапия. Предсказательные факторы требуются для идентификации больных с высоким риском рецидивирования, чтобы повысить эффективность лечения за счет выбора оптимальной схемы лечения. |
Таким образом, будущее исследование спланировано таким образом, чтобы ответить на вопрос, можно ли по уровню c-erbB-2 предсказать более высокую эффективность лечения антрациклином по сравнению с CMF у больных раком молочной железы без поражения лимфоузлов, отобранных на основании высоких показателей uPA и/или РАI-1. Это проспективное рандомизированное испытание будет выполнено в рамках программы BIOMED-2.
Литература
1. Early Breast Cancer Trialists' Collaborative Group (EBCTCG). Tamoxifen for early breast cancer, an overview of the randomised trials- Lancet 1998, 351, 1451-1467.
2. Early Breast Cancer Trialists' Collaborative Group (EBCTCG). Polychemotherapy for early breast cancer: an overview of the randomised trials. Lancet 1998, 352, 930-942.
3. Adjuvant Therapy of Primary Breast Cancer. 6th International Conference. Olma Messed St Gallen. 25-28 February 1998. Eur J Cancer 1998, 34 (Suppl. 1) S3-45 (abstract).
4. Zujewski J, Liu ET. The 1998 St. Gallen's Consensus Conference: an assessment. J Natl Cancer Inst 1998, 90,1587-1589.
5. Clark GM. Prognostic and predictive factors. In Harris JR. Lippmann ME, Morrow M, Hellmann S, eds. Diseases of the Breast. Philadelphia, New York, Lippincott-Raven Publishers, 1996,463.
6. Younes M, Laucirica R, Lack of prognostic significance of histological grade in node-negative invasive breast carcinoma, Clin Cancer Res 1997, 3, 601-604.
7. Clark GM. Prognostic and predictive factors. In Harris JR, Lippmann ME, Morrow M, Hellmann S, eds. Diseases of the Breast- Philadelphia, New York, Lippincott-Raven Publishers, 1996 p. 470.
8. Gray RJ. Flexible methods for analyzing survival data using splines, with applications to breast cancer prognosis. J Am Stat Assoc 1992, 87,942-951.
9. Schmitt M, Thomssen C, Ulm K, et al. Time-varying prognostic impact of tumor biological factors urokinase (uPA), PAl-l, and steroid hormone receptor status in primary breast cancer Br J Cancer 1997,76,306-311.
10. Carlomagno C, Perrone F, Gallo C, et a!. c-crb-B2 over-expression decreases the benefit of adjuvant tamoxifen in early-stage breast cancer without axillary lymph node metastases. J Clin Oncol 1996, 14,2702-2708.
11. Paik S, Bryant J, Park C, et a!. erbB-2 and response to doxorubicin in patients with axillary lymph node-positive, hormone receptor-negative breast cancer. J Natl Cancer Inst 1998, 90(1S), 1361-1370.
12. Hebert-Croteau N, Brisson J, Latreille J, et al. Time trends in systemic adjuvant treatment for node-negative breast cancer. J Clin Oncol 1999,17, 1453-1464.
13. McGuire WL. Breast cancer prognostic factors: evaluation guidelines. J Natl Cancer Inst 1991, 83, 154-155.
14. Clark GM. Integrating prognostic factors. Breast Cancer Res Treat 1992,22, 187-219.
15. Graeff H, Janicke F, Schmitt M. Klinische und prognostische Bedeutung tumorassoziierter Proteasen in der gynakologischen Onkologie. Geburtsh Frawnheilk 1991, 51, 90-99.
16. Janicke F, Schmitt M, Pache L. Urokinase (uPA) and its inhibitor PAI-1 are strong and independent prognostic factors in node-negative breast cancer. Breast Cancer Res Treat 1993, 24, 195-208.
17. Schmitt M, Thomssen C, Janicke F, et al. Clinical significance of the serine protease uPA (urokinase) and its inhibitor PAI-1 as well as the cysteine proteases cathepsin B and L in breast cancer. In Calvo F, Crepin M, Magdelenat H, eds. Breast cancer. Advances in biology and therapeutics. Montrouge, John Libbey Eurotext. 1996, 191-200.
18. Harbeck N, Dettmar P, Thomssen C, et at. Risk-group discrimination in node-negative breast cancer using invasion and proliferation markers: 6-year median follow-up. Br J Cancer 1999,80,419-426.
19. Janicke F, Tbomssen CH, Pache L, ei al. Urokinase (uPA) and PAI-1 as selection criteria for adjuvant chemotherapy in axillary node-negative breast cancer patients. In Schmitt M, Graeff H, Kindermann G, eds. Prospects in diagnosis and treatment of breast cancer: proceedings of the joint international symposium on prospects in diagnosis and treatment of breast cancer, 10-11 November 1993. Munich. Amsterdam, Elsevier Science BV. 1994. 207-218.
20. Sweep CG, Geurts-Moespot J, Grebenschikov N, et al. External quality assessment of trans-European multicentre antigen determinations (enzyme-linked immunosorbent assay) of urokinase-type plasminogen activator (uPA) and its type I inhibitor (PAI-1) in human breast cancer tissue extracts. Br J Cancer 1998, 78, 1434-1441.
