Эффективность рамиприла и витамина ? при атеросклерозе.
Статьи Опубликовано в: "Circulation" 2001г.;№103; С.919-925.Исследование SECURE.
Effects of Ramipril and Vitamin E on Atherosclerosis
The Study to Evaluate Carotid Ultrasound Changes in Patients Treated With
Ramipril and Vitamin E (SECURE)
Lonn E.M., Yusuf S., Dzavik V., Doris C.I., Yi Q., Smith S.,
Moore-Cox A., Bosch J., Riley W.A., Teo K.K. от исследователей SECURE
Введение. Активация ренин-ангиотензин-альдостероновой системы и окислительная модификация липопротеидов низкой плотности (ЛПНП) играют важную роль в развитии атеросклероза. В проспективном двойном слепом исследовании SECURE с факториальным дизайном 3х2 (проводилось в рамках HOPE) изучались эффекты длительной терапии ингибитором ангиотензинпревращающего фермента рамиприлом и витамином Ε на прогрессирование атеросклероза у больных высокого риска.
Методы и результаты. Были рандомизированы 732 больных в возрасте ≥55 лет, у которых имелись сосудистые заболевания или сахарный диабет в сочетании с еще по крайней мере одним фактором риска, но отсутствовали сердечная недостаточность или низкая фракция выброса левого желудочка. Им назначали рамиприл в дозах 2,5 или 10 мг/сут или витамин Ε (RRR-α-токоферола ацетат) или соответствующее плацебо. Средняя длительность наблюдения составила 4,5 года. Прогрессирование атеросклероза оценивали с помощью ультразвукового исследования сонной артерии. Средняя скорость увеличения максимальной толщины интимы-медии сонной артерии составила 0,0217 мм в год в группе плацебо, 0,0180 мм в год в группе рамиприла 2,5 мг/сут и 0,0137 мм в год в группе рамиприла 10 мг/сут (р=0,033). Скорость прогрессирования атеросклероза при применении витамина Ε не отличалась от таковой при приеме плацебо.
Заключение. Длительная терапия рамиприлом оказывает благоприятное влияние на прогрессирование атеросклероза, в то время как витамин Ε не оказывает на него действие.
Circulation 2001;103:919-925.
Экспериментальные и эпидемиологические данные свидетельствуют о том, что активация ренин-ангиотензин-альдос-тероновой системы и окислительная модификация холестерина липопротеидов низкой плотности (ЛПНП) играют важную роль в ате-рогенезе, а длительная терапия ингибитором АПФ или антиоксидантом витамином Ε может оказаться полезной [1,2]. Влияние этих препаратов на развитие атеросклероза у человека изучалось в ограниченном числе рандомизированных исследований. В связи с этим мы провели проспективное рандомизированное клиническое исследование с целью оценки эффектов рамиприла и витамина на развитие атеросклероза. Исследование SECURE проводилось в рамках исследования HOPE, в котором изучалась эффективность этих препаратов в профилактике сердечно-сосудистых осложнений у 9541 больного [3,4].
Методы
Дизайн и характеристики исследования были подробно описаны ранее [5]. Приводится краткое резюме.
Больные
В исследование HOPE и его субисследование SECURE включали пациентов с высоким риском развития сердечно-сосудистых осложнений [3-5]. Набор больных проходил с декабря 1993 г по август 1995 г в 6 канадских центрах. Два из них имели опыт в области двухмерной эхографии сонной артерии. В исследования включали больных в возрасте ≥55 лет, у которых имелись сосудистые заболевания или сахарный диабет в сочетании с еще по крайней мере одним сердечно-сосудистым фактором риска и были зарегистрированы адекватные изображения при исходной эхографии сонных артерий. Критерием адекватности служила возможность точного измерения толщины интимы-медии сонной артерии минимум в 4 заранее выбранных участках. Критериями исключения были сердечная недостаточность, снижение фракции выброса левого желудочка менее 40%, инфаркт миокарда, нестабильная стенокардия или инсульт в течение предыдущего месяца, терапия ингибитором АПФ или витамином Е, неконтролируемая гипертония (>160/100 мм рт. ст.), явная нефропатия или серьезные заболевания, которые могли помешать участию в исследовании. Все пациенты дали письменное информированное согласие, а протокол исследования был утвержден этическими комитетами всех центров.
Дизайн исследования, рандомизация, терапия и наблюдение
SECURE было рандомизированным двойным слепым параллельным исследованием с факториальным дизайном 3х2. При вводном визите оценивали критерии отбора и проводили исходную эхографию (рис.). Пациентов, отвечавших критериям отбора, включали в вводную фазу, во время которой они принимали ра-миприл в дозе 2,5 мг/сут (простым слепым методом) в течение 7-10 дней. Затем измеряли сывороточные уровни креатинина и калия и назначали плацебо рамиприла на 10-14 дней. Из 818 больных, включенных в вводную фазу, 86 были исключены из исследования в течение 3 недель, а оставшиеся 732 пациента были рандо-мизированы. Им назначали рамиприл в дозах 10 или 2,5 мг/сут, витамин Ε (RRR-α-токоферо-ла ацетат) или плацебо рамиприла и витамина Ε и проводили второе исходное ультразвуковое исследование. В группе рамиприла 10 мг/сут проводили форсированное титрование дозы до целевой или максимальной переносимой в течение 1 мес.
Пациентов обследовали через 1 месяц после рандомизации, а затем каждые 6 месяцев. Все визиты и ультразвуковые исследования были завершены к 1 июля 1999 г. Систолическое и ди-астолическое АД измерялось опытными медицинскими сестрами во время рандомизации, через 1 месяц, 2 года и в конце исследования с помощью стандартного сфигмоманометра по стандартному протоколу (измерение проводили в утренние часы, в то время как препарат пациенты принимали вечером, использовали манжету адекватного размера, пациенты находились в положении лежа ≥5 минут, после чего АД регистрировали дважды на каждой руке; определяли среднее значение минимальных показателей на правой и левой руке).
Секторальная эхография
Исходно и в конце исследования (через 4-5 лет после рандомизации; медиана 4,5 года) дважды проводили эхографию сонных артерий (с интервалом максимум 3 недели), а через 1,5-2,2 года после рандомизации выполняли однократное ультразвуковое исследование. Методика исследования подробно описана ранее [5]. Высокочастотную эхографию проводили 3 опытных и сертифицированных специалиста. Использовали стандартизованный протокол исследования и интерпретации изображений [6,7]. В продольной проекции регистрировали максимальную толщину интимы-медии (ТИМ) в каждом из 12 сегментов сонной артерии длиной 1 см (внутренняя сонная артерия, бифуркация, общая сонная артерия). Анализ изображений проводился двумя сертифицированными специалистами слепым методом. Для каждого больного рассчитывали среднюю максимальную ТИМ на основании значений в 12 сегментах. Разница средней максимальной ТИМ между 732 парными исходными измерениями составила 0,014±0,17 мм, средняя абсолютная разница - 0,12±0,11 мм, коэффициент корреляции Пирсона — 0,87. В конце исследования средняя разница средней максимальной ТИМ между 641 парным измерением составила 0,004±0,09 мм, средняя абсолютная разница -0,06±0,06 мм, коэффициент корреляции - 0,97. При детальном анализе меж- и интраиндивиду-альной вариабельности была продемонстрирована высокая воспроизводимость результатов и отсутствие ее изменений со временем.
Конечные точки
Первичной конечной точкой исследования была ежегодная скорость увеличения средней максимальной ТИМ. Вторичной конечной точкой служила ежегодная скорость увеличения максимальной ТИМ в отдельных сегментах сонной артерии. В рамках исследования HOPE регистрировали и анализировали также клинические исходы. Это исследование обладало достаточной силой для изучения влияния двух препаратов на риск сердечно-сосудистых осложнений.
Статистический анализ
Анализ проводили в выборке больных, начавших лечение, с помощью программы SAS 6.12. При анализе первичной и вторичной конечной точки не было выявлено взаимодействия между двумя препаратами (р=0,90 ир=0,61 соответственно; метод ANOVA). В связи с этим оценивали разницу между рамиприлом в целом и в разных дозах и плацебо, а также между витамином Ε и соответствующим плацебо. Исходные характеристики сравнивали с помощью метода ANOVA и критерия хи-квадрат. Скорость увеличения средней максимальной ТИМ и максимальной ТИМ в отдельном сегменте для каждого больного рассчитывали на основании результатов серии исследований с помощью метода регрессии (после подтверждения отсутствия значимого отклонения от линейности). Общий эффект рамиприла, эффекты каждой дозы ра-миприла (2,5 и 10 мг) и витамина Ε анализировали с помощью метода ANOVA. Скорость увеличения средней максимальной ТИМ служила зависимой переменной, а проводимая терапия — независимой. С помощью метода ANCOVA проводили анализ с поправкой на изменения систолического и диастолического АД и поправкой на множественные факторы, которые оказывали влияние на скорость увеличения ТИМ по данным однофакторного анализа. С целью поправки на использование одного контроля для сравнения двух доз рамиприла использовали метод Даннета [8]. В первичный анализ включали всех больных, у которых можно было оценить динамику ТИМ, т.е. при наличии двух исходных ультразвуковых исследований и по крайней мере одного исследования в динамике.
Результаты
Исходные характеристики, наблюдение и приверженность
Исходные характеристики не отличались между группами сравнения, за исключением частоты курения, которая была выше в группе больных, получавших витамин Ε (табл. 1). Исходные характеристики 693 больных, которые были включены в первичный анализ в конце исследования, были сходными.
ТАБЛИЦА 1. Исходные характеристики (М±о)
| Рамиприл | Витамин E | ||||
|---|---|---|---|---|---|
| Показатель | плацебо (n=244) | 2,5 м г/сут (n=244) | 10 м г/сут (n=244) | плацебо (n=364) | витамин Ε (n=368) |
| Возраст, лет | 65.6±6.8 | 65.6±6.865 | 65.2±6.2 | 65.7±6.6 | 65.0±6.4 |
| Женщины, % | 21 | 27 | 24 | 24 | 23 |
| АД, мм рт. ст. | 132±17/75±9 | 132±17/76±10 | 132±15/76±9 | 132±17/76±9 | 132±17/76±9 |
| Частота сердечных сокращений в минуту | 66±11 | 66±11 | 66±11 | 66±11 | 66±11 |
| Индекс массы тела, кг/м2 | 28±4 | 28±4 | 28±4 | 28±5 | 28±5 |
| Анамнез, % | |||||
| Коронарная болезнь сердца | 85 | 87 | 81 | 85 | 84 |
| Инфаркт миокарда | 55 | 58 | 57 | 58 | 55 |
| Стабильная стенокардия | 64 | 65 | 54 | 62 | 60 |
| Нестабильная стенокардия | 34 | 34 | 30 | 34 | 32 |
| Инсульт или транзиторная ишемическая атака | 10 | 7 | 12 | 10 | 10 |
| Периферический атеросклероз | 42 | 39 | 38 | 37 | 41 |
| Гипертония | 34 | 35 | 40 | 35 | 37 |
| Диабет | 35 | 32 | 35 | 32 | 36 |
| Курение | |||||
| в настоящее время | 9 | 10 | 10 | 9 | 11 |
| в настоящее время или в прошлом | 74 | 75 | 76 | 70 | 80* |
| Повышение общего холестерина | 48 | 46 | 47 | 46 | 48 |
| Снижение холестерина ЛПВП | 18 | 16 | 19 | 18 | 17 |
| Сопутствующая терапия, % | |||||
| Бета-блокаторы | 43 | 40 | 44 | 43 | 42 |
| Аспирин/другие антиагреганты | 86 | 85 | 82 | 85 | 83 |
| Гиполипидемические средства | 35 | 39 | 29 | 37 | 32 |
| Диуретики | 8 | 11 | 9 | 10 | 8 |
| Антагонисты кальция | 44 | 43 | 40 | 40 | 45 |
| Витамин С | 8 | 10 | 11 | 9 | 11 |
| Бета-каротин | 1 | 1 | 2 | 1 | 2 |
| Поливитамины | 11 | 12 | 6 | 10 | 9 |
| Гормональная заместительная терапия у женщин | 2 | 3 | 3 | 3 | 3 |
| Лабораторные показатели, ммоль/л | |||||
| Общий холестерин | 5.3±1.2 | 5.3±1.0 | 5.3±1.0 | 5.3±1.0 | 5.3±1.25.3±1 |
| Триглицериды | 2.2±1.3 | 2.2±1.3 | 2.2±1.3 | 2.2±1.4 | 2.2±1.32 |
| Холестерин ЛПВП | 1.0±0.3 | 1.0±0.3 | 0.9±0.3 | 0.9±0.3 | 1.0±0.3 |
| Холестерин ЛПНП | 3.5±1.1 | 3.5±1.1 | 3.4±0.8 | 3.4±0.8 | 3.5±1.13.4±0 |
| ТИМ сонной артерии, мм | |||||
| средняя максимальная | 1.1462±0.34 | 1.1477±0.34 | 1.1603±0.32 | 1.1477±0.341.1603 | 1.1564±0.33 |
| максимальная | 2.2653±0.92 | 2.2559±0.84 | 2.2±7860.79 | 2.2883±0.89 | 2.2379±0.81 |
Наблюдение было завершено у всех больных. Через 1,5-2,2 года после рандомизации адекватные эхограммы были зарегистрированы у 690 больных. 17 из 732 больных, включенных в исследование, умерли, 15 пропустили эхографию из-за болезни, а 10 пациентов отказались от исследования или у них не удалось зарегистрировать качественное изображение. У 3 больных эхография не была проведена через 1,5-2,2 года, однако была выполнена в конце исследования. Таким образом, в первичный анализ были включены 693 больных (95% из всех рандомизированных пациентов и 97% из всех рандомизированных пациентов, которые были живы через 1,5-2,2 года после рандомизации). У 637 пациентов были выполнены все 5 запланированных ультразвуковых исследования (87% из всех рандомизированных больных и 95% больных, которые были живы к концу исследования; см. схему).
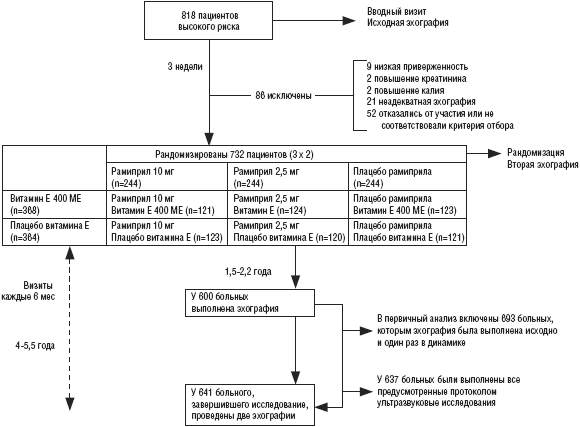
Сведения о приверженности к проводимой терапии приведены в табл. 2. Только кашель был более частой причиной отмены рамиприла по сравнению с плацебо (1,6% в группе плацебо рамиприла, 9,0% в группе рамиприла 2,5 мг и 9,8% в группе рамиприла 10 мг). Витамин Ε не вызывал выраженных побочных реакций.
ТАБЛИЦА 2. Приверженность больных лечению
| Рамиприл* | Витамин E** | ||||
| Год | плацебо | 2,5 мг/сут | 10 мг/сут | плацебо | витамин Ε |
| 1 | 93 | 88 | 85 | 94 | 95 |
| 2 | 85 | 80 | 79 | 91 | 95 |
| 3 | 81 | 76 | 74 | 90 | 90 |
| 4 | 76 | 73 | 69 | 89 | 88 |
| Конец исследования | 72 | 71 | 67 | 86 | 90 |
Изменения АД
Во всех группах АД исходно составляло в среднем 132/76 мм рт. ст. При лечении рами-прилом в обеих дозах было отмечено снижение систолического и диастолического АД по сравнению с плацебо, в то время как динамика АД достоверно не отличалась между группами рамиприла 2,5 и 10 мг/сут (табл. 3). Витамин Ε не оказывал существенного влияния на АД.
ТАБЛИЦА 3. Систолическое и диастолическое АД (мм рт. ст.) до и после лечения рамиприломм (Μ±σ)
|
Исходно |
1 мес |
2 года |
Конец исследования |
Средняя динамика |
|
|
Систолическое |
|||||
|
Плацебо |
131.6±17.1 |
130.4±17.9 |
130.0±15.8 |
134.1±16.9 |
0.1 ± 12.2 |
|
Рамиприл 2,5 мг/сут |
131.7±17.0 |
12±.1 ± 17.0* |
125.2±15.6* |
130.8±16.7** |
-4.6±13.5* |
|
Рамиприл 10 мг/сут |
131.9±15.3 |
127.1±14.8f |
125.9±17.8f |
130.5±16.6** |
-4.1 ± 12.4* |
|
Диастолическое |
|||||
|
Плацебо |
75.4±8.7 |
76.4±9.6 |
74.8±9.8 |
73.4±8.7 |
-0.4±7.3 |
|
Рамиприл 2,5 мг/сут |
76.4±9.3 |
74.4±9.3* |
73.0±9.6f |
72.7±9.0 |
-2.9±7.9* |
|
Рамиприл 10 мг/сут |
76.2±9.2 |
74.8±8.7f |
72.6±9.1* |
72.6±8.9 |
-2.8±7.6* |
Прогрессирование каротидного атеросклероза
По данным однофакторного анализа, на скорость увеличения средней максимальной ТИМ оказывали влияние следующие характеристики: исходная средняя максимальная ТИМ (р=0,0002), высокий уровень холестерина в анамнезе (р=0,0002) или низкий уровень холестерина липопротеидов высокой плотности (ЛПВП) (р=0,0008), концентрации общего холестерина и холестерина ЛПНП (р=0,03 и р=0,01 соответственно) и распределение в группу рамиприла 10 мг/сут (р=0,028). По данным многофакторного анализа, только исходная средняя максимальная ТИМ (р<0,001), дисли-пидемия в анамнезе (р=0,0005) и лечение рами-прилом 10 мг/сут (р=0,046) были независимыми предикторами скорости увеличения средней максимальной ТИМ.
Основные результаты исследования обобщены в табл. 4. Число сегментов сонной артерии, в которых не удалось измерить ТИМ, было низким (в среднем 5%), поэтому первичный анализ проводили без коррекции на отсутствующие данные. Рамиприл в целом снижал ежегодную скорость увеличения средней максимальной ТИМ по сравнению с плацебо (р=0,033). Рамиприл в дозе 10 мг/сут также превосходил плацебо (р=0,028; при коррекции Даннетар=0,027).
ТАБЛИЦА 4. Скорость прогрессирования первичной и вторичной эхографической конечной точки (мм в год) у 693 больных (М±m)*
| Показатель | Рамиприл! | Витамин E | |||
| плацебо (n=227) | 2.5 мг/сут (n=232) | 10 мг/сут (n=234) | плацебо (n=344) | витамин Ε (n=349) | |
| Средняя максимальная ТИМ Максимальная ТИМ | 0.0217±0.0027 0.0277 ±0.0075 | 0.0180±0.0026 0.0280±0.0096 | 0.0180±0.0022 0.00760.0277 | 0.0174±0.0020 0.0141±0.0076 | 0.0180±0.00260.0137±0.002 0.0277±0.0075 |
t Рамиприл вызывал снижение скорости увеличения средней максимальной ТИМ; р=0,033 (p=0.043 после поправки на изменения систолического и диастолического АД и р=0.046 после поправки на множественные факторы [возраст, пол, исходный ИМТ, высокий общий холестерин и низкий холестерин ЛПВП, курение, терапия гиполипидемическими средствами, гипертония, изменения АД и исходные концентрации общего холестерина и холестерина ЛПНП]).
φ p=0.028 рамиприл 10 мг/сут в сравнении с плацебо (р=0.037 после поправки на изменения АД и р=0.046 после поправки на множественные факторы)
Мы проверили надежность наших результатов с помощью дополнительных тестов. При анализе 711 больных, в том числе включенных в первичный анализ, и 18 больных, которые умерли во время исследования или перенесли инфаркт миокарда или инсульт (у этих пациентов не проводили ультразвуковое исследование в период наблюдения; у них предполагали наличие быстрого прогрессирования атеросклероза, критерием которого служил верхний 10-й перцентиль средней максимальной ТИМ для всей выборки SECURE), выявлено снижение скорости прогрессирования атеросклероза при лечении рамиприлом по сравнению с плацебо (р=0,019; р=0,027 при внесении поправки на изменения АД и р=0,027 при внесенные поправки на множественные факторы) и рамиприлом в дозе 10 мг/сут по сравнению с плацебо (р=0, 015, р=0,022 при внесении поправки на изменения АД ир=0,031 при внесении поправки на множественные факторы). Сходная тенденция была отмечена при анализе 637 больных, которым были выполнены все 5 ультразвуковых исследований (р=0,068 для рамиприла во всех дозах в сравнении с плацебо ир=0,055 для рамиприла 10 мг/сут в сравнении с плацебо). Похожие результаты были получены при анализе вторичной конечной точки (скорость увеличения максимальной ТИМ в одном сегменте). Абсолютная разница этой конечной точки между группами рамиприла 10 мг/сут и плацебо превышала разницу скорости увеличения средней максимальной ТИМ, однако она не достигла статистической значимости из-за более высокой вариабельности этого показателя. По данным анализа 637 больных, которым были выполнены все 5 ультразвуковых исследований, рамиприл значительно снижал скорость увеличения максимальной ТИМ в одном сегменте (р=0,003 для рамиприла во всех дозах в сравнении с плацебо и р=0,008 для рамиприла 10 мг по сравнению с плацебо).
Витамин Ε не оказывал влияния на первичную и вторичную конечные точки.
Клинические исходы
Как и ожидалось, в этом относительно небольшом исследовании частота первичной клинической конечной точки (комбинация сердечно-сосудистой смерти, инфаркта миокарда и инсульта) достоверно не отличалась между группами. Ее зарегистрировали у 41 (16,8%) больного группы плацебо, 34 (13,9%) больных группы рамиприла 2,5 мг, 31 (12,7%) больного группы рамиприла 10 мг/сут, 55 (15,1%) больных группы плацебо витамина Ε и 51 (13,9%) больного группы витамина Е. Влияние лечения на клинические конечные точки было продемонстрировано в исследовании HOPE, которое обладало достаточной статистической силой [3,4].
Обсуждение
Исследование SECURE показало, что длительная терапия ингибитором АПФ задерживает прогрессирование атеросклероза, в то время как витамин Ε не оказывает на него действие.
В клинических исследованиях все чаще применяют секторальную эхографию сонных артерий для оценки эффектов различных средств на атеросклероз. Метод характеризуется высокой воспроизводимостью, а его результаты коррелируют с факторами риска и развитием коронарной болезни сердца и инсульта [9]. В предыдущих исследованиях применялись различные оборудование и протоколы сканирования и интерпретации изображений, а также выбирались разные конечные точки. В качестве первичной конечной точки мы измеряли среднюю максимальную ТИМ на основании изучения 12 сегментов сонной артерии, так как этот показатель лучше всего коррелирует с результатами корона-роангиографии у больных коронарным атеросклерозом [10]. Кроме того, он достаточно чувствителен и позволяет выявить изменения, возникающие под влиянием лечения [11]. Мы измеряли максимальную, а не среднюю ТИМ в сегменте, так как такой подход позволяет свести к минимуму пропуски данных, оценить наиболее измененные участки и получить очень стабильные результаты при расчете средних показателей в 12 сегментах артерий [7,11]. Процедура сканирования и интерпретации изображений тщательно валидирована [6,7], а нам удалось добиться высокой воспроизводимости измерений.
Лечение рамиприлом привело к уменьшению скорости прогрессирования атеросклероза. Этот эффект наблюдался у больных высокого риска, большинство из которых уже получали эффективные лекарственные средства, в том числе аспирин (84%), гиполипидемические препараты (34%), бета-блокаторы (43%), диуретики (9%), нитраты (32%) и антагонисты кальция (43%). Хотя абсолютная разница скорости прогрессирования атеросклероза между группами рамиприла и плацебо была небольшой, тем не менее относительное снижение средней максимальной ТИМ при лечении рамиприлом 10 мг/сут составило 37%, что сопоставимо со снижением относительного риска инсульта (на 32%) в исследовании HOPE. Сходные результаты были получены при изучении эффективности ги-похолестеринемических средств, которые оказывали впечатляющее влияние на риск сердечно-сосудистых осложнений, что свидетельствовало о стабилизации атеросклеротического процесса. Наше исследование не обладало статистической силой, необходимой для сравнения двух доз рамиприла. Однако была отмечена тенденция к зависимости эффекта препарата от дозы. Максимальную пользу приносила терапия рамиприлом в дозе 10 мг/сут. В этой же дозе рамиприл применялся в крупном исследовании HOPE, которое подтвердило благоприятный эффект препарата на риск различных сердечно-сосудистых осложнений [3].
Рамиприл оказывал небольшое гипотензивное действие в нашем исследовании, так как у большинства больных отсутствовала артериальная гипертония или она хорошо контролировалась; другие антигипертензивные и антианги-нальные средства применялись более чем у 75% больных. Благоприятный эффект рамиприла на атеросклероз оставался статистически значимым после поправки на наличие артериальной гипертонии и изменения АД. Это свидетельствовало о том, что результаты лечения нельзя полностью объяснить снижением АД, а они могут отражать прямое протективное действие рамиприла на сосуды.
В атеросклеротических поражениях коронарных артерий продемонстрирована повышенная тканевая активность АПФ [12], а длительное применение ингибиторов АПФ вызывало уменьшение площади атеросклеротических изменений аорты, сонных и коронарных артерий у нормо-тензивных животных [13,14]. Эти антиатероген-ные свойства могут быть связаны с ингибирова-нием образования ангиотензина II в тканях и циркуляции и увеличением уровней брадикини-на, вызывающим снижение пролиферации и миграции гладкомышечных клеток, накопления и активации воспалительных клеток, окислительного стреса и повышением образования оксида азота, улучшающего функцию эндотелия [1].
Ранее влияние ингибиторов АПФ на атеросклероз изучались в клинических исследованиях QUIET, SCAT и PART-2 [15-17]. В двух из них (QUIET и SCAT) с помощью коронарной ангиографии не был продемонстрирован благоприятный эффект квинаприла и эналаприла, хотя в исследовании QUIET было отмечено замедление прогрессирования коронарного атеросклероза при лечении квинаприлом в подгруппе больных с повышенным уровнем холестерина ЛПНП. Разница результатов SECURE и этих исследований может быть следствием выбора определенного ингибитора АПФ, дозы препарата, дизайна исследования и методов оценки прогрессирования атеросклероза. Эхография, которая использовалась в SECURE, позволяет изучить состояние стенки артерий и может быть более чувствительным методом, чем коронароан-гиография. В PART-2 рамиприл в дозах 5-10 мг/сут не оказывал влияния на ТИМ, которую измеряли с помощью ультразвукового исследования. Однако в этом исследовании оценивали только толщину общей сонной артерии. В исследовании SECURE рассчитывали средний показатель на основании изучения сегментов общей и внутренней сонной артерии и бифуркации.
Этот показатель может быть более чувствительным к изменениям [11], что позволяет объяснить разницу результатов двух исследований.
Витамин Ε в дозе 400 МЕ/сут не оказывал влияния на прогрессирование атеросклероза. Приверженность к лечению этим препаратом была высокой, другие антиоксидантные витамины использовались редко, а исследование обладало адекватной статистической силой, достаточной для выявления умеренного эффекта лечения (оно позволяло выявить снижение первичной конечной точки на 48% со статистической силой 80% и на 33% со статистической силой 50%). При рассчете размера выборки мы ориентировались на более высокую скорость увеличения ТИМ с учетом имевшихся на тот момент данных. В связи с этим исследование не позволяет полностью исключить небольшой эффект витамина Е.
Мы не измеряли уровни витамина Ε или его влияние на окисление ЛПНП. Однако в предыдущих исследованиях было показано, что применение витамина Е, полученного из естественных источников, в дозе 400 МЕ/сут приводит к значительному повышению содержания а-токо-ферола в плазме и тканях. В сходных или более низких дозах витамин Ε повышает устойчивость ЛПНП к окислению [18,19]. Сходные данные были получены в субисследовании HOPE (R.Hoeschen, 2000). Кроме того, целью нашего исследования было изучение эффектов витамина Е, который принимают миллионы людей в мире без оценки окислительного статуса.
Экспериментальные данные свидетельствуют о важной роли окислительной модификации ЛПНП в атерогенезе, а витамин Ε является эффективным антиоксидантом, который вызывал уменьшение атеросклероза в опытах на животных [2,20], хотя и не постоянно [21]. В эпидемиологическом исследовании было отмечено замедление прогрессирования коронарного атеросклероза у людей, принимающих витамин Ε [22]. Крупные эпидемиологические исследования продемонстрировали кардиопротективные свойства этого витамина. В исследовании Cambridge Heart Antioxidant Study было выявлено снижение числа несмертельных осложнений у больных, получавших витамин Ε после инфаркта миокарда [23], однако наблюдалась тенденция к увеличению смертности. В нескольких более крупных и длительных рандомизированных клинических исследованиях не подтверждена польза применения витамина Ε [4,24]. До настоящего времени влияние витамина Ε на атеросклероз изучалось в небольшом числе рандомизированных исследований. У15 больных с гомозиготной семейной гиперхолестеринемией наблюдалось быстрое увеличение ТИМ сонных артерий при лечении витамином Ε и ее уменьшение при применении статинов [25]. Предварительные результаты Antioxidant Supplementation in Atherosclerosis Prevention (ASAP) свидетельствуют об отсутствии благоприятного влияния на ТИМ сонных артерий витамина Ε по отдельности или в комбинации с витамином С у женщин, хотя отмечен эффект комбинированной терапии у курящих мужчин с гиперхолестеринемией [26].
Результаты исследования SECURE согласуются с результатами HOPE. В целом эти исследования свидетельствуют о том, что рамиприл замедляет прогрессирование атеросклероза и предупреждает развитие сердечно-сосудистых осложнений. Напротив, терапия витамином Ε в течение от 4 до 6 лет не оказывала существенного влияния на развитие атеросклероза или сердечно-сосудистых осложнений. Роль витамина Ε по отдельности или в комбинации с другими анти-оксидантами в различных группах пациентов нуждается в дополнительном изучении.
Литература1. Lonn EM, Yusuf S, Jha P, et al. Emerging role of angiotensin-converting enzyme inhibitors in cardiac and vascular protection. Circulation. 1994; 90:2056 -2069.
2. Steinberg D, Parthasarathy S, Carew TE, et al. Beyond cholesterol: modifications of low-density lipoprotein that increase its atherogenicity. N Engl J Med. 1989;320:915-924.
3. The Heart Outcomes Prevention Evaluation Study Investigators. Effects of an angiotensin-converting enzyme inhibitor, ramipril, on death from cardiovascular causes, myocardial infarction, and stroke in high-risk patients. N Engl J Med. 2000;342:145-153.
4. The Heart Outcomes Prevention Evaluation Study Investigators. Effects of long-term vitamin E supplementation on cardiovascular events in 9541 high-risk persons. N Engl J Med. 2000;342:154-202.
5. Lonn EM, Yusuf S, Doris CI, et al. Study design and baseline characteristics of the Study to Evaluate carotid Ultrasound changes in patients treated with Ramipril and vitamin E (SECURE). Am J Cardiol. 1996;78: 914-919.
6. Riley WA, Barnes RW, Applegate WB, e al. Reproducibility of noninvasive ultrasonic measurement of carotid atherosclerosis: the Asymptomatic Carotid Artery Plaque Study. Stroke. 1992;23:1062-1068.
7. Pitt B, Byington RP, Furberg CD, et al. Effect of amlodipine on the progression of atherosclerosis and the occurrence of clinical events. Circulation. 2000;102:1503-1510.
8. Dunnett CW. A multiple comparisons procedure for comparing several treatments with a control. J Am Stat Assoc. 1955;50:1096-1121.
9. O'Leary DH, Polak JF, Kronmal RA, et al. Carotid-artery inti-ma and media thickness as a risk factor for myocardial infarction and stroke in older adults. N Engl J Med. 1999;340: 14-22.
10. Crouse JR, Craven TE, Hagaman AP, et al. Association of coronary artery disease with segment-specific intimal-medial thickening of the extracranial carotid artery. Circulation. 1995;92:1141-1147.
11. Espeland MA, Craven TE, Riley WA, et al. Reliability of longitudinal ultrasonographic measurements of carotid intimal-medial thickness. Stroke. 1996;27:480-485.
12. Diet F, Pratt RE, Berry GJ, et al. Increased accumulation of tissue ACE in human atherosclerotic coronary artery disease. Circulation. 1996;94: 2756-2767.
13. Chobanian AV, Haudenshild CC, Nickerson C, et al. Antiatherogenic effect of captopril in the Watanabe heritable hyperlipidemic rabbit. Hypertension. 1990;15:327-331.
14. Aberg G, Ferrer P. Effects of captopril on atherosclerosis in cynomolgus monkeys. J Cardiovasc Pharmacol. 1990; 15: S65-S72.
15. Cashin-Hemphill L, Holmvang G, Chan RC, et al. Angiotensinconverting enzyme inhibition as antiatheroscle-rotic therapy: no answer yet: Quinapril Ischemic Event Trial. Am J Cardiol. 1999;83:43- 47.
16. Teo KK, Burton JR, Buller CE, et al. Long term effects of cholesterol lowering and angiotensin-converting enzyme inhibition on coronary atherosclerosis: the Simvastatin/Enalapril Coronary Atherosclerosis Trial (SCAT). Circulation. 2000;102:1748 -1754.
17. MacMahon S, Sharpe N, Gamble G, et al. Randomized, placebocontrolled trial of the angiotensin converting enzyme inhibitor, ramipril, in patients with coronary or occlusive arterial disease. J Am Coll Cardiol. 2000;36:438-443.
18. Burton GW, Traber MG, Acuff RV, et al. Human plasma and tissue α-tocopherol concentrations in response to supplementation with deuterated natural and synthetic vitamin E. Am J Clin Nutr. 1998;67: 669-684.
19. Devaraj S, Adams-Huet B, Fuller CJ, Jialal I. Dose-response comparison of RRR-α-tocopherol and all-racemic a-toco-pherol on LDL oxidation. Arterioscler Thromb Vasc Biol. 1997;17:2273-2279.
20. Verlangieri AJ, Busch MJ. Effects of d-alpha-tocopherol supplementation on experimentally induced primate atherosclerosis. J Am Coll Nutr. 1992; 11:131-138.
21. Godfried SL, Combs GF, Saroka JM, et al. Potentiation of atherosclerotic lesions in rabbits by a high dietary level of vitamin E. Br J Nutr. 1989;61:607- 617.
22. Hodis HN, MackWJ, LaBree L, et al. Serial coronary angiographic evidence that antioxidant vitamin intake reduces progression of coronary atherosclerosis. JAMA. 1995;85: 1483-1492.
23. Stephens NG, Parsons A, Schofield PM, et al. Randomized controlled trial of vitamin E in patients with coronary disease: Cambridge Heart Antioxidant Study (CHAOS). Lancet. 1996;347:781-776.
24. GISSI-Prevenzione trial. Dietary supplementation with n-3 polyunsaturated fatty acids and vitamin E after myocardial infarction: results of the GISSI-Prevenzione trial. Lancet. 1999;354:447- 445.
25. Raal FJ, Pilcher GJ, Veller MG, et al. Efficacy of vitamin E compared with either simvastatin or atorvastatin in preventing the progression of atherosclerosis in homozygous familial hypercholesterolemia. Am J Cardiol. 1999;84:1344 -1346. 26. Salonen JT, NyyssЪnen K, Salonen R, et al. Antioxidant Supplementation in Atherosclerosis Prevention (ASAP) study: a randomized study of the effects of vitamins E and C on 3-year progression of carotid atherosclerosis. J Intern Med. 2000;248:377-386.
Комментарии
ПРАКТИКА ПЕДИАТРА
