Концепция гетерогенности в рациональной терапии ишемического инсульта
СтатьиОпубликовано в журнале:
Русский медицинский журнал Том 13, № 22, 2005
М.В. Путилина, Н.В. Громадская, Н.Е. Лаздан, Н.Ю. Ермошкина
РГМУ
Сосудистые заболевания головного мозга остаются одной из острейших медико-социальных проблем, наносящих огромный экономический ущерб обществу. Особое место среди них занимает церебральный инсульт - в связи с высоким уровнем летальности, значительной инвалидизацией и социальной дезадаптацией пациентов [3,4]. По данным ВОЗ, в прошедшем десятилетии от церебрального инсульта умерло более 5 млн. человек, а из 15 млн. выживших более 80% остались инвалидами. В России каждые 1,5 минуты констатируется инсульт, ежегодно регистрируются около 450 тыс. случаев этого заболевания [4].
Современная концепция инсульта рассматривает его как клинический синдром острого сосудистого поражения мозга [2]. Инсульт является исходом различных по характеру патологических состояний системы кровообращения сосудов, сердца, крови. При этом проявляется его гетерогенность - многообразие этиологических и патогенетических механизмов развития. Это обусловливает выраженный полиморфизм клинической картины. На сегодняшний день в структуре ишемического инсульта выделяют следующие подтипы: атеротромботический, кардиоэмболический, лакунарный, гемодинамический, гемореологической окклюзии. Вероятно, число подтипов будет возрастать по мере накопления информации об этиологии, патогенезе и особенностях клинических проявлений инсульта.
В настоящее время возросла роль гемореологических изменений при развитии цереброваскулярной патологии, что, несомненно, привело к повышению удельного веса гемодинамического подтипа инсульта. Основными причинами гемодинамического инсульта служат изменения магистральных артерий головы или интракраниальных сосудов, а также факторы, вызывающие нестабильность системной гемодинамики с последующей редукцией церебральной перфузии [4,10]. В патогенезе данного подтипа инсульта также имеет значение деформация мелких внутримозговых артерий, характерная для артериальной гипертонии. Тяжесть и обратимость заболевания зависят от состояния церебрального сосудистого резерва и особенностей гемореологии и гемостаза. При недостаточном коллатеральном кровообращении компенсация гемодинамических нарушений осуществляется за счет ауторегуляторных механизмов: миогенного, нейрогенного, нейрогуморального и метаболического [5]. Развитие острой «сосудистой катастрофы» предполагает разбалансировку данной системы. Наличие выраженных гемореологических изменений и нарушений в системе гемостаза и фибринолиза (повышенные показатели гемотокрита, фибриногена, агрегации тромбоцитов) связывают гемодинамический инсульт с атеротромботическим инсультом.
Инсульт - патологическое состояние, требующее комплексного подхода к диагностике и коррекции последствий. Правильно построенный алгоритм позволяет определить основную причину возникновения и механизмы развития острой ишемии мозга и, следовательно, своевременно начать патогенетическую терапию. Вместе с тем некоторые принципы лечения разных подтипов ишемического инсульта могут быть общими, что объясняется существованием универсальных патогенетических процессов в развитии ОНМК.
Большое значение для определения подтипа инсульта имеют инструментальные методы диагностики. С их помощью определяют основную причину ишемии и механизм ее развития. Выбор оптимального метода лечения конкретного больного базируется не только на особенностях патологического процесса, но и на знании преморбидного фона - соматического состояния пациента до развития острого нарушения мозгового кровообращения. Таким образом, современное представление о терапии инсульта должно включать понятие о гетерогенности клинического синдрома ОНМК и времени его развития.
Лечение ОНМК требует комплексного подхода в использовании лекарственных средств. С одной стороны, необходимо медикаментозное воздействие на систему гемостаза, вазодилатацию и метаболические процессы, с другой - возрастает необходимость особого контроля применения фармпрепаратов для избежания риска развития «синдрома обкрадывания» с углублением перфузионного дефицита [8-11]. При нарушении гемодинамических процессов желательно использовать препараты, не вызывающие гиперперфузию, «обкрадывание» и ортостатическую гипотонию, особенно у пациентов пожилого возраста. Одним из таких средств является Галидор (бенциклана фумарат). Галидор имеет многонаправленный механизм действия, обусловленный блокадой фосфодиэстеразы, антисеротониновым действием, кальциевым антагонизмом. Он тормозит агрегацию и адгезию тромбоцитов, препятствует агрегации и адгезии эритроцитов, повышая эластичность и осмотическую резистентность последних. Галидор снижает вязкость крови, нормализует внутриклеточный метаболизм глюкозы, достоверно усиливает оксигенацию тканей. В исследованиях Kohlmeyer (1972) доказано позитивное влияние Галидора на мозговой кровоток в ишемизированной ткани. При хронической недостаточности мозгового кровообращения монотерапия Галидором 400 мг в сутки в течение 8 недель была эффективной у 86% пациентов [6]. Проведенное в 1980 году Eckman и Schneider двойное слепое плацебо-контролируемое исследование эффективности Галидора при остром нарушении мозгового кровообращения выявило клиническое улучшение у 80% больных. Особенностью данного лекарственного средства является сочетание сосудорасширяющего, спазмолитического эффектов с мягким вегетокорректирующим и седативным влиянием [8,9].
Целью проведенного исследования явилось изучение эффективности препарата Галидор у пациентов с гемодинамическим подтипом ишемического инсульта в остром периоде.
Материалы и методы
Под наблюдением находилось 60 пациентов в остром периоде ишемического инсульта в возрасте от 43 до 76 лет (средний возраст 60,1±1,3 года). Характер инсульта был верифицирован по данным магниторезонансной томографии. Срок инсульта составил от 3 до 6 дней. Критериями включения в исследование явилось наличие у пациентов:
- изменений гемореологических показателей;
- гипертонической болезни и атеросклероза или их сочетания.
Из исследования исключались пациенты с тяжелым инсультом, выраженной соматической патологией, сосудистой деменцией, выраженной сердечной патологией (для исключения кардиоэмболического подтипа инсульта), а также с изменением полей зрения вследствие нарушения кровообращения в бассейне задней мозговой артерии. Лечение всех пациентов первые три дня пребывания в стационаре проводилось по классическим канонам терапии острейшего периода инсульта. Учитывая ведущую роль сосудистого фактора в патогенезе ишемического инсульта, больные получали базовую терапию, улучшающую реологические показатели крови. Все пациенты были поделены на 2 группы, сопоставимые по всем показателям. С 3-6 дня пребывания в стационаре основная группа (30 человек) получала Галидор в дозе 400 мг, внутривенно капельно в течение 10 дней, затем 2 раза в день по 200 мг перорально в течение 21 дня. Дополнительно по показаниям назначались сахаропонижающие и гипотензивные средства. Больным контрольной группы лечение проводилось по стандартным методикам, включавшим применение антиагрегантных, вазоактивных и ноотропных препаратов.
Для оценки эффективности лечения использовали: клинико-неврологическое обследование (шкала NIH, индекс Бартель), анкетный метод оценки психо-вегетативных нарушений, нейропсихологическое исследование (шкала MMSE), оценку качества жизни (шкала SF-36), тесты Спилбергера, шкалу Сандоз, пробу Шульте, определение среднего балла уровня депрессии по шкале HADS, тест «десяти слов».
Степень и уровень поражения магистральных сосудов головы определяли с помощью ультразвуковой допплерографии экстра- и интракраниальных артерий. Для уточнения характера и локализации инсульта использовалась магнитно-резонансная томография.
С целью выяснения патогенетического подтипа ОНМК (концепция гетерогенности) определялись реологические и биохимические показатели крови (общий холестерин, протромбин, фибриноген, индекс атерогенности, глюкоза, MHO), проводилось изучение функциональной активности тромбоцитов. Оценка агрегационной способности тромбоцитов производилась фотометрически, по методу Борна.
Пациенты обследовались в первые дни пребывания в стационаре и перед выпиской. Оценка эффективности лечения - степени потенциального улучшения - рассчитывалась по следующей формуле:
| ОЭ = | (А-В) Max-Min | · 100 (%) |
В - оценка в баллах при поступлении;
Мах - максимальная оценка в баллах при поступлении;
Min - минимальная оценка в баллах при поступлении.
Субъективная оценка эффективности терапии проводилась пациентами по следующей схеме: «хорошо» - 4 балла, «удовлетворительно» - 3 балла, «неудовлетворительно» - 0 баллов.
Таблица 1. Динамика жалоб у пациентов до и после лечения
| Жалобы | Основная группа | Контрольная группа | ||
| До лечения, % | После лечения, % | До лечения, % | После лечения, % | |
| Головная боль | 100 | 20 | 95 | 50 |
| Головокружение | 20 | 0 | 30 | 20 |
| Шум в голове | 66 | 10 | 70 | 35 |
| Шум в ушах | 66 | 10 | 70 | 35 |
| Пошатывание при ходьбе | 100 | 20 | 100 | 66 |
| Нарушение речи | 60 | 10 | 60 | 50 |
| Раздражительность | 60 | 22 | 64 | 54 |
| Тревожность | 100 | 10 | 100 | 60 |
| Снижение памяти | 96 | 10 | 90 | 78 |
| Двигательные нарушения | 60 | 30 | 60 | 50 |
| Снижение работоспособности | 100 | 33 | 100 | 80 |
| Нарушение сна | 55 | 0 | 51 | 33 |
Таблица 2. Динамика средних показателей клинического состояния больных до и после лечения
| Показатель, баллы | Контрольная группа | Основная группа | ||
| До лечения | После лечения | До лечения | После лечения | |
| Шкала NIH | 12,3±0,4 | 9,1±0,9* | 12,0±0,1 | 7,3±0,9* |
| Шкала качества жизни (SF-36) | 34,0±1,3 | 53,8±1,3* | 33,8±2,4 | 68,0±1,6* |
| Индекс Бартель | 42,3±0,4 | 55,0±0,1* | 42,3±0,1 | 68,1±0,8* |
Результаты исследования
После проведенного лечения у пациентов уменьшилось количество жалоб на головную боль, раздраженность, плаксивость, снижение внимания, плохой сон,
Таблица 3. Динамика средних показателей нейропсихологического тестирования больных до и после лечения
| Показатель, в баллах | Контрольная группа | Основная группа | ||
| До лечения | После лечения | До лечения | После лечения | |
| Шкала MMSE | 22,3±0,1 | 25,8±0,1 * | 22,0±0,3 | 24,1±0,2* |
| Шкала Сандоз | 30,3±0,1 | 23,8±0,6* | 30,1±0,1 | 15,7±0,2* |
| Субъективная шкала оценки самочувствия | 43,2±0,2 | 47,2±0,1* | 42,9±0,3 | 57,3±0,Г |
| Уровень депрессии (HADS) | 13,4±0,2 | 11,2±0,1* | 13,2±0,4 | 9,8±0,5* |
Такие выводы косвенно подтверждаются исследованием способности пациентов к запоминанию и воспроизведению вербального материала с помощью методики «десяти слов». В группе больных, получавших Галидор, отмечалось увеличение объема кратковременной памяти при повышении способности к заучиванию слов. Полученные результаты были сопоставимы с показателями контрольной группы, получавшей ноотропные препараты. Однако точность кратковременной памяти, нарушения семантического опосредования и обобщения были ниже у пациентов основной группы. У всех больных после лечения улучшились сомнологические характеристики: сократился период засыпания, исчезли ночные пробуждения, увеличилась субъективная балльная оценка сна. В основной группе динамика этих показателей была более выраженной, что, вероятно, определяется вегетокорригирующим действием Галидора.
Состояние церебральной гемодинамики в обеих группах до начала лечения характеризовалась выраженным стенозом от 50% до 60% в экстракраниальных отделах сонных артерий. Спектр кровотока был диффузно изменен по атеросклеротическому типу. В интракраниальных отделах сонных и позвоночных артерий гемодинамически значимого препятствия кровотоку не определялось. Регистрировалось снижение линейной скорости артериального кровотока. К 21 дню пребывания в стационаре положительная динамика показателей церебрального кровотока была более значима у пациентов, получавших Галидор (табл. 4).
Таблица 4. Динамика изменений показателей УЗДГ до и после лечения
| Показатель | Контрольная группа | Основная группа | ||
| До лечения | После лечения | До лечения | После лечения | |
| Уровень стеноза, % | 54,1±1,3 | 48,4±0,2 | 56,0±1,2 | 43,3±0,1 |
| Линейная скорость кровотока СМА Л, см/с | 49,0±0,1 | 58,3±0,1* | 46,1±0,8 | 70,0±0,1* |
| Линейная скорость кровотока СМА П, см/с | 44,4±0,1 | 52,1±0,2* | 43,3±0,1 | 64,3±0,1* |
| Линейная скорость кровотока ПА Л, см/с | 21,3±0,3 | 22,1±0,1 | 20,3±0,2 | 22,4±0,3* |
| Линейная скорость кровотока ПА П, см/с | 18,2±0,1 | 19,1±0,1 | 19,1±0,3 | 19,3±0,1 |
| Линейная скорость кровотока ОА, см/с | 49,4+0,4 | 58,3±0,2* | 48,7±0,1 | 72,7±0,1* |
Степень выраженности стеноза в среднем уменьшилась на 15%, в контрольной группе на 5%. В исследованиях, проведенных ранее, у 20 пациентов со стенозом средней мозговой артерии увеличение скорости общего мозгового кровотока зарегистрировано на 20%, а в зоне ишемии на 40% после внутривенного введения 150 мг препарата [9]. У пациентов с ишемическим инсультом по атеротромботическому или гемодинамическому типу Галидор использовался в дозе 400 мг, что позволило усилить реперфузионный эффект. При этом скорость общего мозгового кровотока в среднем увеличилась на 50% (в контрольной группе - на 20%). Во время приема препарата не было зафиксировано синдрома «обкрадывания».
Нейровизуализация с помощью метода МРТ подтвердила локализацию и характер очага ишемии. После проведенной терапии регистрировалось уменьшение зоны перифокального отека и зон лакунарной ишемии (рис. 1, 2). Оценка динамики мозговой перфузии не проводилась.
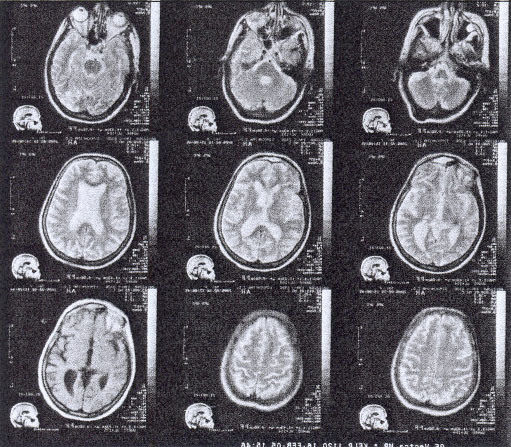
Рис. 1. Больная С, 70 лет; МРТ до начала лечения
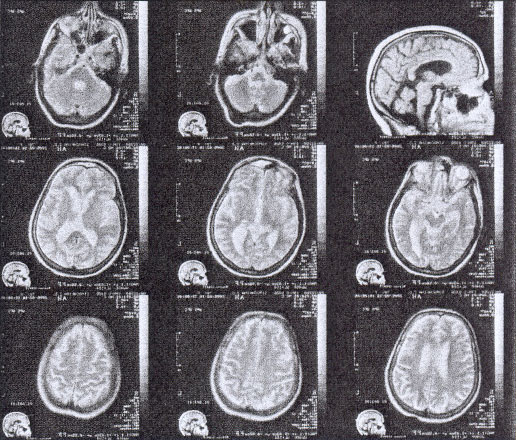
Рис. 2. Больная С, 70 лет; МРТ после курса лечения Галидором
Известно, что препарат Галидор активно воздействует на реологические свойства периферической крови [8,11]. До лечения у пациентов обеих групп были увеличены показатели общего холестерина, фибриногена, протромбинового индекса, индекса атерогенности, на фоне усиленной агрегации тромбоцитов (табл. 5, 6).
Таблица 5. Динамика реологических и биохимических показателей крови до и после лечения
| Показатель, в баллах | Контрольная группа | Основная группа | ||
| До лечения | После лечения | До лечения | После лечения | |
| Общий холестерин, ммоль/л | 5,9±1,2 | 5,7±1,0 | 6,2±1,3 | 5,6±0,8" |
| Фибриноген, ммоль/л | 4,8±0,8 | 4,3±0,2 | 4,7±0,6 | 3,6±0,Г |
| Глюкоза, ммоль/л | 7,0±1,5 | 5,2±1,0* | 7,1±1,2 | 5,2±1,0* |
| Индекс атерогенности, % | 5,5±0,2 | 5,0±0,2* | 5,7±0,3 | 3,6±0,1* * |
| Протромбиновый индекс, % | 110,5±1,8 | 100,3±1,3* | 110,8±1,0 | 90,3±1,0* |
| MHO | 1,6±0,1 | 1,2±0,03" | 1,7±0,2 | 1,2±0,5** |
Таблица 6. Динамика изменения скорости агрегации тромбоцитов до и после лечения
| Концентрация АДФ, мкмоль/л | Скорость агрегации тромбоцитов, % | |||
| Контрольная группа | Основная группа | |||
| До лечения | После лечения | До лечения | После лечения | |
| 0,6 | 40,1±1,03 | 38,1±0,3* | 41,2±1,1 | 32,1±0,3* |
| 1,25 | 44,6±0,7 | 42,6±0,5* | 45,3±0,8 | 38,7±0,8* |
| 2,5 | 60,3±0,6 | 59,1±0,3 | 61,1±0,8 | 49,1±0,9** |
| 5,0 | 78,0±1,2 | 74,0±1,3* | 76,9±1,2 | 68,8±0,7* |
Анализ полученных результатов выявил улучшение всех исследуемых параметров у пациентов обеих групп. В контрольной группе в ряде случаев данные были недостоверны. На фоне лечения Галидором количество больных с нарушениями гемореологических свойств уменьшилось с 90 до 30%. Особенно выраженное действие препарата было зафиксировано при исследовании свертывающей системы крови и скорости агрегации тромбоцитов. Уровень фибриногена понизился на 25% по сравнению с исходными цифрами (в контроле на 15%); протромбиновый индекс уменьшился на 18% (в контроле на 10%); индекс атерогенности изменился в сторону снижения на 37% (в контроле на 10%). Скорость агрегации тромбоцитов была достоверно меньшей при всех концентрациях АДФ после курса терапии Галидором.
Широкое использование любого лекарственного средства в неврологической практике определяется не только его высокой клинической эффективностью, но и отсутствием или наличием минимального количества побочных эффектов и осложнений. В основной группе у одного пациента после приема Галидора появились единичные экстрасистолы, у двух больных отмечались тошнота и боли в эпигастральной области. Все симптомы купировались после отмены препарата. Других нежелательных явлений зафиксировано не было. Хорошая переносимость препарата зарегистрирована у 90% больных. Расчетная эффективность терапии составила 83% в основной группе и 50% в контрольной. Субъективная оценка проведенному курсу лечения составила 90% в основной группе и 50% в контрольной. Полученные результаты исследования свидетельствуют о возможности эффективного и безопасного применения Галидора у пациентов в острой стадии ишемического инсульта. Препарат положительно влияет на состояние цереброваскулярной реактивности и улучшает перфузионный резерв. В первую очередь Галидор назначается больным с атеротромботическим и гемодинамическим подтипами ишемического инсульта. При кардиоэмболическом типе он не используется, так как может вызвать неадекватные изменения гемодинамики и сердечного ритма. Таким образом, концепция лечения острого периода ишемического инсульта в настоящее время включает в себя теорию гетерогенности. Выбор стратегии терапии больных с ОНМК должен основываться на знании патогенетических механизмов и рациональном использовании вазоактивных препаратов.
Литература
