Терапия болезни Паркинсона с использованием Пронорана (пирибидила)
Статьи Опубликовано в журнале:«ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ»; № 3; 2007; стр. 64-65.
Н.В. Федорова, Т.К. Кулуа, И.П. Чиеирь
Кафедра неврологии Российской медицинской академии постдипломного образования, Уентр экстрапирамидных заболеваний Росздрава, Москва
The Combined Therapy Of Parkinson's' Disease
N.V. Fedorova, T.K. Kulua, I.P, Chigir
Проноран (пирибидил) относится к группе неэрголиновых агонистов дофаминовых рецепторов. Он является единственным агонистом, повышающим активность как дофаминергической, так и норадренергической систем мозга.
Целью настоящего исследования явилось изучение эффективности пронорана при лечении больных на ранней и поздней стадии болезни Паркинсона. Задачами исследования являлись: изучение эффективности пронорана при лечении двигательных нарушений на ранней и поздней стадии болезни Паркинсона; оценка действия пронорана на повседневную активность и качество жизни больных; исследование динамики суточной дозы ДОФА-содержащих средств (ДСС) и продолжительности действия однократной дозы ДСС при комбинированном лечении пронораном и препаратами леводопы на поздних стадиях болезни Паркинсона; изучение влияния терапии пронораном на выраженность лекарственных дискинезий, моторных флюктуаций; изучение влияния пронорана на выраженность тревоги, депрессии и когнитивных нарушений при болезни Паркинсона.
Материал и методы
Наблюдали 35 пациентов с болезнью Паркинсона в возрасте от 55 до 73 лет (62,5±7,4), в том числе 20 больных с I—II стадией по шкале Хена и Яра и 15 больных с III—IV стадией. Степень тяжести болезни по шкале Хена и Яра составила 2,3±0,78 балла (1,6±0,3 для ранней стадии, 2,9±0,5 для поздней стадии). Продолжительность заболевания у больных с ранними стадиями в среднем составила 3,5±2,5 года, а с развернутыми стадиями — 7,1±5 лет.
Все пациенты с развернутыми стадиями болезни принимали препараты леводопы; средняя доза достигала 511,5±180,5 мг/сут, продолжительность терапии леводопой— 4,2±2,8 года. У 10 больных отмечался феномен истощения однократной дозы ДСС, у 6 — феномен застывания, у 4 — феномен включения — выключения. Лекарственные дискинезии наблюдались у 7 больных в виде хореиформных гиперкинезов пика дозы (у 4 больных) и дистоний окончания действия дозы (3 больных).
Проноран назначался больным в течение 4 мес. Начальная доза препарата составляла 50 мг/сут. В дальнейшем она постепенно увеличивалась до 150—200 мг/сут (в среднем 146,4±23,7 мг/сут).
Для оценки эффективности терапии пронораном использовались следующие методы: клинико-неврологическое обследование с количественной оценкой двигательных нарушений с помощью унифицированной рейтинговой шкалы болезни Паркинсона (3-я версия) (Unified Parkinson's Disease Rating Scale — UPDRS), шкалы Хена и Яра, шкалы равновесия и двигательной активности M. Tinetti, шкалы оценки флюктуаций и дискинезий, оценка когнитивных нарушений с использованием Векслеровской шкалы интеллекта для взрослых (WAIS), Векслеровская шкала памяти (WMS), тестов на вербальную активность А.Р. Лурия, исследование аффективных нарушений с применением шкалы депрессии Гамильтона и шкалы тревоги Спилбергера.
Результаты и обсуждение
Через 4 мес лечения пронораном отмечалось достоверное снижение степени двигательных нарушений с уменьшением показателей шкалы UPDRS на 30,7% и на 24,6% для ранней и развернутой стадии соответственно (табл. 1 и 2). Повседневная активность увеличилась на 35,3% у больных с ранними стадиями БП и на 27,5% у больных с развернутыми стадиями БП. Двигательная активность возросла на 27,8% от исходного уровня у больных с ранними стадиями БП и на 23,5% с развернутыми стадиями БП.
Таблица 1
Показатели двигательной активности у больных на ранней стадии болезни Паркинсона, баллы
| Шкала | До лечения | После лечения |
| UPDRS | ||
| II часть | 11,6±2,7 | 7,5±2,3* |
| III часть | 25,9±6,0 | 18,7±5,6* |
| общий балл | 39,8±9,0 | 27,6±7,1* |
| Tinetti | ||
| устойчивость | 20,5±1,46 | 22,5±1,6* |
| походка | 10,8±2,2 | 12,3±2,3 |
| общий балл | 31,37±3,05 | 34,8±3,6* |
Таблица 2
Показатели двигательной активности у больных на развернутой стадии болезни Паркинсона, баллы
| Шкала | До лечения | После лечения |
| UPDRS | ||
| II часть | 16,0±2,03 | 11,6±3,2* |
| III часть | 37,0±7,6 | 28,3±8,8* |
| общий балл | 59,8±11,7 | 45,1±14,3 |
| Tinetti | ||
| устойчивость | 16,8±3,7 | 20,1±3,7* |
| походка | 8,6±2,8 | 11,4±2,6 |
| общий балл | 25,4±6,03 | 31,5±6,04* |
| Продолжительность выключения (мин) | 123,2±134,2 | 81,8±99,1 |
| Продолжительность включения (мин) | 676,3±147,7 | 879,2±148,7 |
| Шкала дискинезии (балл) | 0,7±0,9 | 0,6±0,9 |
Улучшились показатели устойчивости и походки (по шкале Тинетти): нарушения достоверно снизились на фоне лечения пронораном на 10,9% и на 24% у больных с ранними и развернутыми стадиями соответственно.
Достоверное уменьшение гипокинезии и ригидности отмечено в обеих группах больных: для ранних стадий на 28,3 и 32,7% (рис. 1), для поздних стадий на 29,2 и 24,4% (рис. 2) соответственно.
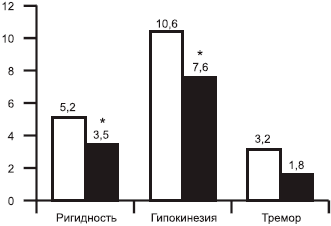
Рис. 1. Показатели основных симптомов до (светлые столбики) и после (темные столбики) лечения пронораном на ранних стадиях болезни Паркинсона, баллы.
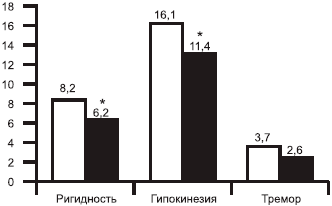
Рис. 2. Показатели основных симптомов до (светлые столбики) и после (темные столбики) пронораном на развернутых стадиях болезни Паркинсона.
Оценка фармакотерапевтической эффективности пронорана показала, что у 10 больных с развернутыми стадиями на 30% увеличилась продолжительность периода включения, снизилась продолжительность периода выключения на 33,6%. Кроме того, отмечалось увеличение средней продолжительности действия однократной дозы ДСС на 4,8%.
На фоне лечения пронораном в течение 4 мес отмечалось уменьшение выраженности когнитивных расстройств: отмечено улучшение показателей по шкале деменции Маттиса на 3,7% (р<0,0004), преимущественно за счет улучшения внимания (табл. 3). Достоверно улучшились показатели выполнения теста на логическую память (на 30,1%), теста на зрительную память (на 8,3%), теста «арифметика» (на 16,9%). Уменьшилась также степень депрессии (на 23,9%) (р<0,0007), выраженность личностной тревожности (на 4,4%), реактивной тревожности (на 6,8%). Более подробно эти данные приведены в табл. 3.
Таблица 3.
Показатели когнитивных и аффективных нарушений у пациентов с болезнью Паркинсона
| До лечения | После лечения | |
| Общая оценка когнитивных функций (шкала деменции S. Mattis) | 108,4±5,4 | 112,4±3,6* |
| Память (WMS) | ||
| логическая память | 9,3±2,6 | 12,1±2,5* |
| зрительная память | 8,3±3,02 | 9,7±3,5* |
| Мышление (WAIS) | ||
| «сходства» | 18,3±3,7 | 19,6±2,8 |
| «арифметика» | 11,8±2,7 | 13,8±2,8* |
| Речь | ||
| вербальная активность — слова | 25,2±8,4 | 26,5±8,4 |
| вербальная активность — глаголы | 18,4±5,9 | 19,1±6,2 |
| вербальная активность — слова на «л» | 11,3±4,2 | 11,4±5,4 |
| Шкала депрессии Гамильтона | 14,8±4,8 | 11,3±4,3* |
| Шкала Спилбергера | ||
| реактивная тревожность | 35,2±7,1 | 32,8±10,7 |
| личностная тревожность | 55,6±8,04 | 53,2±8,1 |
Побочные эффекты в виде тошноты, рвоты отмечались у 3 больных в начале титрования дозы пронорана, которые впоследствии регрессировали на фоне приема мотилиума. У 4 больных наблюдалось возникновение головной боли, головокружения, которые исчезли при снижении дозы пронорана.
Таким образом, лечение пронораном больных в виде монотерапии на ранней стадии и в комбинации с леводопой на развернутых стадиях болезни Паркинсона вызывает регресс основных двигательных расстройств, в том числе и тремора. Эффективность пронорана на ранней стадии БП сопоставима с эффектом препаратов леводопы. Ранняя комбинация пронорана с ДОФА-содержащими препаратами позволяет уменьшить риск возникновения моторных флюктуаций и лекарственных дискинезий, снизить потребность быстрого наращивания дозы леводопы. Терапия пронораном больных на разных стадиях болезни Паркинсона вызывает улучшение повседневной активности, показателей качества жизни, уменьшение когнитивных и аффективных расстройств. Назначение пронорана больным с развернутыми стадиями болезни Паркинсона приводит к увеличению продолжительности периода «включения», снижению продолжительности периода «выключения», нарастанию продолжительности и эффективности действия однократной дозы дофамин-содержащих средств. Как известно, проноран занимает особую роль среди других агонистов дофаминовых рецепторов, поскольку он влияет на адренергическую и норадренергическую нейротрансмиссию. По-видимому именно это позволяет ему влиять на широкий спектр нарушений при болезни Паркинсона — двигательные, аффективные, когнитивные расстройства и ряд немоторных симптомов заболевания.
