Ингибитор фосфодиэстеразы 4 рофлумиласт в лечении хронической обструктивной болезни легких
СтатьиЗ.Р. Айсанов, Е.Н. Калманова, О.Ю. Стулова
Хроническая обструктивная болезнь легких (ХОБЛ) -хроническое воспалительное заболевание дыхательных путей, паренхимы легких и легочных кровеносных сосудов, возникающее в результате воздействия поступающих с воздухом раздражителей, таких как табачный дым и другие загрязняющие вещества внешней среды.
Для ХОБЛ характерно неуклонно прогрессирующее снижение функции внешнего дыхания (ФВД), и это, пожалуй, самый специфичный функциональный и прогностический признак заболевания. Изменения ФВД легли в основу общепринятой классификации ХОБЛ и стали главной терапевтической мишенью в крупных клинических исследованиях - их первичной или одной из главных конечных точек.
Хотя современная диагностика ХОБЛ и классификация заболевания по степени тяжести построены на регистрации бронхиальной обструкции и степени ее выраженности, воспаление дыхательных путей присутствует уже на ранних стадиях болезни, а его выраженность увеличивается по мере утяжеления ХОБЛ [1, 2]. Хотя и ХОБЛ, и бронхиальная астма относятся к группе обструктивных заболеваний легких, в основе которых лежит воспалительный процесс, сама природа воспаления и каскад воспалительных реакций при этих заболеваниях существенно различаются (рис. 1). Кроме того, в отличие от бронхиальной астмы при ХОБЛ поражаются не только дыхательные пути, но и в значительной степени легочная паренхима, при этом ограничение воздушного потока не полностью обратимо и неуклонно прогрессирует.
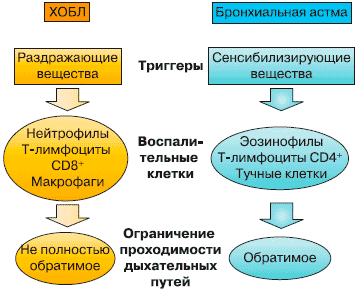
Рис. 1. Воспаление при ХОБЛ и при бронхиальной астме.
Хроническое воспаление играет ключевую роль в патогенезе ХОБЛ, его механизмы достаточно сложны, но принципиально важно выделить следующие его особенности. Воспаление носит системный характер, приводя к морфологическим изменениям в легких - бронхоконстрикции, отеку слизистой оболочки бронхов, гиперсекреции слизи, эмфиземе, что в совокупности приводит к ограничению проходимости дыхательных путей. Основными клетками, принимающими участие в воспалительном процессе, являются нейтрофилы, Т-лимфоциты (CD8+) и макрофаги [1, 3]. Эти клетки накапливаются в легких и запускают каскад воспалительных реакций, которые приводят к ограничению бронхиальной проводимости и воздушного потока, а также к системному воспалению вне легких. Высвобождаются воспалительные медиаторы, такие как фактор некроза опухоли а, матриксные металлопротеиназы и интерлейкины 1, 6, 8. В основе обострений ХОБЛ лежит дальнейшее усиление процесса воспаления, присутствующего и в стабильном состоянии [3-6].
Таким образом, сама природа воспалительного процесса при ХОБЛ и логика научного поиска подсказывали, что необходимо разрабатывать препараты, которые могли бы воздействовать на специфический характер воспаления при этом заболевании и его ключевые звенья.
Роль фосфодиэстеразы-4 в воспалении при ХОБЛ
Несмотря на сложность и многогранность воспаления при ХОБЛ, в нем присутствуют ключевые звенья. Одним из этих звеньев является фосфодиэстераза (ФДЭ) 4-го типа - энзим, регулирующий метаболизм циклического аденозинмонофосфата (цАМФ) в провоспалительных и иммунных клетках, а также катализирующий переход цАМФ в его неактивную форму - АМФ.
Ингибиторы ФДЭ-4 тормозят разрушение цАМФ и способствуют поддержанию высоких внутриклеточных уровней цАМФ, что снижает активность провоспалительных функций клеток (рис. 2) [7, 8]. Насколько данный механизм клинически значим и универсален? Хотя семейство ФДЭ состоит из 11 изоформ, ФДЭ-4 является цАМФ-специфической и преобладающей изоформой, которая экспрессируется иммунными и провоспалительными клетками. ФДЭ-4 является основным регулятором метаболизма цАМФ практически во всех провоспалительных и структурных клетках, вовлеченных в хроническое воспаление при ХОБЛ.
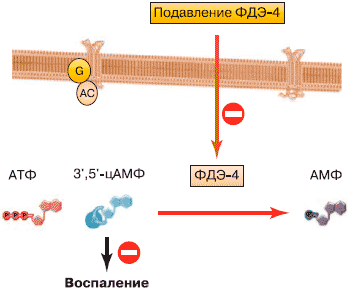
Рис. 2. Роль фосфодиэстеразы-4 в воспалении при ХОБЛ [7].
Ингибиторы фосфодиэстеразы-4
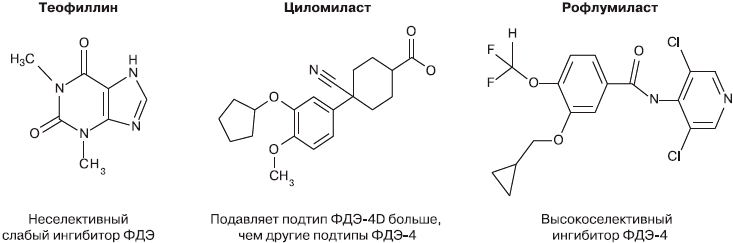
Способность ингибировать ФДЭ нашли в свое время у применяемого с 1930-х годов теофиллина (рис. 3). Применение неселективных ингибиторов, подобных теофиллину, было ограничено большим числом лекарственных взаимодействий и узким диапазоном терапевтических доз, что приводило к частым нежелательным явлениям со стороны сердечно-сосудистой системы и желудочно-кишечного тракта [9]. Кроме того, теофиллин, будучи слабым и неселективным ингибитором фосфодиэстераз, не способен оказывать влияние на ФДЭ-4 в своих терапевтических концентрациях.
Рис. 3. Ингибиторы ФДЭ-4.
Высокое содержание ФДЭ-4 в провоспалительных и структурных клетках сделало этот фермент одной из наиболее привлекательных терапевтических целей для воздействия на хроническое воспаление при ХОБЛ. Другой причиной роста интереса к ингибиторам ФДЭ было выявление 11 разных изоформ фермента, имевших различную тканевую принадлежность и свойства, что обещало возможности для адресной терапии с меньшим количеством системных нежелательных явлений.
Шел интенсивный поиск новых молекул, которые могли бы в терапевтических концентрациях подавлять ФДЭ-4. Эта работа привела к созданию селективных ингибиторов ФДЭ-4 второго поколения, таких как циломиласт и рофлумиласт, которые изначально разрабатывались как противовоспалительные препараты для лечения ХОБЛ и бронхиальной астмы [10, 11].
В отличие от рофлумиласта циломиласт демонстрировал некоторую селективность в отношении 4D-подтипа ФДЭ, что стало причиной высокой частоты нежелательных явлений со стороны желудочно-кишечного тракта (тошнота, рвота) и в итоге привело к запрету на применение этого препарата [12]. Рофлумиласт обладает намного большей активностью, чем циломиласт (табл. 1), и при этом воздействует на подтипы ФДЭ-4, которые вызывают меньше нежелательных явлений [13].
Таблица 1
Сравнительная активность ингибиторов ФДЭ [10]
| Ингибитор | Подавление ФДЭ-4 (ингибирующая на 50% концентрация, нмоль/л) | Доза для лечения ХОБЛ |
| Рофлумиласт | 0,8 | 0,5 мг 1 раз в сутки |
| Циломиласт | 120 | 15 мг 2 раза в сутки |
| Ролипрам | 1100 | - |
| Теофиллин | >10000 | 100-600 мг 1 раз в сутки |
Рофлумиласт был в 2010 г. зарегистрирован в Европе под торговым названием Даксас (таблетки по 500 мг для приема один раз в сутки), а в 2011 г. - в США (торговое название Daliresp).
Возможности клинического применения рофлумиласта
Влияние на воспалительные маркеры
В исследованиях, проведенных на животных моделях, рофлумиласт показал способность подавлять основные патогенетические механизмы ХОБЛ: воспаление, связанное с воздействием табачного дыма, дисфункцию мукоцилиарного аппарата, фиброзные и эмфизематозные изменения легочной ткани, оксидативный стресс и ремоделирование легочных сосудов.
В двойном слепом рандомизированном плацебоконтролируемом перекрестном исследовании с участием 38 больных ХОБЛ (объем форсированного выдоха за 1-ю секунду (ОФВ1) в среднем составил 61 % от должного) было показано, что назначение рофлумиласта (500 мкг 1 раз в сутки в течение 4 нед) приводит к уменьшению содержания в мокроте нейтрофилов, лимфоцитов, макрофагов и эозинофилов, интерлейкина 8, эластазы нейтрофилов, эозинофильного катионного протеина и α2-макроглобулина, а также к уменьшению высвобождения фактора некроза опухоли α из клеток крови [14]. Данное уменьшение активности специфичного для ХОБЛ воспаления сочеталось с достоверным улучшением ФВД до и после приема бронходилататоров. Полученные результаты представлялись интересными в свете ранее проведенных исследований. Способность рофлумиласта влиять на содержание нейтрофилов в слизистой оболочке дыхательных путей позволяла предположить, что этот препарат может контролировать воспаление и поддерживать его на уровне, близком к ремиссии, а также, возможно, предотвращать обострения.
Для изучения характера и степени воспаления дыхательных путей при обострении ХОБЛ были проведены иммуногистохимические анализы биопсий слизистой оболочки долевого бронха и цитологические анализы мокроты у 11 пациентов во время обострения и у 12 пациентов перед обострением. Было показано, что во время обострения число нейтрофилов достоверно повышается (р < 0,01) [15].
В исследовании, проведенном у 46 курильщиков и бывших курильщиков (средний возраст 64 года), было показано, что у пациентов с обструкцией дыхательных путей в индуцированной мокроте содержалось больше нейтрофилов (77%), чем у пациентов без обструкции (60%) [16]. Содержание нейтрофилов также было выше (77%) у пациентов с хроническим выделением мокроты, чем без него (57%). Повышенные уровни нейтрофилов коррелировали с более быстрым снижением ОФВ1 за 15-летний период наблюдения. У пациентов с наибольшим процентом нейтрофилов в индуцированной мокроте отмечалась максимальная скорость снижения параметров ФВД. Эти результаты представляются очень важными для объяснения того, как противовоспалительный препарат, не являющийся бронходилататором, может влиять на скорость снижения ФВД.
Влияние на обострения ХОБЛ и ФВД
Снижение частоты и тяжести обострений является одной из главных целей лечения ХОБЛ, определенных экспертами в Глобальной стратегии по диагностике, лечению и профилактике ХОБЛ (GOLD - Global strategy for the diagnosis, management and prevention of COPD) [17].
Обострения ХОБЛ связаны с повышением активности воспаления, которое существует после острого периода и удлиняет срок восстановления после обострения [18]. В ранее упомянутом исследовании [15] у пациентов с ХОБЛ были получены четкие доказательства того, что обострения связаны с повышением активности воспаления в виде роста содержания нейтрофилов в мокроте и биоптатах бронхов. В дополнение к этому у пациентов с частыми обострениями даже в стабильном состоянии отмечается более высокая активность воспаления в дыхательных путях [19].
В когортном многоцентровом 3-летнем исследовании ECLIPSE (Evaluation of COPD Longitudinally to Identify Predictive Surrogate Endpoints), где принимали участие 2138 пациентов с ХОБЛ, было наглядно продемонстрировано, что по мере увеличения тяжести ХОБЛ обострения становятся более частыми и более тяжелыми (табл. 2) [20]. Наилучшим предиктором обострений на всех стадиях ХОБЛ было наличие обострений в предшествующем году. Кроме того, была показана необходимость выделять подгруппу пациентов с частыми обострениями (что может быть сделано при сборе анамнеза) и осуществлять для них специальные меры по профилактике обострений.
Таблица 2
Тяжесть ХОБЛ и частота обострений в исследовании ECLIPSE [20]
| Стадия ХОБЛ по GOLD |
Число обострений в год на 1 пациента |
Доля пациентов с частыми обострениями, % |
| II | 0,85 | 22 |
| III | 1,34 | 33 |
| IV | 2,00 | 47 |
Для изучения влияния рофлумиласта на обострения ХОБЛ были проведены два сходных по дизайну 12-месячных рандомизированных плацебоконтролируемых двойных слепых исследования в параллельных группах -М2-111 и М2-112. Суммарно в них участвовали 2686 пациентов, а различие заключалось в том, что в первое из них включали пациентов с ХОБЛ в соответствии с критериями Американского торакального общества, а во второе - в соответствии с критериями GOLD [21, 22]. При объединенном анализе данных было выявлено статистически значимое снижение частоты обострений ХОБЛ при лечении рофлумиластом на 14,3% (95% доверительный интервал (ДИ) -25,0 ... -0,02; р = 0,03).
При проведении ретроспективного анализа с целью выявить подгруппы пациентов, которые получили наибольшую пользу от лечения рофлумиластом, было показано, что наличие хронического бронхита (хронического кашля с мокротой) коррелирует с более выраженным снижением частоты обострений. У этой категории больных частота обострений при терапии рофлумиластом снизилась на 26,2%, тогда как у пациентов с эмфиземой и без хронического бронхита лишь на 1,1%. В результате пациенты с клиническими симптомами хронического бронхита были выделены в качестве целевой популяции для дальнейших исследований. Эта категория больных ХОБЛ также характеризовалась функциональными признаками выраженного ограничения бронхиальной проходимости и наличием обострений в анамнезе.
Объединенный анализ двух других 52-недельных рандомизированных плацебоконтролируемых исследований [23] с применением рофлумиласта (500 мкг 1 раз в сутки, n = 1537) или плацебо (n = 1554) показал, что терапия рофлумиластом сопровождалась улучшением ОФВ1 до приема бронходилататора в среднем на 48 мл по сравнению с плацебо (р < 0,0001). Рофлумиласт достоверно улучшил также постбронходилатационный ОФВ1 - на 55 мл по сравнению с плацебо (р < 0,0001). Улучшение ФВД после применения бронходилататора было достоверным уже через 4 нед применения рофлумиласта и сохранялось на всем протяжении 52-недельного лечебного периода. Полученные данные означали, что прием рофлумиласта вызывает дополнительные положительные эффекты при добавлении к терапии бронходилататором.
Кроме того, использование рофлумиласта достоверно снизило частоту среднетяжелых и тяжелых обострений ХОБЛ - на 17% по сравнению с плацебо (р = 0,0003). Это сопровождалось увеличением периода времени до возникновения обострения в группе рофлумиласта по сравнению с группой плацебо - относительный риск 0,89, р = 0,02.
Ретроспективный анализ объединенных данных 12-месячных клинических исследований показал, что рофлумиласт достоверно снизил среднюю частоту обострений (на 1 пациента в год) во всех группах пациентов [24]. Время до возникновения любого обострения было достоверно больше у пациентов, получавших рофлумиласт, чем у пациентов в группе плацебо (табл. 3). Относительный риск развития обострений в группе рофлумиласта составил для первого обострения 0,89 (р = 0,019), для второго - 0,79 (р = 0,001), для третьего - 0,73 (р = 0,003). При этом эффекты рофлумиласта были наиболее выраженными у пациентов с 2 или более обострениями за предыдущий год (частота обострений в исследовании 1,51 для рофлумиласта против 1,95 для плацебо; различие на 22%). Итак, клиническая эффективность рофлумиласта наиболее выражена у пациентов с частыми обострениями в анамнезе (рис. 4).
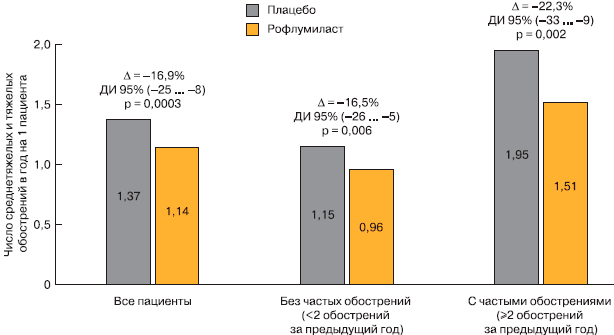
Рис. 4. Эффективность рофлумиласта в зависимости от частоты обострений в анамнезе [24].
Таблица 3.
Влияние рофлумиласта на частоту обострений [24]
|
Число обострений за 12 мес |
Доля пациентов с обострениями, % | |
| рофлумиласт | плацебо | |
| 2 | 11,5 | 13,6 |
| 3 | 5,9 | 6,8 |
| 4 | 2,4 | 3,5 |
| 5 | 1,0 | 2,1 |
Эффективность рофлумиласта в комбинации с другими препаратами
Бронходилататоры длительного действия
В ранее упоминавшихся 52-недельных исследованиях М2-124 и М2-125 около половины пациентов продолжали принимать β2-агонисты длительного действия во время лечения [23]. В группе рофлумиласта частота обострений снижалась независимо от того, принимали ли пациенты сопутствующую поддерживающую терапию ХОБЛ. Анализ эффектов рофлумиласта в подгруппе пациентов, принимавших β2-агонисты длительного действия, выявил, что частота обострений снижалась у них на 21% по сравнению с плацебо (р = 0,0011) [25]. Помимо этого лечение рофлумиластом достоверно улучшило показатели ОФВ1 до и после применения бронходилататора по сравнению с плацебо у всех пациентов независимо от того, получали ли они одновременно β2-агонисты длительного действия или нет (рис. 5) [23].
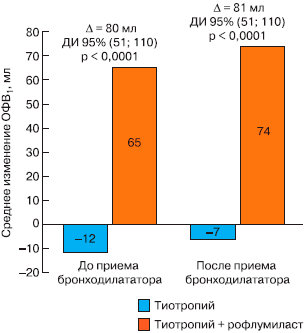
Рис. 5. Влияние рофлумиласта на ОФВ1 при добавлении к терапии тиотропием [23].
Эффекты рофлумиласта изучали в 24-недельном исследовании у пациентов с ХОБЛ, принимавших антихолинергический бронходилататор длительного действия тиотропий [26]. Рофлумиласт при добавлении к лечению тиотропием достоверно улучшал ОФВ1 до и после применения бронходилататора по сравнению с плацебо (р < 0,0001). Улучшение показателей ФВД становилось очевидным уже через 4-8 нед лечения рофлумиластом и сохранялось на всем протяжении исследования.
Положительные эффекты рофлумиласта и бронходилататоров длительного действия являются аддитивными, поскольку эти препараты обладают разными механизмами действия. Иными словами, добавление к терапии рофлумиласта позволяет получить дополнительные благоприятные эффекты помимо тех, что уже были достигнуты с помощью препаратов первого ряда для поддерживающей терапии ХОБЛ.
Ингаляционные глюкокортикостероиды
В исследованиях М2-111 и М2-112 пациентам разрешалось продолжать лечение ингаляционными глюкокортикостероидами (ИГКС) в дозе, не превышающей эквивалент 2000 мкг беклометазона дипропионата, если они использовали ИГКС в постоянной дозе не менее 3 мес до включения в исследование. Поэтому около 60% всех больных (1622 пациента) одновременно с исследуемыми препаратами принимали ИГКС [21].
При объединенном анализе данных этих исследований выяснилось, что рофлумиласт снизил частоту среднетяжелых и тяжелых обострений ХОБЛ у пациентов, получавших ИГКС, на 18,8%. Эти данные свидетельствуют о различии механизмов противовоспалительного действия рофлумиласта и ИГКС (рис. 6).
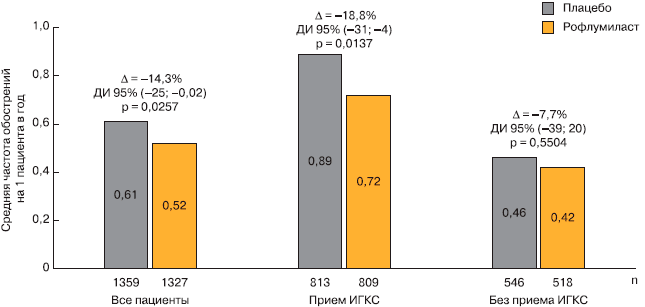
Рис. 6. Влияние рофлумиласта на частоту обострений при добавлении к терапии ИГКС [21].
Большая способность рофлумиласта снижать количество обострений у пациентов, получающих ИГКС, может частично объясняться тем, что ИГКС принимали пациенты с более тяжелым течением ХОБЛ. Такие больные подвергаются более высокому риску обострения, о чем свидетельствует более высокая частота обострений в группе плацебо у пациентов, получавших ИГКС (0,89 случая в год), чем у не получавших ИГКС (0,46 случая в год). Таким образом, у этой категории больных влияние противовоспалительной терапии на частоту обострений может проявляться в большей степени [22]. Кроме того, у больных ХОБЛ с фенотипом хронического бронхита, которые получали ИГКС, прием рофлумиласта снизил частоту среднетяжелых и тяжелых обострений на 30,2% по сравнению с плацебо.
Заключение
Имеющиеся на сегодняшний день данные, полученные в крупных клинических исследованиях на широкой популяции пациентов, свидетельствуют о большом потенциале рофлумиласта как первого представителя принципиально нового класса препаратов, нацеленных на лечение специфичного для ХОБЛ воспаления. Анализ совокупных результатов показал, что наибольшая эффективность рофлумиласта отмечается у пациентов с тяжелым течением ХОБЛ с клиническими проявлениями хронического бронхита. Эта эффективность подтверждается улучшением легочной функции, а также уменьшением частоты обострений при добавлении рофлумиласта к поддерживающей терапии бронходилататорами длительного действия и ингаляционными глюкокортикостероидами.
Заурбек Рамазанович Айсанов - профессор, зав. отделом клинической физиологии и клинических исследований НИИ пульмонологии ФМБА России. 1. Hogg J.C. et al. // N. Engl. J. Med. 2004. V. 350. P. 2645.
Елена Николаевна Калманова - канд. мед. наук, зав. отделением функциональной и ультразвуковой диагностики ГКБ № 57 г. Москвы.
Ольга Юрьевна Стулова - канд. мед. наук, зав. лабораторией клинической эпидемиологии НИИ пульмонологии ФМБА России.ЛИТЕРАТУРА
2. Saetta M. // Am. J. Respir. Crit. Care Med. 1999. V. 160. P. S17.
3. Barnes P.J., Hansel T.T. // Lancet. 2004. V. 364. P. 985.
4. Barnes PJ. Chemokines in COPD // Chronic Obstructive Pulmonary Disease / Ed. by R.A. Stockley et al. Oxford, 2007. P. 860.
5. Papi A. et al. //Am. J. Respir. Crit. Care Med. 2006. V. 173. P. 1114.
6. Perera W. et al. // Eur. Respir. J. 2007. V. 29. P. 527.
7. Rabe K.F. // Expert Rev. Resp. Med. 2010. V. 4. P. 543.
8. Hatzelmann A. et al. // Pulm. Pharmacol. Ther. 2010. V. 23. P. 235.
9. Boswell-Smith V. et al. // J. Allergy Clin. Immunol. 2006. V. 117. P. 1237.
10. Wang D., Cui X. //Int. J. Chron. Obstruct. Pulmon. Dis. 2006. V. 1. P. 373.
11. Spina D.//Br.J. Pharmacol. 2008. V. 155. P. 308.
12. Rennard S. et al. // Drugs. 2008. V. 68. Suppl. 2. P. 3.
13. Hatzelmann A., SchudtC.//J. Pulm. Exp. Ther. 2001. V. 297. P. 267.
14. Grootendorst D.C. et al.//Thorax. 2007. V. 62. P. 1081.
15. Saetta M. et al. // Am. J. Respir. Crit. Care Med. 1994. V. 150. P. 1646.
16. Stanescu D. etal. //Thorax. 1996. V. 51. P. 267.
17. Global Initiative for Chronic Obstructive Lung Disease. Global strategy for the diagnosis, management, and prevention of COPD. Bethesda, MD, 2010.
18. Perera W. et al. // Eur. Respir. J. 2007. V. 29. P. 527.
19. Bhowmilk A. et al. //Thorax. 2000. V. 55. P. 114.
20. Hurst J.R. et al. // N. Engl. J. Med. 2010. V. 363. P. 1128.
21. Calverley P.M.A. et al. // Am. J. Respir. Crit. Care Med. 2007. V. 176. P. 154.
22. Martinez F.J. et al. Defining patient populations in COPD: Experience with roflumilast. COPD7 2010. Poster 12.
23. Calverley P.M.A. et al. // Lancet. 2009. V. 374. P. 685.
24. Bateman E. et al. Efficacy of roflumilast in patients with a history of frequent exacerbations: Pooled data from pivotal 12-mont studies // European Respiratory Society Annual Congress 2010. Barcelona, 2010. P4003.
25. Hanania N.A. et al. // Am. J. Respir. Crit. Care Med. 2010. V. 181. P. A4435.
26. Fabbri L.M. et al. // Lancet. 2009. V. 374. P. 695.
