Данные открытого в параллельных группах активно-контролированного постмаркетингового исследования эффективности и безопасности препарата триттико в сравнении со стандартной терапией пациентов с непсихотическими депрессивными расстройствами
Статьи Опубликовано в журнале:«МЕЖДУНАРОДНЫЙ НЕВРОЛОГИЧЕСКИЙ ЖУРНАЛ»; № 2(56); 2013.
Авторы: Чабан О.С., Хаустова Е.А., Безшейко В.Г., Украинский НИИ социальной и судебной психиатрии и наркологии МЗ Украины, г. Киев, Дорожная клиническая больница № 1, ст. Киев
Рубрики: Неврология, Психиатрия
Разделы: Клинические исследования
Резюме
В статье приведен обзор исследований эффективности тразодона в терапии депрессии, тревоги, инсомнии и болевых проявлений, а также представлено собственное открытое контролируемое рандомизированное 8-недельное исследование сравнительной эффективности и безопасности препарата тразодон у пациентов с депрессивным эпизодом. Полученные результаты подтвердили превосходство в эффективности мультифункционального препарата Триттико по сравнению со стандартной терапией депрессии не только по более быстрому началу действия, но также по наличию высокой анксиолитической активности и действенности в отношении редукции инсомнии.
У статті наведений огляд досліджень ефективності тразодону в терапії депресії, тривоги, інсомнії й больових проявів, а також подано власне відкрите контрольоване рандомізоване 8-тижневе дослідження порівняльної ефективності й безпеки препарату тразодон у пацієнтів із депресивним епізодом. Отримані результати підтвердили перевагу в ефективності мультифункціонального препарату Триттико порівняно зі стандартною терапією депресії не тільки за більш швидким початком дії, але також за наявністю високої анксіолітичної активності й дієвості щодо редукції інсомнії.
The paper reviewed the trials of trazodone effectiveness for depression, anxiety, insomnia and pain manifestations treatment. As well the paper presents the authors' open-label controlled randomized comparative investigation of trazodone effectiveness and safety in patients with depressive episode. The results confirm the benefits of multimodal agent Trittico in comparison with the standard therapy of depression as to the more rapid action and higher anxiolytic activity and effectiveness in regard to insomnia reduction.
Ключевые слова
депрессия, инсомния, тразодон. депресія, інсомнія, тразодон. depression, insomnia, trazodone.
Актуальность исследования
Согласно современным данным депрессия является одним из наиболее распространенных заболеваний, приводящих к нетрудоспособности и ранней смертности. Так, по данным ВОЗ, по состоянию на сегодня депрессия занимает лидирующую позицию среди всех групп заболеваний по индексу YLD (Years Lived with Disability, количество лет, прожитых с нетрудоспособностью) и 4-е место по индексу DALY (Disability Adjusted Life Years, сумма потенциальных лет жизни, утраченных из-за преждевременной смерти и нетрудоспособности). Ожидается, что к 2020 году группа депрессивных расстройств выйдет на 2-е место по индексу DALY [1]. В связи с этим разработка эффективных методов лечения депрессии является одной из наиболее приоритетных задач современной медицины.
Согласно результатам эпидемиологического исследования, проведенного в Украине, распространенность психических расстройств в общей популяции составляет 31,6 %.
Наиболее распространенные расстройства — алкогольная зависимость и рекуррентное депрессивное расстройство. Распространенность рекуррентного депрессивного расстройства в общей популяции составила 8,61 % среди мужчин и 19,48 % среди женщин, а за последний год — 4,87 и 11,34 % соответственно.
Проблему лечения депрессии усугубляет низкий процент первичных обращений по поводу данного заболевания — 4,7 % [2], а также тот факт, что даже своевременно назначенная фармакотерапия не всегда эффективна. Так, по данным систематического Кохрановского обзора (2009), среднее число пациентов, которых необходимо пролечить, чтобы достичь определенного благоприятного исхода или предотвратить один неблагоприятный исход, в сравнении с контрольной группой для трициклических антидепрессантов (ТЦА) составляет 9 и для селективных ингибиторов обратного захвата серотонина (СИОЗС) — 7 [3]. При этом клинический ответ в виде ≥ 50% редукции симптомов по шкале Гамильтона для оценки депрессии (HAM-D) при лечении СИОЗС и ТЦА находится в диапазоне 53–64 % и 43–70 % соответственно [4, 5]. Депрессивные расстройства часто сопутствуют соматической патологии. Так, распространенность депрессии при ИБС составляет 18 %, при сахарном диабете 2-го типа — 24 %, при бронхиальной астме — 25 % [6, 7]. Кроме того, при депрессии часто наблюдаются симптомы других психических нарушений, таких как генерализованное тревожное расстройство, обсессивно-компульсивное расстройство, расстройство личности. Так, согласно данным исследований у 50–60 % пациентов с депрессией на протяжении жизни наблюдалось хотя бы 1 коморбидное тревожное расстройство [8]. Следует отметить, что тревога при депрессии может быть как субсиндромальной, так и иметь полную клиническую картину тревожного расстройства. Такая высокая коморбидность депрессии свидетельствует о необходимости тщательной диагностики и индивидуального подхода к терапии пациентов, страдающих этим расстройством.
Медикаментозное лечение депрессий проводится, как правило, с помощью антидепрессантов. Препараты этого класса нормализуют патологически измененный аффект, а также уменьшают обусловленные депрессией идеомоторные и соматовегетативные нарушения. Некоторые из них обладают седативными и гипнотическими свойствами.
При рассмотрении клинических показаний к применению антидепрессантов следует помнить об особенностях действия и специфических свойствах отдельных фармакологических групп. Так, большинство трициклических антидепрессантов (амитриптилин, нортриптилин, имипрамин, кломипрамин, дибензепин и др.) обладают универсальной активностью (воздействие на широкий спектр депрессий). Известно, что их применение сопровождается побочными эффектами, в ряде случаев препятствующими продолжению лечения, однако ТЦА можно рассматривать как наиболее хорошо исследованные и надежные средства терапии депрессии. Большую группу составляют препараты иной химической структуры, разработанные в отличие от ТЦА эмпирическим путем, с учетом современных представлений о патогенезе депрессивных расстройств. К их числу относятся селективные ингибиторы обратного захвата норадреналина (мапротилин, миансерин и др.), селективные ингибиторы обратного захвата серотонина (флуоксетин, пароксетин, сертралин, флувоксамин), ингибиторы МАО-А (моклобемид, брофаромин, метралиндол, перлиндол), ингибиторы обратного захвата серотонина и норадреналина (ИОЗСН: венлафаксин, милнаципран). Препараты этой группы обладают избирательной психотропной активностью и по эффективности сопоставимы с антидепрессантами первого поколения. При этом их отличием является меньшая выраженность побочных эффектов и, следовательно, хорошая переносимость.
Дифференциация антидепрессантов по химической структуре или фармакодинамическим свойствам еще не позволяет обосновать клинические показания к их применению. Более того, несмотря на разнообразие имеющихся антидепрессантов, они не в полной мере обеспечивают потребности лечения. Выраженный клинический эффект на этапе первичной купирующей терапии фиксируется лишь в 50–60 % случаев, а полной стабильной ремиссии на этой фазе лечения достигает менее трети больных [2–4, 9].
Среди существующих клинико-терапевтических концепций выделяется концепция «идеального» антидепрессанта. Эта концепция в отличие от традиционных, позволяющих оценить исключительно психотропную активность препарата (концепции симптомов-мишеней, валентности и спектра психотропных средств), расширяет возможности выбора терапии с учетом не только собственно антидепрессивного действия. К свойствам «идеального» антидепрессанта относятся простота схемы лечения, безопасность дозирования, отсутствие способности вызывать лекарственную зависимость и/или синдром отмены, не позволяющие прекратить терапию даже по достижении полного лечебного эффекта.
Таким образом, оптимальная тактика выбора антидепрессанта предполагает учитывать следующие факторы: мишень терапии — симптом, синдром, синдромокомплекс; побочные эффекты препарата; индивидуальность эффекта; возможность продолжить поддерживающую терапию препаратом первого выбора; ресоциализирующий эффект; комплайенс-эффект; стоимость лечения.
Современная концепция терапии депрессии отдает предпочтение «мультимодальным» или «мультифункциональным» препаратам (D. Nutt, S. Stahl, 2012), к которым относится Триттико (тразодон) — препарат из группы ингибиторов и антагонистов обратного захвата серотонина.
Тразодон — антидепрессант, который принадлежит к группе антагонистов и ингибиторов обратного захвата серотонина (5-HT), мультифункциональный психофармакологический препарат с уникальным рецепторным профилем. По своему фармакологическому действию влияние тразодона на рецепторы серотонина более выражено, чем влияние на ингибирование обратного захвата. На 5-НТ2а-рецепторы он влияет как антагонист, на 5-НТ1А-рецепторы — как частичный агонист, а также он блокирует альфа-1-адренорецепторы. Тразодон имеет более низкую аффинность к 5-НТ2с и альфа-2-адренергическим рецепторам. Его способность ингибирования обратного захвата серотонина значительно ниже, чем у флуоксетина [цит. по 11]. В связи с эффектом тразодона на рецепторы серотонина он был отнесен к числу мультифункциональных антидепрессантов (S. Stahl, 2009).
Поскольку тразодон обладает неодинаковой степенью воздействия на те или иные рецепторы, его эффект является дозозависимым. При применении малых доз проявляются эффекты, связанные с самой сильной аффинностью, а эффекты, связанные с более слабой аффинностью, проявляются при более высоких дозах. Тразодон, применяемый в дозе 50 мг, полностью насыщает 5-HT2a-рецепторы, в значительной степени блокирует альфа-1-адренергические рецепторы, связывает только половину рецепторов Н1 и локусов обратного захвата серотонина. Этого достаточно для оказания седативного и гипнотического эффектов (улучшения качества и длительности сна). Для получения антидепрессивного эффекта и полного насыщения транспортера серотонина необходимо применение дозы 150–300 мг/сут. По своему эффекту ингибирования 5-HT2c-рецепторов тразодон похож на миртазапин, целый ряд трициклических антидепрессантов и агомелатин. Эффект тразодона, связанный с транспортерами допамина и норадреналина, слишком мало выражен и не имеет клинического значения. Побочные эффекты тразодона в первую очередь связаны с его антагонизмом к Н1 и альфа-1-адренергическим рецепторам [10], при этом данный антагонизм также во многом объясняет появление эффекта с первых дней применения препарата.
Терапия депрессии
Тразодон имеет доказанную эффективность в лечении депрессии. В рандомизированном двойном слепом плацебо-контролируемом исследовании, проведенном D.V. Sheehan и соавторами (2009), данный препарат показал большую эффективность, чем плацебо. Среднее уменьшение количества баллов по HAM-D-17 в группе пациентов, которые принимали тразодон, составило 11,4 (стандартное отклонение = 8,2), а в группе, которая получала плацебо, — 9,3 (стандартное отклонение = 7,9). Соответствующее процентное изменение по HAM-D-17 в экспериментальной группе находилось на уровне 49 %, а в контроле — 41 %. Указанное различие в показателях наблюдалось начиная с 1-й недели терапии и сохранялось до конца исследования (6 недель). На протяжении всего экспериментального периода не было обнаружено ни одного серьезного побочного эффекта, связанного с этим препаратом. Также не наблюдалось значимых изменений в лабораторных параметрах и ЭКГ [14]. В систематическом обзоре, проведенном G. Gartlehner и соавторами (2011), было выявлено, что эффективность тразодона была сопоставима с таковой у других антидепрессантов второго поколения. При этом изучаемые препараты различались лишь спектром побочных эффектов. Так, при использовании венлафаксина отмечалось частое возникновение тошноты и рвоты, сертралина — диареи, миртазапина — увеличение веса. При приеме бупропиона и тразодона сексуальная дисфункция возникала значительно реже в сравнении с другими антидепрессантами [15].
Сравнительный анализ эффективности тразодона и флуоксетина демонстрирует равное улучшение по HAM-D-21, шкале общего клинического впечатления для оценки улучшения состояния (CGI-I) и GMT (Guild Memory Test) у пациентов с депрессией, проходивших курс лечения указанными препаратами. Если говорить о побочных эффектах, при лечении флуоксетином наиболее частыми были ринит и тремор, а при лечении тразодоном — сонливость и головокружение. Также при лечении флуоксетином наблюдалось значительно более частое возникновение «активирующих» побочных эффектов, таких как ажитация, тревога и инсомния. В группе флуоксетина 15,4 % пациентов сообщили об указанных нежелательных явлениях, в группе тразодона — 3,3 %. В то же время в отношении седации (сонливость, астения) наблюдалась противоположная тенденция (42,6 % в группе тразодона и 21,5 % — флуоксетина). Частота отмены препарата в связи с побочными эффектами в исследуемых группах достоверно не отличалась [16].
В другом двойном слепом рандомизированном клиническом исследовании по оценке эффективности флуоксетина и тразодона в терапии амбулаторных пациентов с депрессивным расстройством было выявлено, что клинический ответ, определяемый по ≥ 50% редукции баллов по HAM-D, был одинаковым среди изучаемых групп. Также было обнаружено, что тразодон в большей степени улучшал сон в сравнении с флуоксетином. Прием флуоксетина был связан с более частым увеличением массы тела и менее частым головокружением в сравнении с тразодоном [17].
Результаты еще одного исследования по оценке эффективности данных препаратов показали большее улучшение по HAM-D и CGI-I в группе тразодона в сравнении с флуоксетином на 3-й неделе терапии. В дальнейшем более значительная редукция симптомов отмечалась в группе флуоксетина. По мнению авторов этой научной работы, полученные данные указывают на более быстрый антидепрессивный эффект тразодона [18].
В одном из исследований сравнивалась эффективность тразодона и пароксетина в отношении терапии депрессии. Результаты продемонстрировали сопоставимую действенность этих препаратов согласно HAM-D, шкале общего клинического впечатления для оценки тяжести состояния (CGI-S), CGI-I и шкале Монтгомери — Асберг для оценки депрессии (MADRS). Количество пациентов с клиническим ответом и ремиссией существенно не отличалось среди исследуемых групп. В группе больных, которые принимали пароксетин (20–40 мг/сут) и тразодон (150–400 мг/сут), эти показатели составили 91 и 87 %, а также 68 и 69 % соответственно [19].
Таблица 1.
Возможные функции постсинаптических серотониновых рецепторов (адаптировано по S. М. Stahl, 2009) [12]
| 5-НТ1а-рецепторы | 5-НТ2а-рецепторы | 5-НТ2с-рецепторы |
| — Антидепрессивная — Анксиолитическая — Прокогнитивная — Гормональная регуляция — Угнетение кортикальных пирамидных нейронов | — Сон — Сексуальная функция — Тревога — Регуляция высвобождения допамина — Регуляция высвобождения глутамата — Возбуждение кортикальных пирамидных нейронов | — Сон — Сексуальная функция — Тревога — Аппетит, ожирение — Регуляция высвобождения допамина и норадреналина — Регуляция высвобождения глутамата |
Сравнение эффективности тразодона пролонгированного действия (150–450 мг/сут) и сертралина (50–100 мг/сут) также продемонстрировало сопоставимые изменения по HAM-D, MADRS, CGI-I и CGI-S. Однако клинический ответ при приеме сертралина наблюдался у меньшего количества пациентов в сравнении с тразодоном (HAM-D — 63 и 74 %; MADRS — 66 и 78 % соответственно). Среднее изменение по этим шкалам существенно не отличалось среди исследуемых групп. Анализ симптомов согласно HAM-D (тревога/соматизация, когнитивные нарушения, ретардация, нарушения сна) показал, что в конце экспериментального периода в группе тразодона расстройства сна встречались значительно реже, чем в группе сертралина. Более того, тразодон достоверно превосходил сертралин в коррекции нарушений сна. Нежелательные побочные явления регистрировались у 42 % пациентов, которые принимали тразодон (преимущественно связанные с нервной системой), и у 43 % — сертралин (преимущественно гастроинтестинальные) [20].
Метаанализ, проведенный G.I. Papacostas, M. Fava (2007), подтвердил данные о том, что тразодон и СИОЗС значимо не различаются в плане эффективности и переносимости в терапии депрессивного расстройства. Согласно результатам этой работы доля пациентов, ответивших на терапию тразодоном/нефазодоном и СИОЗС, составила 61,1 % и 61,7 % соответственно. Показатели общей частоты отмены препарата (р = 0,334), отмены вследствие побочных эффектов (р = 0,676) и неэффективности терапии (р = 0,289) также значимо не различа-лись [21].
Терапия тревожных расстройств
Эффективность тразодона в отношении тревожных расстройств изучалась в работе K. Rickels и соавторов (1993). В этом рандомизированном двойном слепом плацебо-контролируемом клиническом исследовании проводилось сравнение тразодона с имипрамином и диазепамом. Средняя суточная доза составила 143, 255 и 26 мг соответственно. В исследование включили больных с генерализованным тревожным расстройством, которые набрали как минимум 18 баллов по шкале Гамильтона для оценки тревоги. Согласно результатам, начиная с 3-й недели анксиолитическая эффективность тразодона и имипрамина была сравнима с таковой у диазепама. При этом такие симптомы, как напряжение и беспокойство, лучше контролировались антидепрессантами. Существенное улучшение исследователи отметили у 73 % пациентов из группы, которая получала имипрамин, у 69 % — из группы, которая принимала тразодон, и у 66 % — диазепам. Улучшение в группе плацебо зарегистрировали лишь у 47 % обследуемых. Среди пациентов, принимающих антидепрессанты, побочные эффекты встречались несколько чаще, чем в группе диазепама, однако частота возникновения побочных эффектов, связанных с нарушением внимания, была одинаковой среди всех групп [22].
D.S. Charney и соавторы (1986) сравнивали эффективность имипрамина (30–300 мг/сут), алпразолама (1,5–8 мг/сут) и тразодона (50–400 мг/сут) у пациентов с паническим расстройством. Как показали результаты, и имипрамин, и алпразолам были высокоэффективны в отношении редукции симптомов генерализированной тревоги, частоты панических атак и фобического избегания. Терапевтическое действие алпразолама наблюдалось уже на первой неделе приема, а имипрамина — на 4-й неделе терапии. По мнению авторов, тразодон был менее действенен ввиду того, что терапевтический эффект при этом расстройстве достигается путем влияния на норадренергическую систему, в то время как препараты, которые действуют преимущественно на серотонинергическую систему, обладают меньшей эффективностью [23]. Вместе с тем в 8-недельном слепом исследовании были получены противоположные результаты, свидетельствующие об эффективности тразодона у пациентов с паническим расстройством и агорафобией с паническими атаками. В этом исследовании средняя суточная доза препарата составила 300 мг. Исследователи оценивали генерализованную и паническую тревогу, фобии и депрессию у пациентов, а также проводили поведенческий избегающий тест. Результаты показали существенное улучшение по всем вышеперечисленным симптомам. Авторы заключили, что тразодон имеет специфическое антипаническое и антифобическое действие и отметили важность сертонинергических механизмов в формировании данных тревожных расстройств [24].
Терапия расстройств сна
Расстройство сна у пациентов с депрессией является довольно распространенным явлением. В связи с этим в последнее десятилетие наблюдается усиленное внимание ученых к этиологии и лечению этой проблемы. Зачастую у пациентов с депрессией наблюдается недостаточная эффективность сна (т.е. недостаточный отдых после ночного сна), увеличение времени, необходимого для засыпания, частые пробуждения, укорочение фазы медленноволнового сна и фазы быстрого движения глаз (REM — rapid eye movement). В последнее время начали появляться данные и о других изменениях REM-фазы. В первую очередь это пролонгирование первого REM-периода, увеличение плотности REM и увеличение общего времени REM-фазы [25]. Эти изменения становятся еще более выраженными при повторных эпизодах депрессии [26].
Несмотря на то что современные антидепрессанты обладают схожей эффективностью в отношении терапии депрессии, большинство из них недостаточно действенны в лечении инсомнии. На сегодняшний день существует обширная доказательная база в отношении использования тразодона в качестве гипнотика. Этот препарат является эффективным в лечении как инсомнии без депрессии, так и ассоциированной с депрессией, а также инсомнии, вызванной активирующими антидепрессантами.
Так, в коротком сообщении в The American Journal of Psychiatry A. Nierenberg и соавторы (1994) представили результаты исследования с участием 17 пациентов с депрессией и инсомнией, возникшей вследствие приема флуоксетина и бупропиона. Исследуемым препаратом был тразодон, его эффективность сравнивалась с плацебо. Оценка сна проводилась при помощи Питтсбургского индекса качества сна (PSQI) и опросника для оценки симптомов депрессии Йель — Нью Хевен (Yale-New Haven Depressive Symptom Inventory). Согласно результатам значимые различия между экспериментальной группой и контролем наблюдались в общем количестве баллов и баллов, набранных по субшкале ранних пробуждений опросника Йель — Нью Хевен, а также в длительности сна согласно питтсбургскому индексу. Также наблюдалась тенденция к уменьшению количества ночных пробуждений согласно опроснику Йель — Нью Хевен в группе, которая принимала тразодон. Общее улучшение сна наблюдалось у 67 % пациентов, принимавших тразодон, и только у 13 % из группы плацебо [27].
Эффективность тразодона в отношении инсомнии изучалась также у пациентов с неорганической бессонницей, связанной с депрессивным эпизодом или рекуррентным депрессивным расстройством с использованием полисомнографии. Прием тразодона в дозе 100 мг был связан с нормализацией медленноволновой и REM-фазы сна, приводил к улучшению субъективной оценки качества сна, эмоциональной сферы и числовой памяти в сравнении с группой плацебо [30].
Таким образом, согласно результатам исследований тразодон является эффективным препаратом в терапии первичной и вторичной инсомнии, индуцированной приемом препаратов или вследствие депрессии, прием которого связан с улучшением качества сна, увеличением его длительности, уменьшением частоты ночных пробуждений. Это подтверждается и инструментальными методами оценки сна, которые демонстрируют нормализацию медленноволновой и REM-фазы сна.
Современные руководства также положительно оценивают влияние тразодона на больных с инсомнией. Так, согласно Clinical Practice Guidelines for the Management of Patients with Insomnia in Primary Care, опубликованным Министерством здоровья и социальной политики Испании, тразодон является одной из лучших альтернатив в терапии инсомнии. По мнению авторов, результаты исследований наглядно демонстрируют клиническое улучшение показателей качества сна и уменьшение количества ночных пробуждений у пациентов с инсомнией при депрессии. Однако данные относительно латентности и общей длительности сна не достигают уровня статистической значимости. Также в руководстве отмечается, что положительное влияние тразодона прослеживается и среди пациентов с первичной инсомнией. В связи с тем, что дозы, необходимые для лечения первичной инсомнии, должны быть меньше, чем те, которые используются в лечении депрессии, на данный момент не представляется возможным делать какие-либо выводы о частоте и тяжести побочных эффектов. Также необходимо проведение дополнительных рандомизированных контролируемых исследований для более детального изучения эффективности тразодона в лечении первичной инсомнии [32].
Таким образом, в научной медицинской литературе присутствует большое количество данных об эффективности тразодона в терапии депрессии, тревоги, инсомнии и болевых проявлений. Вместе с тем комп-лексная эффективность мультифункционального препарата тразодон в украинской популяции была изучена недостаточно.
Методы и материалы
Нами было проведено открытое контролируемое рандомизированное 8-недельное исследование сравнительной эффективности и безопасности препарата Тразодон у пациентов с депрессивным эпизодом. Основную группу составили 50 пациентов, проходивших терапию данным препаратом, контрольную группу — 50 пациентов, принимавших стандартные антидепрессанты.
Критериями включения в исследование были возраст 18–65 лет, диагноз «депрессивный эпизод» (F32), «рекуррентное депрессивное расстройство» (F33) или «непсихотическое депрессивное расстройство органической природы» (F06.36).
Из клинического исследования исключались пациенты с высоким риском суицида, гиперчувствительности к любому из применяемых препаратов, психотическими расстройствами, грубыми органическими поражениями ЦНС, злокачественными опухолями и другими состояниями, сопровождающимися значимыми отклонениями в лабораторных тестах.
Исследование проведено в соответствии с требованиями протокола с использованием оптимальных доз препарата. Длительность терапии составила 8 недель с последующим переводом пациентов на поддерживающую терапию вне исследования.
Для оценки эффективности назначенного лечения использовалась шкала Гамильтона для оценки депрессии, шкала Гамильтона для оценки тревоги (HAM-A), опросник оценки качества жизни (SF-36), Питтсбургский индекс качества сна. Динамика изменений выраженности симптомов депрессии и тревоги по HAM-A и HAM-D оценивалась в начале лечения и по окончании каждой недели исследования. Влияние изучаемых препаратов на сон и качество жизни по шкалам PSQI и SF-36 соответственно оценивалось в исходном периоде и по окончании экспериментального периода.
Всего нами было скринировано 116 и рандомизировано 100 пациентов. 16 больных выбыло в связи с несоответствием критериям включения. Пациентов, принявших участие в исследовании, случайным образом распределили на 2 равные группы с назначением Триттико в дозе 250–450 мг 2 раза в сутки (титрация с 50 мг) или стандартной терапии (СИОЗС, ИОЗСН) (рис. 1).
Рисунок 1. Схема проведения исследования 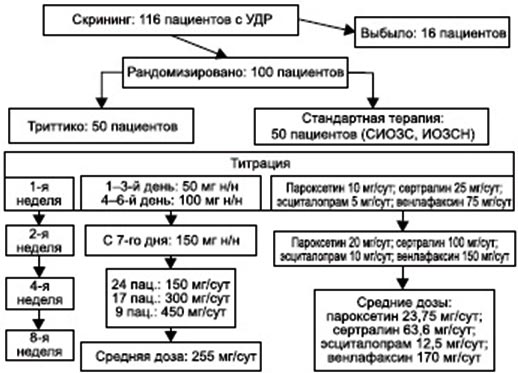
Согласно демографическим показателям средний возраст пациентов основной группы составил 39,5 ± 4,9 года, контрольной группы — 40,3 ± 4,7 года. 68 % больных, принимавших участие в клиническом исследовании, были женского пола. Всего 59 % больных имели диагноз депрессивного эпизода разной степени выраженности, 37 % — рекуррентного депрессивного расстройства и 4 % — непсихотического депрессивного расстройства органической природы. Распределение нозологий по группам представлено в табл. 3.
Таблица 2.
Дизайн исследования
| Скрининг | Недели терапии | ||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||
| HAM-D | + | + | + | + | + | + | + | + | + |
| НАМ-А | + | + | + | + | + | + | + | + | + |
| PSQI | + | + | |||||||
| SF-36 | + | + | |||||||
Таблица 3.
Распределение пациентов по диагностическим рубрикам МКБ-Юиз группы, которая получала Триттико (n = 50), и группы, которая получала стандартную терапию (n = 50)
| Диагностические рубрики МКБ-10 | Экспериментальная группа | Группа сравнения | ||
| Абс. | % | Абс. | % | |
| Депрессивный эпизод | 30 | 60 | 29 | 58 |
| Рекуррентное депрессивное расстройство | 18 | 36 | 19 | 38 |
| Непсихотическое депрессивное расстройство органической природы | 2 | 4 | 2 | 4 |
Лечение смогли закончить все 100 рандомизированных пациентов. Следует отметить, что терапевтический эффект Триттико в данном исследовании в сравнении со стандартным лечением проявлялся быстро. В частности, на первой неделе терапии в группе Триттико регистрировалось снижение на 6,2 ± 4,3, а на второй — на 9,3 ± 4,6 балла по HAM-D, в то время как в группе стандартной терапии этот показатель составил 5,3 ± 3,9 и 8,1 ± 4,1 балла соответственно (рис. 2). Общее снижение количества набранных баллов по шкале HAM-D за экспериментальный период составило 12,9 ± 5,7 в группе, которая получала Триттико, и 12,6 ± 6,1 в группе, которая получала стандартную терапию, со статистически незначимой межгрупповой разницей. Клинически значимое улучшение согласно HAM-D после проведенной терапии наблюдалось у 67,2 % пациентов из группы, которая принимала Триттико, и у 65,8 % — из группы сравнения.
Рисунок 2. Динамика изменений по HAM-D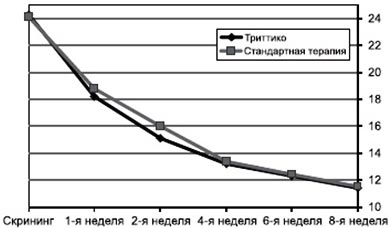
Также следует отметить большую редукцию таких симптомов по шкале HAM-D, как инсомния и соматические проявления тревоги, в группе Триттико в сравнении со стандартной терапией.
Наиболее распространенными симптомами, связанными с тревогой, были раздражительность (41 %), чувство беспокойства (33 %) и затруднение концентрации внимания (29 %). После проведенного курса лечения в обеих группах отмечалось снижение количества баллов, набранных по шкале HAM-A, в сравнении с исходным периодом. В группе Триттико общее снижение по данной шкале составило 11,3 ± 5,9 балла и в группе стандартной терапии — 10,8 ± 5,3 балла. Обращает на себя внимание более быстрое начало действия Триттико в сравнении со стандартными антидепрессантами. Так, в экспериментальной группе на 1-й неделе терапии наблюдалось снижение на 5,4 ± 2,9 балла по HAM-A, в то время как в группе сравнения этот показатель составил 3,5 ± 2,5. В этом временном срезе межгрупповое различие по данному показателю было статистически значимым (p = 0,04; рис. 3).
Рисунок 3. Динамика изменений по HAM-D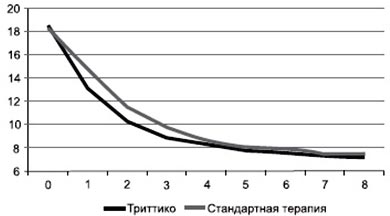
Что касается шкалы PSQI, после проведенного лечения положительные изменения регистрировались у пациентов из обеих групп. Однако следует отметить статистически значимые межгрупповые различия в пользу группы Триттико в отношении приема сно-творных препаратов, времени до засыпания и субъек-тивного качества сна (рис. 4).
Рисунок 4. Сравнение показателей по PSQI у пациентов из группы Триттико и стандартной терапии по окончании экспериментального периода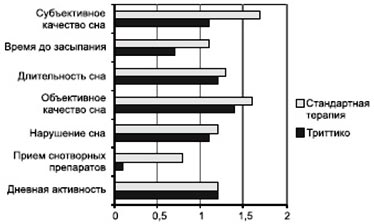
Проведенное обследование пациентов с использованием шкалы SF-36 во время скрининга и по окончании экспериментального периода продемонстрировало существенные улучшения в отношении физического и психического компонента здоровья в обеих группах. Значимые межгрупповые различия отмечались по субшкале боли (p Рисунок 5. Сравнение изменений по шкале SF-36 после 8 недель терапии и в исходном периоде (указаны средние значения для обеих групп) между группами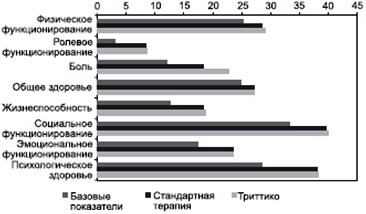
Выводы
Открытое контролируемое рандомизированное исследование подтвердило эффективность препарата Триттико в терапии пациентов с униполярной депрессией. В частности, это подтверждает положительная динамика, наблюдаемая в отношении редукции симптомов по шкале HAM-D, сравнимая с таковой при применении стандартной терапии. При этом терапевтический эффект препарата Триттико проявлялся раньше в сравнении с другими антидепрессантами.
Соответственно, анксиолитический эффект Триттико также проявляется раньше, чем таковой при применении стандартной терапии, что подтверждается данными, полученными при использовании HAM-A. Сходный противотревожный эффект тразодона также отметили K. Rickels и соавторы (1982). В их работе существенное уменьшение симптомов тревоги наблюдалось у 69 % пациентов, принимающих тразодон, в сравнении с 66 % в группе больных, которые принимали диазепам, 73 % в группе имипрамина и 47 % — при приеме плацебо [22]. Однако следует отметить, что в указанной работе выборка состояла из пациентов с генерализованным тревожным расстройством, набравших более 18 баллов по шкале HAM-A.
Как показывают результаты исследований, анксио-литическая активность некоторых антидепрессантов может быть обусловлена их влиянием на 5-HT2-рецепторы [37]. В то же время одной из особенностей тразодона является его влияние на этот вид рецепторов серотонина [38], что и объясняет его большую эффективность в отношении редукции симптомов тревоги в сравнении со стандартной терапией.
Также изучаемый препарат демонстрирует эффективность в отношении лечения инсомнии, превосходящую таковую у других упомянутых выше антидепрессантов. Результаты нашего исследования являются сходными с данными других рандомизированных клинических исследований. В частности, в работе A.A. Nierenberg и соавторов (1994) указывается, что прием тразодона достоверно увеличивает продолжительность сна и величину PSQI в сравнении с плацебо [27]. А в исследовании, проведенном B.R. Kallepalli и соавторами (1997), применение тразодона было связано с более быстрым разрешением инсомнии у пациентов в возрасте 13–17 лет с депрессивным расстройством в сравнении с флуоксетином [39].
Ключевую роль в отношении редукции инсомнии, как и снижения интенсивности тревоги, играет способность тразодона блокировать 5-HT2-рецепторы. Это находит свое подтверждение в клинических исследованиях, в которых блокирование данных рецепторов увеличивало продолжительность сна и нормализовало его архитектонику [40].
Таким образом, данное клиническое исследование подтвердило превосходство в эффективности мультифункционального препарата Триттико по сравнению со стандартной терапией депрессии не только по более быстрому началу действия, но также по наличию выраженного анксиолитического эффекта и редукции инсомнии.
СПИСОК ЛИТЕРАТУРЫ:
1. World Health Organization. Mental health: Depression (http://www.who.int/mental_health/management/depression/definition/en/).
2. Пинчук И.Я. Распространенность психических расстройств в Украине // Журн. АМН Украины. — 2010. — Т. 16, № 1. — С. 168-176.
3. Arroll B., Elley C. R., Fishman T. et al. Antidepressants versus placebo for depression in primary care // Cochrane Database of Systematic Reviews. — 2009. — V. 3. — Art. №: CD007954.
4. Arroll B., Macgillivary S., Ogston S. et al. Efficacy and Tolerability of Tricyclic Antidepressants and SSRIs Compared With Placebo for Treatment of Depression in Primary Care: A Meta-Analysis // Ann. Fam. Med. — 2005. — V. 3. — P. 449-456.
5. Hirschfeld R.M. Efficacy of SSRIs and newer antidepressants in severe depression: comparison with TCAs // J. Clin. Psychiatry. — 1999. — V. 60. — P. 326-335.
6. Rouchell A.M. Major Depression in primary care // The Ochsner Joutnal. — 2000. — V. 2. — P. 79-84.
7. Filipcic I., Popovic-Grle S., Marchinko D. et al. Screening for depression disorder in patients with chronic somatic illness // Coll. Antropol. — 2007. — V. 1. — P. 139-143.
8. Kaufman J., Charney D. Comorbidity of mood and anxiety disorders // Depress Anxiety. — 2000. — V. 12. — P. 69-76.
9. Ciraulo D.A., Shader R.I. Pharmacotherapy of Depression. — 2nd ed. — New York: Humana Press, 2011. — 436 p.
10. Nilsen O.G., Dale O. Single Dose Pharmacokinetics of Trazodone in Healthy Subjects // Pharmacology & Toxicology. — 1992. — V. 71. — P. 150-153.
11. Фрешска Э. Многофункциональный механизм действия тразодона и область его клинического применения // Вестник Ассоциации психиатров Украины. — 2013. — № 1.
12. Stahl S.M. Mechanism of action of trazodone: a multifunctional drug // CNS Spectr. — V. 14(10).
13. Jarema M., Dudek D., Landowski J. et al. Trazodone: mechanism of action and its position in the treatment of depression // Psychiatr. Pol. — 2011. — V. 45. — P. 611-625.
14. Sheehan D.V., Croft H.A., Gossen R. et al. Extended-release Trazodone in Major Depressive Disorder: A Randomized, Double-blind, Placebo-controlled Study // Psychiatry (Edgmount). — 2009. — V. 6. — P. 20-33.
15. Gartlehner G., Hansen R.A., Morgan L.C. et al. Second-Generation Antidepressants in the Pharmacologic Treatment of Adult Depression: An Update of the 2007 Comparative Effectiveness Review. — AHRQ Publication № 12-EHC012-EF, Rockville: Agency for Healthcare Research and Quality, 2011. — 954 p.
16. Beasley C.M., Dornseif B.E., Pultz J.A. et al. Fluoxetine versus trazodone: efficacy and activating-sedating effects // J. Clin. Psychiatry. — 1991. — V. 52. — P. 294-299.
17. Debus J.R., Rush A.J., Himmel C. et al. Fluoxetine versus trazodone in the treatment of outpatients with major depression // J. Clin. Psychiatry. — 1988. — V. 49. — P. 422-426.
18. Perry P.J., Garvey M.J., Kelly M.W. et al. A comparative trial of fluoxetine versus trazodone in outpatients with major depression // J. Clin. Psychiatry. — 1989. — V. 50. — P. 290-294.
19. Kasper S., Olivieri L., Di Loreto G., Dionisio P. A comparative, randomized, double-blind study of trazodone prolonged-release and paroxetine in the treatment of patients with major depressive disorder // Current Medical Research and Opinion. — 2005. — V. 21. — P. 1139-1146.
20. Munizza C., Oliviery L., Di Loreto G. et al. A comparative, randomized, double-blind study of trazodone prolonged-release and sertraline in the treatment of major depressive disorder // Current Medical Research and Opinion. — 2006. — V. 22. — Р. 1703-1713.
21. Papakostas G.I., Fava M.A. A meta-analysis of clinical trials comparing the serotonin(5HT)-2 receptor antagonists, trazodone and nefazodone with selective serotonin reuptake inhibitors for the treatment of major depressive disorder // Eur. Psychiatry. — 2007. — V. 22. — P. 444-447.
22. Rickels K., Downing R., Schweizer E., Hassman H. Antidepressants for the treatment of generalized anxiety disorder. A placebo-controlled comparison of imipramine, trazodone, and diazepam // Arch. Gen. Psychiatry. — 1993. — V. 50(11). — P. 884-895.
23. Charney D.S., Woods S.W., Goodman W.K. et al. Drug treatment of panic disorder: The comparative efficacy of imipramine, alprazolam, and trazodone // J. Clin. Psychiatry. — 1986. — V. 47(12). — P. 580-586.
24. Mavissakalian M., Perel J., Browler K. Trazodone in the treatment of panic disorder and agoraphobia with panic attacks // Am. J. Psychiatry. — 1987. — V. 144. — P. 785-787.
25. Akiskal H.S., Lemmi H., Yerevanian B. et al. The usefulness of the REM latency test in psychiatric diagnosis: a study of 81 depressed outpatients // Psychiatr. Res. — 1982. — V. 7. — P. 101-110.
26. Kupfer D.J., Ehlers C.L., Frank E. et al. EEG sleep and recurrent depression // Biol. Psychiatry. — 1988. — V. 30. — P. 641-655.
27. Nierenberg A.A., Adler L.A., Peselow E. et al. Trazodone for antidepressant-associated insomnia // Am. J. Psychiatry. — 1994. — V. 151(7). — P. 1069-1072.
28. Walsh J.K., Erman M., Erwin C. et al. Subjective Hypnotic efficacy of trazodone and zolpidem in DSM III-R primary insomnia // Human Psychopharm. Clin. Exp. — 1998. — V. 13(3). — P. 191-198.
29. Zavesicka L., Brunovsky M., Horacek J. et al. Trazodone improves the results of cognitive behavior therapy of primary insomnia in non-depressed // Neuroendocrinol. Lett. — 2008. — V. 29. — P. 895-901.
30. Saletu-Zyhlarz G.M., Abu-Bakr M.H., Anderer P. et al. Insomnia related to dysthymia: polysomnographic and psychometric comparison with normal controls and acute therapeutic trials with trazodone // Neuropsychobiology. — 2001. — V. 44. — P. 139-149.
31. Schwartz T., Nihalani N., Virk S. et al. A comparison of the effectiveness of two hypnotic agents for the treatment of insomnia // Int. J. Psychiatr. Nurs. Res. — 2004. — V. 10. — P. 1146-1150.
32. Guideline development group for the management of patients with insomnia in primary care. Clinical Practice Guidelines for the Management of Patients with Insomnia in Primary Care. — Ministry of Health and Social Policy, 2009. — 160 p.
33. Verdu B., Decosterd I., Buclin T. et al. Antidepressants for the treatment of chronic pain // Drugs. — 2008. — V. 68. — V. 2611-2632.
34. Botney M., Fields H.L. Amitriptyline potentiates morphine analgesia by a direct action on the central nervous system // Ann. Neurol. — 1983. — V. 13. — P. 160-164.
35. Ventafridda V., Bonezzi C., Caraceni A. et al. Antidepressants for cancer pain and other painful syndromes with deafferantation component: comparison of amitriptyline and trazodone // Ital. J. Neurol. Sci. — 1987. — V. 8. — P. 579-587.
36. Wilson R.C. The use of low-dose trazodone in the treatment of painful diabetic neuropathy // JAPMA. — 1999. — V. 89. — P. 468-471.
37. Deakin J.F. 5HT2 receptors, depression and anxiety // Pharmacol. Biochem. Behav. — 1988. — V. 29(4). — P. 819-820.
38. Roth B.L., Shapiro D.A. Insights into the structure and function of 5-HT(2) family serotonin receptors reveal novel strategies for therapeutic target development // Expert Opin. Ther. Tartgets. — 2001. — V. 5(6). — P. 685-695.
39. Kallepalli B.R., Bhatara V.S., Foqas B.S. et al. Trazodone is only slightly faster than fluoxetine in relieving insomnia in adolescents with depressive disorders // J. Child Adolesc. Psychopharmacol. — 1997. — V. 7(2). — P. 97-107.
40. Thase M.E. Antidepressant treatment of the depressed patient with insomnia // J. Clin. Psychiatry. — 1999. — V. 17. — P. 28-31.
